Analiza objtociowa miareczkowa zadania z rozwizaniem cz III

Analiza objętościowa (miareczkowa) zadania z rozwiązaniem / cz. III Ø redoksymetria: ü manganometria, ü cerometria, ü jodometria, ü bromianometria

Redoksymetria v Redoksymetria – dział analizy miareczkowej z wykorzystaniem reakcji redukcji i utlenienia: Ø odczynnikiem miareczkującym może być substancja utleniająca lub redukująca, Ø reakcje redukcji i utlenienia (redox) są sprzężone, elektrony z reduktora przechodzą na utleniacz, Ø liczba elektronów przekazanych przez reduktor jest zawsze równa liczbie elektronów przyjętych przez utleniacz.

Redoksymetria – manganometria v Manganometria: Ø odczynnikiem miareczkującym jest roztwór manganianu(VII) potasu KMn. O 4 o stężeniu 0, 01 mol/cm 3 lub 0, 02 mol/dm 3 Ø indykatorem / wskaźnikiem reakcji jest odczynnik miareczkujący przyjmując barwę w zależności od stopnia utlenienia: Ø właściwości utleniające zależą od środowiska reakcji: ü środowisko silnie kwasowe bladoróżowy • Mn. O 4 - + 8 H+ + 5 e- Mn 2+ + 4 H 2 O ü środowisko obojętne lub zbliżone do obojętnego brunatny • Mn. O 4 - + 2 H 2 O + 3 e- Mn. O 2 + 4 OHü środowisko mocno zasadowe zielony • Mn. O 4 - + 1 e- Mn. O 42 -

Redoksymetria - cerometria v Cerometria: Ø odczynnikiem miareczkującym jest roztwór Ce(SO 4)2 w 0, 25 molowym kwasie siarkowym(VI), Ø lub (NH 4)4[Ce(SO 4)4] ∙ 2 H 2 O, który jest znacznie lepiej rozpuszczalny w rozcieńczonym kwasie siarkowym(VI), Ø indykatorem / wskaźnikiem jest ferroina (związek kompleksowy żelaza z fenantroliną), forma utleniona ma barwę bladoniebieską, zredukowana barwę czerwoną, Ø kation Ce 4+ w środowisku silnie kwasowym ma silne właściwości utleniające: ü Ce 4+ + 1 e- Ce 3+

Redoksymetria - jodometria v Jodometria: Ø odczynnikiem miareczkującym jest jod, który jest słabym utleniaczem i bezpośrednio może reagować z silnymi reduktorami (As. O 33 -, S 2 O 32 -, Sn 2+) Ø przebieg reakcji zależy o potencjału redukcyjnego układu drugiego składnika, ü I 2 + 2 e - ↔ 2 IØ odmianą jodometrii jest bezpośrednie oznaczenie utleniaczy nadmiarem roztworu KI, w którym wydzielony wolny jod odmiareczkowuje się mianowanym roztworem Na 2 S 2 O 3 Ø indykatorem / wskaźnikiem jest kleik skrobiowy, który w obecności śladów jodu przybiera barwę niebieską.

Redoksymetria – bromianometria v Bromianomrtria: Ø odczynnikiem miareczkującym jest anion Br. O 3 -, który w środowisku silnie kwasowym posiada mocne właściwości utleniające i reaguje wg poniższych równań: ü Br. O 3 - + 6 e- + 6 H+ Br- + 3 H 2 O ü Br. O 3 - + 5 Br- + 6 H+ 3 Br 2 + 3 H 2 O (r. synproporcjonowania), Ø indykatorami / wskaźnikami mogą są barwniki organiczne (oranż metylowy, czerwień metylowa, kwas indygosulfonowy) z którymi reaguje wolny brom, Ø bromianometria stosuje się głównie do oznaczania związków organicznych o silnych właściwościach redukujących, a także cyny, talu, arsenu, antymonu.

Graficzna ilustracja miareczkowana v. Przebieg miareczkowania przedstawia się graficznie podając zależność potencjału redoks od objętości użytego odczynnika lub ułamka zmiareczkowania oznaczanej substancji, Ø potencjał redoks układu określa równanie Nernsta: • Eo – potencjał standardowy układu, [Utl], [Red] – stężenia molowe formy utlenionej i zredukowanej, n – liczba moli elektronów wymienionych w reakcji rdoks, Ø w trakcie miareczkowania w roztworze zmienia się stosunek stężeń formy utlenionej do zredukowanej

Graficzna ilustracja miareczkowana / cd. Ø w roztworze miareczkowanym przebiega reakcja redos: ü n 1 ∙ Utl 1 + n 2 ∙ Red 2 ↔ n 1 ∙ Red 1 + n 2 ∙ Utl 2 ü reagującym układom odpowiadaja potencjały redoks: ü w punkcie równoważnikowym PR potencjały redoks są równe: E 1 = E 2 = EPR : • n 1 ∙ EPR – n 1 ∙ Eo 1 = n 2 ∙ EPR – n 2 ∙ Eo 2 stąd ü w określonych warunkach potencjał redoks zależy wyłącznie od stosunku formy utlenionej do zredukowanej, rozcieńczanie roztworu w trakcie miareczkowania nie ma wpływu na kształt krzywej oraz na wielkość skoku krzywej, ü jeżeli n 1 = n 2 krzywa miar. jest symetryczna w stosunku do PR.
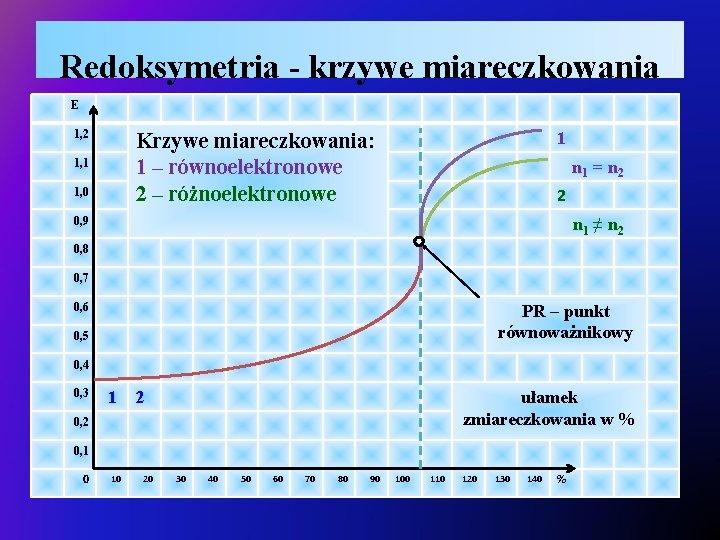
Redoksymetria - krzywe miareczkowania E 1, 2 1 Krzywe miareczkowania: 1 – równoelektronowe 2 – różnoelektronowe 1, 1 1, 0 n 1 = n 2 2 0, 9 n 1 ≠ n 2 0, 8 0, 7 0, 6 PR – punkt równoważnikowy 0, 5 0, 4 0, 3 1 2 ułamek zmiareczkowania w % 0, 2 0, 1 0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 %

Przykładowe zadanie z rozwiązaniem v Zad. 1. Ø Oblicz potencjał redoks układu Mn. O 4 - / Mn 2+ w przypadku: a) do 50 cm 3 roztworu KMn. O 4 o stężeniu 0, 025 mol/dm 3 wprowadzono 80 cm 3 roztworu Fe. SO 4 o stężeniu 0, 04 mol/dm 3, b) do 50 cm 3 roztworu KMn. O 4 o stężeniu 0, 02 mol/dm 3 wprowadzono 120 cm 3 Fe. SO 4 o stężeniu 0, 05 mol/dm 3, c) 60 cm 3 roztworu KMn. O 4 o stężeniu 0, 02 mol/dm 3 zredukowano w 60% za pomocą 0, 03 molowego roztworu Sn. Cl 2, d) 60 cm 3 roztworu KMn. O 4 o stężeniu 0, 02 mol/dm 3 zredukowano w 90% za pomocą 0, 03 molowego roztworu Sn. Cl 2, Eo. Mn. O 4 -/Mn 2+ = 1, 507 V. Ø Rozwiązanie: Ø dla ppkt. a i b : ü Mn. O 4+ + 5 Fe 2+ + 5 e- + 8 H+ Mn 2+ + 5 Fe 3+ + 4 H 2 O / n = 5

Przykładowe zadanie z rozwiązaniem v Zad. 1. Rozwiązanie ppkt. a i b: Ø ü ü ü a) obliczenie stężeń formy utlenionej i zredukowanej Mn. O 4 -: NMn. O 4 -(pocz. ) = 50 cm 3 ∙ 0, 025 mmol/cm 3 = 1, 25 mmol, NFe 2+ = 100 cm 3 ∙ 0, 04 mmol/cm 3 = 4 mmol, 5 mmol Fe 2+ ------ 1 mmol Mn. O 44 mml Fe 2+ ------x ------------------------ü [Red] = x = 0, 8 mmol, ü [Utl] = ∆N(Utl) = 1, 25 mmol – 0, 8 mmol = 0, 45 mmol Ø obliczenie potencjału redukcyjnego:

Przykładowe zadanie z rozwiązaniem v Zad. 1. Rozwiązanie ppkt. a i b: Ø ü ü ü b) obliczenie stężeń formy utlenionej i zredukowanej Mn. O 4 -: NMn. O 4 -(pocz. ) = 50 cm 3 ∙ 0, 025 mmol/cm 3 = 1, 25 mmol, NFe 2+ = 120 cm 3 ∙ 0, 05 mmol/cm 3 = 6 mmol, 5 mmol Fe 2+ ------ 1 mmol Mn. O 46 mml Fe 2+ ------x ------------------------ü [Red] = x = 1, 2 mmol, ü [Utl] = ∆N(Utl) = 1, 25 mmol – 1, 2 mmol = 0, 05 mmol Ø obliczenie potencjału redukcyjnego:

Przykładowe zadanie z rozwiązaniem v Zad. 1. Rozwiązanie ppkt. c i d: Ø ü ü ü Ø c) obliczenie stężeń formy utlenionej i zredukowanej Mn. O 4 -: NMn. O 4 -(pocz. ) = 60 cm 3 ∙ 0, 02 mmol/cm 3 = 1, 2 mmol, [Red] = 0, 6 ∙ 1, 2 mmol = 0, 72 mmol, [Utl] = ∆N(Utl) = 1, 2 mmol – 0, 72 mmol = 0, 48 mmol Ø ü ü Ø d) obliczenie stężeń formy utlenionej i zredukowanej Mn. O 4 -: [Red] = 0, 9 ∙ 1, 2 mmol = 1, 08 mmol, [Utl] = ∆N(Utl] = 1, 2 mmol – 1, 08 mmol = 0, 12 mmol obliczenie potencjału redukcyjnego:

Przykładowe zadanie z rozwiązaniem v Zad. 2. Ø Połączono roztwory: a) 50 cm 3 roztworu Ce(SO 4)2 o stężeniu 0, 128 mol/dm 3 i 40 cm 3 roztworu Fe. SO 4 o stężeniu 0, 16 mol/dm 3, b) 30 cm 3 roztworu Sb. Cl 3 o stężeniu 0, 2 mol/dm 3 i 50 cm 3 KBr. O 3 o stężeniu 0, 048 mol/dm 3, Ø Eo. Fe 3+/Fe 2+ = 0, 77 V, Eo. Br. O 3 -/Br- = 1, 33 V, Eo. Ce 4+/Ce 3+ = 1, 72 V Ø Oblicz potencjały redoks otrzymanych układów. Ø Rozwiązanie – ppkt. a: ü Fe 2+ + Ce 4+ Fe 3+ + Ce 3+ ; n 1 + n 2 = 1 + 1 = 2, ü 1 mmol Fe 2+ reaguje z 1 mmol Ce 4+, ü NCe 4+ = V ∙ Cm = 50 cm 3 ∙ 0, 128 mmol/cm 3 = 6, 4 mmol, ü NFe 2+ = V ∙ Cm = 40 cm 3 ∙ 0, 16 mmol/cm 3 = 6, 4 mmol, ü w układzie został osiągnięty punkt równoważnikowy - PR

Przykładowe zadanie z rozwiązaniem v Zad. 2. rozwiązanie – ppkt. a cd. : Ø ü ü ü ppkt. b: Br. O 3 - + 3 Sb 3+ + 18 Cl- + 6 H+ Br- + 3 Sb. Cl 6 - + 3 H 2 O 1 mmol Br. O 3 - utlenia 3 mole Sb 3+ / n = 6, NSb 3+ = V ∙ Cm = 30 cm 3 ∙ 0, 2 mmol/cm 3 = 6 mmol, NBr. O 3 - = V ∙ Cm = 50 cm 3 ∙ 0, 048 mmol/cm 3 = 2, 4 mmol, obliczenie stężenia formy utlenionej anionu bromianowego i formy zredukowanej Br- po reakcji: ü ∆NBr. O 3 - = 2, 4 mmol – 1/3 ∙ 6 mmol = 0, 4 mmol, ü ∆NBr- = 2, 4 mmol - 0, 4 mmol = 2 mmol,

Przykładowe zadanie z rozwiązaniem v Zad. 3. Ø Oblicz skok krzywej miareczkowania 50 cm 3 roztworu Fe. SO 4 o stężeniu 0, 16 mol/dm 3 za pomocą roztworu K 2 Cr 2 O 7 o stężeniu 0, 04 mol/dm 3 w środowisku kwasowym przy zmiareczkowaniu w zakresie ± 1%. Ø Eo. Fe 3+/Fe 2+ = 0, 77 V, Eo. Cr 2 O 72 -/2 Cr 3+ = 1, 23 V. Ø Rozwiązanie: Ø niedomiareczkowanie w zakresie 1% ü 6 Fe 2+ + Cr 2 O 72 - + 14 H+ 6 Fe 3+ + 2 Cr 3+ + 7 H 2 O ü 6 mmol Fe 2+ reaguje z 1 mmol Cr 2 O 72 -, ü NFe 2+/zred. = 50 cm 3 ∙ 0, 16 ∙ mmol/cm 3 ∙ 0, 01 = 0, 08 mmol, ü NFe 3+/utl. = 50 cm 3 ∙ 0, 16 mmol/cm 3 ∙ 0, 99 = 7, 92 mmol,

Przykładowe zadanie z rozwiązaniem v Zad. 3. – rozwiązanie cd. : Ø przemiareczkowanie o 1%: ü NCr 2 O 72 -/utl. = 1/6 ∙ NFe 2+ ∙ 0, 01 = 1/6 ∙ 8 mmol ∙ 0, 01 = = 0, 0133 mmol ü NCr 3+/zred. = 1/6 ∙ NFe 2+ = 1/6 ∙ 8 = 1, 333 mmol Ø obliczenie skoku krzywej miareczkowania: ü ∆E = E(+1%) – E(-1%) = 1, 21 V – 0, 888 V = 0, 322 V

Przykładowe zadanie z rozwiązaniem v Zad. 4. Ø Do zmiareczkowania 0, 25 g kwasu H 2 C 2 O 4 ∙ 2 H 2 O w środowisku mocno kwasowym zużyto 48 cm 3 roztworu KMn. O 4. Oblicz stężenie molowe roztworu odczynnika miareczkującego. Ø ü ü Rozwiązanie: 2 Mn. O 4 - + 5 C 2 O 42 - + 16 H+ 2 Mn 2+ + 10 CO 2+ 8 H 2 O 2 mole KMn. O 4 utleniają 5 moli kwasu szczawiowego MH 2 C 2 O 4 ∙ 2 H 2 O = 126 g/ mol = 0, 126 g/mmol NH 2 C 2 O 4 = 0, 25 g : MH 2 C 2 O 4∙ 2 H 2 O = 0, 25 g : 0, 126 g/mmol ≈ ≈ 1, 984 mmol

Przykładowe zadanie z rozwiązaniem v Zad. 5. Ø Do roztworu KI wprowadzono 25 cm 3 roztworu KMn. O 4 o stężeniu 0, 02 mol/dm 3 w środowisku mocno kwasowym Na zmiareczkowanie wydzielonego jodu zużyto 27, 7 cm 3 roztworu Na 2 S 2 O 3. Oblicz stężenie molowe roztworu odczynnika miareczkującego. Ø Rozwiązanie: ü 2 Mn. O 4 - + 10 I- + 16 H+ 2 Mn 2+ + 5 I 2+ 8 H 2 O, ü 5 I 2 + 10 S 2 O 32 - 10 I- + 5 S 4 O 62 -, ü na 2 mole Mn. O 4 - przypada 10 moli S 2 O 32 - czyli 1 : 5 ü Cm ≈ 0, 09 mmol/cm 3
- Slides: 19




































