Analiza objtociowa miareczkowa zadania z rozwizaniem cz IV

Analiza objętościowa (miareczkowa) zadania z rozwiązaniem / cz. IV Ø argentometria, Ø kompleksometria

Argentometria v Argentometria – analiza miareczkowa strąceniowa: Ø polega na wytrąceniu z miareczkowanego roztworu trudno rozpuszczalnego osadu pod wpływem odczynnika miareczkującego, Ø odczynnikiem miareczkującym jest roztwór Ag. NO 3, który z jonami X- (Cl-. Br-, I-) i SCN- (rodankowy) tworzy trudno rozpuszczalne osady soli srebra: Agl, Ag. Br, Ag. I, Ag. SCN, Ø wskaźnikiem może być: ü K 2 Cr. O 4 - metoda Mohra, nadmiar Ag+ tworzy czerwonobrunatny trudno rozpuszczalny osad Ag 2 Cr. O 4, ü NH 4 SCN + Fe 3+ - metoda Volharda, nadmiar SCNz kationami Fe 3+ tworzy barwny kompleks, ü w miarę wprowadzania odczynnika miareczkującego stężenie oznaczanego jonu w analizowanym roztworze zmienia się powoli a w pobliżu PR zmienia się skokowo.

Argentometria – krzywe miareczkowania strąceniowego v Krzywe miareczkowania strąceniowego: Ø określa zależność wykładnika stężenia strącanego jonu (p. X = log [X]) od: ü objętości roztworu miareczkującego ü lub ułamka zmiareczkowania oznaczanego jonu, Ø przebieg krzywej zależy od stężeń reagujących roztworów, Ø położenie punktów równoważnikowych (PR 1 i PR 2) zależy od iloczynu rozpuszczalności (KSO) osadu powstającego w trakcie miareczkowania, Ø część dolna krzywej odpowiada aktualnym stężeniom oznaczanego jonu w analizowanym roztworze,

Argentometria – krzywe miareczkowania strąceniowego v Krzywe miareczkowania strąceniowego cd. : Ø po przekroczeniu PR dalsze punkty krzywej oblicza się z iloczynu stężenia jonu wprowadzanego i KSO tworzącego się osadu (przy założeniu, że jony powstające w dysocjacji elektrolitycznej trudno rozpuszczalnego osadu nie maja wpływu na rozpuszczalność tego osadu), Ø wielkość skoku miareczkowania w analizie strąceniowej zależy od : ü stężenia reagujących roztworów, ü wartości iloczynu rozpuszczalności osadu powstającego w trakcie miareczkowania,
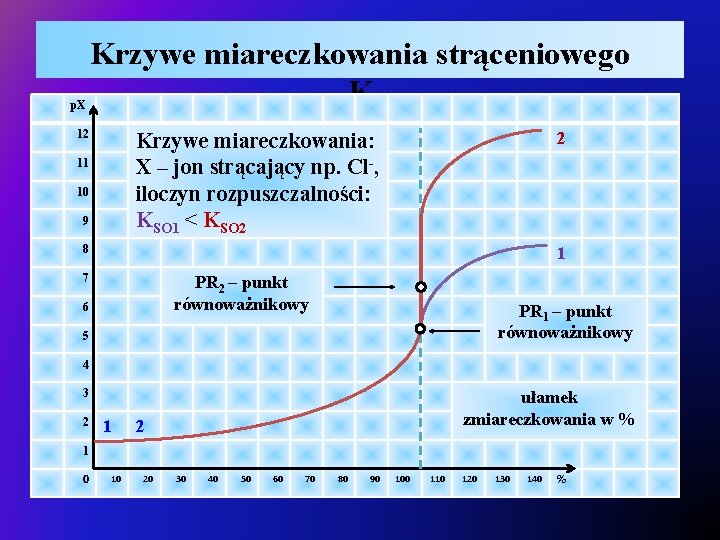
p. X Krzywe miareczkowania strąceniowego K 12 2 Krzywe miareczkowania: X – jon strącający np. Cl-, iloczyn rozpuszczalności: KSO 1 < KSO 2 11 10 9 8 1 7 PR 2 – punkt równoważnikowy 6 PR 1 – punkt równoważnikowy 5 4 3 2 1 ułamek zmiareczkowania w % 2 1 0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 %

Przykładowe zadania z rozwiązaniem v Zad. 1. Ø Próbkę stopu srebra i złota o masie 2, 25 g roztworzono w kwasie HNO 3, po oddzieleniu od Au i rozcieńczeniu roztworu Ag. NO 3 zmiareczkowano metodą Volhrada zużywając 45, 2 cm 3 roztworu NH 4 SCN o stężeniu 0, 25 mol/dm 3. Oblicz % zawartość srebra w stopie. Ø Rozwiązanie: ü Ag+ + SCN- Ag. SCN, stąd: NAg = NNH 4 SCN , ü NNH 4 SCN = V ∙ Cm = 45, 2 cm 3 ∙ 0, 25 mmol/cm 3 = 11, 3 mmol, ü MAg = 107, 868 g/mol = 0, 107868 g/mmol,

Przykładowe zadania z rozwiązaniem / cd. v Zad. 2. Ø Próbkę soli kamiennej o masie 0, 25 g rozpuszczono w wodzie destylowanej a następnie zmiareczkowano 34, 5 cm 3 roztworu Ag. NO 3 o stężeniu 0, 1 mol/dm 3. Oblicz % zawartość Na. Cl w soli kamiennej zakładając, że nie zawiera ona anionów, które z Ag+ tworzą sole praktycznie nierozpuszczalne w wodzie. Ø Rozwiązanie: ü Ag+ + Cl- Ag. Cl, stąd: NAg = NNa. Cl , ü NAg. NO 3 = V ∙ Cm = 34, 5 cm 3 ∙ 0, 1 mmol/cm 3 = 3, 45 mmol, ü MNa. Cl = 58, 45 g/mol = 0, 05845 g/mmol

Przykładowe zadania z rozwiązaniem / cd. v Zad. 3. Ø Próbkę węglanu sodu o masie 2, 25 g zawierającą domieszkę Na. Cl rozpuszczono w wodzie destylowanej i zakwaszono HNO 3. Tak przygotowany roztwór zmiareczkowano 22 cm 3 roztworu Ag. NO 3 o stężeniu 0, 1 mol/dm 3. Nadmiar kationów Ag+ zmiareczkowano 14, 2 cm 3 roztworu rodanku amonu o stężeniu 0, 1 mol/dm 3. Oblicz % zawartość domieszki Na. Cl. Ø Rozwiązanie: ü Ag+ + Cl- Ag. Cl, Ag+ + SCN- Ag. SCN, stąd: ü NNa. Cl = (VAg. NO 3 – VNH 4 SCN) ∙ 0, 1 mmol/cm 3 ü NNa. Cl = (22 cm 3 – 14, 2 cm 3) ∙ 0, 1 mmol/cm 3 = 0, 78 mmol ü MNa. Cl = 58, 45 g/mol = 0, 05845 g/mmol

Przykładowe zadania z rozwiązaniem / cd. v Zad. 4. Ø Obliczyć p. Ag i p. X (p. Cl, p. Br, p. I, p. SCN) w następujących przypadkach: a) 40 cm 3 roztworu Ag. NO 3 o stężeniu 0, 15 mol/dm 3 zmieszano z 35 cm 3 roztworu KI o stężeniu 0, 2 mol/dm 3, KSO/Ag. I = 8, 52 ∙ 10 -17, a) 40 cm 3 roztworu Ag. NO 3 o stężeniu 0, 125 mol/dm 3 zmieszano z 60 cm 3 roztworu NH 4 SCN o stężeniu 0, 12 mol/dm 3, KSO/Ag. SCN = 1, 03 ∙ 10 -12, b) 80 cm 3 roztworu Ag. NO 3 o stężeniu 0, 02 mol/dm 3 zmieszano c) z 50 cm 3 roztworu NH 4 SCN o stężeniu 0, 032 mol/dm 3, KSO/Ag. SCN = 1, 03 ∙ 10 -12, d) 30 cm 3 roztworu Ag. NO 3 o stężeniu 0, 15 mol/dm 3 zmiareczkowano w 85% roztworem KBr o stężeniu 0, 1 mol/dm 3, KSO/Ag. Br = 5, 35 ∙ 10 -12.

Przykładowe zadania z rozwiązaniem / cd. Ø ü • • • ü Rozwiązanie 4 a: obliczenie liczby milimoli reagentów: Ag+ + I- Ag. I, NAg. NO 3 = V ∙ Cm = 40 cm 3 ∙ 0, 15 mmol/cm 3 = 6 mmol, NKI = V ∙ Cm = 35 cm 3 ∙ 0, 2 mmol/cm 3 = 7 mmol, ∆NKI = NKI - NAg. NO 3 = 7 mmol – 6 mmol = 1 mmol, Vc = VAg. NO 3 + VKI = 40 cm 3 + 35 cm 3 = 75 cm 3, obliczenie stężenia molowego I- w otrzymanym roztworze: ü obliczenie stężenia molowego Ag+ wynikającego z KSO/Ag. I:

Przykładowe zadania z rozwiązaniem / cd. Ø Rozwiązanie 4 a cd. : ü obliczenie p. I i p. Ag: • p. I = - log [I-] = - log 1, 33 ∙ 10 -2 = 2 – 0, 12 = 1, 88 , • p. Ag = - log [Ag+] = - log 6, 41 ∙ 10 -15 = 15 – 0, 81 = 14, 19. • obliczenie p. I i p. Ag drugim sposobem: • p. Ag + p. I = p. KSO = - log 8, 52 ∙ 10 -17 = 17 – 0, 93 = 16, 07, • p. I = p. KSO – p. Ag = 16, 7 – 14, 19 = 1, 88 , • p. Ag = 16, 07 – p. I = 16, 7 – 1, 88 = 14, 19.

Przykładowe zadania z rozwiązaniem / cd. Ø ü • • • ü Rozwiązanie 4 b: obliczenie liczby milimoli reagentów: Ag+ + SCN- Ag. SCN, NAg+ = V ∙ Cm = 40 cm 3 ∙ 0, 125 mmol/cm 3 = 5 mmol, NSCN- = V ∙ Cm = 60 cm 3 ∙ 0, 12 mmol/cm 3 = 7, 2 mmol, ∆NSCN- = NSCN- - NAg+= 7, 2 mmol – 5 mmol = 2, 2 mmol, Vc = VAg. NO 3 + VNH 4 SCN = 40 cm 3 + 60 cm 3 = 100 cm 3, obliczenie stężenia [SCN-] w otrzymanym roztworze: ü obliczenie stężenia molowego Ag+ wynikającego z KSO/Ag. SCN:

Przykładowe zadania z rozwiązaniem / cd. Ø ü • • ü Rozwiązanie 4 c: obliczenie liczby milimoli reagentów: Ag+ + SCN- Ag. SCN, NAg+ = V ∙ Cm = 80 cm 3 ∙ 0, 02 mmol/cm 3 = 1, 6 mmol, NSCN- = V ∙ Cm = 50 cm 3 ∙ 0, 032 mmol/cm 3 = 1, 6 mmol, NSCN- = NAg+ obliczenie: p. Ag = p. SCN :

Przykładowe zadania z rozwiązaniem / cd. Ø ü • • ü Rozwiązanie 4 d: obliczenie liczby milimoli reagentów: Ag+ + Br- Ag. Br, NAg+ = V ∙ Cm = 30 cm 3 ∙ 0, 15 mmol/cm 3 = 4, 5 mmol, NBr- = 0, 85 ∙ NAg+ = 0, 85 ∙ 4, 5 mmol = 3, 825 mmol, ∆NAg+ = 4, 5 mmol – 3, 825 mmol = 0, 675 mmol, obliczenie objętości roztworu KBr i łacznej objętości : • Vc = VAg. NO 3 + VKBr = 30 cm 3 + 38, 25 cm 3 = 68, 25 cm 3, ü obliczenie [Ag+]w roztworze i p. Ag oraz p. B: • p. Ag = - log [Ag+] = - log 9, 89 ∙ 10 -3 = 2 • p. Br = - log KSO – p. Ag = - log 5, 35 ∙ 10 -12 – 2 = 11, 27 – 2 = 9, 27

Kompleksometria – miareczkowanie EDTA v Odczynnikiem miareczkowania jest wersanian dwusodowy – EDTA (sól kwasu etylenodiaminotetraoctowego). HOOC – CH 2 - COONa / N – CH 2 – N / Na. OOC – CH 2 – COOH Ø EDTA w roztworze wodnym z wieloma kationami metali tworzy kompleksy chelatowe (kleszczowe) dobrze rozpuszczalne w wodzie,

Kompleksometria – miareczkowanie EDTA Ø EDTA reaguje zawsze w stosunku molowym 1 : 1 bez względu na ładunek dodatni na kationie, Ø trwałość kompleksu zależy w znacznym od p. H roztworu, Ø punkt końcowy miareczkowania oznacza się za pomocą wskaźników kompleksowych, które przy określonym p. H tworzą z metalami połączenia kompleksowe o zabarwienie odmiennym niż barwa samego wskaźnika, Ø kompleksy wskaźników z kationami metali muszą być mniej trwałe niż kompleksy tych metali z EDTA, Ø w trakcie miareczkowania EDTA w pierwszej kolejności wiąże w kompleksy wolne kationy metali, a następnie kationy związane w kompleks ze wskaźnikiem, roztwór zmienia barwę charakterystyczną dla soli sodowej wskaźnika,

Kompleksometria – miareczkowanie EDTA Ø ü ü ü Ø podstawowymi wskaźnikami komplksometrycznymi są: czerń eriochromowa T, muresksyd, fiolet pirokatechinowy kationy wybranych metali można oznaczyć metodą kompleksometryczną dobierając: ü właściwe p. H roztworu, ü wskaźniki ü wiążące w trwałe związki / kompleksy (cyjankowe, fluorkowe, fosforanowe) kationy innych metali będących zanieczyszczeniami w analicie, Ø metody kompleksometryczne mogą być zastosowanie do oznaczenia również anionów, np. . : CO 32 -, SO 42 -, C 2 O 42 -.

Kompleksometria – miareczkowanie EDTA v Reakcja kompleksowania w roztworze: Ø Me + L ↔ Me. L ü Me – kation metalu, L – ligand, Me. L – utworzony kompleks, Ø miara trwałości kompleksu jest jego stała trwałości β wyrażona równaniem: iloraz stężenia molowego kompleksu i iloczynu stężeń molowych kationu i ligandu Ø jeżeli kompleks jest wystarczający trwały (β = 107 ÷ 1010), to położenie punktu na krzywej miareczkowania przed osiągnieciem PR oblicza się z wyrażenia:

Kompleksometria – miareczkowanie EDTA Ø w punkcie PR występuje tylko związek kompleksowy i jony pochodzące z jego dysocjacji stąd [Me] = [L], w związku z tym po podstawieniu do równania (poniżej / lewa strona) i po przekształceniu stężenie molowe Me można obliczyć z wyrażenia (poniżej / prawa strona): Ø w punkcie PR stężenie molowe Me. L określa wyrażenie: Ø w punkcie PR stężenie molowe Me określa wyrażenie: ü gdzie VLPR – w punkcie PR

Kompleksometria – miareczkowanie EDTA Ø po przekroczeniu punktu PR stężenia molowe ligandów, kompleksu i kationów metalu określają poniższe wyrażenia:
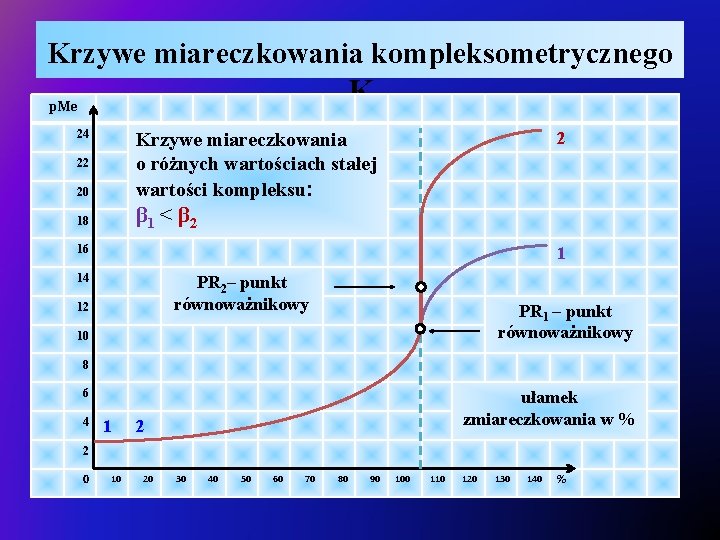
Krzywe miareczkowania kompleksometrycznego K p. Me 24 20 Krzywe miareczkowania o różnych wartościach stałej wartości kompleksu: 18 β 1 < β 2 22 2 16 1 14 PR 2– punkt równoważnikowy 12 PR 1 – punkt równoważnikowy 10 8 6 4 1 ułamek zmiareczkowania w % 2 2 0 10 20 30 40 50 60 70 80 90 100 110 120 130 140 %

Przykładowe zadania z rozwiązaniem v Metodę kompleksometrii stosuje się do oznaczania twardości wody (zawartość Ca 2+ i Mg 2+). Próbki wody miareczkuje się EDTA w obecności czerni eriochromowej T przy p. H ≈ 10, co pozwala oznaczyć ogólną zawartość wapnia i magnezu. W odrębnej próbie oznacza się wapń tym samym odczynnikiem - EDTA w obecności mureksydu przy p. H ≥ 12. v Zad. 1. Ø Oblicz zawartość wapnia i magnezu (g/dm 3), jeżeli do zmiareczkowania 25 cm 3 próbki roztworu wobec czerni eriochromowej T przy p. H = 10 zużyto 14, 5 cm 3 roztworu EDTA o stężeniu 0, 02 mol/dm 3. Na zmiareczkowanie próbki roztworu o tej samej objętości wobec mureksydu przy p. H = 12 zużyto 8, 25 cm 3 EDTA o stężeniu 0, 02 mol/dm 3.

Przykładowe zadania z rozwiązaniem Ø ü ü ü • • Zad. 1. - Rozwiązanie: Ca 2+ + L Ca. L , Mg 2+ + Mg. L, MCa = 40, 08 g/mol, MMg = 24, 31 g/mol, oznaczenie Ca wobec mureksydu przy p. H = 12: m. Ca = VEDTA ∙ Cm. EDTA ∙ MCa ∙ 1000 cm 3 : 25 cm 3 = = 0, 00825 dm 3 ∙ 0, 02 mol/dm 3 ∙ 40, 08 g/mol ∙ 40 = ≈ 0, 2645 g/ dm 3, obliczenie ilości gramów magnezu: na zmiareczkowanie magnezu zużyto: ∆VEDTA = 14, 5 cm 3 – 8, 25 cm 3 = 6, 25 cm 3, m. Mg = VEDTA ∙ Cm. EDTA ∙ MMg ∙ 1000 cm 3 : 25 cm 3 = = 0, 00625 dm 3 ∙ 0, 02 mol/dm 3 ∙ 24, 31 g/mol ∙ 40 = ≈ 0, 1216 g/ dm 3.

Przykładowe zadania z rozwiązaniem /cd. v W kompleksometrii można zastosować odwrotną metodę, tzn. miareczkuje się nadmiarem roztworu EDTA, a jego nadmiareczkuje się mianowanym roztworem Mg. SO 4. v Zad. 2. Ø Próbkę Cu. Cl 2 wprowadzono do 50 cm 3 roztworu EDTA o stężeniu 0, 015 mol/dm 3, jego nadmiar zmiareczkowano 14, 5 cm 3 roztworu Mg. SO 4 o stężeniu 0, 01 mol/dm 3. Oblicz masę próbki Cu. Cl 2 w analicie. Ø ü ü ü Rozwiązanie: MCu. Cl 2 = 134, 45 g/mol NEDTA = VEDTA ∙ Cm. EDTA = 50 cm 3 ∙ 0, 015 mmol/cm 3 = 0, 75 mmol, NMg. SO 4 = VMg. SO 4 ∙ Cm. Mg. SO 4 = 14, 5 cm 3 ∙ 0, 01 mmol/cm 3 = = 0, 145 mmol, ü m. Cu. Cl 2 = (VEDTA – VEDTA/Mg) ∙ MCu. Cl 2, ü m. Cu. Cl 2 = (0, 75 mmol – 0, 145 mmol) ∙ 0, 13445 g/mmol ≈ 0, 0813 g

Przykładowe zadania z rozwiązaniem /cd. v Zad. 3. Ø Próbkę stopu miedzi i cynku o masie 0, 5 g roztworzono w przemianach chemicznych. Po rozdzieleniu roztworu soli cynkowej od miedzi, zmiareczkowano go zużywając 32 cm 3 roztworu EDTA o stężeniu 0, 05 mol/dm 3. Oblicz procentowy udział cynku w stopie. Ø Rozwiązanie: ü MZn = 65, 37 g/mol = 0, 06537 g/mmol, ü m. Zn = VEDTA ∙ Cm. EDTA ∙ MZn , ü m. Zn= 32 cm 3 ∙ 0, 05 mmol/cm 3 ∙ 0, 06537 g/mmol ≈ 0, 105 g,
- Slides: 25















































