Universidade Estadual de Campinas Faculdade de Cincias Mdicas



































- Slides: 51

Universidade Estadual de Campinas Faculdade de Ciências Médicas Departamento de Farmacologia Estudo de Bioequivalência de duas formulações de pantoprazol em voluntários sadios de ambos os sexos Aluna: Maria Carla Petrellis Orientador: Prof. Dr. Gilberto De Nucci 2004

Bioequivalência - Considerações Adoção de uma política de medicamentos genéricos • Produção • Garantia de Qualidade • Prescrição • Dispensação e uso É parte fundamental das diretrizes para promoção do uso racional de medicamentos em nosso País

Medicamento Genérico: na concepção da OMS, “ produto farmacêutico intercambiável” • deve apresentar a mesma segurança e eficácia do medicamento de referência • produzido após a expiração da proteção patentária ou outros direitos de exclusividade pela DCI (Denominação Comun Internacional), ou seja não apresenta marca

Medicamentos Bioequivalentes (F. D. A): São equivalentes farmacêuticos ou alternativas farmacêuticas que , ao serem administrados: • na mesma dose molar, • a mesma indicação terapêutica • nas mesmas condições experimentais, (mesma via de administração) Não apresentam diferenças estatísticas significantes quanto: • à velocidade de absorção • à extensão de absorção

Parâmetros para determinar a Bioequivalência • ASC (0 -t) = Área sob a curva de concentração sangüínea vs tempo • Cmax = Pico de concentração plasmática do fármaco • t(max) = Tempo para atingir o pico da concentração máxima

Validação de Métodos Bioanalíticos A etapa crítica no Estudo de Bioequivalência é o desenvolvimento e validação de ensaios bioanalíticos Consiste na realização de experimentos Encontrar condições necessárias para a quantificação do analito em questão

Metodologias • Cromatografia Líquida de Alta Eficiência (CLAE, LC-MS/MS) • Cromatografia Gasosa (CG, CG-MS/MS) • Métodos Imunológicos (RIA, EMIT e ELISA)

Parâmetros da Validação Bioanalítica Especificidade - Seletividade Especificidade: o método produz uma única resposta analítica para um único analito Seletividade: a habilidade de uma técnica analítica em distinguir e quantificar, ou não, uma droga em relação a outras resposta de diferentes componentes presentes nos fluidos biológicos

Linearidade* Habilidade de se obter resultados diretamente proporcionais à concentração do analito na amostra Fatores na avaliação de curva de calibração: • Precisão e exatidão menor ou igual a 15% nas determinações nominais da curva de calibração, exceto para as concentrações do LOQ • Precisão e exatidão menor ou igual a 20% nas determinações nominais do LOQ * International Conference of Harmonization - ICH, Guideline for Validation of Analytical Procedure Methodology, 1996; Comissionof European Communities – Comittee for Proprietary Medicinal Products 111/5626/94 final draft, 1994; Buick et al. , 1990.

• quatro das seis concentrações nominais devem estar de acordo com critérios acima mencionados, incluindo os pontos do LOQ e os pontos de calibração de menor concentração. • Valor de coeficiente de correlação linear ou igual ou maior que 0. 95

Precisão Grau análises de concordância entre os resultados de individuais, quando o procedimento analítico é aplicado em diversas vezes em uma mesma amostra analítica, em idênticas condições experimentais. Swartz e Krull 1998; Buick et al. , 1990; Causon, R. 1997; Brittain, 1998; Relatório final da ISO (International Organization for Standardization), 1990/1991; Hartmann et al. , 1994; Shan et al. , 1992; Buick et al. , 1990; USPXX 1990; Brooks, 1985 Buick et al. , 1990

• Repetibilidade (Precisão intra-ensaio): Habilidadade de repetições da metodologia empregada nas mesmas condições laboratoriais, considerando um único dia de análise • Reprodutibilidade (Precisão inter-ensaio): Habilidade de repetições da mesma metodologia aplicada sob diferentes condições laboratoriais, em subseqüentes ocasiões que podem variar semanas ou até meses

Exatidão É definida como o grau de concordância entre os valores individuais encontrados em relação aos valores reais ou nominais • Um único dia “ Exatidão Intra-ensaio” • Dias diferentes “Exatidão Inter-ensaio” * Causon, R. 1997; Swartz e Krull 1998; Buick et al. , 1990; Brittain, 1998 e Mehta, 1989.

Limite de Quantificação (LQ) Representa a mais baixa concentração de um composto de investigação que atende os requisitos para precisão e exatidão do ensaio analítico

Recuperação A recuperação avalia a eficiência da extração e sua variabilidade. Embora recuperações próximas de 100% sejam desejáveis, baixas recuperações podem ser utilizadas (50 -60%) se forem precisas, exatas e reprodutíveis. Estabilidade Deve ser considerada durante a fase do desenvolvimento analítico

Critérios de Aceitabilidade • Precisão: Os CV% do inter-day para os QCs é 15%, e 20% para o LOQ QC, avaliados em um mínimo de 3 lotes. • Exatidão: A média dos valores do inter-day devem ser menores que 15% do valor nominal dos QCs, e não desviar mais que 20% para LOQ QC. • Sensibilidade: O menor ponto da curva de calibração aceitável como limite de quantificação (LOQ) do método é aquele com CV% 20% (interday).

Pantoprazol POTENTE INIBIDOR DE LONGA DURAÇÃO DA BOMBA ÁCIDA DA SUPERFÍCIE DAS CÉLULAS PARIETAIS GÁSTRICAS

Objetivos

• Avaliar a bioequivalência de duas formulações de pantoprazol baseada na comparação dos valores obtidos parâmetros farmacocinéticos de cada formulação calculados a partir de medida das concentrações plasmáticas de pantoprazol • Validar a metodologia analítica por LC-MS/MS empregada na quantificação das concentrações de pantoprazol em amostras de plasma humano

Protocolo do Estudo

Seleção dos Voluntários • Vinte e dois voluntários sadios de ambos os sexos • Idade entre 18 e 45 anos (média= 30 ± 1 ano) • Peso Corporal entre 55 e 100 kg (média 77, 5 ± 10, 1 kg) • Entrevista e exames clínicos pré-estudo • Assinatura do Termo de Consentimento Livre Esclarecido do estudo • Protocolo Clínico Aprovado pela Comissão de Ética da Faculdade de Ciências Médicas da Universidade Federal do Ceará

Protocolo Clínico • Delineamento aleatório cruzado, aberto de dois períodos, com intervalos de 15 dias entre as doses de pantoprazol • Hospitalização por 24 horas na Unidade de Farmacologia Clínica • Internação seguida de dieta padrão até 23: 00 hs • Jejum após 23: 00 hs, e início do estudo clínico às dose única por via oral de 40 mg de pantoprazol • Dieta padrão às 12: 00 e às 18: 00 hs • Restrições: alimentos contendo xantinas 7: 00 hs,

Coleta das amostras • Amostras de sangue foram coletadas através de escalpe em veia superficial do antebraço do voluntário • Os intervalos de coleta: antes (zero), 0. 25, 0. 5, 0. 75, 1. 0, 1. 25, 1. 5, 2. 0, 2. 5, 3. 0, 5. 0, 6. 0, 8. 0 e 12. 0 horas • As amostras foram centrifugadas durante 10 minutos a 4000 rpm • Obtenção do soro e armazenamento na temperatura de - 20°C

Protocolo Analítico • Princípio do Método: Cromatografia Líquida de Alta Eficiência de fasereversa , acoplada a espectrometria de massa (LCMS/MS) Extração Líquido-Líquido com emprego de dietileter: diclorometano (70: 30 v/v) como solvente extrator

PREPARO DAS SOLUÇÕES PADRÕES Pantoprazol • Solução estoque de Pantoprazol (1. 0 mg/m. L) em metanol: água (50: 50) • Concentração final de 10 g/m. L Carbamazepina (P. I) • Solução estoque de carbamazepina (1. 0 mg/m. L) em metanol: água (50: 50) • concentrações finais de 100 g/m. L e 1 g/m. L

PREPARO DA CURVA DE CALIBRAÇÃO E AMOSTRAS DE CONTROLE DE QUALIDADE (C. Q) Curva de calibração • contaminação de plasma humano controle • emprego da solução padrão de pantoprazol (10 g/m. L) • obtenção dos seguintes pontos da curva de calibração: Branco, Branco + PI, 35, 50, 70, 100, 200, 500 e 1000 ng/m. L

Controle de qualidade: • contaminação de plasma humano controle • • emprego da solução padrão de pantoprazol (10 g m. L) obtenção dos seguintes níveis de concentração: CQA – 120 ng/m. L CQB – 800 ng/m. L CQC – 600 ng/m. L (fator de diluição 1: 5) • temperatura de armazenamento - 20 °C

EXTRAÇÃO DE AMOSTRAS • 0. 5 m. L de amostras de plasma: voluntários, pontos de da curva de calibração, controle de qualidade em tubos de ensaio • 0. 05 m. L de carbamazepina (1 g/m. L) • breve agitação, repouso por 5 minutos • 4 m. L de dietileter-diclorometano (70: 30), em seguida vigorosa agitação por 30 segundos, seguido centrifugação

• obtenção da fase orgânica e transferência para tubos de ensaio revestidos de silicone • evaporação em banho- maria (37°C) sob fluxo constante de nitrogênio • reconstituição das amostras analíticas com 200 L de fase móvel, em seguida breve agitação • acondicionamento das amostras analíticas em vials do injetor automático para posterior análise

CONDIÇÕES CROMATOGRÁFICAS E ESPECTROMETRIA DE MASSA Sistema de Cromatografia: • Cromatografia Líquida Alta Eficiência de fase - reversa • Bomba binária Column Chromatography: • Coluna analítica de fase-reversa : Genesis 4 m C 8; 150 x 4. 6 mm diâmetro interno na temperatura de 40 °C Fase Móvel: 80% Acetonitrila – 0. 1% ácido trifluoroacético(TFA) – 20% Água Deionizada Fluxo constante: 0. 9 m. L/min por gradiente isocrático

Eluente: 100 L/min analisado no detector MS/MS Injetor Automático: alíquotas de 40 L/min na temperatura 10 °C Tempo de Eluição: 4 minutos Tempo de Retenção: Pantoprazol (1. 86 min) e Carbamazepina (2. 2 min) Detector: O Espectrômetro de massa do tipo Quatro II equipado com “ atmospheric pressure ionization (API) electrspray” , operando de modo positivo (MS+) • Pantoprazol : 366. 1 > 91. 50 , 50 V e 35 e. V • Carbamazepina: 236. 89 > 194. 09 , 25 V e 15 e. V

Resultados

Validação Analítica

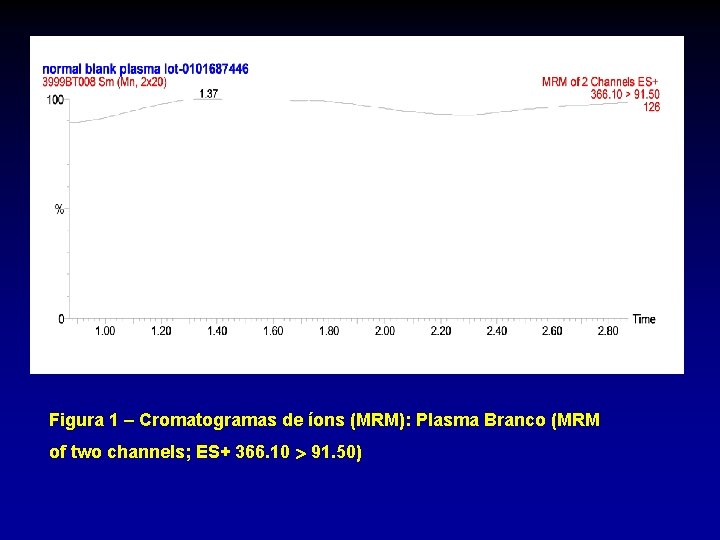
Figura 1 – Cromatogramas de íons (MRM): Plasma Branco (MRM of two channels; ES+ 366. 10 91. 50)

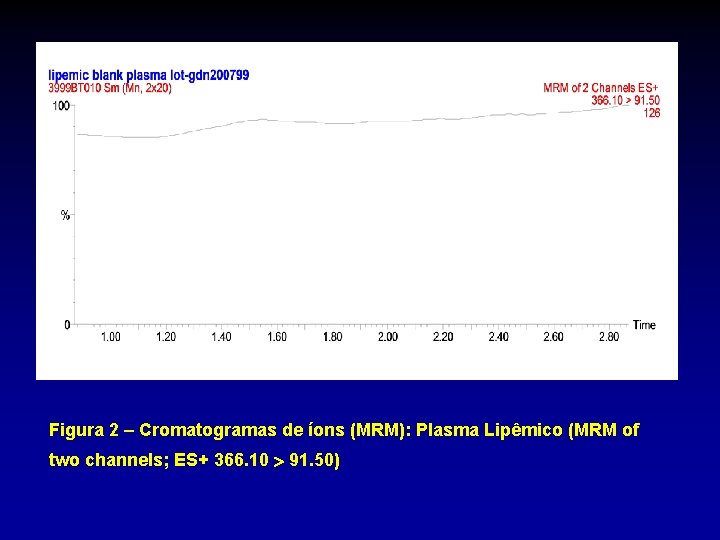
Figura 2 – Cromatogramas de íons (MRM): Plasma Lipêmico (MRM of two channels; ES+ 366. 10 91. 50)

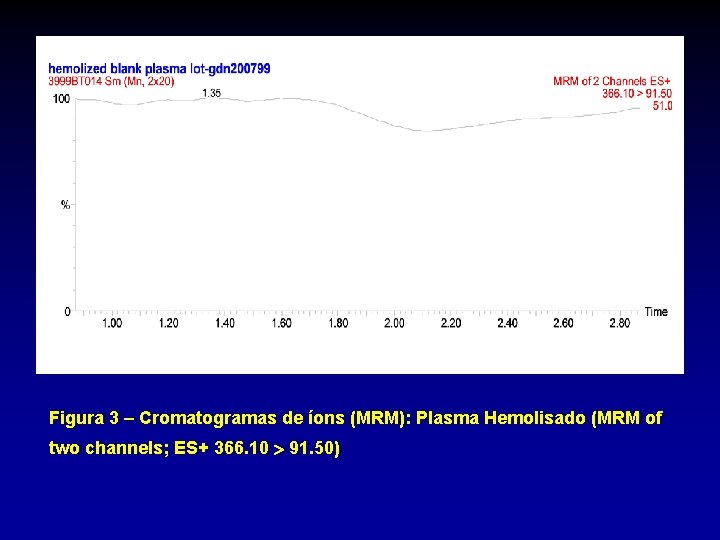
Figura 3 – Cromatogramas de íons (MRM): Plasma Hemolisado (MRM of two channels; ES+ 366. 10 91. 50)

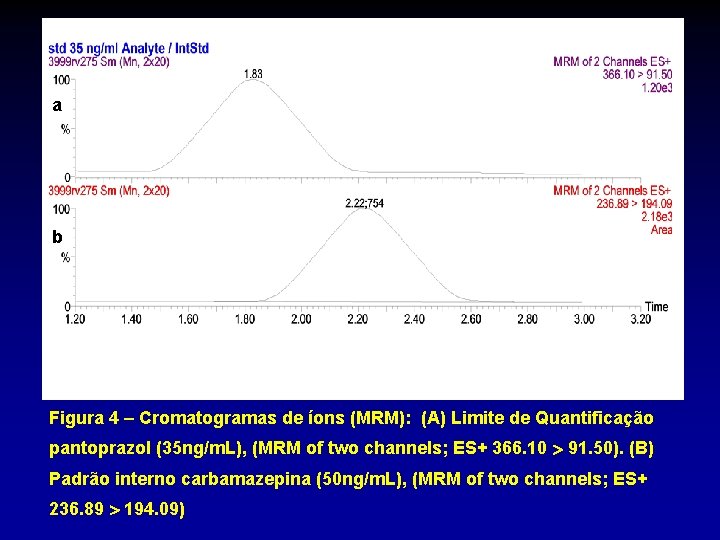
a b Figura 4 – Cromatogramas de íons (MRM): (A) Limite de Quantificação pantoprazol (35 ng/m. L), (MRM of two channels; ES+ 366. 10 91. 50). (B) Padrão interno carbamazepina (50 ng/m. L), (MRM of two channels; ES+ 236. 89 194. 09)

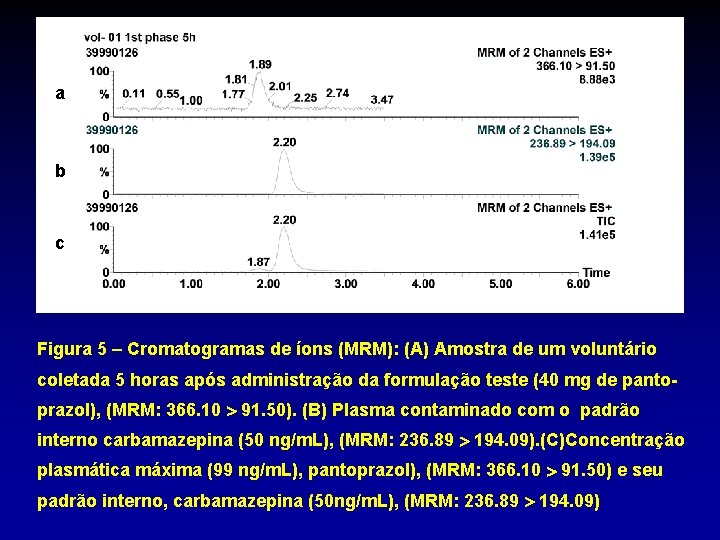
a b c Figura 5 – Cromatogramas de íons (MRM): (A) Amostra de um voluntário coletada 5 horas após administração da formulação teste (40 mg de pantoprazol), (MRM: 366. 10 91. 50). (B) Plasma contaminado com o padrão interno carbamazepina (50 ng/m. L), (MRM: 236. 89 194. 09). (C)Concentração plasmática máxima (99 ng/m. L), pantoprazol), (MRM: 366. 10 91. 50) e seu padrão interno, carbamazepina (50 ng/m. L), (MRM: 236. 89 194. 09)

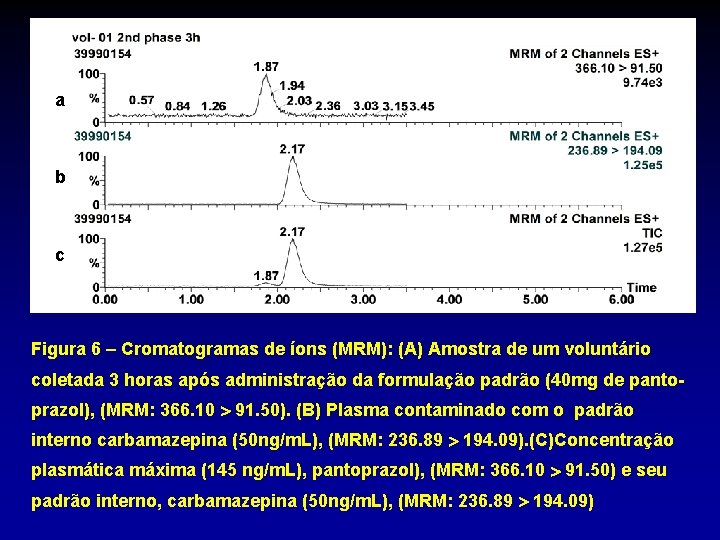
a b c Figura 6 – Cromatogramas de íons (MRM): (A) Amostra de um voluntário coletada 3 horas após administração da formulação padrão (40 mg de pantoprazol), (MRM: 366. 10 91. 50). (B) Plasma contaminado com o padrão interno carbamazepina (50 ng/m. L), (MRM: 236. 89 194. 09). (C)Concentração plasmática máxima (145 ng/m. L), pantoprazol), (MRM: 366. 10 91. 50) e seu padrão interno, carbamazepina (50 ng/m. L), (MRM: 236. 89 194. 09)

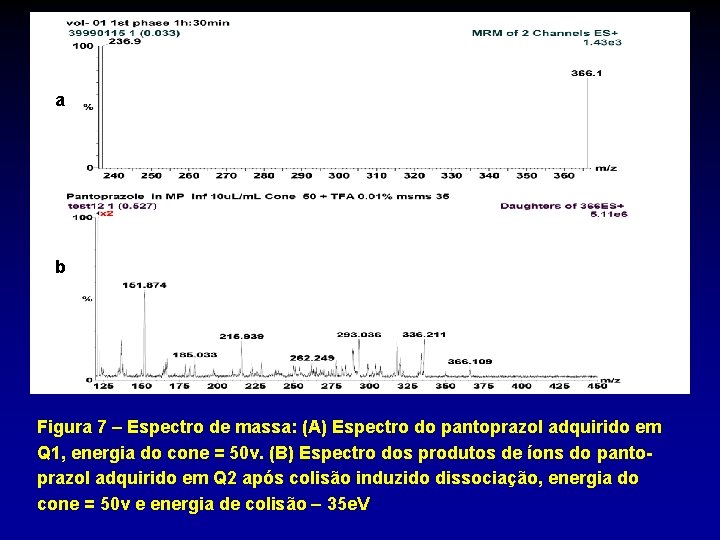
a b Figura 7 – Espectro de massa: (A) Espectro do pantoprazol adquirido em Q 1, energia do cone = 50 v. (B) Espectro dos produtos de íons do pantoprazol adquirido em Q 2 após colisão induzido dissociação, energia do cone = 50 v e energia de colisão – 35 e. V

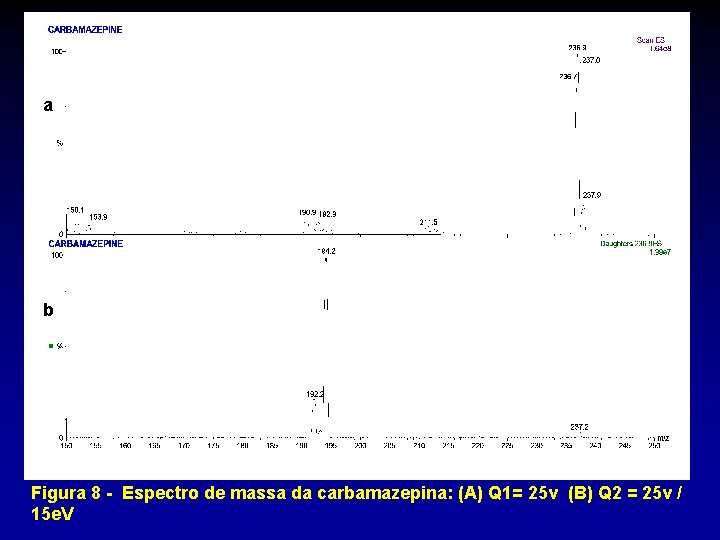
a b Figura 8 - Espectro de massa da carbamazepina: (A) Q 1= 25 v (B) Q 2 = 25 v / 15 e. V

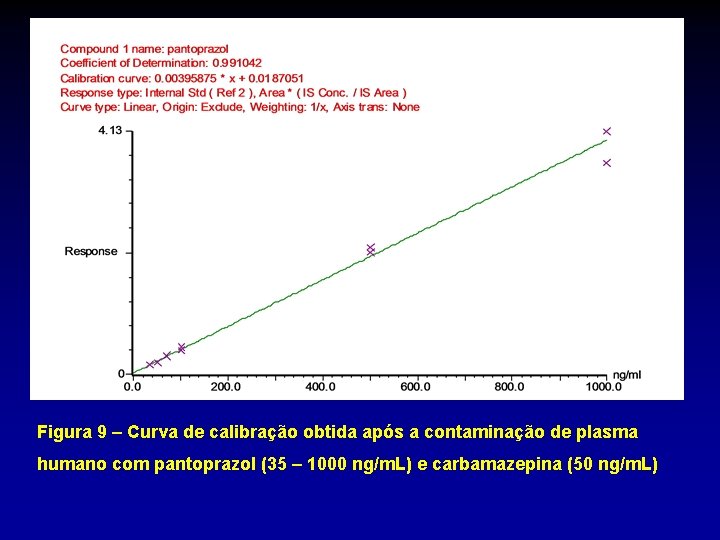
Figura 9 – Curva de calibração obtida após a contaminação de plasma humano com pantoprazol (35 – 1000 ng/m. L) e carbamazepina (50 ng/m. L)

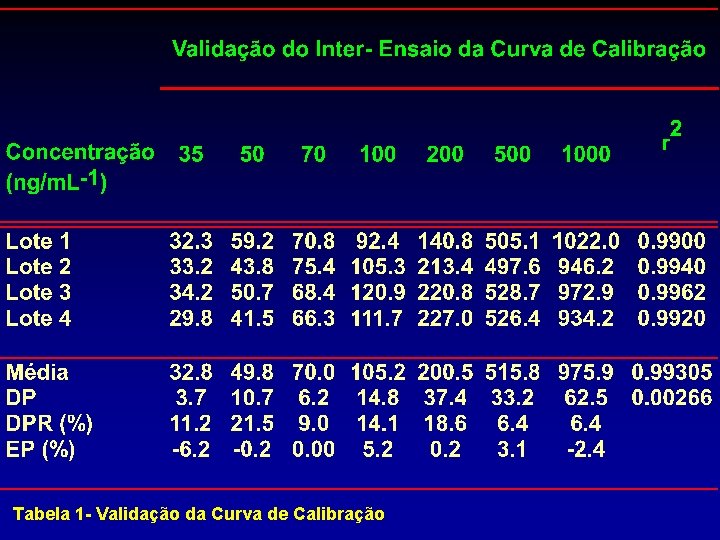
Tabela 1 - Validação da Curva de Calibração

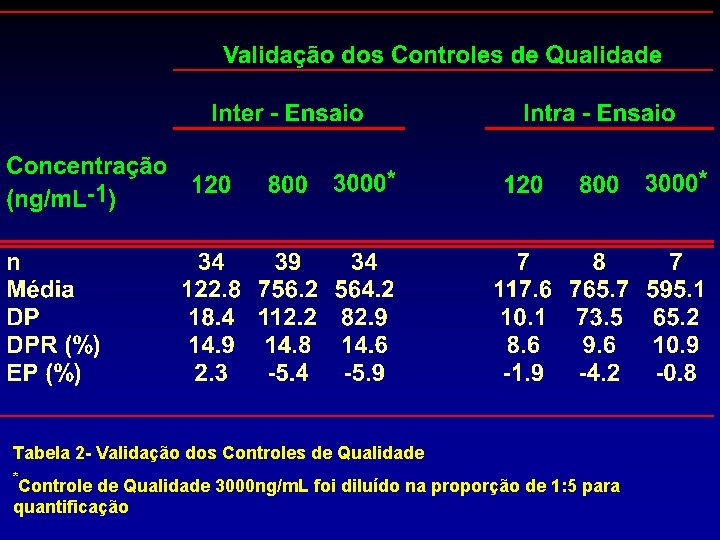
Tabela 2 - Validação dos Controles de Qualidade * Controle de Qualidade 3000 ng/m. L foi diluído na proporção de 1: 5 para quantificação

Parâmetros Farmacocinéticos

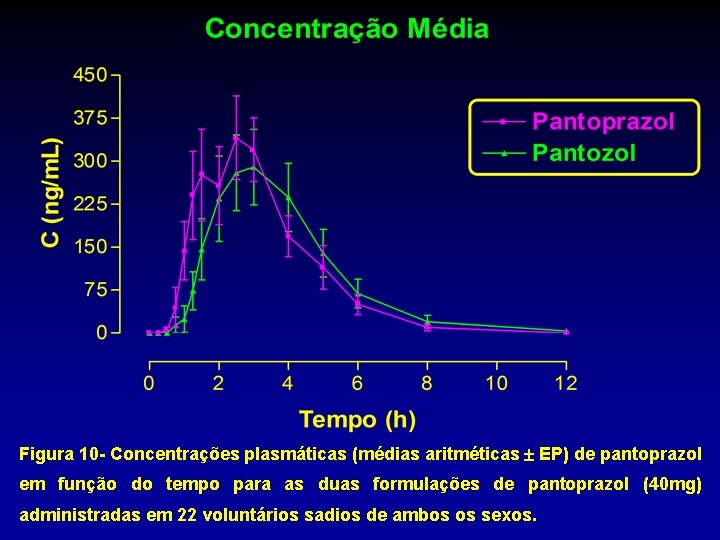
Figura 10 - Concentrações plasmáticas (médias aritméticas EP) de pantoprazol em função do tempo para as duas formulações de pantoprazol (40 mg) administradas em 22 voluntários sadios de ambos os sexos.


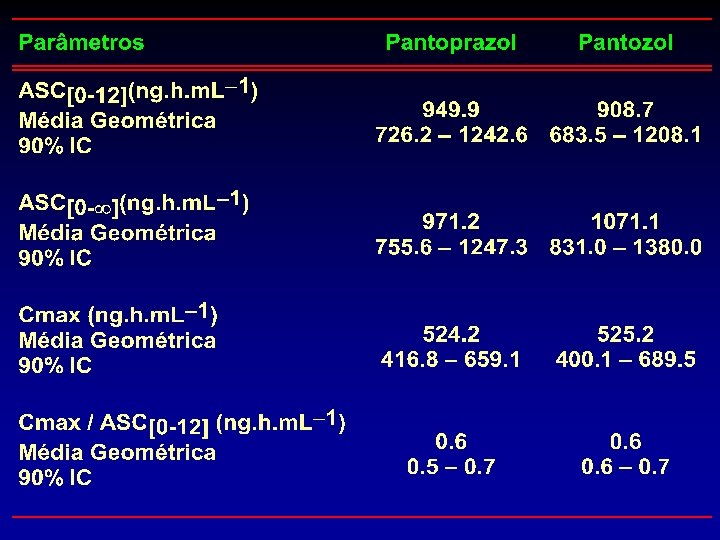
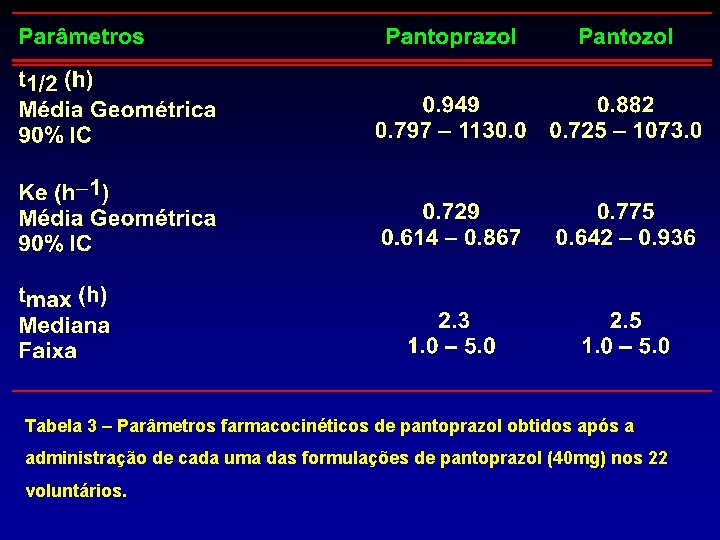
Tabela 3 – Parâmetros farmacocinéticos de pantoprazol obtidos após a administração de cada uma das formulações de pantoprazol (40 mg) nos 22 voluntários.


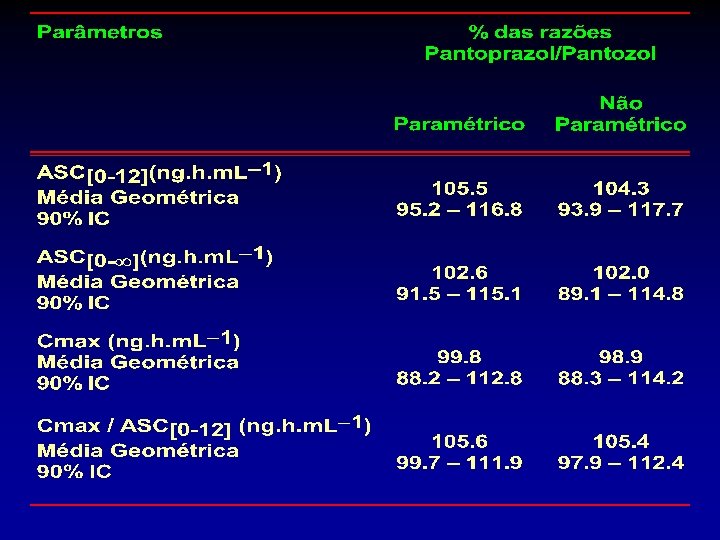
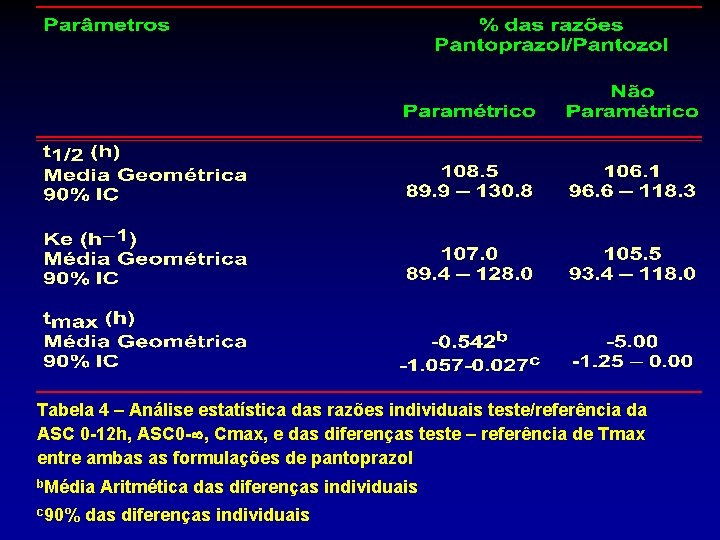
Tabela 4 – Análise estatística das razões individuais teste/referência da ASC 0 -12 h, ASC 0 - , Cmax, e das diferenças teste – referência de Tmax entre ambas as formulações de pantoprazol b. Média c 90% Aritmética das diferenças individuais

Conclusão