Reazioni degli alcheni Addizione elettrofila Prof O Taglialatela






- Slides: 40

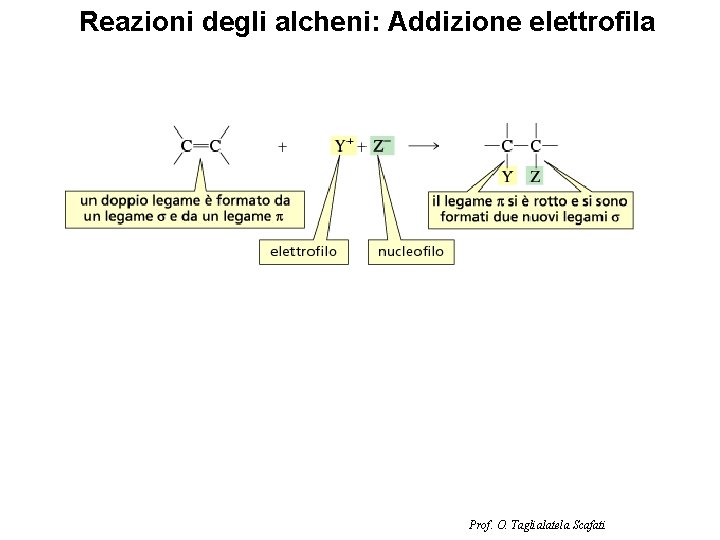
Reazioni degli alcheni: Addizione elettrofila Prof. O. Taglialatela Scafati

Addizione HX ed idratazione OH H 2 O/HNO 3 Osservazioni sperimentali: 1) Se i due carboni dell’alchene hanno diverso grado di sostituzione il nucleofilo va sul carbonio più sostituito (Regioselettività); 2) Se si crea 1 o più centri stereogenici, si formano uguali quantità dei due enantiomeri (miscela racemica) Prof. O. Taglialatela Scafati

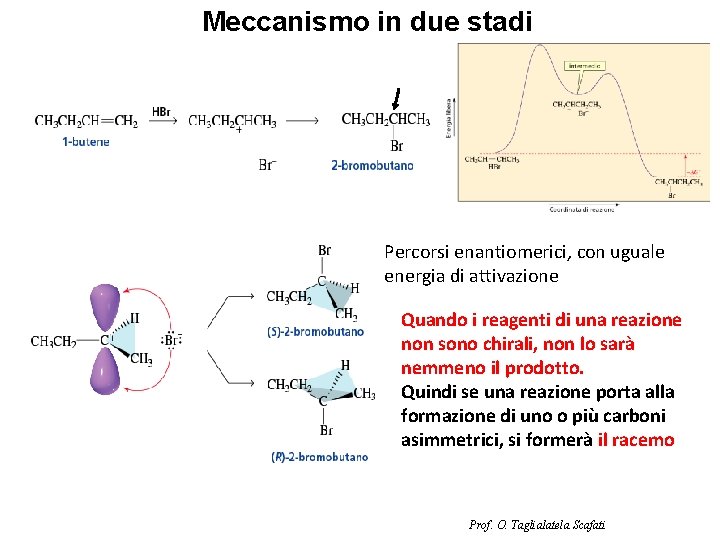
Meccanismo in due stadi Percorsi enantiomerici, con uguale energia di attivazione Quando i reagenti di una reazione non sono chirali, non lo sarà nemmeno il prodotto. Quindi se una reazione porta alla formazione di uno o più carboni asimmetrici, si formerà il racemo Prof. O. Taglialatela Scafati

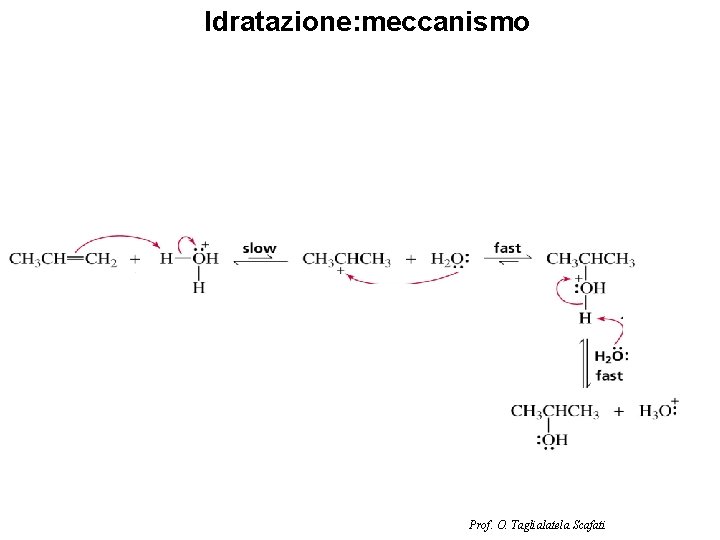
Idratazione: meccanismo Prof. O. Taglialatela Scafati

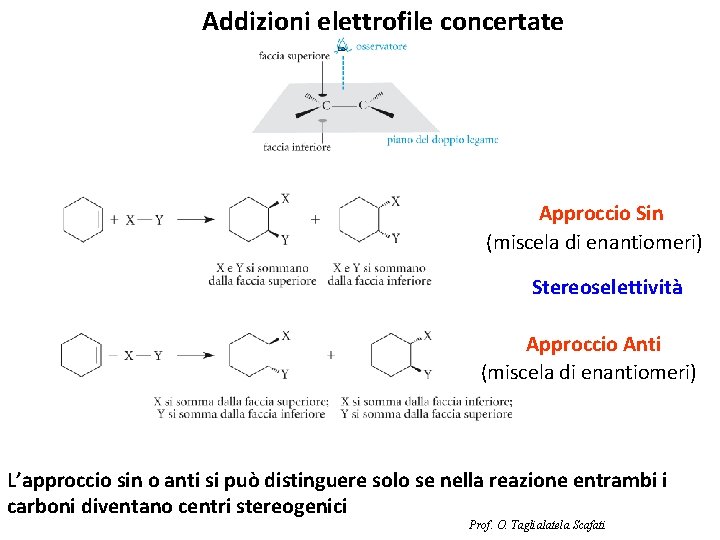
Addizioni elettrofile concertate Approccio Sin (miscela di enantiomeri) Stereoselettività Approccio Anti (miscela di enantiomeri) L’approccio sin o anti si può distinguere solo se nella reazione entrambi i carboni diventano centri stereogenici Prof. O. Taglialatela Scafati

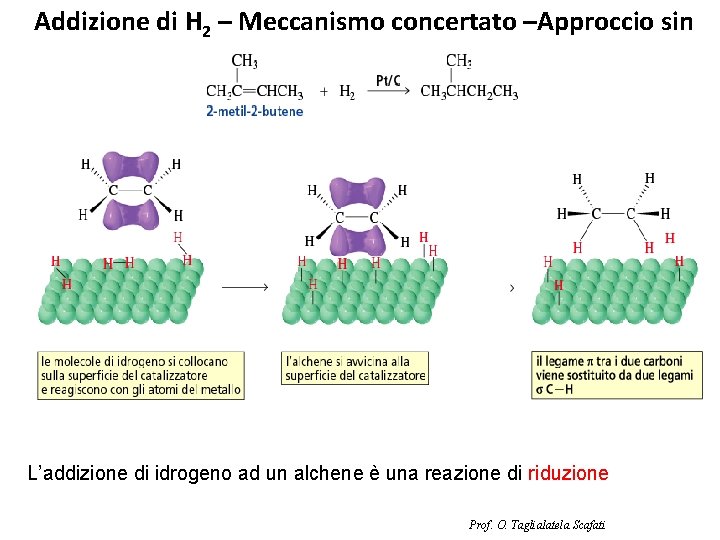
Addizione di H 2 – Meccanismo concertato –Approccio sin L’addizione di idrogeno ad un alchene è una reazione di riduzione Prof. O. Taglialatela Scafati

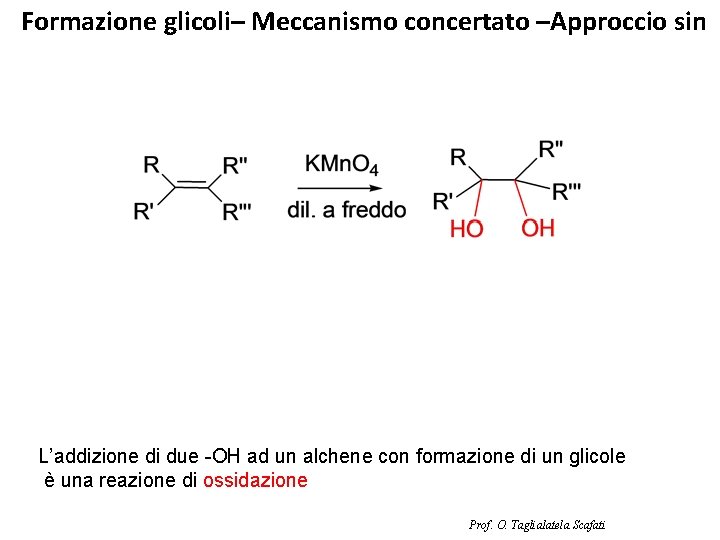
Formazione glicoli– Meccanismo concertato –Approccio sin L’addizione di due -OH ad un alchene con formazione di un glicole è una reazione di ossidazione Prof. O. Taglialatela Scafati

Reazioni di ossidoriduzione in chimica organica • Se la reazione aumenta il numero di legami C-H o diminuisce il numero di legami C-O, C-N, o C-X (dove X indica un alogeno), il composto è stato ridotto. • Se la reazione diminuisce il numero di legami C-H o aumenta il numero di legami C-O, C-N, o C-X (dove X indica un alogeno), il composto è stato ossidato. Prof. O. Taglialatela Scafati

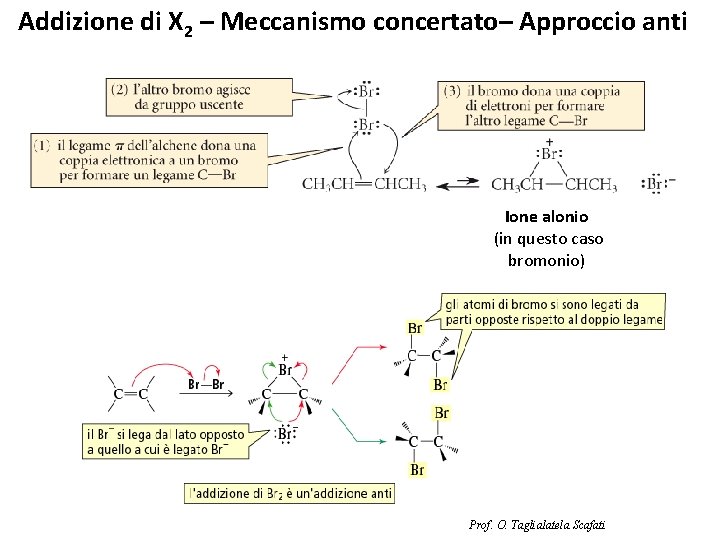
Addizione di X 2 – Meccanismo concertato– Approccio anti Ione alonio (in questo caso bromonio) Prof. O. Taglialatela Scafati

Prof. O. Taglialatela Scafati

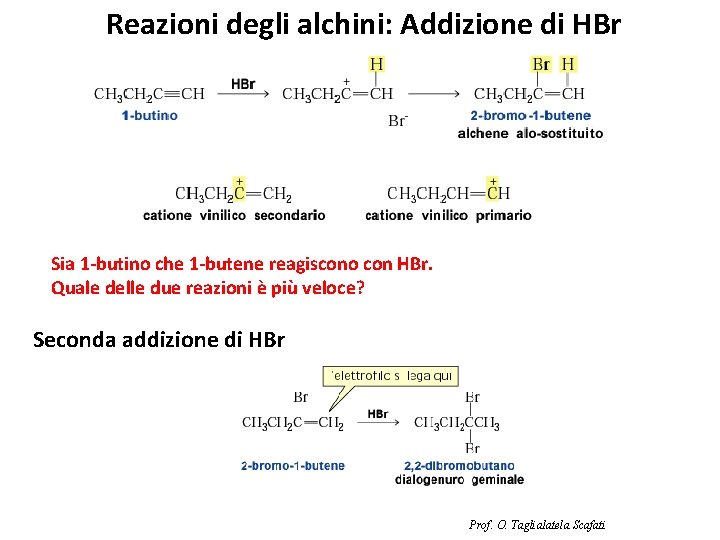
Reazioni degli alchini: Addizione di HBr Sia 1 -butino che 1 -butene reagiscono con HBr. Quale delle due reazioni è più veloce? Seconda addizione di HBr Prof. O. Taglialatela Scafati

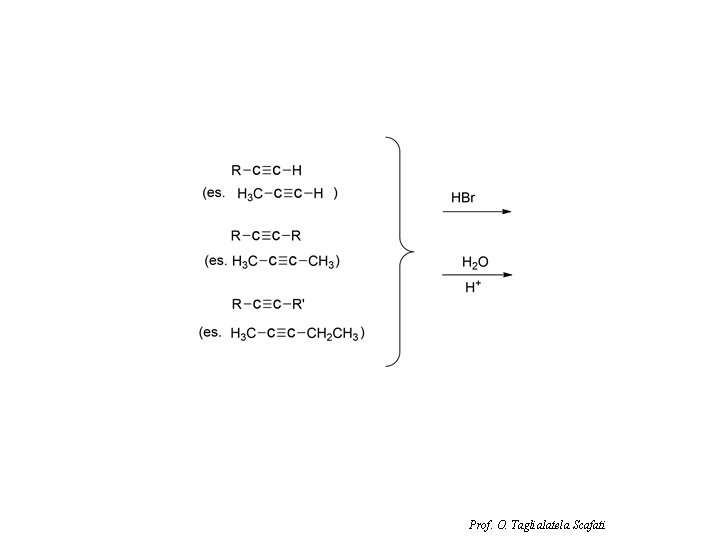
Idratazione degli alchini Hg 2+ I tautomeri sono isomeri in rapido equilibrio. I tautomeri cheto-enolici differiscono per la posizione di un doppio legame e di un idrogeno. Prof. O. Taglialatela Scafati

Prof. O. Taglialatela Scafati

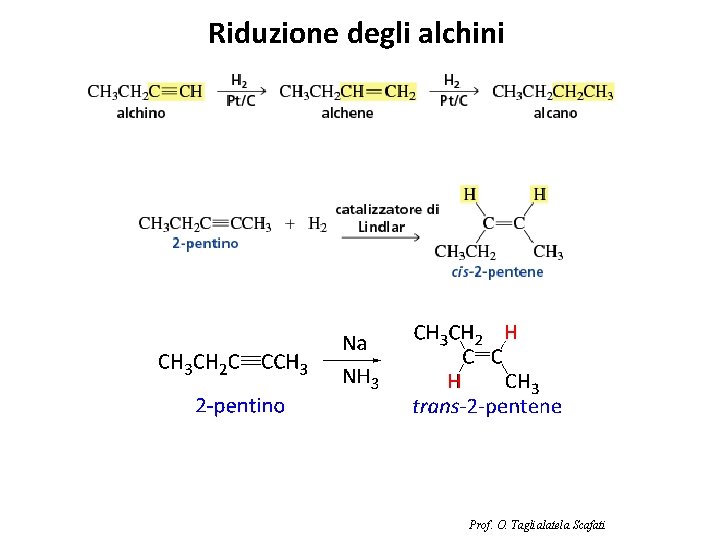
Riduzione degli alchini Prof. O. Taglialatela Scafati

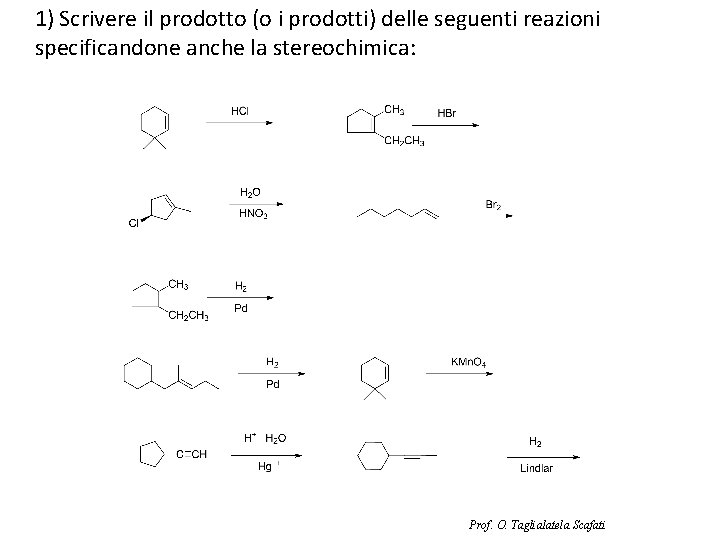
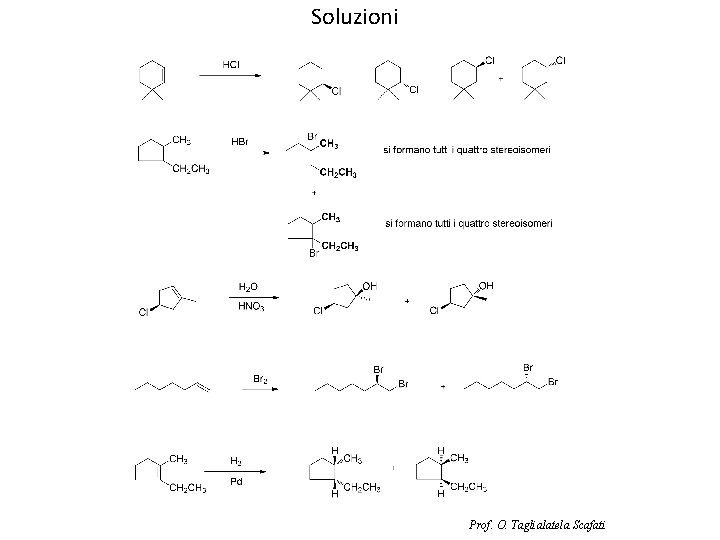
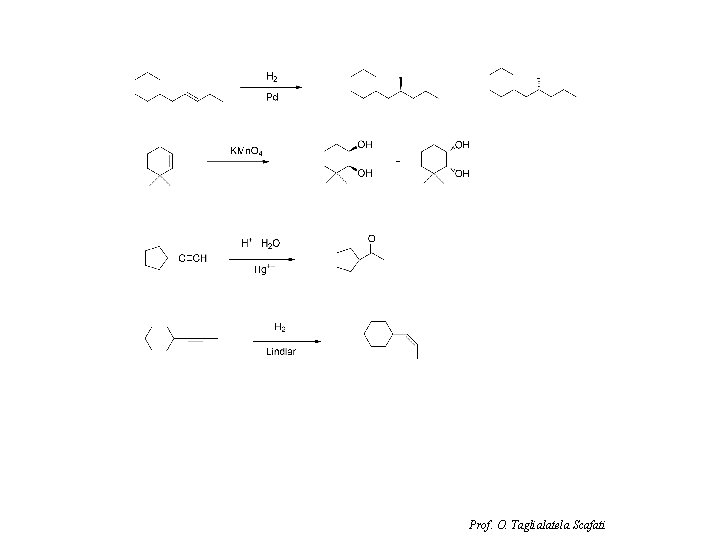
1) Scrivere il prodotto (o i prodotti) delle seguenti reazioni specificandone anche la stereochimica: Prof. O. Taglialatela Scafati

Soluzioni Prof. O. Taglialatela Scafati

Prof. O. Taglialatela Scafati

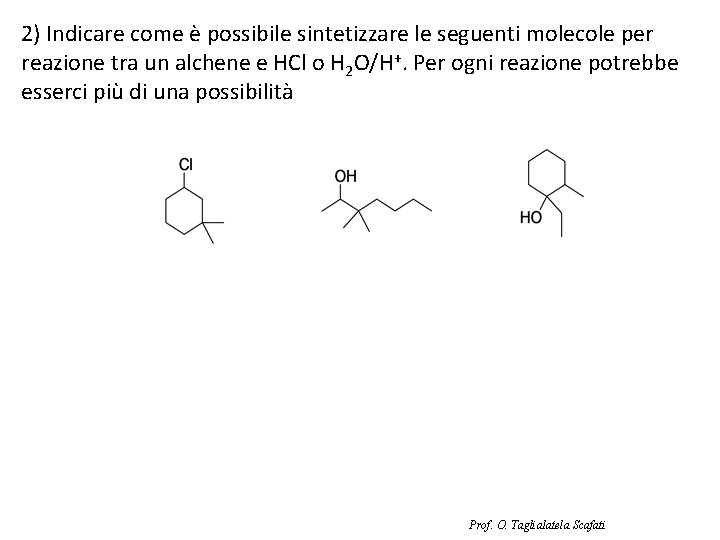
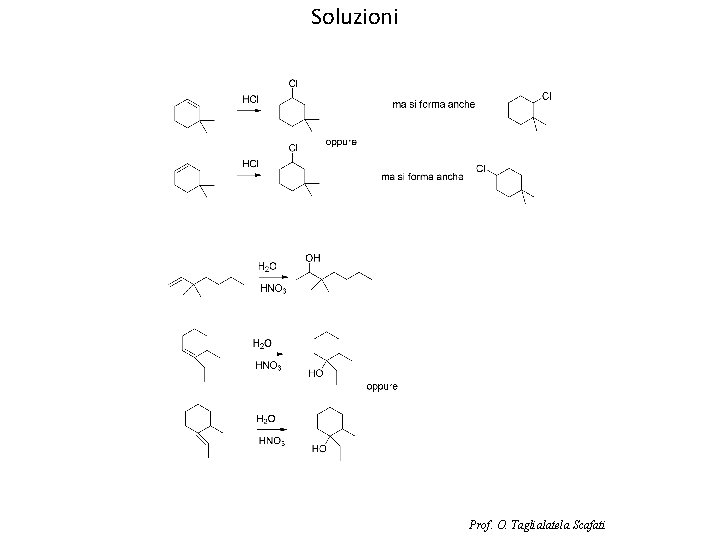
2) Indicare come è possibile sintetizzare le seguenti molecole per reazione tra un alchene e HCl o H 2 O/H+. Per ogni reazione potrebbe esserci più di una possibilità Prof. O. Taglialatela Scafati

Soluzioni Prof. O. Taglialatela Scafati

Acidità degli alchini terminali acido più forte ione ammiduro base più forte ione acetiluro base più debole acido più debole top 252 Lo ione acetiluro è un utile nucleofilo acido più debole base più forte acido più forte Prof. O. Taglialatela Scafati

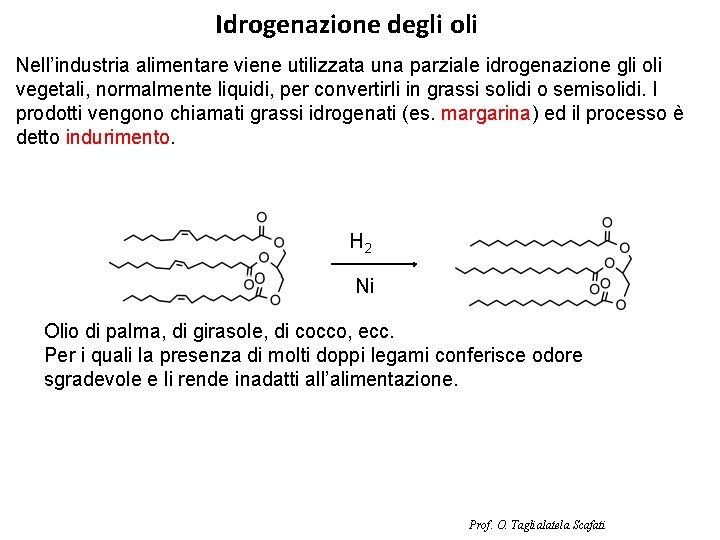
Idrogenazione degli oli Nell’industria alimentare viene utilizzata una parziale idrogenazione gli oli vegetali, normalmente liquidi, per convertirli in grassi solidi o semisolidi. I prodotti vengono chiamati grassi idrogenati (es. margarina) ed il processo è detto indurimento. H 2 Ni Olio di palma, di girasole, di cocco, ecc. Per i quali la presenza di molti doppi legami conferisce odore sgradevole e li rende inadatti all’alimentazione. Prof. O. Taglialatela Scafati

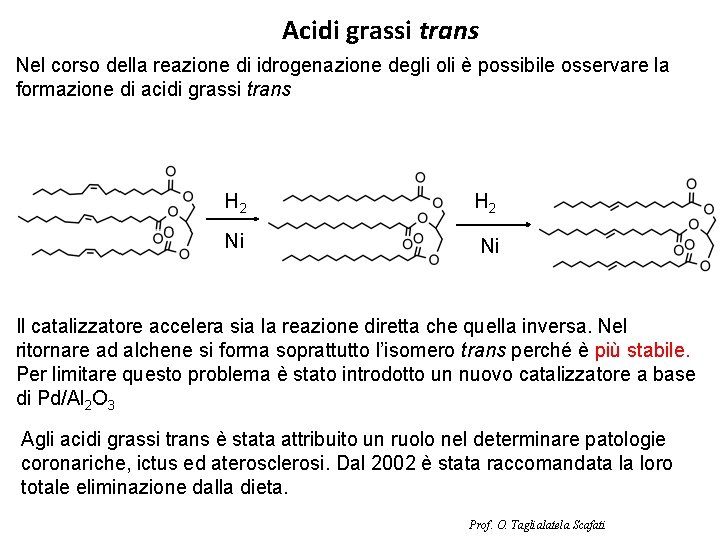
Acidi grassi trans Nel corso della reazione di idrogenazione degli oli è possibile osservare la formazione di acidi grassi trans H 2 Ni Ni Il catalizzatore accelera sia la reazione diretta che quella inversa. Nel ritornare ad alchene si forma soprattutto l’isomero trans perché è più stabile. Per limitare questo problema è stato introdotto un nuovo catalizzatore a base di Pd/Al 2 O 3 Agli acidi grassi trans è stata attribuito un ruolo nel determinare patologie coronariche, ictus ed aterosclerosi. Dal 2002 è stata raccomandata la loro totale eliminazione dalla dieta. Prof. O. Taglialatela Scafati

Ossidazione dei lipidi L’ossigeno reagisce con gli acidi grassi insaturi presenti nelle membrane cellulari e 1) danneggia le membrane alterando la funzionalità cellulare 2) produce molecole dannose per l’organismo (radicali liberi) Esistono due forme della molecola di ossigeno entrambe in grado di reagire ma con velocità e meccanismi diversi. La forma detta ossigeno tripletto (3 O 2 ) è quella presente normalmente nell’atmosfera; quando in seguito a diversi fattori, essa acquista energia può trovarsi in uno stadio a maggiore energia detto ossigeno singoletto, 1 O 2. L’ossidazione da parte di questa forma dell’ossigeno è molto più veloce ed efficace. Oleico Linolenico Ossigeno tripletto 1 27 77 Ossigeno singoletto 300000 400000 700000 L’ossigeno singoletto è centomila volte più reattivo rispetto al tripletto Prof. O. Taglialatela Scafati

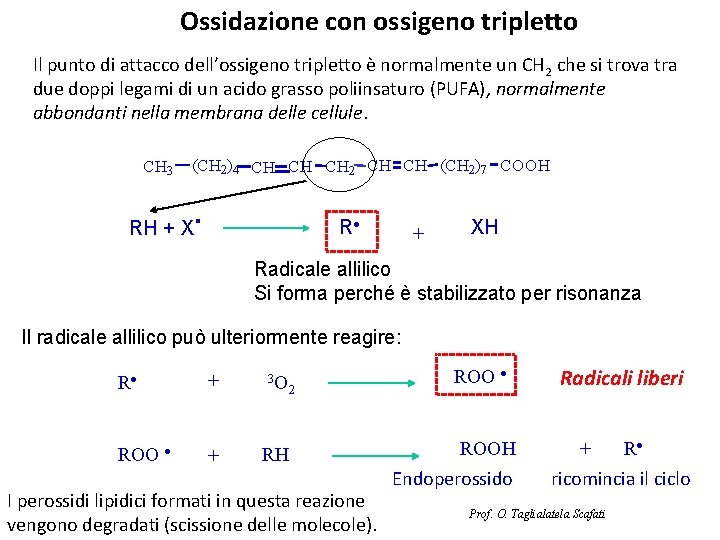
Ossidazione con ossigeno tripletto Il punto di attacco dell’ossigeno tripletto è normalmente un CH 2 che si trova tra due doppi legami di un acido grasso poliinsaturo (PUFA), normalmente abbondanti nella membrana delle cellule. CH 3 (CH 2)4 CH CH CH 2 CH CH (CH 2)7 COOH RH + X . R + XH Radicale allilico Si forma perché è stabilizzato per risonanza Il radicale allilico può ulteriormente reagire: R + 3 O ROO + RH 2 I perossidi lipidici formati in questa reazione vengono degradati (scissione delle molecole). ROOH Endoperossido Radicali liberi + R ricomincia il ciclo Prof. O. Taglialatela Scafati

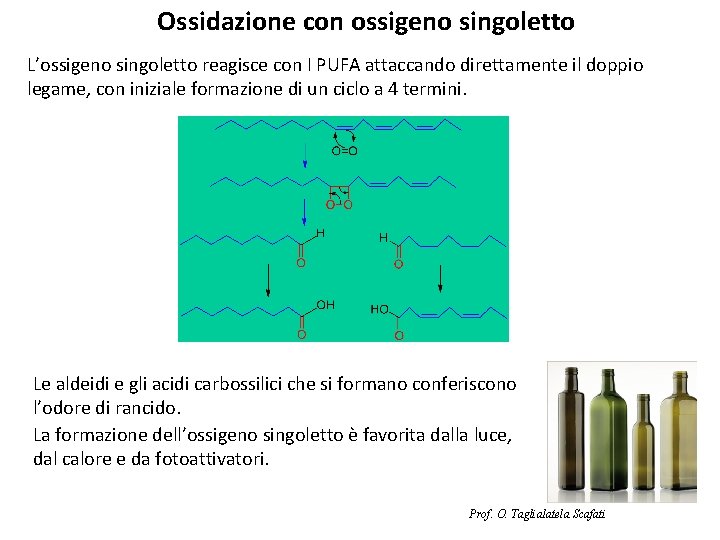
Ossidazione con ossigeno singoletto L’ossigeno singoletto reagisce con I PUFA attaccando direttamente il doppio legame, con iniziale formazione di un ciclo a 4 termini. Le aldeidi e gli acidi carbossilici che si formano conferiscono l’odore di rancido. La formazione dell’ossigeno singoletto è favorita dalla luce, dal calore e da fotoattivatori. Prof. O. Taglialatela Scafati

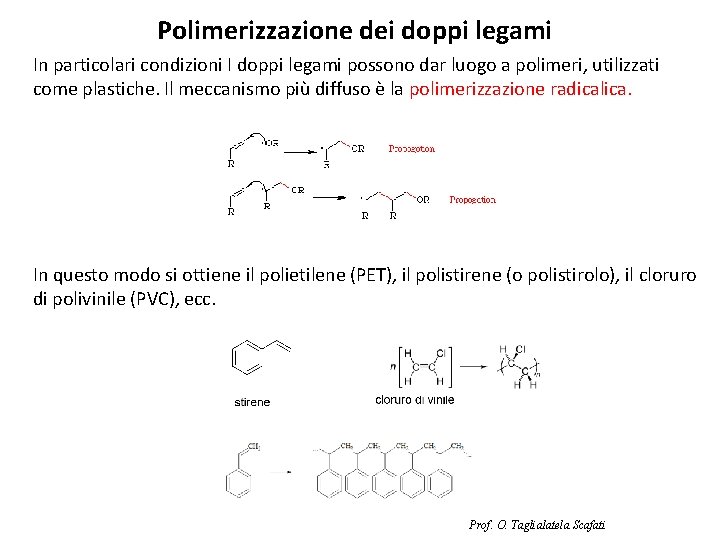
Polimerizzazione dei doppi legami In particolari condizioni I doppi legami possono dar luogo a polimeri, utilizzati come plastiche. Il meccanismo più diffuso è la polimerizzazione radicalica. In questo modo si ottiene il polietilene (PET), il polistirene (o polistirolo), il cloruro di polivinile (PVC), ecc. Prof. O. Taglialatela Scafati

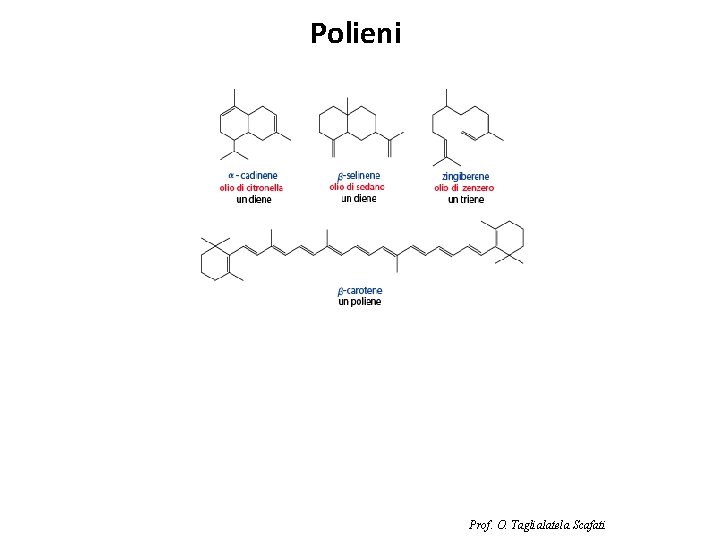
Polieni Prof. O. Taglialatela Scafati

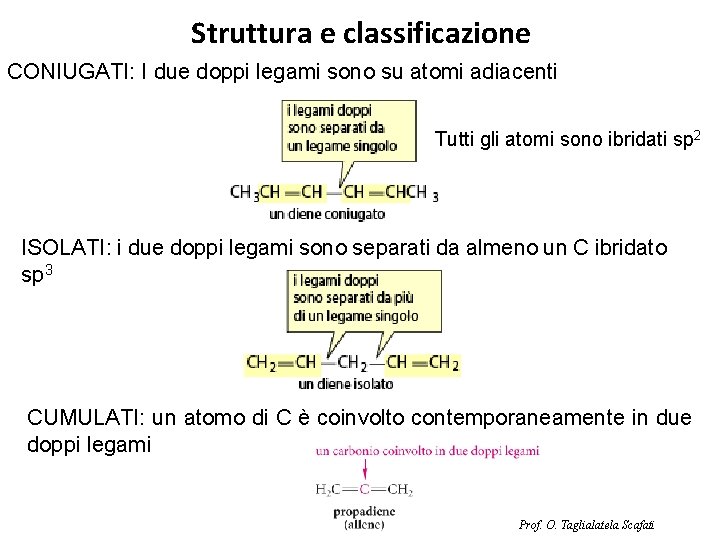
Struttura e classificazione CONIUGATI: I due doppi legami sono su atomi adiacenti Tutti gli atomi sono ibridati sp 2 ISOLATI: i due doppi legami sono separati da almeno un C ibridato sp 3 CUMULATI: un atomo di C è coinvolto contemporaneamente in due doppi legami Prof. O. Taglialatela Scafati

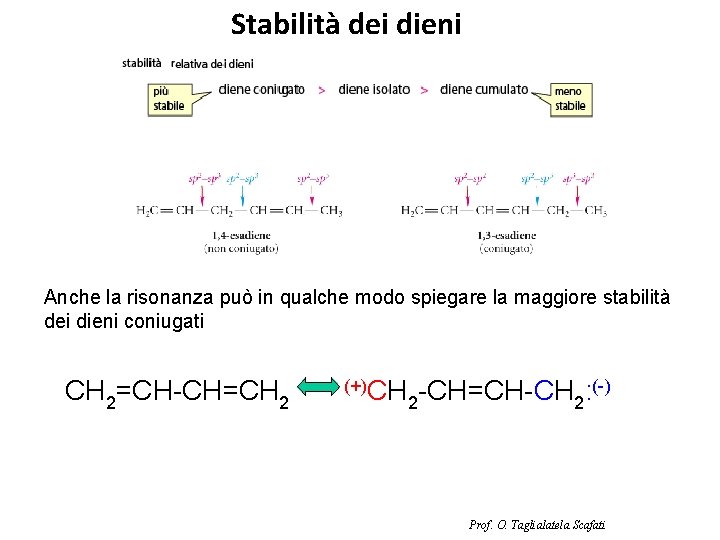
Stabilità dei dieni Anche la risonanza può in qualche modo spiegare la maggiore stabilità dei dieni coniugati CH 2=CH-CH=CH 2 (+)CH (-) -CH=CH-CH : 2 2 Prof. O. Taglialatela Scafati

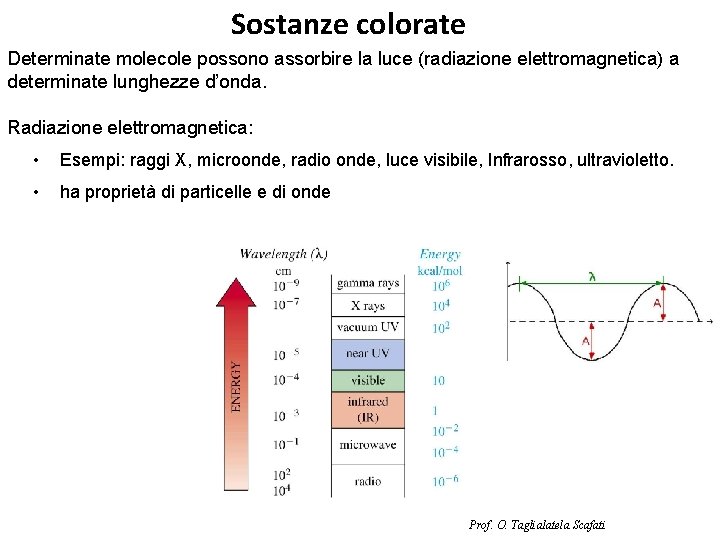
Sostanze colorate Determinate molecole possono assorbire la luce (radiazione elettromagnetica) a determinate lunghezze d’onda. Radiazione elettromagnetica: • Esempi: raggi X, microonde, radio onde, luce visibile, Infrarosso, ultravioletto. • ha proprietà di particelle e di onde Prof. O. Taglialatela Scafati

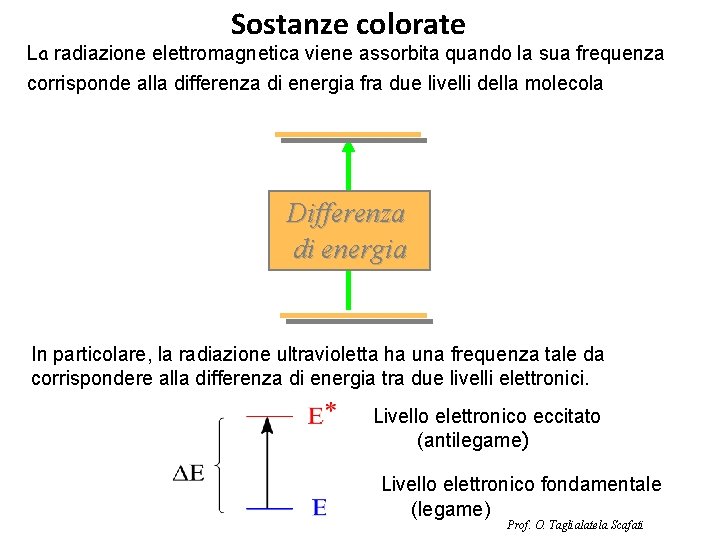
Sostanze colorate La radiazione elettromagnetica viene assorbita quando la sua frequenza corrisponde alla differenza di energia fra due livelli della molecola Differenza di energia In particolare, la radiazione ultravioletta ha una frequenza tale da corrispondere alla differenza di energia tra due livelli elettronici. Livello elettronico eccitato (antilegame) Livello elettronico fondamentale (legame) Prof. O. Taglialatela Scafati

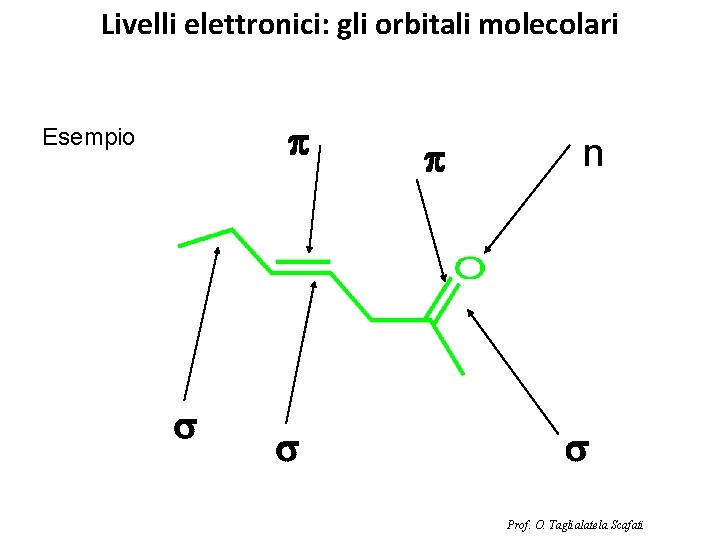
Livelli elettronici: gli orbitali molecolari p Esempio s s p n s Prof. O. Taglialatela Scafati

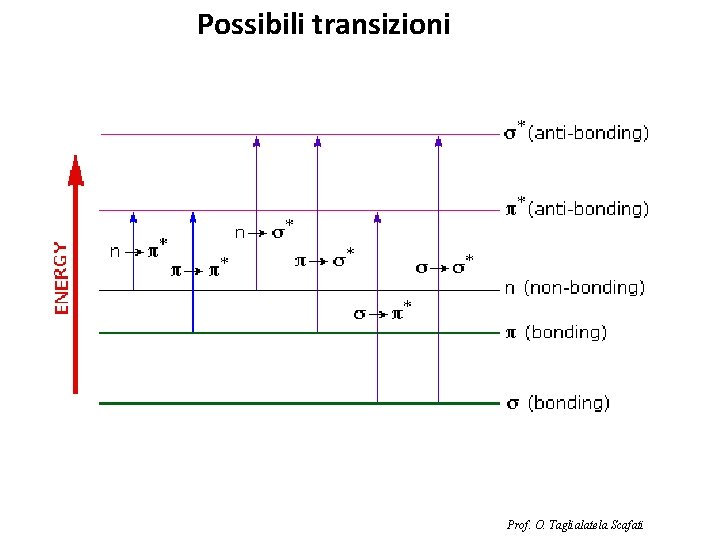
Possibili transizioni Prof. O. Taglialatela Scafati

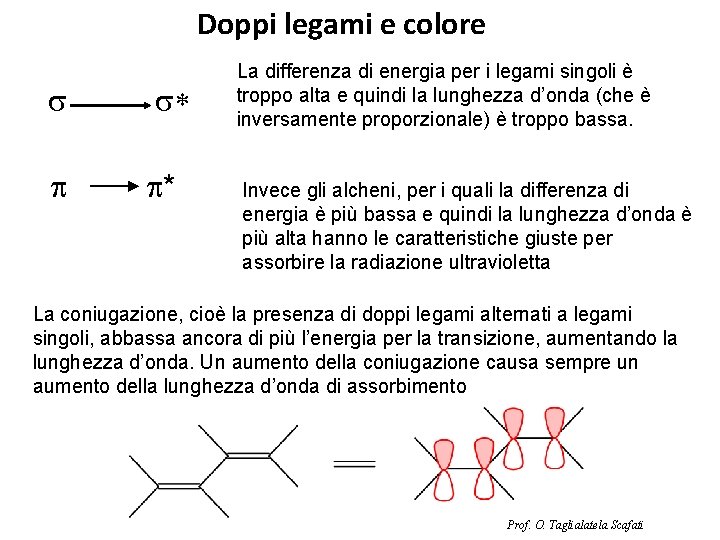
Doppi legami e colore s s* * La differenza di energia per i legami singoli è troppo alta e quindi la lunghezza d’onda (che è inversamente proporzionale) è troppo bassa. Invece gli alcheni, per i quali la differenza di energia è più bassa e quindi la lunghezza d’onda è più alta hanno le caratteristiche giuste per assorbire la radiazione ultravioletta La coniugazione, cioè la presenza di doppi legami alternati a legami singoli, abbassa ancora di più l’energia per la transizione, aumentando la lunghezza d’onda. Un aumento della coniugazione causa sempre un aumento della lunghezza d’onda di assorbimento Prof. O. Taglialatela Scafati

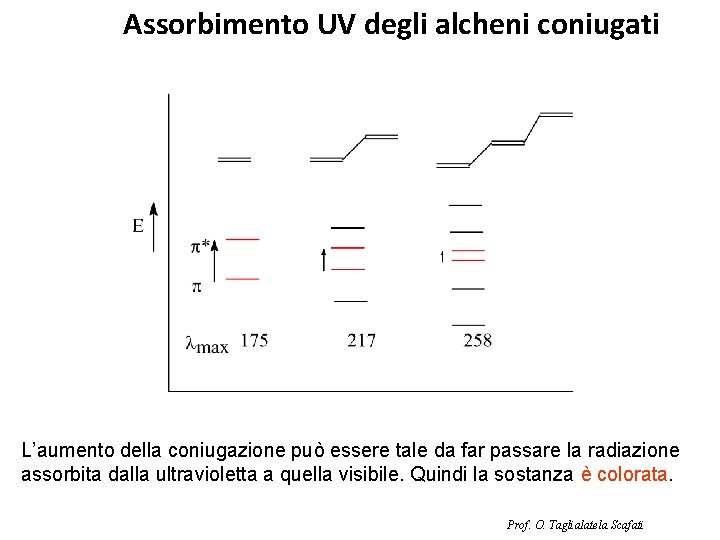
Assorbimento UV degli alcheni coniugati L’aumento della coniugazione può essere tale da far passare la radiazione assorbita dalla ultravioletta a quella visibile. Quindi la sostanza è colorata. Prof. O. Taglialatela Scafati

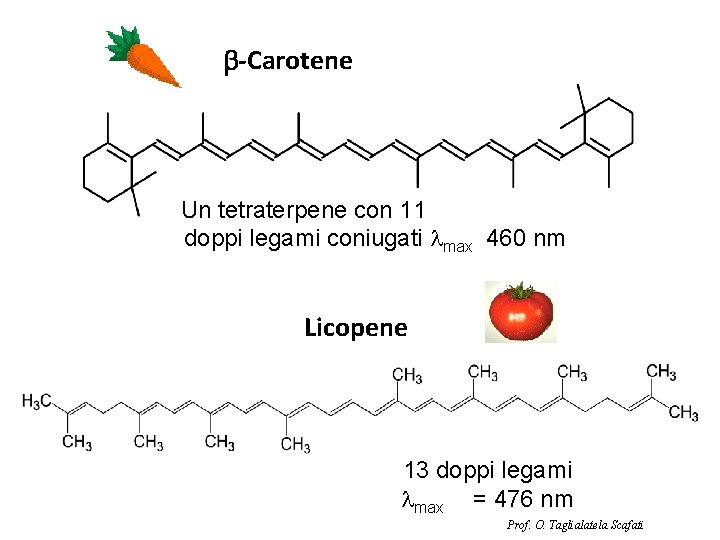
b-Carotene Un tetraterpene con 11 doppi legami coniugati lmax 460 nm Licopene 13 doppi legami lmax = 476 nm Prof. O. Taglialatela Scafati

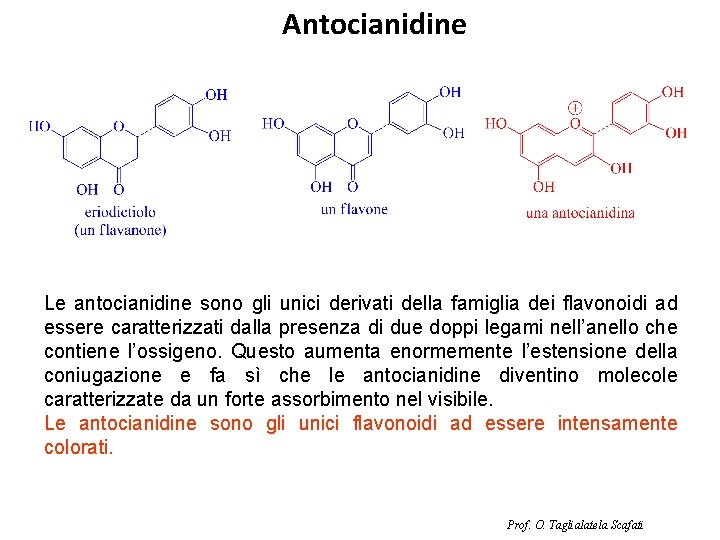
Antocianidine Le antocianidine sono gli unici derivati della famiglia dei flavonoidi ad essere caratterizzati dalla presenza di due doppi legami nell’anello che contiene l’ossigeno. Questo aumenta enormemente l’estensione della coniugazione e fa sì che le antocianidine diventino molecole caratterizzate da un forte assorbimento nel visibile. Le antocianidine sono gli unici flavonoidi ad essere intensamente colorati. Prof. O. Taglialatela Scafati

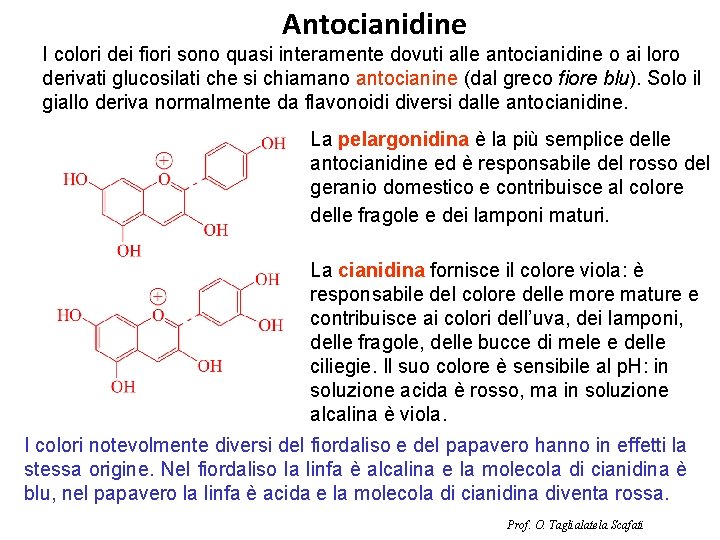
Antocianidine I colori dei fiori sono quasi interamente dovuti alle antocianidine o ai loro derivati glucosilati che si chiamano antocianine (dal greco fiore blu). Solo il giallo deriva normalmente da flavonoidi diversi dalle antocianidine. La pelargonidina è la più semplice delle antocianidine ed è responsabile del rosso del geranio domestico e contribuisce al colore delle fragole e dei lamponi maturi. La cianidina fornisce il colore viola: è responsabile del colore delle more mature e contribuisce ai colori dell’uva, dei lamponi, delle fragole, delle bucce di mele e delle ciliegie. Il suo colore è sensibile al p. H: in soluzione acida è rosso, ma in soluzione alcalina è viola. I colori notevolmente diversi del fiordaliso e del papavero hanno in effetti la stessa origine. Nel fiordaliso la linfa è alcalina e la molecola di cianidina è blu, nel papavero la linfa è acida e la molecola di cianidina diventa rossa. Prof. O. Taglialatela Scafati

Betalaine In alcune piante la colorazione è da attribuire a molecole diverse dalle antocianidine, per esempio alle betalaine. Le betalaine, ottenute ad es. da barbabietole o da fico d’india, sono anche utilizzate come coloranti alimentari (E 162). A differenza delle antocianidine tendono meno a cambiare colore con il p. H, ma sono più instabili al calore. Prof. O. Taglialatela Scafati

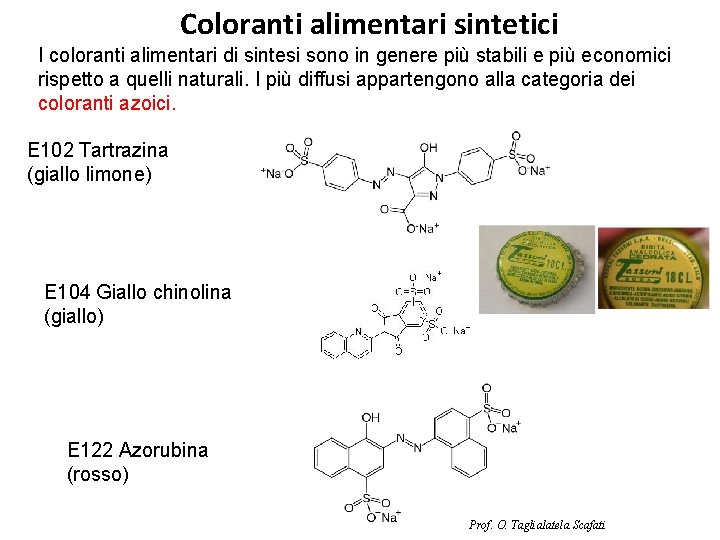
Coloranti alimentari sintetici I coloranti alimentari di sintesi sono in genere più stabili e più economici rispetto a quelli naturali. I più diffusi appartengono alla categoria dei coloranti azoici. E 102 Tartrazina (giallo limone) E 104 Giallo chinolina (giallo) E 122 Azorubina (rosso) Prof. O. Taglialatela Scafati