Reazioni degli alcheni Reazioni degli alcheni Il meccanismo


- Slides: 24

Reazioni degli alcheni

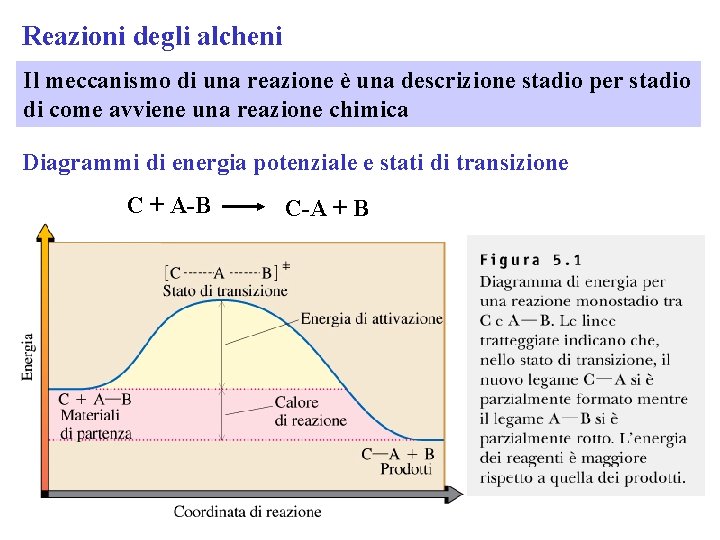
Reazioni degli alcheni Il meccanismo di una reazione è una descrizione stadio per stadio di come avviene una reazione chimica Diagrammi di energia potenziale e stati di transizione C + A-B C-A + B

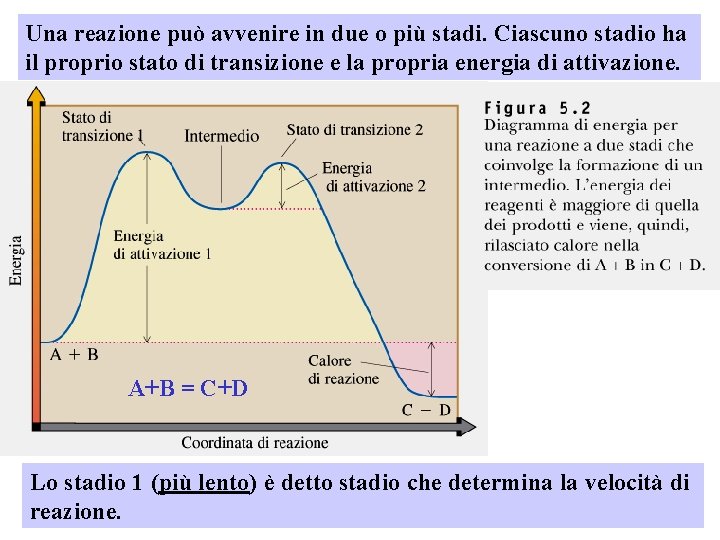
Una reazione può avvenire in due o più stadi. Ciascuno stadio ha il proprio stato di transizione e la propria energia di attivazione. A+B = C+D Lo stadio 1 (più lento) è detto stadio che determina la velocità di reazione.

Nucleofilo: una specie con una coppia di elettroni non condivisa su un atomo. molecole anioniche molecole neutre I nucleofili sono anche basi di Lewis poiché posseggono una coppia di elettroni non condivisa. Tuttavia basicità e nucleofilicità sono proprietà differenti per cui non tutte le basi possono essere dei buoni nucleofili (e viceversa).

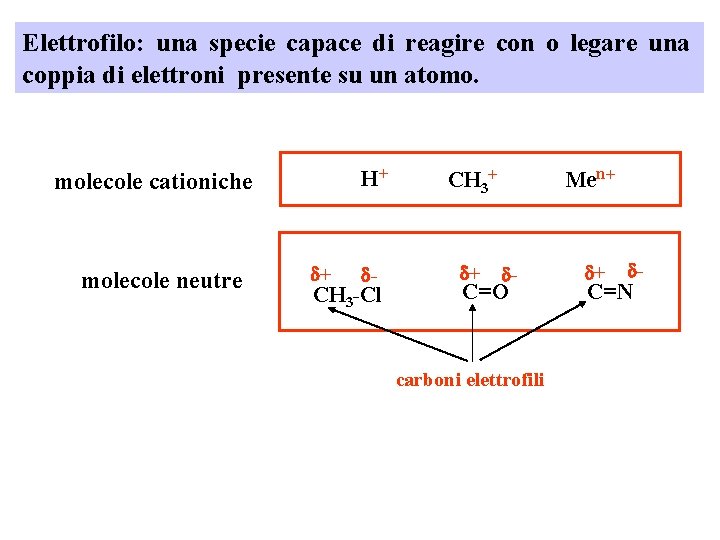
Elettrofilo: una specie capace di reagire con o legare una coppia di elettroni presente su un atomo. molecole cationiche molecole neutre d+ H+ CH 3+ d- d+ CH 3 -Cl Men+ d- C= O carboni elettrofili d+ d- C= N

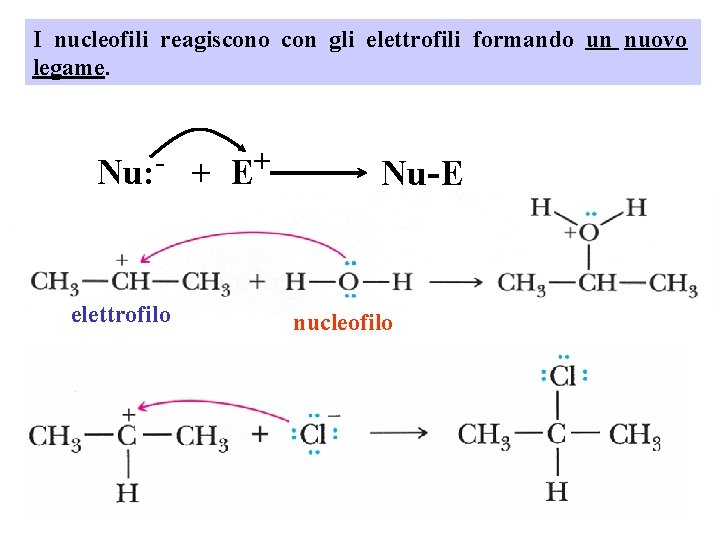
I nucleofili reagiscono con gli elettrofili formando un nuovo legame. Nu: elettrofilo + + E Nu-E nucleofilo

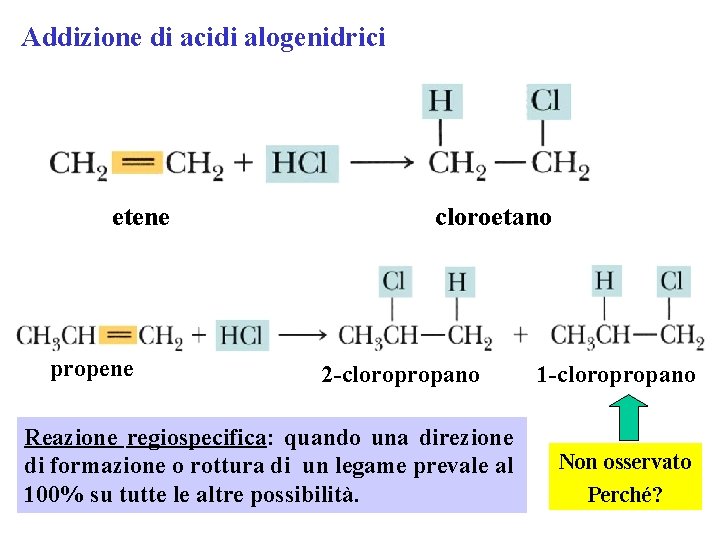
Addizione di acidi alogenidrici etene propene cloroetano 2 -cloropropano Reazione regiospecifica: quando una direzione di formazione o rottura di un legame prevale al 100% su tutte le altre possibilità. 1 -cloropropano Non osservato Perché?

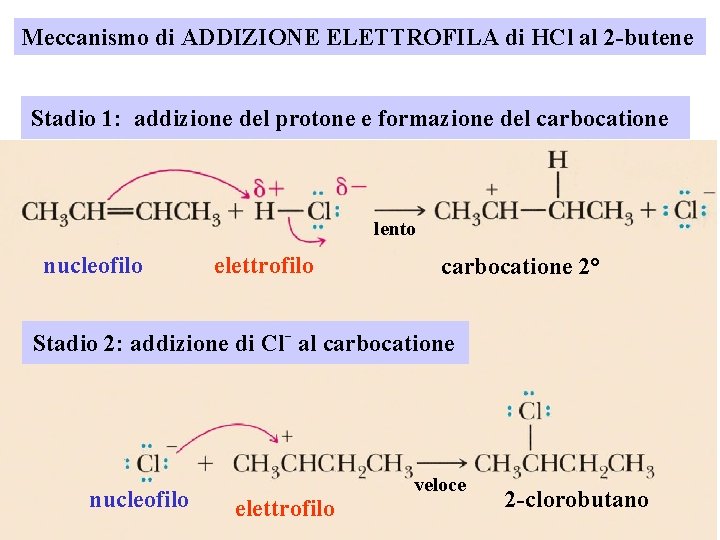
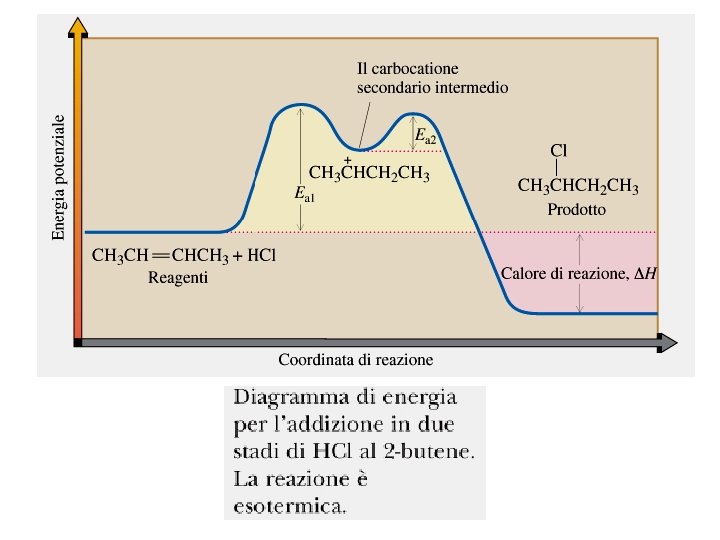
Meccanismo di ADDIZIONE ELETTROFILA di HCl al 2 -butene Stadio 1: addizione del protone e formazione del carbocatione lento nucleofilo elettrofilo carbocatione 2° Stadio 2: addizione di Cl- al carbocatione nucleofilo elettrofilo veloce 2 -clorobutano


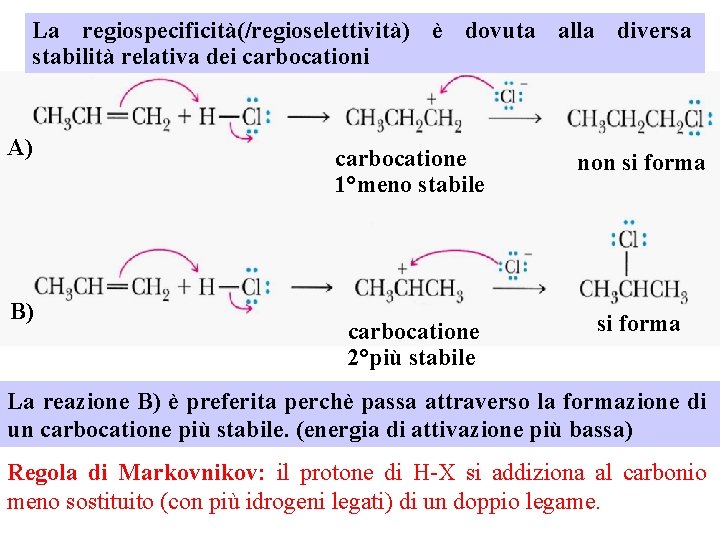
La regiospecificità(/regioselettività) è dovuta alla diversa stabilità relativa dei carbocationi A) B) carbocatione 1°meno stabile non si forma carbocatione 2°più stabile si forma La reazione B) è preferita perchè passa attraverso la formazione di un carbocatione più stabile. (energia di attivazione più bassa) Regola di Markovnikov: il protone di H-X si addiziona al carbonio meno sostituito (con più idrogeni legati) di un doppio legame.

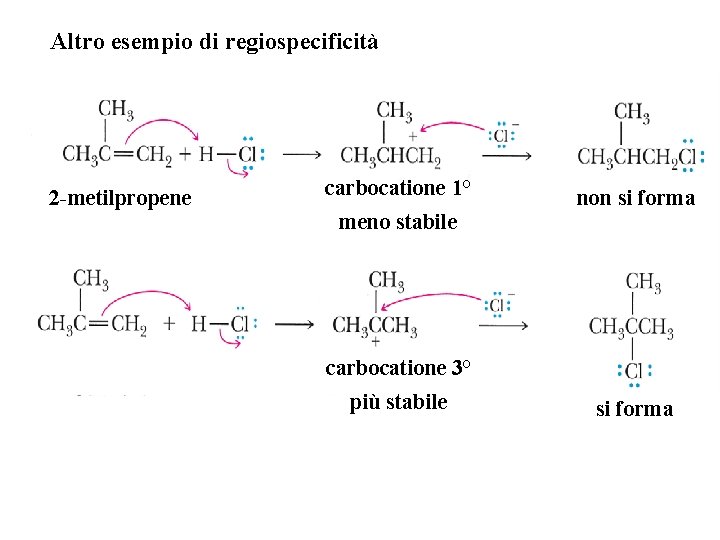
Altro esempio di regiospecificità 2 -metilpropene carbocatione 1° meno stabile non si forma carbocatione 3° più stabile si forma

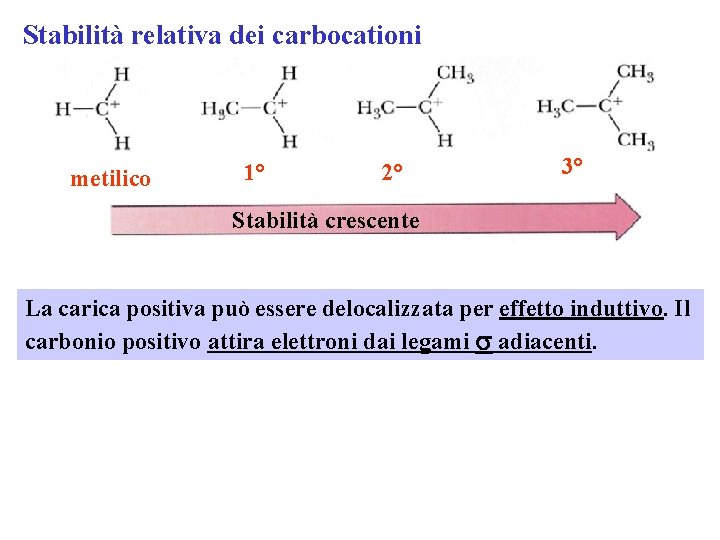
Stabilità relativa dei carbocationi metilico 1° 2° 3° Stabilità crescente La carica positiva può essere delocalizzata per effetto induttivo. Il carbonio positivo attira elettroni dai legami s adiacenti.

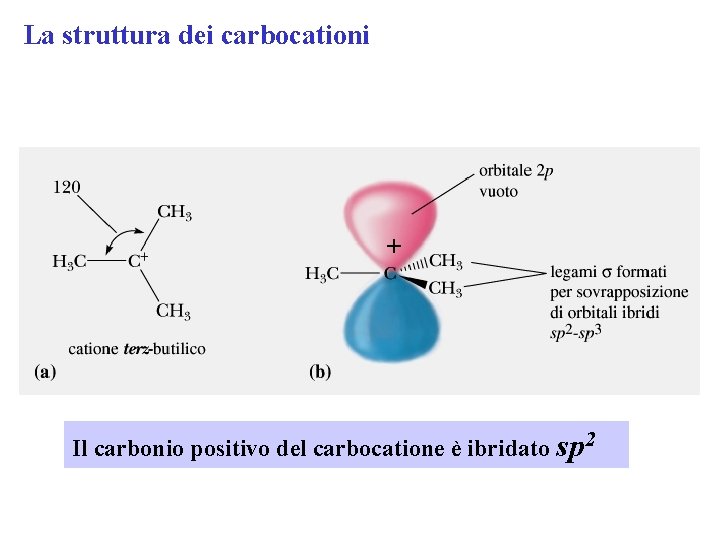
La struttura dei carbocationi + Il carbonio positivo del carbocatione è ibridato sp 2

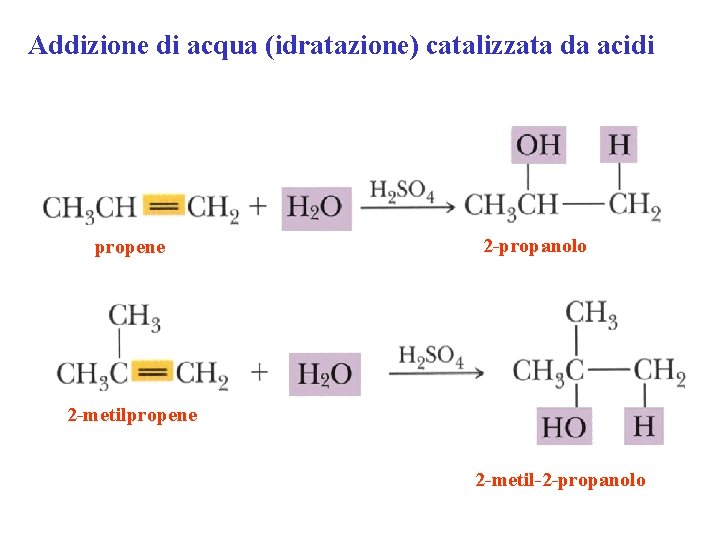
Addizione di acqua (idratazione) catalizzata da acidi propene 2 -propanolo 2 -metilpropene 2 -metil-2 -propanolo

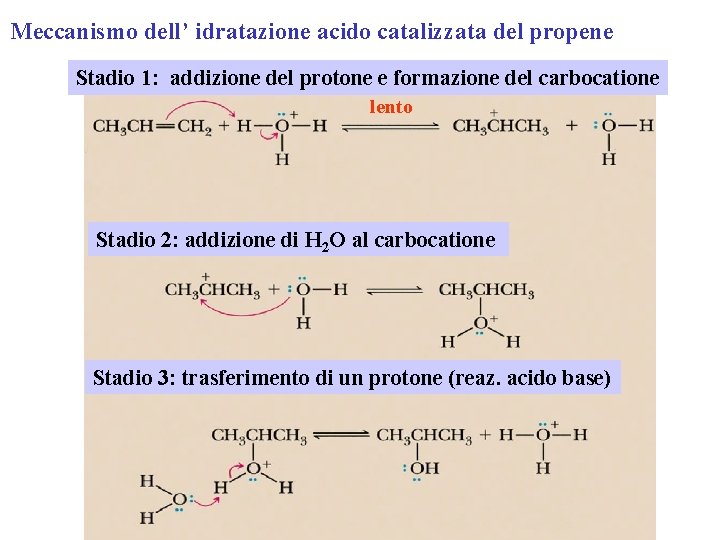
Meccanismo dell’ idratazione acido catalizzata del propene Stadio 1: addizione del protone e formazione del carbocatione lento Stadio 2: addizione di H 2 O al carbocatione Stadio 3: trasferimento di un protone (reaz. acido base)

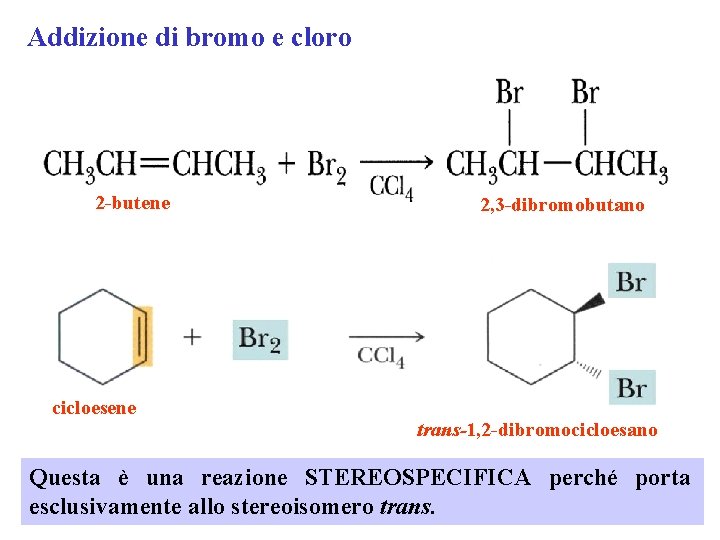
Addizione di bromo e cloro 2 -butene cicloesene 2, 3 -dibromobutano trans-1, 2 -dibromocicloesano Questa è una reazione STEREOSPECIFICA perché porta esclusivamente allo stereoisomero trans.

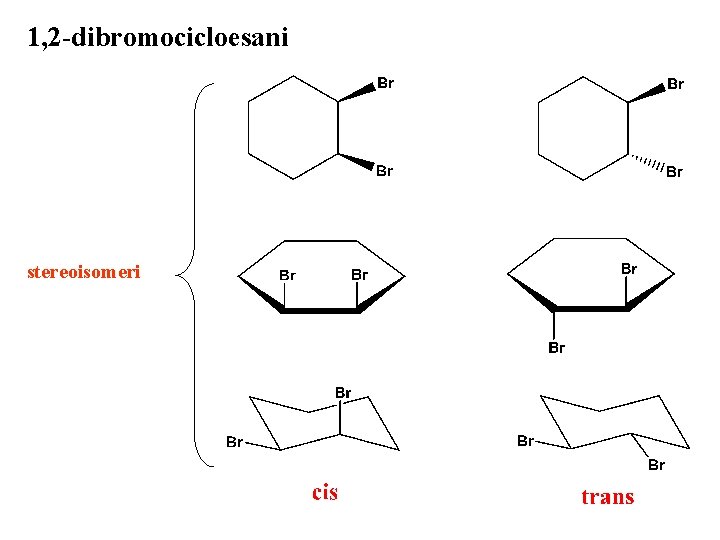
1, 2 -dibromocicloesani stereoisomeri

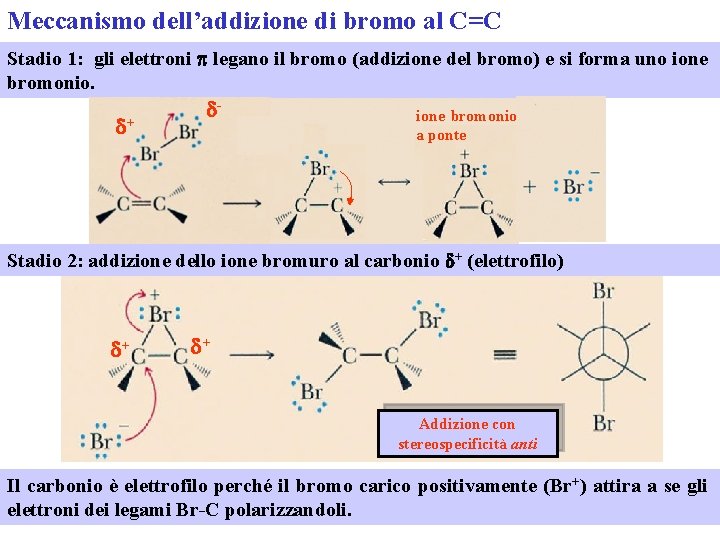
Meccanismo dell’addizione di bromo al C=C Stadio 1: gli elettroni p legano il bromo (addizione del bromo) e si forma uno ione bromonio. d+ d- ione bromonio a ponte Stadio 2: addizione dello ione bromuro al carbonio d+ (elettrofilo) d+ d+ Addizione con stereospecificità anti Il carbonio è elettrofilo perché il bromo carico positivamente (Br+) attira a se gli elettroni dei legami Br-C polarizzandoli.

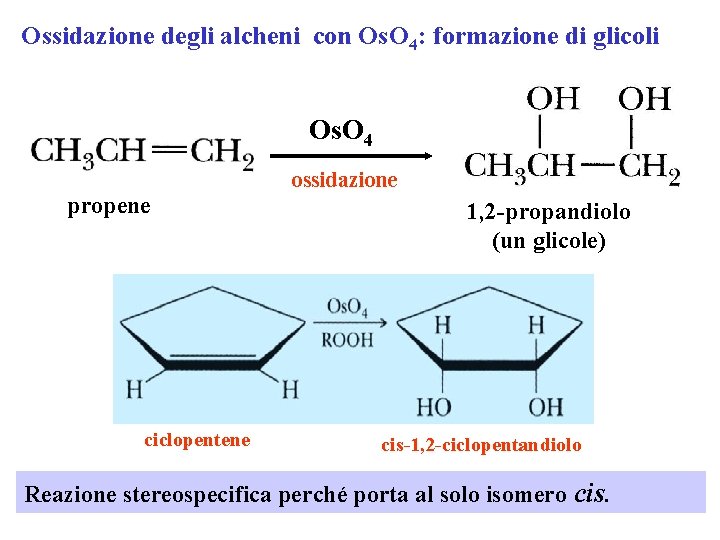
Ossidazione degli alcheni con Os. O 4: formazione di glicoli Os. O 4 propene ciclopentene ossidazione 1, 2 -propandiolo (un glicole) cis-1, 2 -ciclopentandiolo Reazione stereospecifica perché porta al solo isomero cis.

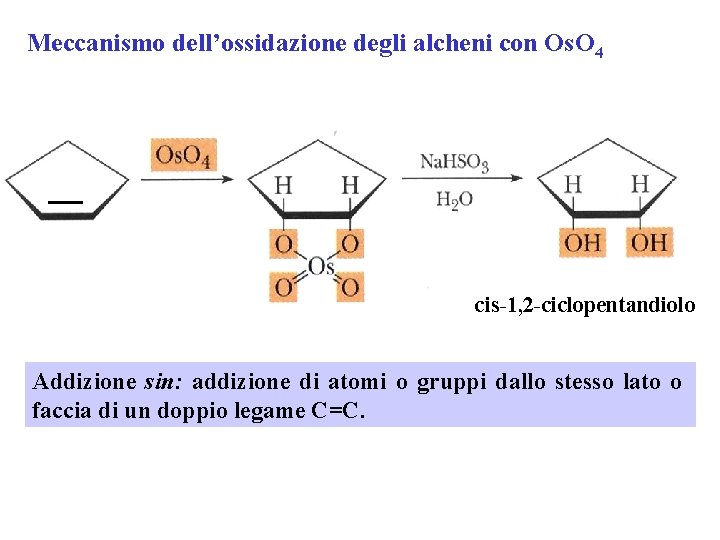
Meccanismo dell’ossidazione degli alcheni con Os. O 4 cis-1, 2 -ciclopentandiolo Addizione sin: addizione di atomi o gruppi dallo stesso lato o faccia di un doppio legame C=C.

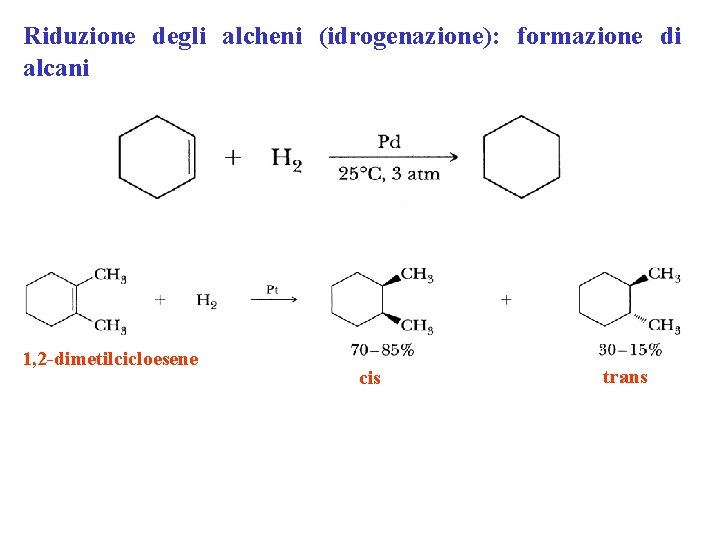
Riduzione degli alcheni (idrogenazione): formazione di alcani 1, 2 -dimetilcicloesene cis trans

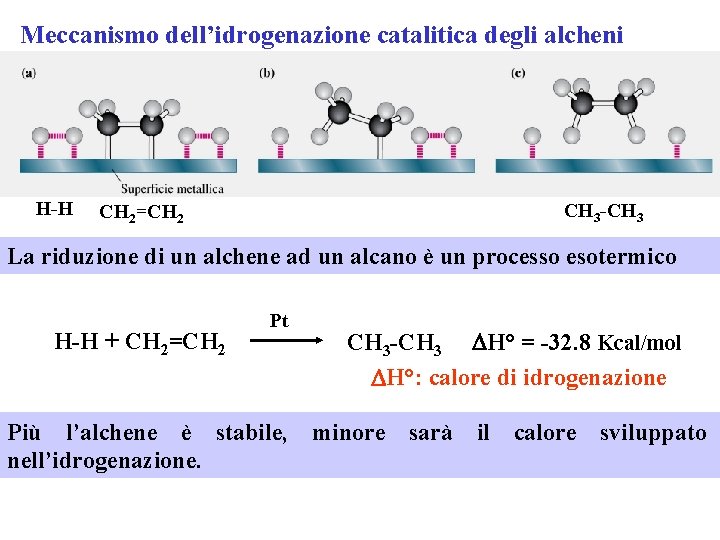
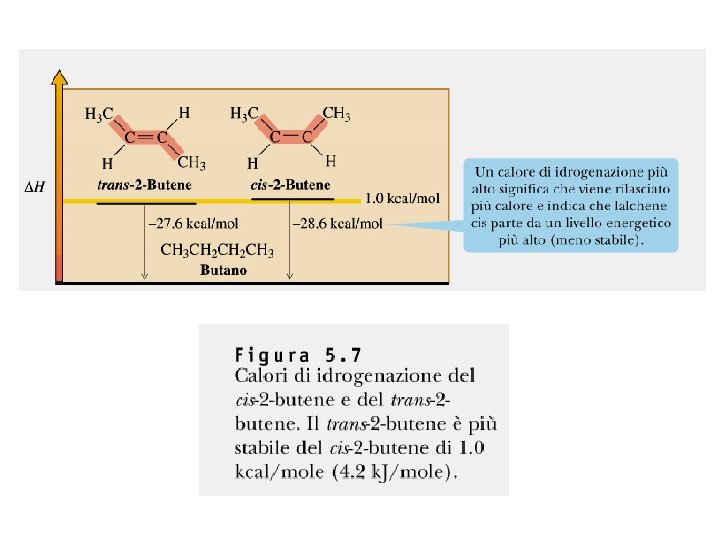
Meccanismo dell’idrogenazione catalitica degli alcheni H-H CH 3 -CH 3 CH 2=CH 2 La riduzione di un alchene ad un alcano è un processo esotermico H-H + CH 2=CH 2 Pt CH 3 -CH 3 DH° = -32. 8 Kcal/mol DH°: calore di idrogenazione Più l’alchene è stabile, minore sarà il calore sviluppato nell’idrogenazione.


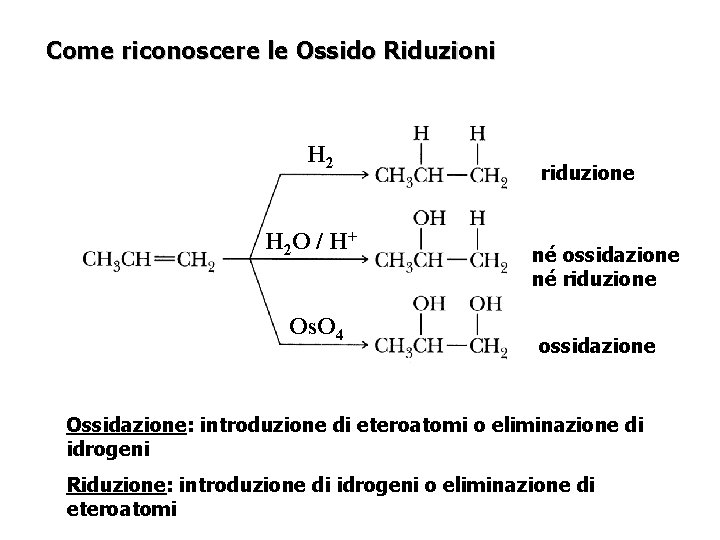
Come riconoscere le Ossido Riduzioni H 2 O / H + Os. O 4 riduzione né ossidazione né riduzione ossidazione Ossidazione: introduzione di eteroatomi o eliminazione di idrogeni Riduzione: introduzione di idrogeni o eliminazione di eteroatomi