Alcheni Struttura e Legami Sono idrocarburi insaturi Formula

Alcheni

Struttura e Legami • Sono idrocarburi insaturi • Formula generale Cn. H 2 n • Il doppio legame che può essere terminale o interno. • Cicloalcheni: doppio legame in un ciclo • Sono chiamati anche olefine doppio legame terminale doppio legame interno cicloesene 2
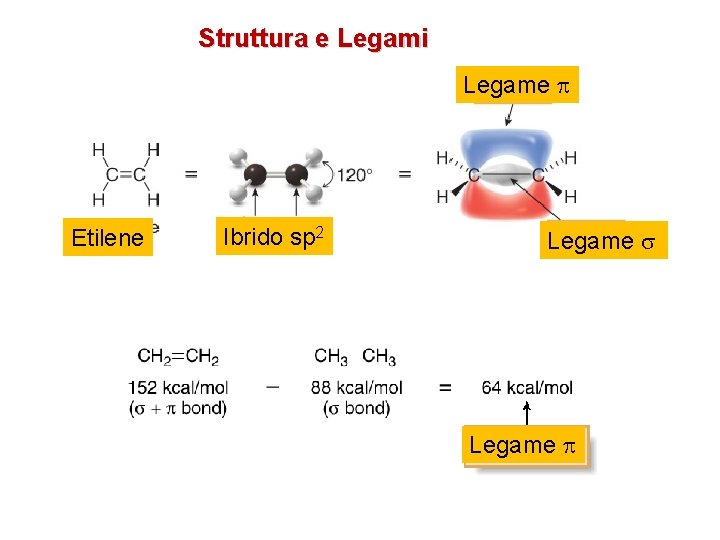
Struttura e Legami Legame Etilene Ibrido sp 2 Legame s Legame
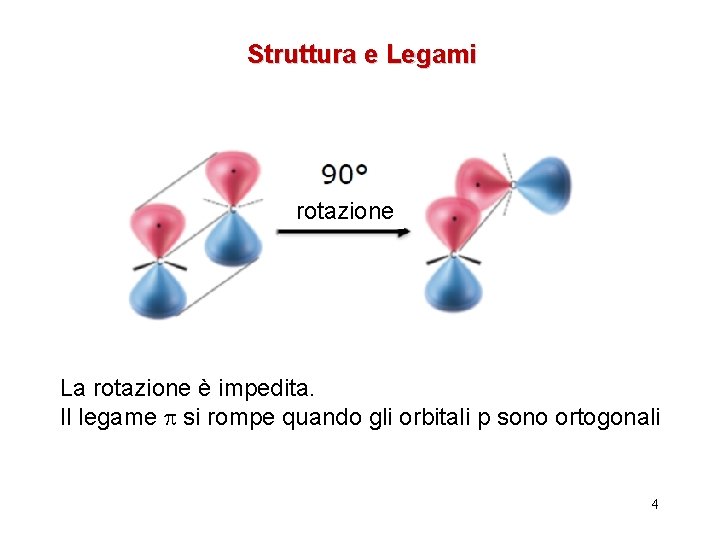
Struttura e Legami rotazione La rotazione è impedita. Il legame si rompe quando gli orbitali p sono ortogonali 4
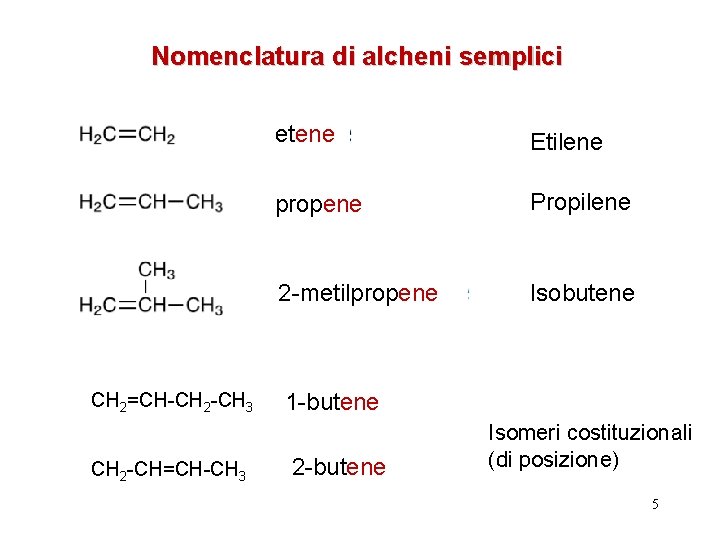
Nomenclatura di alcheni semplici CH 2=CH-CH 2 -CH 3 CH 2 -CH=CH-CH 3 etene Etilene propene Propilene 2 -metilpropene Isobutene 1 -butene 2 -butene Isomeri costituzionali (di posizione) 5
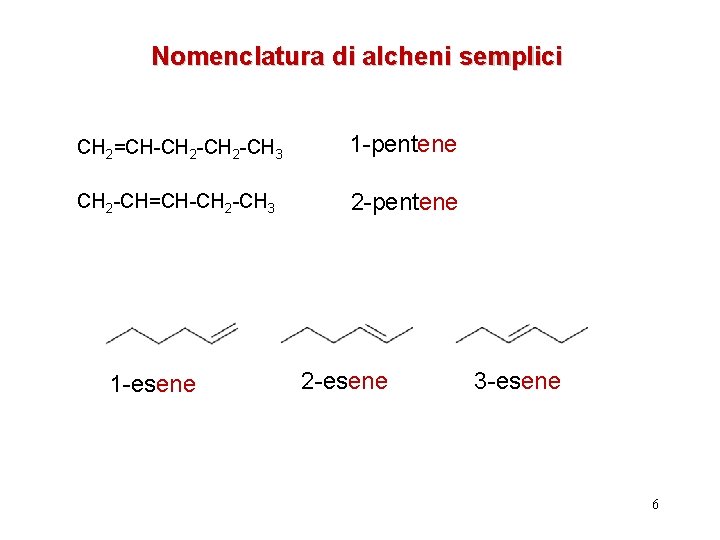
Nomenclatura di alcheni semplici CH 2=CH-CH 2 -CH 3 1 -pentene CH 2 -CH=CH-CH 2 -CH 3 2 -pentene 1 -esene 2 -esene 3 -esene 6
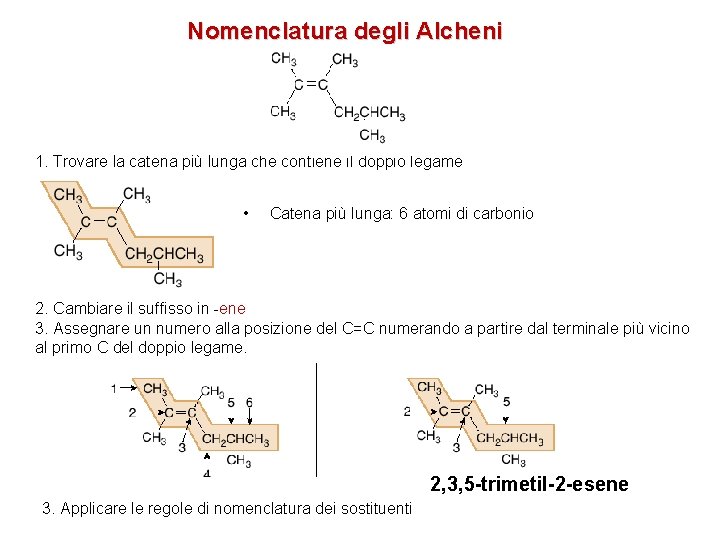
Nomenclatura degli Alcheni 1. Trovare la catena più lunga che contiene il doppio legame • Catena più lunga: 6 atomi di carbonio 2. Cambiare il suffisso in -ene 3. Assegnare un numero alla posizione del C=C numerando a partire dal terminale più vicino al primo C del doppio legame. 2, 3, 5 -trimetil-2 -esene 3. Applicare le regole di nomenclatura dei sostituenti
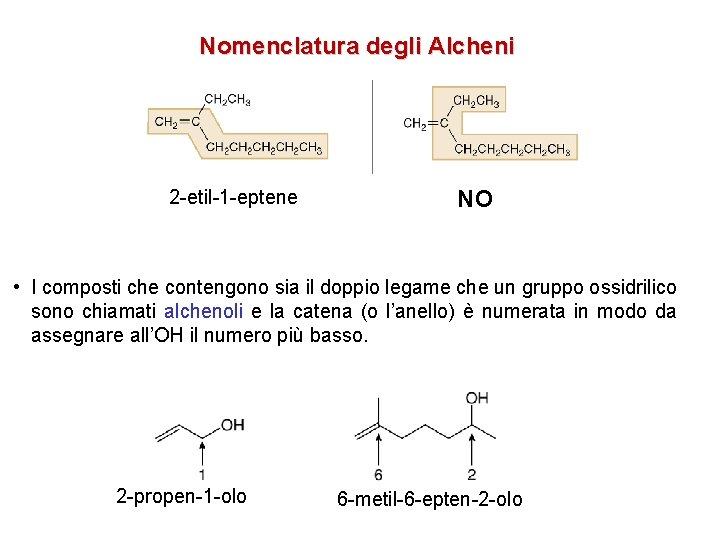
Nomenclatura degli Alcheni 2 -etil-1 -eptene NO • I composti che contengono sia il doppio legame che un gruppo ossidrilico sono chiamati alchenoli e la catena (o l’anello) è numerata in modo da assegnare all’OH il numero più basso. 2 -propen-1 -olo 6 -metil-6 -epten-2 -olo
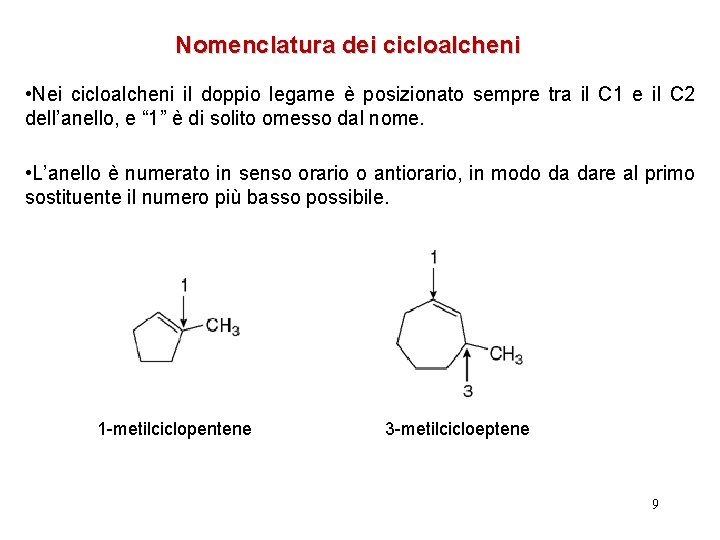
Nomenclatura dei cicloalcheni • Nei cicloalcheni il doppio legame è posizionato sempre tra il C 1 e il C 2 dell’anello, e “ 1” è di solito omesso dal nome. • L’anello è numerato in senso orario o antiorario, in modo da dare al primo sostituente il numero più basso possibile. 1 -metilciclopentene 3 -metilcicloeptene 9
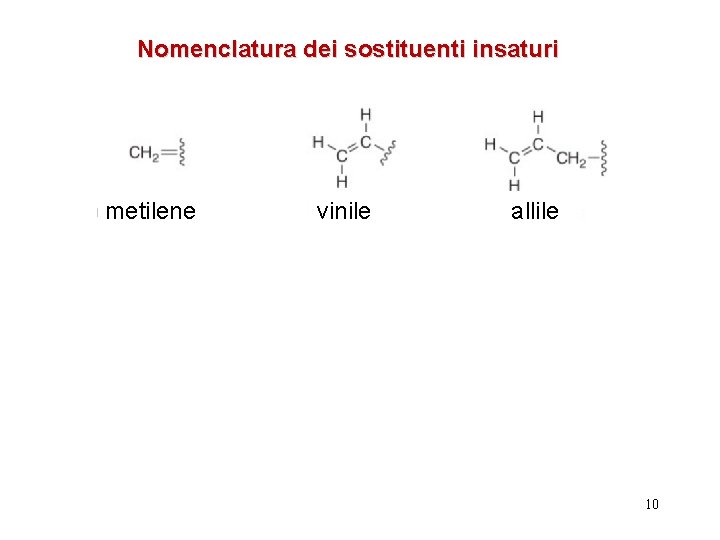
Nomenclatura dei sostituenti insaturi metilene vinile allile 10
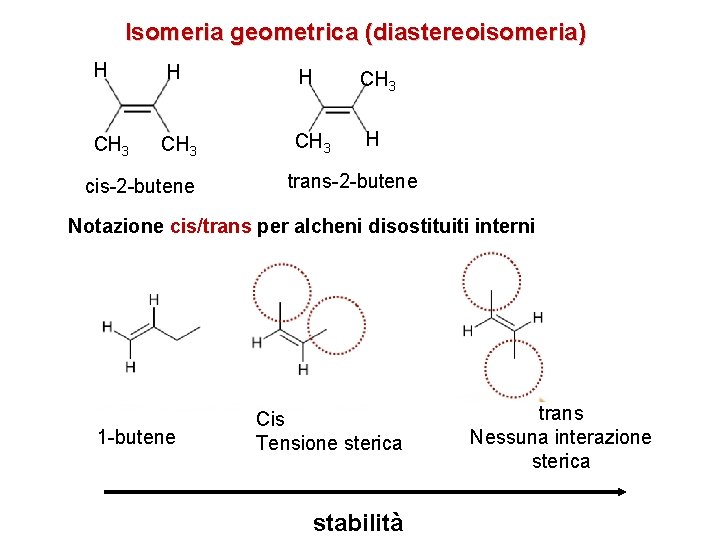
Isomeria geometrica (diastereoisomeria) H H H CH 3 H cis-2 -butene trans-2 -butene Notazione cis/trans per alcheni disostituiti interni 1 -butene Cis Tensione sterica stabilità trans Nessuna interazione sterica
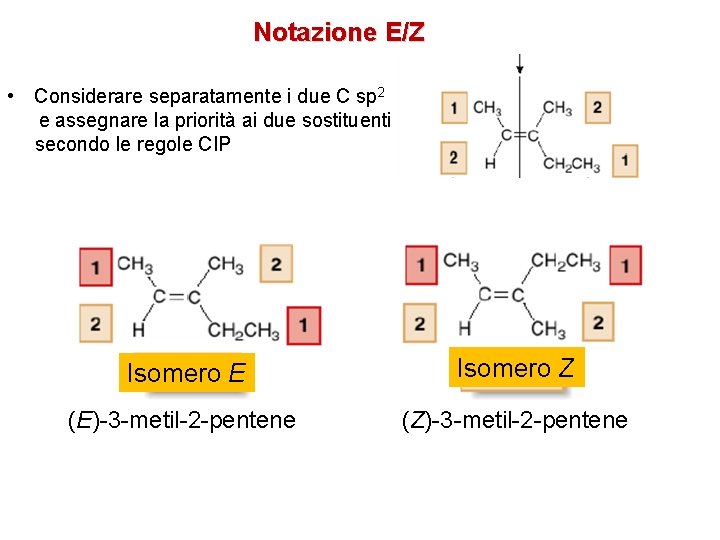
Notazione E/Z • Considerare separatamente i due C sp 2 e assegnare la priorità ai due sostituenti secondo le regole CIP Isomero E Isomero Z (E)-3 -metil-2 -pentene (Z)-3 -metil-2 -pentene

Proprietà Fisiche • Le proprietà fisiche degli alcheni sono simili a quelle degli alcani di peso molecolare comparabile. • Gli alcheni hanno bassi punti di fusione e di ebollizione. • I punti di fusione e di ebollizione aumentano con l’aumentare del numero di atomi di carbonio. • Gli alcheni sono solubili in solventi organici e insolubili in acqua. • Il legame singolo C—C tra un gruppo alchilico ed un carbonio del doppio legame di un alchene è leggermente polare, perchè il carbonio dell’alchile, ibridato sp 3, dona densità elettronica al carbonio alchenilico, ibridato sp 2. 13
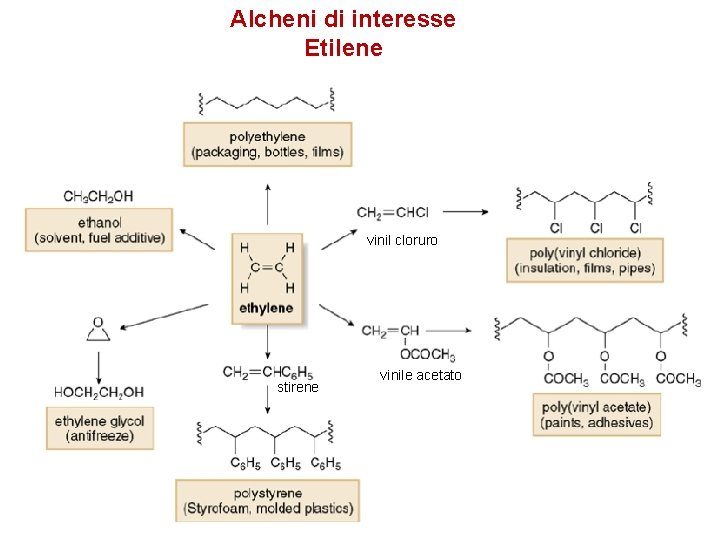
Alcheni di interesse Etilene vinil cloruro stirene vinile acetato
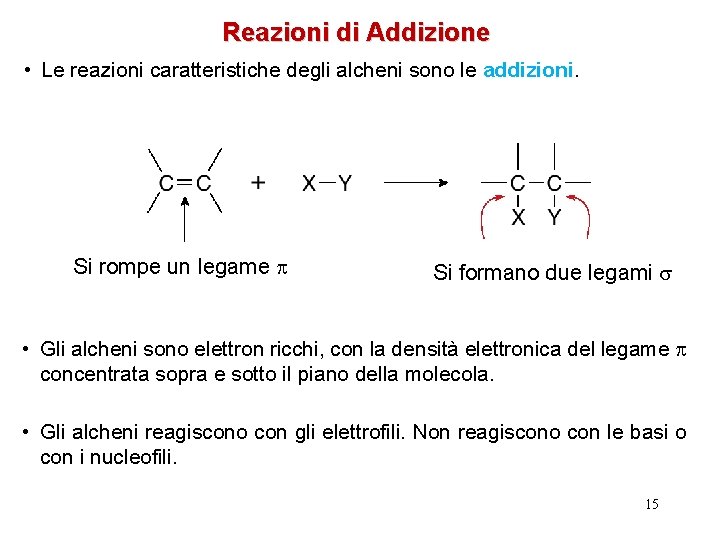
Reazioni di Addizione • Le reazioni caratteristiche degli alcheni sono le addizioni. Si rompe un legame Si formano due legami s • Gli alcheni sono elettron ricchi, con la densità elettronica del legame concentrata sopra e sotto il piano della molecola. • Gli alcheni reagiscono con gli elettrofili. Non reagiscono con le basi o con i nucleofili. 15
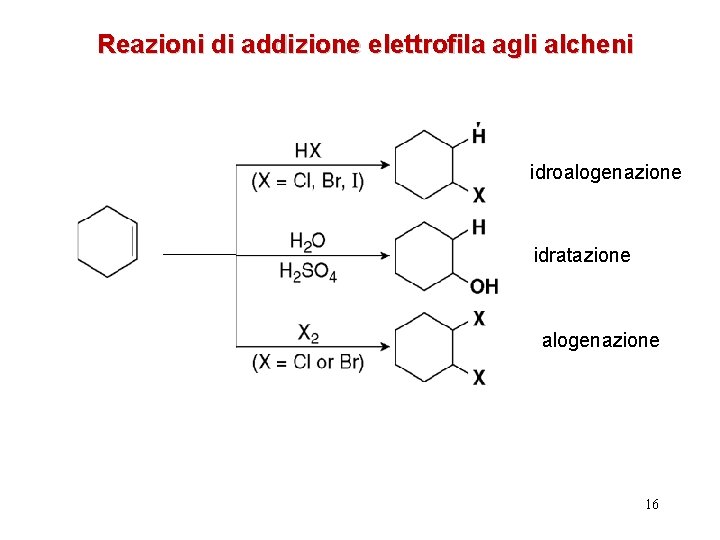
Reazioni di addizione elettrofila agli alcheni idroalogenazione idratazione alogenazione 16
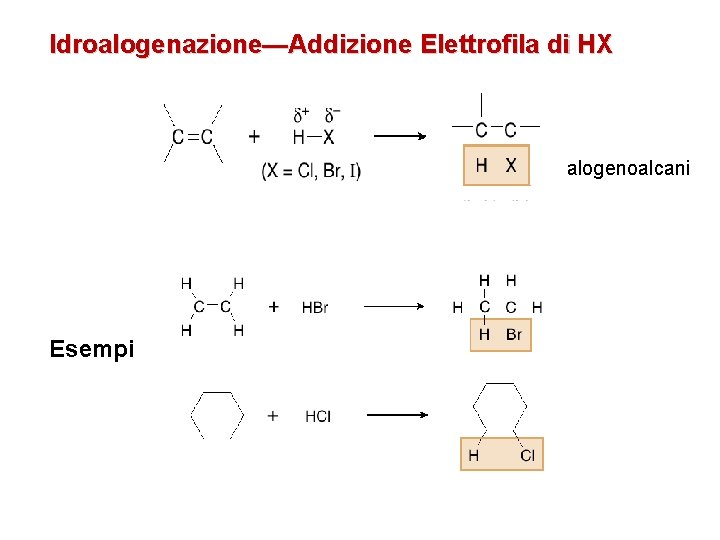
Idroalogenazione—Addizione Elettrofila di HX alogenoalcani Esempi
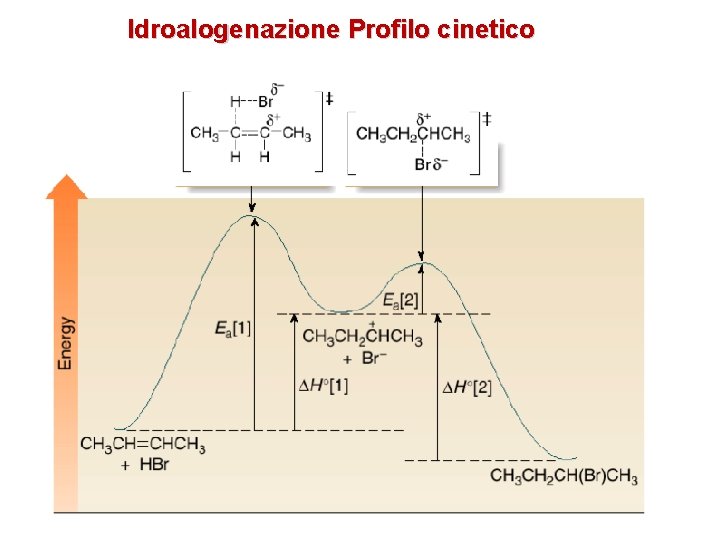
Idroalogenazione Profilo cinetico 18
![Meccanismo • Meccanismo a due stadi. • Stadio [1] l’alchene dona una coppia di Meccanismo • Meccanismo a due stadi. • Stadio [1] l’alchene dona una coppia di](http://slidetodoc.com/presentation_image_h/0a3755551782d54cae60c0e3ad7a78c3/image-19.jpg)
Meccanismo • Meccanismo a due stadi. • Stadio [1] l’alchene dona una coppia di elettroni ad H-Br, con formazione di un legame C-H e un carbocatione • Stadio [2], Br¯ dona una coppia di elettroni al carbocatione, formando il legame C-Br [1] slow lento veloce [2] 2 -bromobutano 19
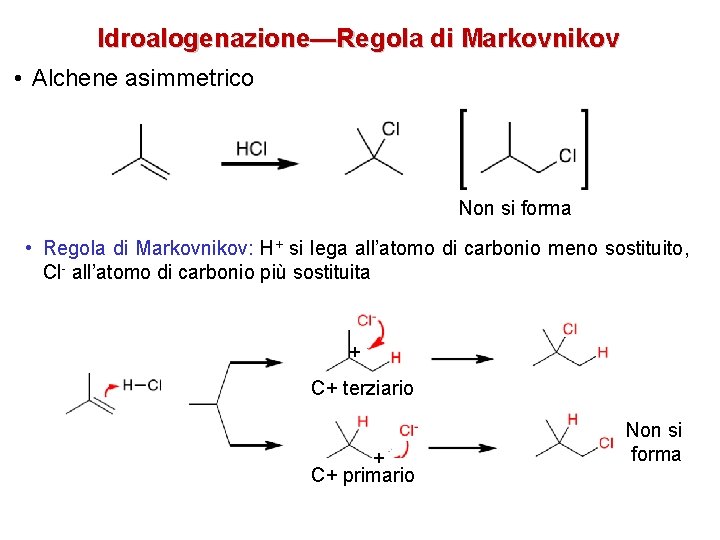
Idroalogenazione—Regola di Markovnikov • Alchene asimmetrico Non si forma • Regola di Markovnikov: H+ si lega all’atomo di carbonio meno sostituito, Cl- all’atomo di carbonio più sostituita + C+ terziario + C+ primario Non si forma

Idroalogenazione—Sommario • Il meccanismo è a due stadi • Lo stadio lento è formazione del carbocatione • E’ seguita la regola di Markonikov: se l’alchene è asimmetrico, l’idrogeno si lega sul C meno sostituito 21
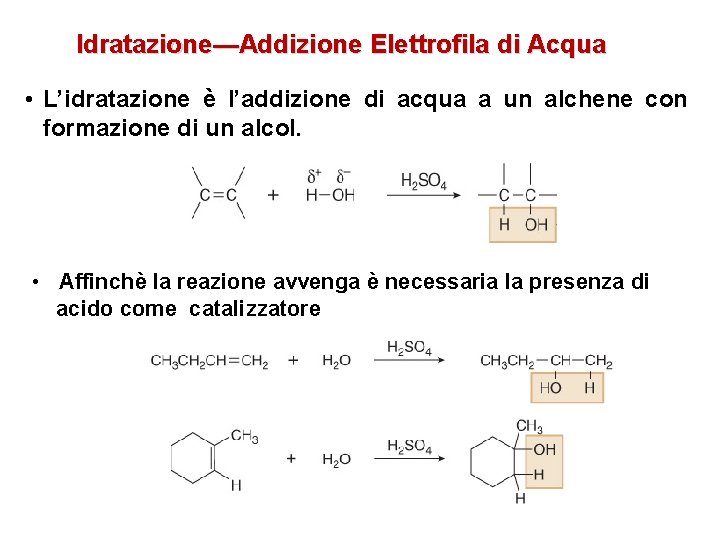
Idratazione—Addizione Elettrofila di Acqua • L’idratazione è l’addizione di acqua a un alchene con formazione di un alcol. • Affinchè la reazione avvenga è necessaria la presenza di acido come catalizzatore
![Addizione Elettrofila di H 2 O - Meccanismo [1] [2] [3] Attacco nucleofilo del Addizione Elettrofila di H 2 O - Meccanismo [1] [2] [3] Attacco nucleofilo del](http://slidetodoc.com/presentation_image_h/0a3755551782d54cae60c0e3ad7a78c3/image-23.jpg)
Addizione Elettrofila di H 2 O - Meccanismo [1] [2] [3] Attacco nucleofilo del legame ad H 3 O+, con formazione di un legame C-H e un carbocatione Attacco nucleofilo dell’ H 2 O, con formazione di un legame C-OH 2+ Reazione acido base Si rigenera H 3 O+ (catalizzatore) 23
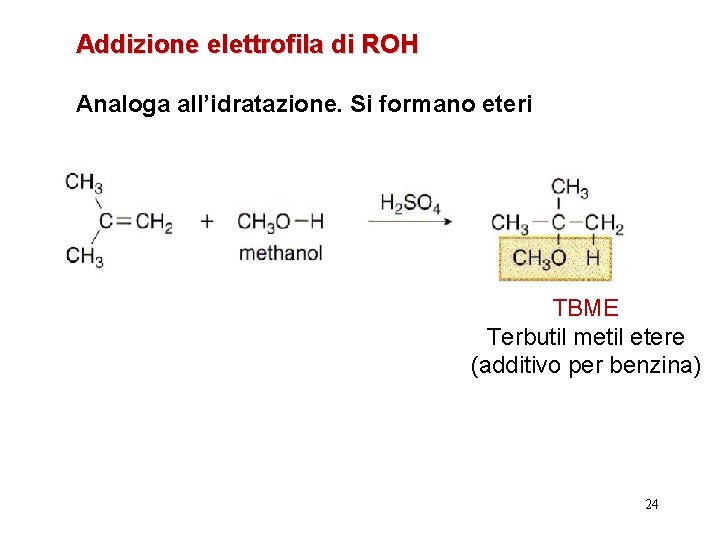
Addizione elettrofila di ROH Analoga all’idratazione. Si formano eteri TBME Terbutil metil etere (additivo per benzina) 24
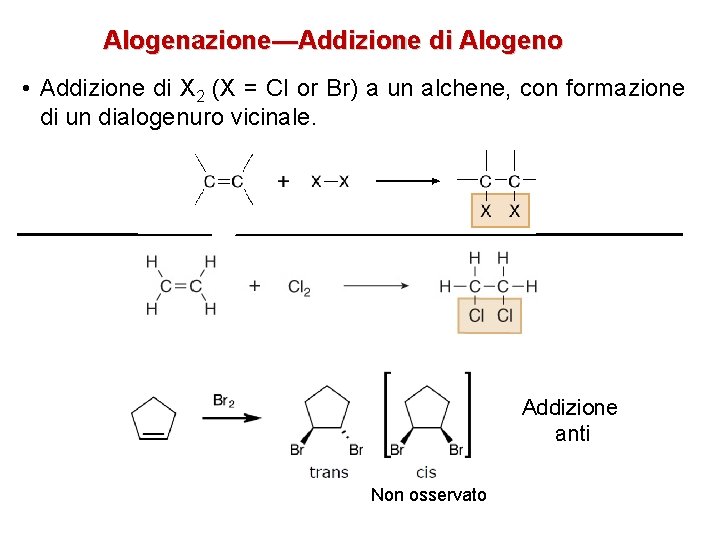
Alogenazione—Addizione di Alogeno • Addizione di X 2 (X = Cl or Br) a un alchene, con formazione di un dialogenuro vicinale. Addizione anti Non osservato
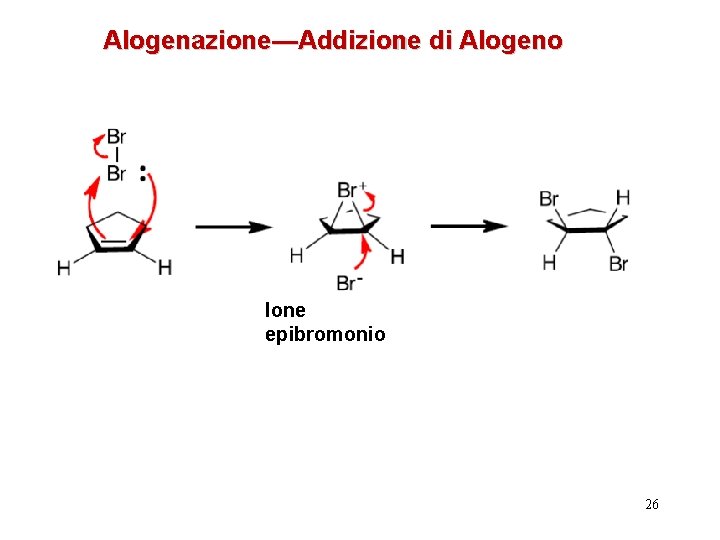
Alogenazione—Addizione di Alogeno Ione epibromonio 26
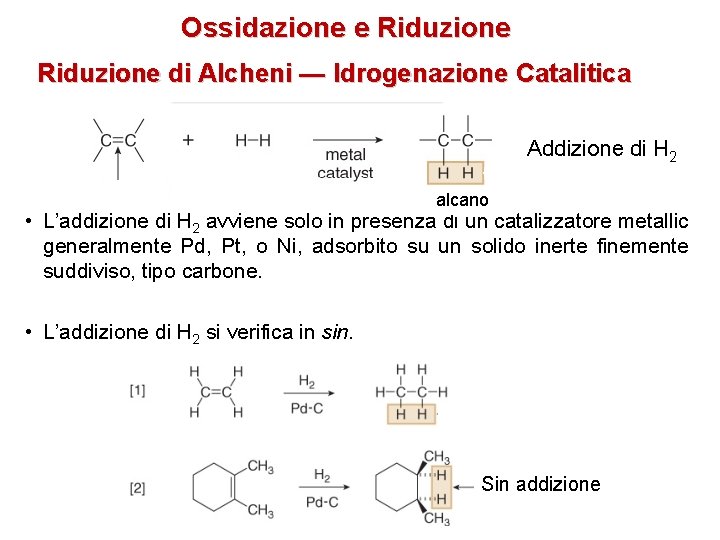
Ossidazione e Riduzione di Alcheni — Idrogenazione Catalitica Catalizzatore metallico Addizione di H 2 alcano • L’addizione di H 2 avviene solo in presenza di un catalizzatore metallic generalmente Pd, Pt, o Ni, adsorbito su un solido inerte finemente suddiviso, tipo carbone. • L’addizione di H 2 si verifica in sin. Sin addizione
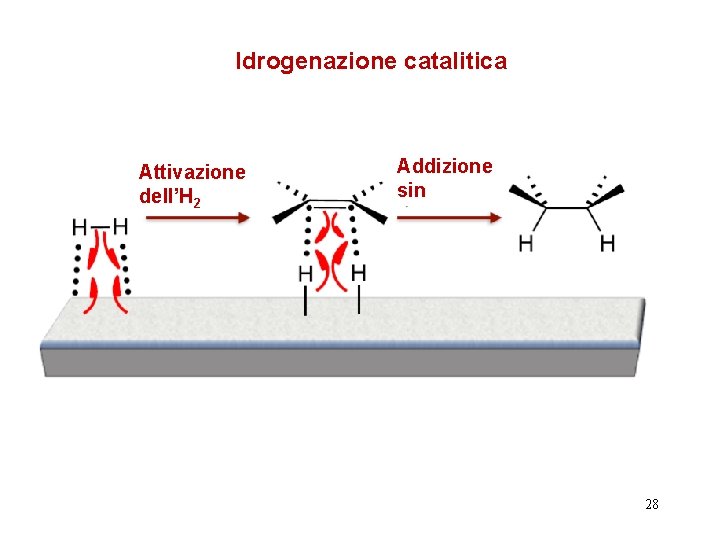
Idrogenazione catalitica Attivazione dell’H 2 Addizione sin 28
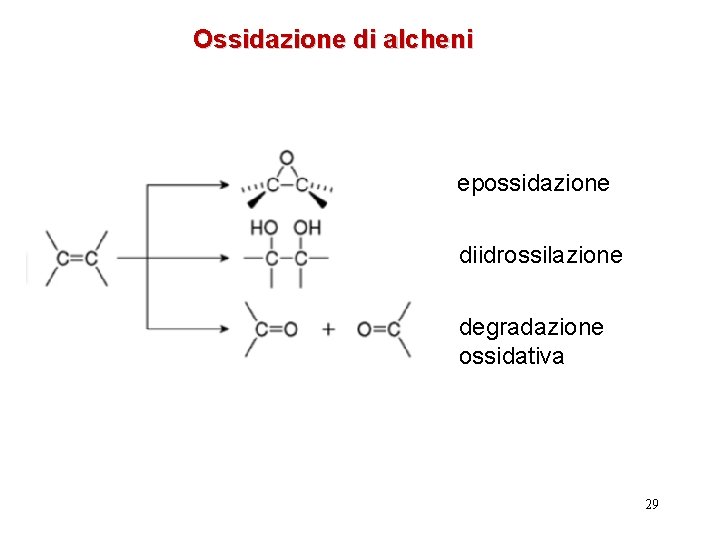
Ossidazione di alcheni epossidazione diidrossilazione degradazione ossidativa 29
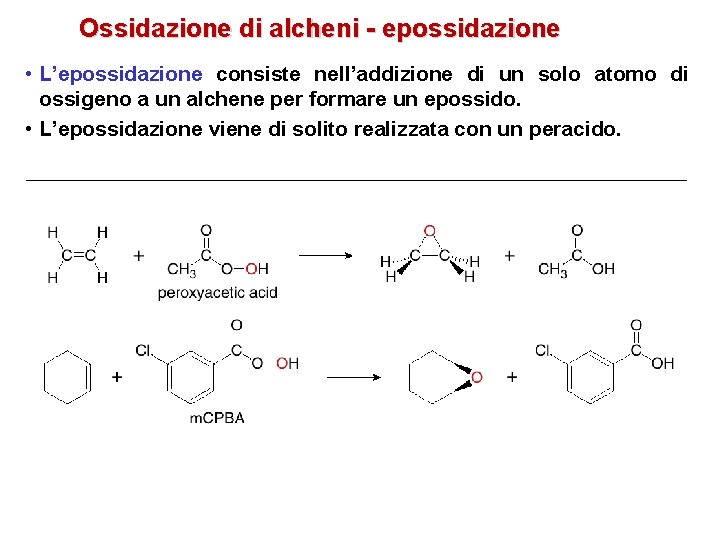
Ossidazione di alcheni - epossidazione • L’epossidazione consiste nell’addizione di un solo atomo di ossigeno a un alchene per formare un epossido. • L’epossidazione viene di solito realizzata con un peracido.
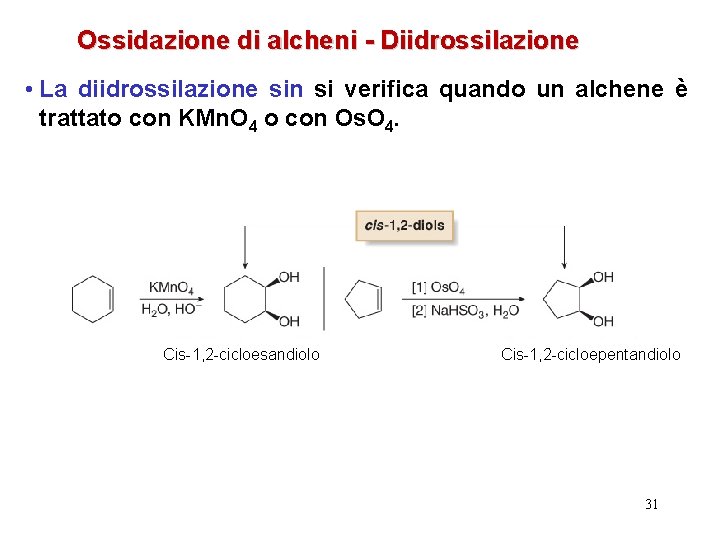
Ossidazione di alcheni - Diidrossilazione • La diidrossilazione sin si verifica quando un alchene è trattato con KMn. O 4 o con Os. O 4. Cis-1, 2 -cicloesandiolo Cis-1, 2 -cicloepentandiolo 31
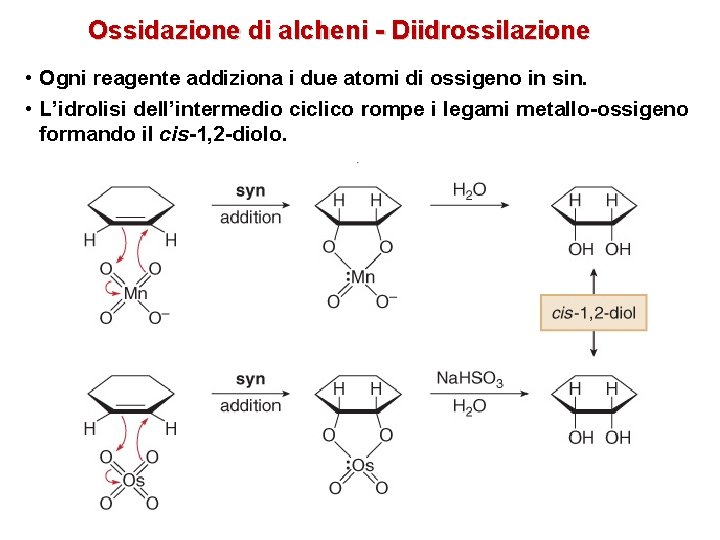
Ossidazione di alcheni - Diidrossilazione • Ogni reagente addiziona i due atomi di ossigeno in sin. • L’idrolisi dell’intermedio ciclico rompe i legami metallo-ossigeno formando il cis-1, 2 -diolo.
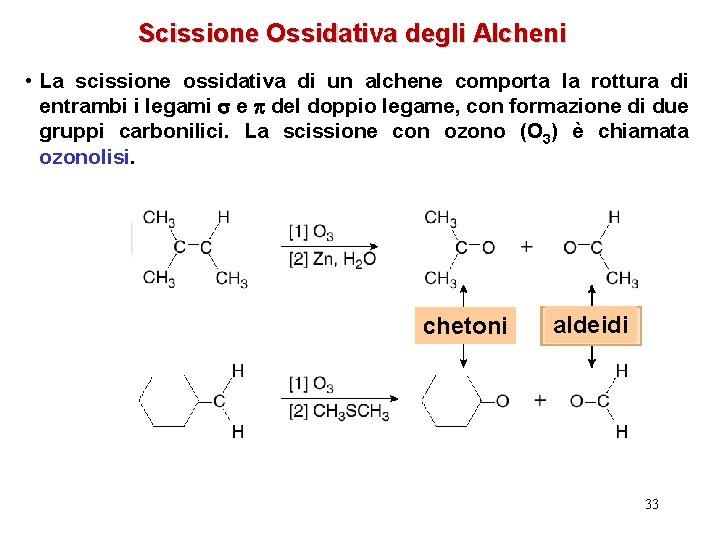
Scissione Ossidativa degli Alcheni • La scissione ossidativa di un alchene comporta la rottura di entrambi i legami e del doppio legame, con formazione di due gruppi carbonilici. La scissione con ozono (O 3) è chiamata ozonolisi. chetoni aldeidi 33
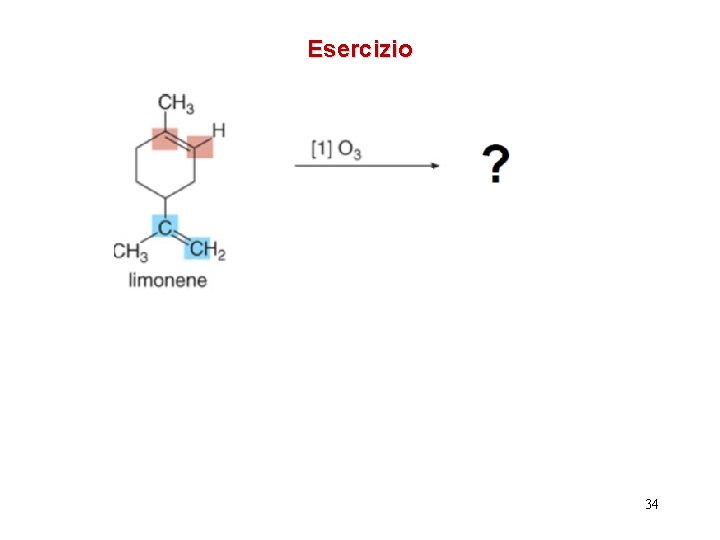
Esercizio 34

Alcheni in sintesi Problema Intermedio sintetico

36
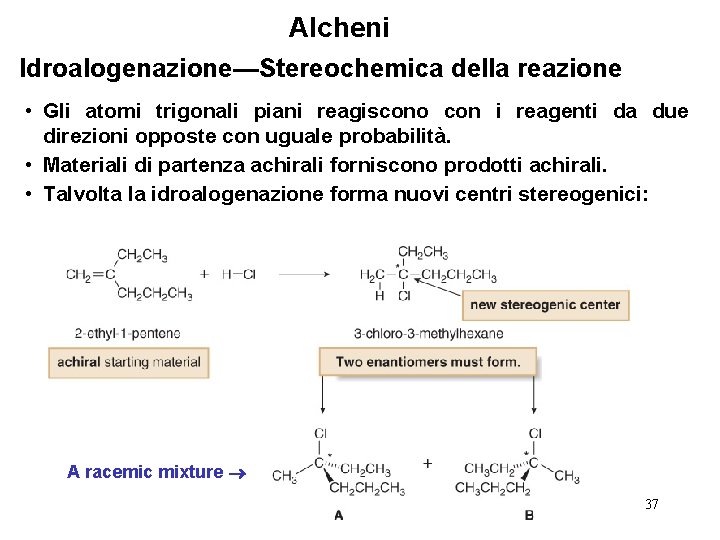
Alcheni Idroalogenazione—Stereochemica della reazione • Gli atomi trigonali piani reagiscono con i reagenti da due direzioni opposte con uguale probabilità. • Materiali di partenza achirali forniscono prodotti achirali. • Talvolta la idroalogenazione forma nuovi centri stereogenici: A racemic mixture 37

Alcheni Idroalogenazione—Stereochemica della reazione • Il meccanismo della idroalogenazione chiarisce il motivo della formazione di due enantiomeri. L’addizione iniziale di H+ avviene da entrambi i lati del piano del doppiolegame. • Entrambi i modi di addizione generano lo stesso carbocatione achirale. Si può utilizzare una qualunque delle rappresentazioni di queso carbocatione per disegnare il secondo stadio del meccanismo. 38

Alogenazione—Addizione di Alogeno • Gli alogeni si addizionano ai legami perche’ gli alogeni sono polarizzabili. • Il doppio legame elettron-ricco induce un dipolo in una molecola di alogeno adiacente, rendendo uno degli atomi di alogeno elettrondeficiente e l’altro elettron-ricco (X +-X ). • L’atomo di alogeno elettrofilo è quindi attratto dal doppio legame nucleofilo, rendendo possibile l’addizione. • L’evidenza dimostra che l’alogenazione segue un meccanismo diverso da quelli della idroalogenazione o della idratazione. Per esempio, l’addizione di Br 2 al cicloesene è di tipo anti, formando lo stereoisomero trans. Questo suggerisce che i carbocationi non sono degli intermedi delle alogenazioni. 39
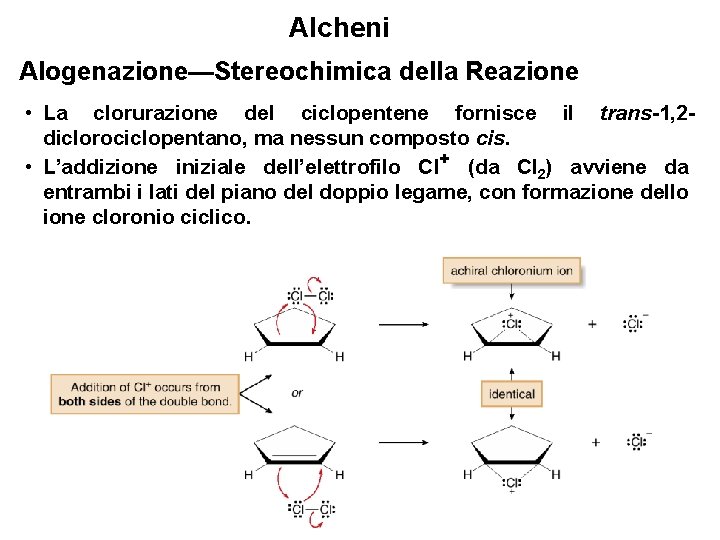
Alcheni Alogenazione—Stereochimica della Reazione • La clorurazione del ciclopentene fornisce il trans-1, 2 diclorociclopentano, ma nessun composto cis. • L’addizione iniziale dell’elettrofilo Cl+ (da Cl 2) avviene da entrambi i lati del piano del doppio legame, con formazione dello ione cloronio ciclico. 40
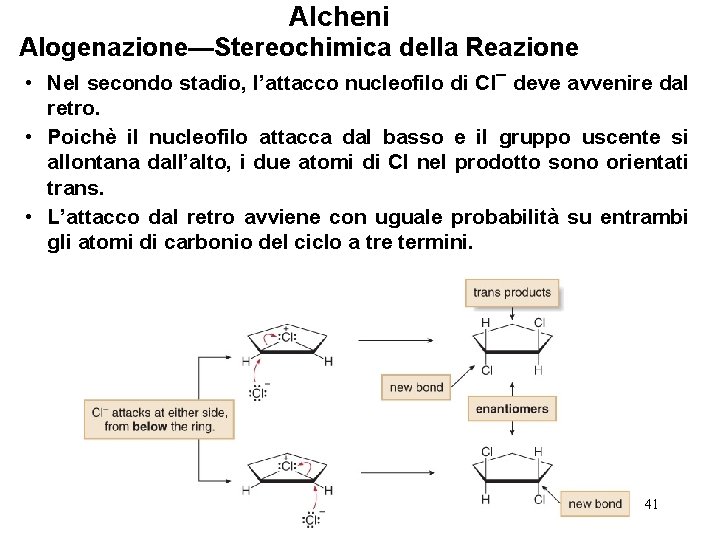
Alcheni Alogenazione—Stereochimica della Reazione • Nel secondo stadio, l’attacco nucleofilo di Cl¯ deve avvenire dal retro. • Poichè il nucleofilo attacca dal basso e il gruppo uscente si allontana dall’alto, i due atomi di Cl nel prodotto sono orientati trans. • L’attacco dal retro avviene con uguale probabilità su entrambi gli atomi di carbonio del ciclo a tre termini. 41
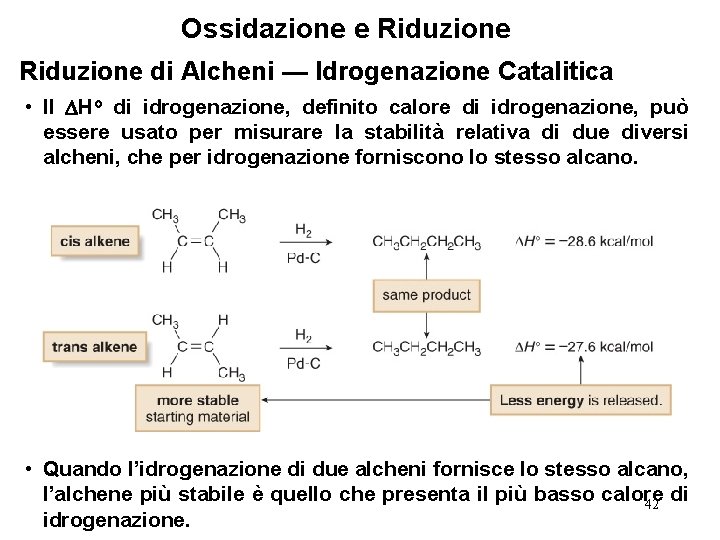
Ossidazione e Riduzione di Alcheni — Idrogenazione Catalitica • Il Ho di idrogenazione, definito calore di idrogenazione, può essere usato per misurare la stabilità relativa di due diversi alcheni, che per idrogenazione forniscono lo stesso alcano. • Quando l’idrogenazione di due alcheni fornisce lo stesso alcano, l’alchene più stabile è quello che presenta il più basso calore di 42 idrogenazione.
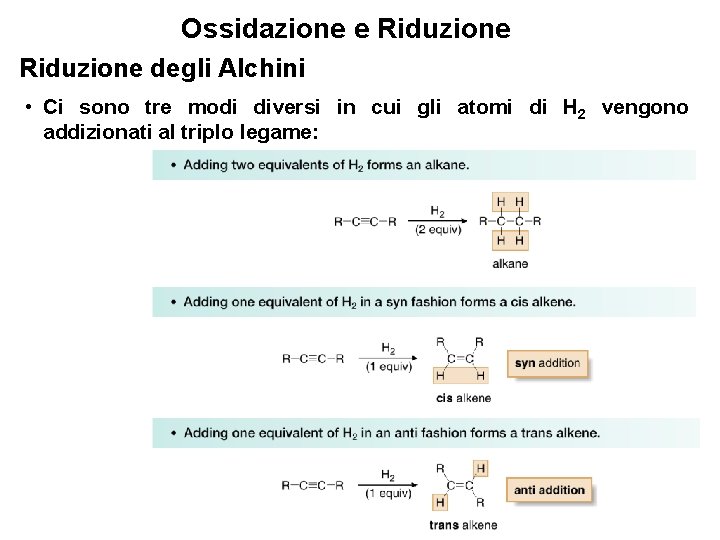
Ossidazione e Riduzione degli Alchini • Ci sono tre modi diversi in cui gli atomi di H 2 vengono addizionati al triplo legame: 43

Ossidazione e Riduzione Sommario delle Riduzioni degli Alchini Figura 12. 3 Sommario: Tre metodi per ridurre un triplo legame 44
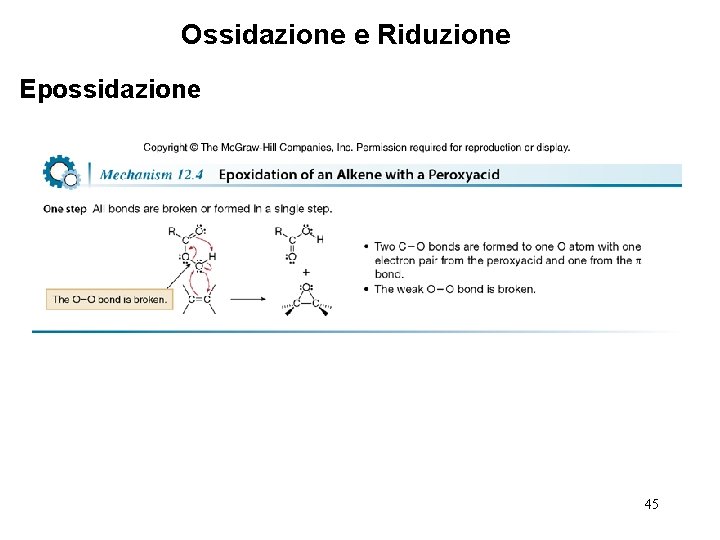
Ossidazione e Riduzione Epossidazione 45
- Slides: 45