QUMICA 10 1 QUMICA 10 2 QUMICA 10

























- Slides: 29

QUÍMICA 10 1

QUÍMICA 10 2

QUÍMICA 10 SUMÁRIO: Ordens de grandeza e escalas de comprimento. Dimensões à escala atómica e nanotecnologia. Constituição do átomo. Massa isotópica e massa atómica relativa média. Resolução de exercícios e problemas consolidação dos conteúdos lecionados. para 3

QUÍMICA 10 O ÁTOMO ORDEM DE GRANDEZA Potência de base dez mais próxima de um número escrito em notação científica. Escalas de comprimento e ordens de grandeza. 4

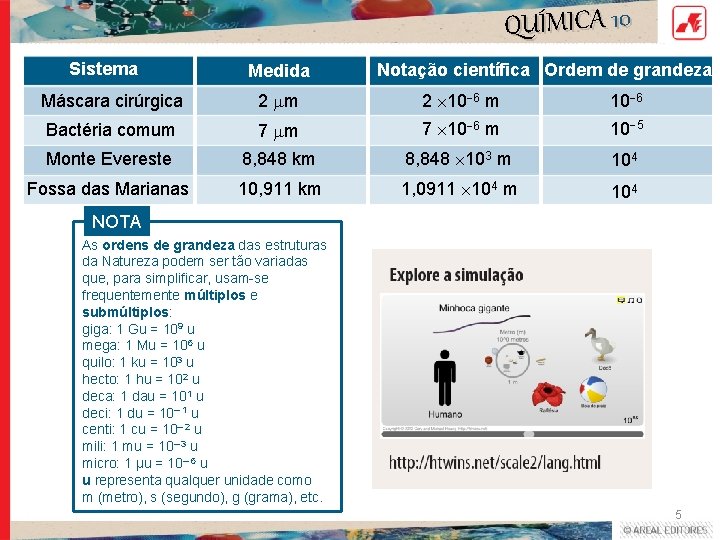
QUÍMICA 10 Sistema Medida Notação científica Ordem de grandeza Máscara cirúrgica 2 m 2 10 6 m 10 6 Bactéria comum 7 10 6 m 10 5 Monte Evereste 8, 848 km 8, 848 103 m 104 Fossa das Marianas 10, 911 km 1, 0911 104 m 104 NOTA As ordens de grandeza das estruturas da Natureza podem ser tão variadas que, para simplificar, usam-se frequentemente múltiplos e submúltiplos: giga: 1 Gu = 109 u mega: 1 Mu = 106 u quilo: 1 ku = 103 u hecto: 1 hu = 102 u deca: 1 dau = 101 u deci: 1 du = 10– 1 u centi: 1 cu = 10– 2 u mili: 1 mu = 10– 3 u micro: 1 μu = 10– 6 u u representa qualquer unidade como m (metro), s (segundo), g (grama), etc. 5

QUÍMICA 10 Exercício resolvido As estruturas que podem ser objeto de estudo da Química têm dimensões muito variadas. Por exemplo: A. Diâmetro da célula eucariótica: 40 m. B. Altura média de um ser humano: 1, 7 m. C. Raio médio da Terra: 6371 km. D. Diâmetro do Sol: 1, 39 Gm. Escreva cada um dos valores em notação científica na unidade do SI e indique a sua ordem de grandeza. Proposta de resolução A. 40 m = 40 10 6 m = 4, 0 10 5 m, logo é da ordem de grandeza 10 5. B. 1, 7 m = 1, 7 100 m, logo é da ordem de grandeza 100. C. 6371 km = 6371 103 m = 6, 371 106 m, logo é da ordem de grandeza 107. D. 1, 39 Gm = 1, 39 109 m, logo é da ordem de grandeza 109. 6

QUÍMICA 10 Exercício proposto Indique a ordem de grandeza e apresente cada um dos seguintes valores, em notação científica, na unidade do SI. A. Diâmetro médio do cabelo humano: 80 m. B. Comprimento de uma baleia azul: 30 m. C. Diâmetro da Lua: 3480 km. D. Distância da órbita da Lua à Terra: 384 Mm. Proposta de resolução A. 80 μm = 80 10– 6 m = 8, 0 10– 5 m, logo e da ordem de grandeza 10– 4; B. 30 m = 3, 0 101 m, logo e da ordem de grandeza 101; C. 3480 km = 3480 103 m = 3, 480 106 m, logo e da ordem de grandeza 106; D. 384 Mm = 384 106 m = 3, 84 108 m, logo e da ordem de grandeza 108. 7

QUÍMICA 10 DIMENSÕES À ESCALA ATÓMICA Numa laranja do tamanho da Terra, os átomos teriam o tamanho de cerejas e o núcleo atómico continuaria invisível; num átomo com a dimensão da maior cúpula do mundo, a da catedral de São Pedro, em Roma, o núcleo teria o tamanho de um grão de sal. NOTA As dimensões à escala atómica são tão reduzidas que é usual a utilização de outros submúltiplos como: nanómetro: 1 nm = 1 10 -9 m angstrom: 1 Å = 1 10 -10 m picómetro: 1 pm = 1 10 -12 m Ordem de grandeza dos raios das partículas – escala atómica. 8

QUÍMICA 10 Exercício resolvido Na figura ao lado observa-se uma camada de grafeno, obtida com microscópio de efeito de túnel, onde os pontos azuis desenhados representam os átomos de carbono. Qual é a ordem de grandeza da distância média entre os átomos de carbono, em unidade do SI? Proposta de resolução Como 1, 42 Å = 1, 42 10– 10 m e a ordem de grandeza é a potência de base 10 mais próxima do número, neste caso, a distância média entre os átomos de carbono é da ordem dos 10– 10 m. 9

QUÍMICA 10 Exercício proposto Com base na figura do exercício resolvido, qual seria a ordem de grandeza da distância média entre os átomos de carbono no grafeno se esse número fosse expresso em nanómetro? Proposta de resolução Como 1, 42 Å = 0, 142 nm = 1, 42 10 1 nm, a distância média entre os átomos de carbono é da ordem dos 10 1 nm. 10

QUÍMICA 10 NANOTECNOLOGIA A nanotecnologia dedica-se ao estudo da manipulação da matéria à escala atómica e molecular e permite o desenvolvimento de aplicações “alucinantes”. Dimensão do nanómetro 11

QUÍMICA 10 Exercício resolvido Transcreva, do texto Aplicar a Química: “Nanotecnologia”, das páginas 11 e 12 do manual, a afirmação que melhor define o conceito de nanotecnologia e identifique dois exemplos de aplicação desta tecnologia. Proposta de resolução A frase que melhor define o conceito de nanotecnologia é “A nanotecnologia dedica-se ao estudo da manipulação da matéria à escala atómica e molecular e permite aos engenheiros desenvolver aplicações “alucinantes” ”. São vários os exemplos de aplicação, podendo destacar-se a área da eletrónica e da computação, onde já foi possível criar um ecrã flexível, ou a área de engenharia dos materiais, com criação de materiais com propriedades extraordinárias como tecidos que regulam a temperatura e eliminam fungos e bactérias. 12

QUÍMICA 10 Exercício proposto Procure outros dois exemplos de notícias que surgiram recentemente sobre futuras aplicações da nanotecnologia. 13

QUÍMICA 10 CONSTITUIÇÃO DO ÁTOMO • A A existência primeira ideia de átomo na antiga Dalton, em 1808, retomou a surgiu teoria ado modelo de átomos continuava dividir os Grécia com Leucipo e Demócrito. atómico. cientistas ainda no início do séc. XX, até que, em 1905, Einstein provou a sua existência a partir da explicação do movimento browniano. Demócrito (460 a. C. -370 a. C. ) John Dalton (1766 -1844) Químico, físico e meteorologista inglês que impulsionou a teoria atómica. Albert Einstein (1879 -1955) Prémio Nobel da Física em 1921 pela sua contribuição na Física Teórica. 14

QUÍMICA 10 CONSTITUIÇÃO DO ÁTOMO • Uns anos antes, em 1897, Thomson descobriu o eletrão, partícula com carga negativa, com o tubo de raios catódicos e propôs o modelo do “pudim de passas”. Joseph Thomson (1856 -1940) Prémio Nobel da Física em 1906 pelas investigações sobre a condutividade elétrica em gases. Modelo atómico proposto por Thomson: modelo do “pudim de passas”. 15

QUÍMICA 10 CONSTITUIÇÃO DO ÁTOMO • Utilizando Em 1932, um Chadwick feixe decomprovou partículas alfa, que Rutherford no núcleo também percebeu existem que a maior partesem partículas do volume carga edocom átomo massa era, semelhante na realidade, aoespaço protão vazio, – os propondo o modelo planetário. neutrões. Ernest Rutherford James Chadwick (1871 -1937) Prémio Nobel da Química em 1908 pelas investigações sobre desintegração de elementos químicos. (1891 -1974) Prémio Nobel da Física em 1935 pela descoberta do neutrão. Modelo atómico proposto por Rutherford: “modelo planetário”. 16

QUÍMICA 10 O ÁTOMO TABELA I – PROPRIEDADES DAS PARTÍCULAS SUBATÓMICAS Nome (símbolo) Carga Massa / u Localização Protão (p+) +1 1, 00728 Núcleo Neutrão (n 0) 0 1, 00866 Núcleo Eletrão (e ) 1 0, 00054858 Em torno do núcleo CARGA NUCLEAR Carga do núcleo do átomo, positiva e igual à soma das cargas dos protões. 17

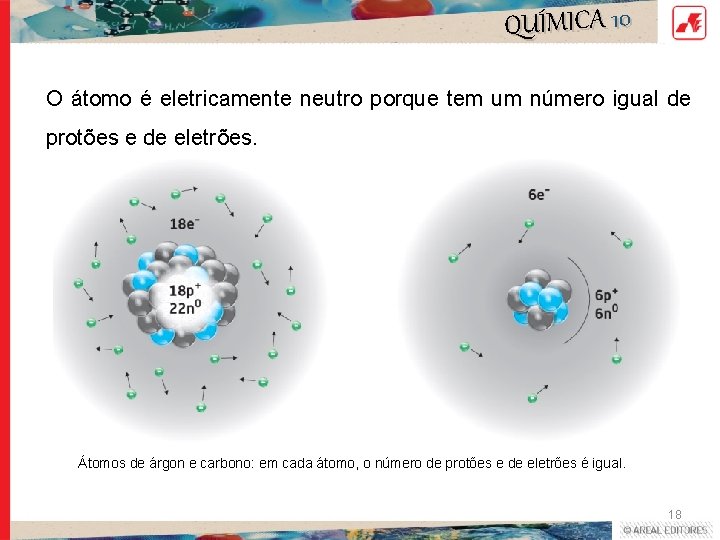
QUÍMICA 10 O átomo é eletricamente neutro porque tem um número igual de protões e de eletrões. Átomos de árgon e carbono: em cada átomo, o número de protões e de eletrões é igual. 18

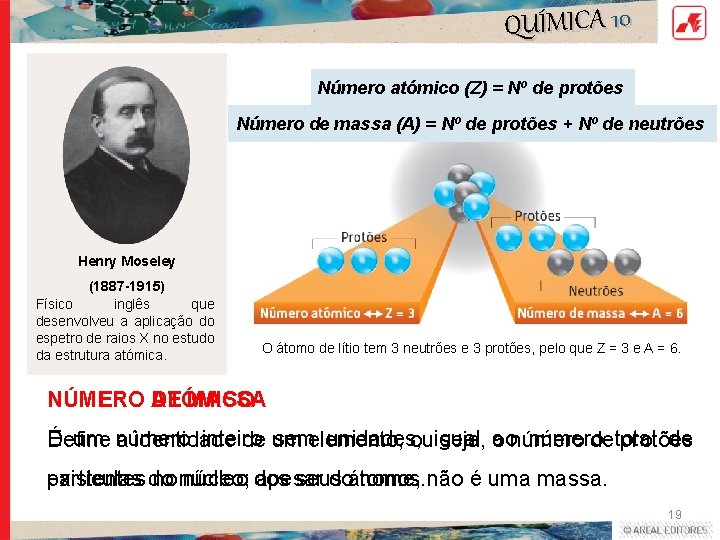
QUÍMICA 10 Número atómico (Z) = Nº de protões Número de massa (A) = Nº de protões + Nº de neutrões • Moseley, em 1913, determinou o número de cargas Henry Moseley (1887 -1915) Físico inglês que desenvolveu a aplicação do espetro de raios X no estudo da estrutura atómica. positivas no núcleo atómico, atualmente designado de número atómico (Z). O átomo de lítio tem 3 neutrões e 3 protões, pelo que Z = 3 e A = 6. NÚMERO DE MASSA ATÓMICO É um número inteiro semelemento, unidades, aonúmero de Define a identidade de um ouigual seja, o de total protões partículas apesar doátomos. nome, não é uma massa. existentes do no núcleo; núcleo dos seus 19

QUÍMICA 10 Representação de um átomo de um elemento químico. 20

QUÍMICA 10 ISÓTOPOS Átomos do mesmo elemento (têm, portanto, o mesmo número atómico) com diferentes números de neutrões, apresentando, por isso, números de massa distintos. Francis William Aston (1877 -1945) Prémio Nobel da Química em 1922 pela descoberta dos isótopos de um grande número de elementos químicos. O hidrogénio tem três isótopos com números de massa 1, 2 e 3 (contendo 0, 1 e 2 neutrões, respetivamente) designados prótio, deutério e trítio. 21

QUÍMICA 10 Exercício resolvido Considere os átomos a seguir representados: Nota: as letras X, Y, R, W não representam os símbolos verdadeiros dos elementos químicos. 1. Indique o número de protões, o número de neutrões, o número de eletrões e a carga nuclear do átomo R. 2. Quantos elementos químicos estão representados? Proposta de resolução 1. O número de protões é igual ao número atómico, logo, é 6; Para o átomo ser eletricamente neutro, o número de eletrões deverá ser igual, ou seja, 6; O número de neutrões (n) pode ser obtido pela expressão: n = A - Z = 8; A carga nuclear é determinada pelo número de protões, logo, é + 6. 22

QUÍMICA 10 Exercício resolvido Considere os átomos a seguir representados: Nota: as letras X, Y, R, W não representam os símbolos verdadeiros dos elementos químicos. 1. Indique o número de protões, o número de neutrões, o número de eletrões e a carga nuclear do átomo R. 2. Quantos elementos químicos estão representados? Proposta de resolução 2. Cada elemento químico tem um único número atómico que o identifica. Por isso, os 4 átomos apresentados referem-se apenas a 3 elementos diferentes, uma vez que os átomos Y e W pertencem ao mesmo elemento (Z = 17), sendo isótopos entre si. 23

QUÍMICA 10 Exercício proposto Considere os átomos. Atendendo à constituição destes átomos, indique o que têm em comum entre si. Proposta de resolução O átomo de carbono-14 é constituído por 6 protões, 6 eletrões e 8 neutrões enquanto o átomo de oxigénio-16 é constituído por 8 protões, 8 eletrões e 8 neutrões, logo, têm igual número de neutrões. Átomo de oxigénio-14 tem 8 protões, 8 eletrões e 6 neutrões, logo, tem igual número de protões e eletrões que o átomo de oxigénio-16 uma vez que possuem o mesmo número atómico e são isótopos. Em relação ao carbono-14, o oxigénio-14 tem apenas em comum o número de massa, ou seja, o número de nucleões. 24

QUÍMICA 10 MASSA ATÓMICA RELATIVA É o número de vezes que a massa de um átomo é maior do que 1/12 da massa do átomo do isótopo carbono-12. A massa atómica relativa é uma grandeza adimensional. MASSA ISOTÓPICA RELATIVA É a massa atómica relativa de um isótopo de um dado elemento que se define como o número de vezes que a massa atómica do isótopo desse elemento é maior do que 1/12 da massa atómica do isótopo carbono-12. 25

QUÍMICA 10 MASSA ATÓMICA RELATIVA MÉDIA DE UM ELEMENTO É a massa atómica relativa de um elemento e corresponde à média ponderada das massas isotópicas dos vários isótopos de um elemento químico que se encontram na Natureza. TABELA II – MASSAS ATÓMICAS RELATIVAS E ABUND NCIA DOS ISÓTOPOS DO CLORO Isótopo Massa isotópica relativa Abundância natural / % 35 Cℓ 34, 97 75, 8 37 Cℓ 36, 97 24, 2 Ar (Cℓ) = 34, 97 0, 758 + 36, 97 0, 242 = 35, 45 26

QUÍMICA 10 A massa atómica relativa média de um elemento pode ser consultada na Tabela Periódica. • O valor obtido não é um número inteiro, pois resulta de uma média ponderada; • O resultado é mais próximo da massa atómica relativa do isótopo mais abundante, pois tem maior peso na média do que a do isótopo menos abundante. 27

QUÍMICA 10 Exercício resolvido O cobre (29 Cu) é formado pelos isótopos cobre-63 e cobre-65, representando o primeiro 69, 09% da massa total de cobre. Sabendo que a massa atómica relativa média do cobre é 63, 55 e que a massa isotópica relativa do 63 Cu é 62, 93, calcule para o outro isótopo: a) a abundância relativa; b) a massa isotópica relativa. Proposta de resolução a) A abundância natural do isótopo é: 65 Cu = 100% 69, 09% = 30, 91% b) 28

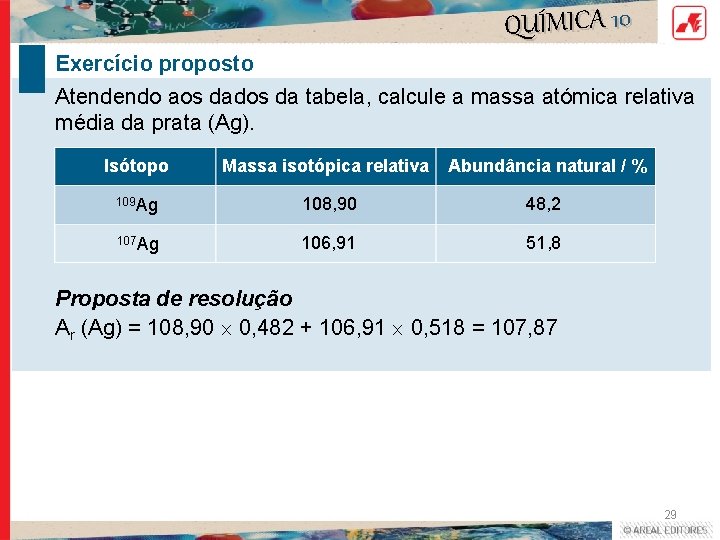
QUÍMICA 10 Exercício proposto Atendendo aos dados da tabela, calcule a massa atómica relativa média da prata (Ag). Isótopo Massa isotópica relativa Abundância natural / % 109 Ag 108, 90 48, 2 107 Ag 106, 91 51, 8 Proposta de resolução Ar (Ag) = 108, 90 0, 482 + 106, 91 0, 518 = 107, 87 29