a qumica da vida Biologia Qumica Biolgica Qumica

É a química da vida! Biologia Química Biológica Química Fisiológica Biologia Molecular Química É a ciência que faz a conexão entre a biologia e a química A vida, no seu nível mais básico é, essencialmente, um fenômeno bioquímico É a base para disciplinas como: Química de Alimentos, Nutrição, Microbiologia, Engenharia Bioquímica, Toxicologia etc.

A bioquímica, naturalmente, lida com as moléculas encontradas nos organismos (e alimentos), chamadas de BIOMOLÉCULAS; são elas, basicamente: a) Aminoácidos que formam polímeros chamados peptídeos e PROTEÍNAS b) Carboidratos que formam polímeros chamados POLISSACARÍDEOS ou carboidratos complexos c) Gorduras (LIPÍDEOS), que podem formar estruturas supra-moleculares

d) Bases nitrogenadas que formam a base de polímeros chamados ÁCIDOS NUCLÉICOS e) Muitos outros compostos orgânicos, e. g. , ácidos carboxílicos f) Compostos inorgânicos como CO 2, NH 3, O 2, e sobretudo ÁGUA, além de íons como Fe 2+, Ca 2+, Mg 2+, Na+, K+, Cl-, etc.

É extremamente vasta! Aumenta cada mês em milhares de páginas! Simplificadamente podemos dividí-la em livros-texto, artigos de revisão e artigos de pesquisa 1) A. L. Lehninger, D. L. Nelson, M. M. Cox, Princípios de Bioquímica. 2) Marzzoco; Torres. Bioquímica Básica. 3) Harper. Bioquímica. 4) Champe. Bioquímica Ilustrada 5) A. Bracht, E. L. Ishii-Iwamoto, Métodos de Laboratório em Bioquímica

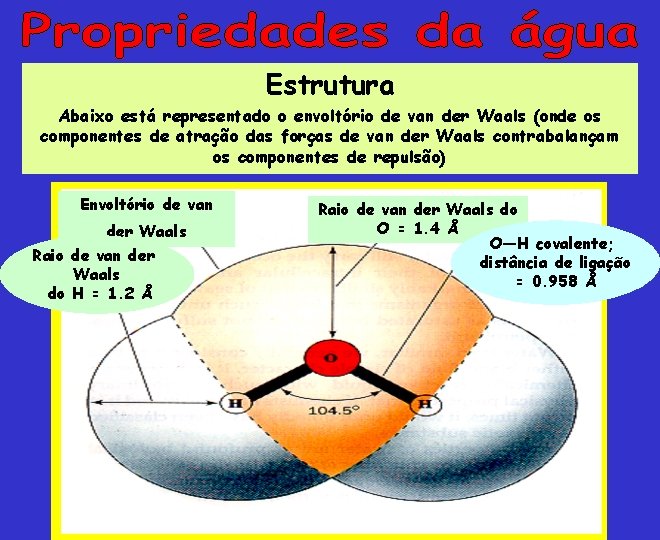
Estrutura Abaixo está representado o envoltório de van der Waals (onde os componentes de atração das forças de van der Waals contrabalançam os componentes de repulsão) Envoltório de van der Waals Raio de van der Waals do H = 1. 2 Å Raio de van der Waals do O = 1. 4 Å O—H covalente; distância de ligação = 0. 958 Å




Por quê a água dissolve sais? A estrutura cristalina dos sais é mantida por forças iônicas;
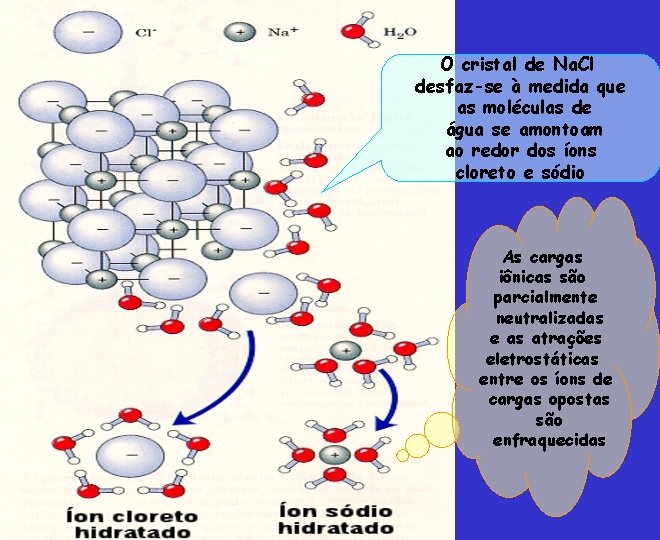
O cristal de Na. Cl desfaz-se à medida que as moléculas de água se amontoam ao redor dos íons cloreto e sódio As cargas iônicas são parcialmente neutralizadas e as atrações eletrostáticas entre os íons de cargas opostas são enfraquecidas

Solventes com altas constantes dielétricas podem solvatar (“envolver”; no caso da água “hidratar”) as moléculas do soluto, conforme ilustrado pelo esquema abaixo:
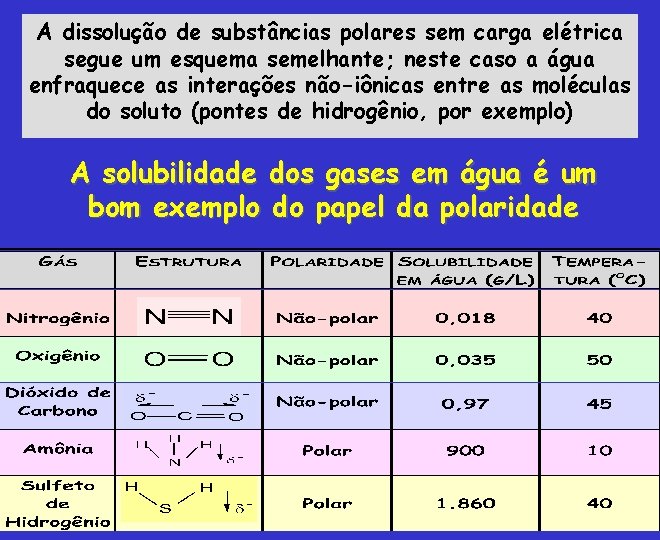
A dissolução de substâncias polares sem carga elétrica segue um esquema semelhante; neste caso a água enfraquece as interações não-iônicas entre as moléculas do soluto (pontes de hidrogênio, por exemplo) A solubilidade dos gases em água é um bom exemplo do papel da polaridade
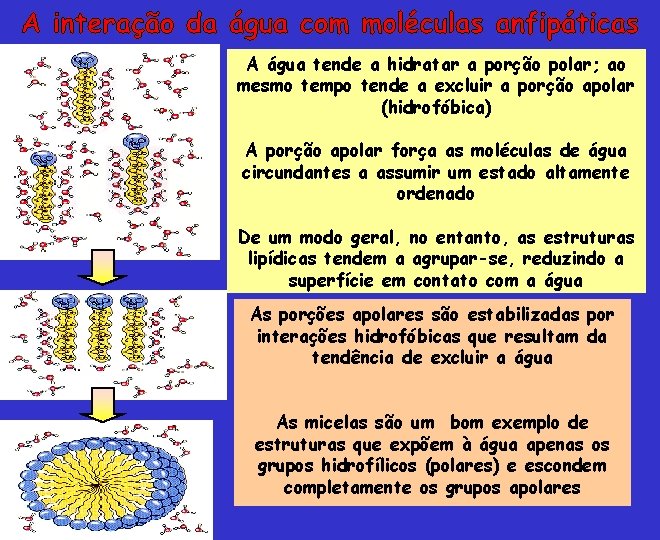
A água tende a hidratar a porção polar; ao mesmo tempo tende a excluir a porção apolar (hidrofóbica) A porção apolar força as moléculas de água circundantes a assumir um estado altamente ordenado De um modo geral, no entanto, as estruturas lipídicas tendem a agrupar-se, reduzindo a superfície em contato com a água As porções apolares são estabilizadas por interações hidrofóbicas que resultam da tendência de excluir a água As micelas são um bom exemplo de estruturas que expõem à água apenas os grupos hidrofílicos (polares) e escondem completamente os grupos apolares
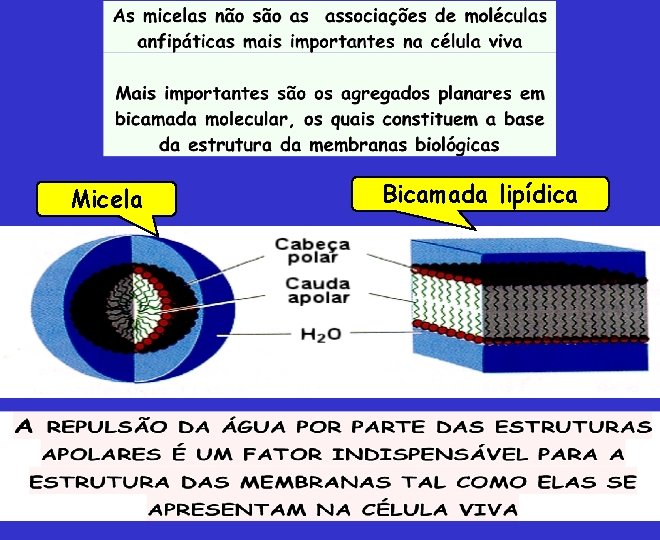
Micela Bicamada lipídica

Uma característica importante da água é que as suas moléculas estão constantemente reagindo entre si da seguinte maneira: Salto protônico Isto significa que em qualquer solução aquosa sempre haverá uma certa quantidade do íon hidrônio (H 3 O+) e do íon hidroxila (HO ) Estes íons tem grande mobilidade, maior que a dos outros íons, pois os prótons saltam de uma molécula para outra.
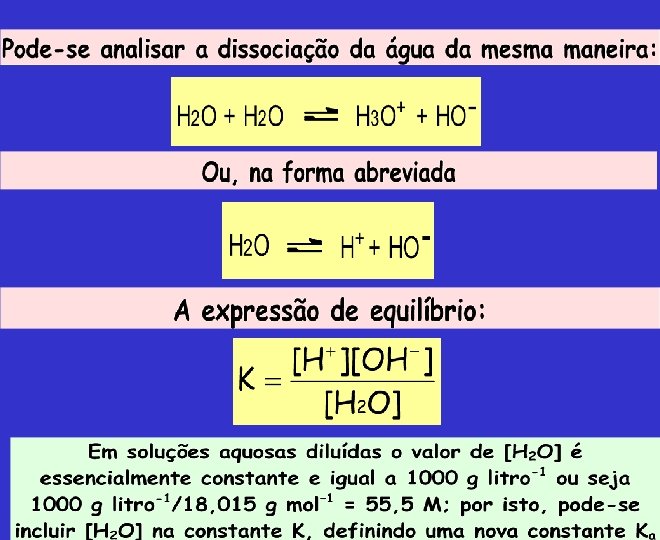


A escala de p. H é prática e costuma ser usada entre 0 e 14 Na água pura p. H = log[H+] = log(10 7)= 7 Também na água pura: p. OH = 14 – p. H = 14 – 7 = 7
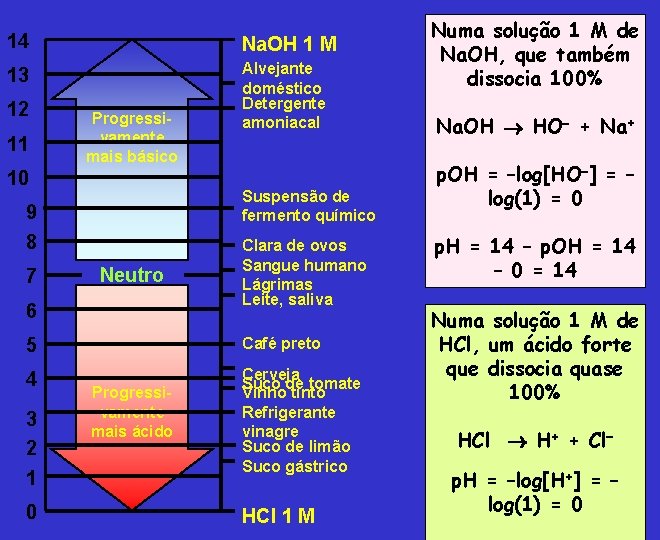
14 Na. OH 1 M 13 Alvejante doméstico Detergente amoniacal 12 11 Progressivamente mais básico 10 Suspensão de fermento químico 9 8 7 Neutro 6 Clara de ovos Sangue humano Lágrimas Leite, saliva 5 Café preto 4 Cerveja Suco de tomate Vinho tinto Refrigerante vinagre Suco de limão Suco gástrico 3 2 1 0 Progressivamente mais ácido HCl 1 M Numa solução 1 M de Na. OH, que também dissocia 100% Na. OH HO + Na+ p. OH = –log[HO ] = – log(1) = 0 p. H = 14 – p. OH = 14 – 0 = 14 Numa solução 1 M de HCl, um ácido forte que dissocia quase 100% HCl H+ + Cl p. H = –log[H+] = – log(1) = 0

ou, rearranjando



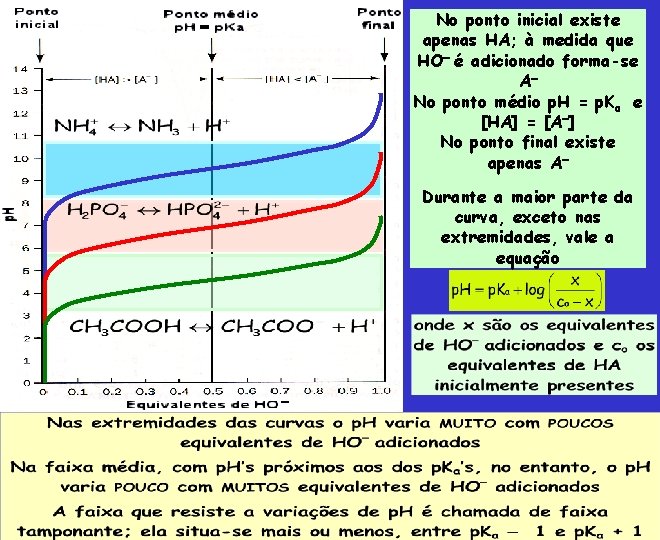
No ponto inicial existe apenas HA; à medida que HO é adicionado forma-se A No ponto médio p. H = p. Ka e [HA] = [A ] No ponto final existe apenas A Durante a maior parte da curva, exceto nas extremidades, vale a equação
- Slides: 25