METODY SPEKTROSKOPOWE Spektroskopi nazywa si zesp metod badawczych

METODY SPEKTROSKOPOWE

Spektroskopią nazywa się zespół metod badawczych i analitycznych, które zajmują się badaniem niesprężystego oddziaływania promieniowania elektromagnetycznego lub cząsteczkowego z materią. W wyniku takiego oddziaływania zachodzi wymiana energii i energia może ulegać różnym procesom np. absorpcji, emisji, , rozproszeniu. W zależności od właściwości materii i energii promieniowania oddziaływania między nimi mogą mieć różny charakter i mogą im towarzyszyć różne procesy. Spektroskopia zajmuje się teorią i interpretacją widm powstających w wyniku oddziaływań między promieniowaniem a materią. Podziału metod spektroskopowych można dokonać według: zakresu promieniowania elektromagnetycznego (długość fali (częstotliwość promieniowania)), rodzaju układu materialnego, formy wymiany energii między promieniowaniem a materią (zjawiska zachodzące w układzie).
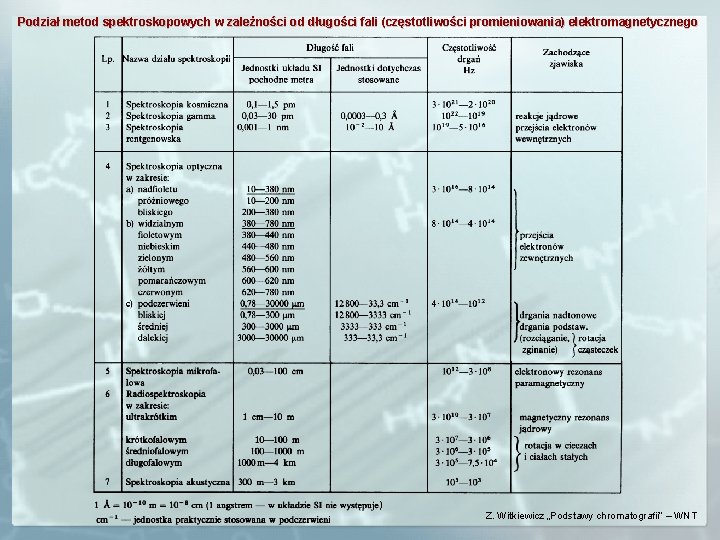
Podział metod spektroskopowych w zależności od długości fali (częstotliwości promieniowania) elektromagnetycznego Z. Witkiewicz „Podstawy chromatografii” – WNT
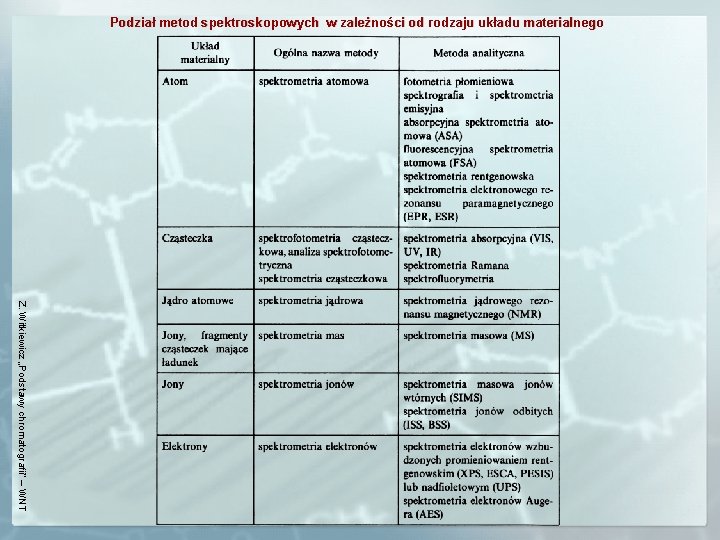
Podział metod spektroskopowych w zależności od rodzaju układu materialnego Z. Witkiewicz „Podstawy chromatografii” – WNT
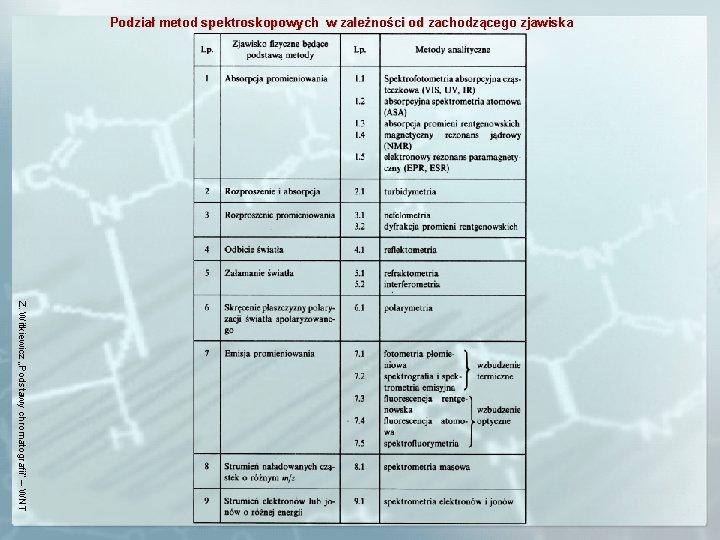
Podział metod spektroskopowych w zależności od zachodzącego zjawiska Z. Witkiewicz „Podstawy chromatografii” – WNT

SPEKTROFOTOMETRIA ABSORPCYJNA CZĄSTECZKOWA SPEKTROFOTOMETRIA UV/VIS

Spektrofotometrię dzieli się pod względem długości zastosowanego promieniowania na trzy podstawowe działy: spektrofotometria w nadfiolecie – UV 200 -380 nm, spektrofotometria w świetle widzialnym – VIS 380 -780 nm, spektrofotometria w podczerwieni – IR 1 -16 m. Spektrofotometria absorpcyjna UV/VIS jest metodą wykorzystującą do celów analitycznych zjawisko absorpcji promieniowania elektromagnetycznego w zakresie UV/VIS przez cząsteczki substancji absorbującej co prowadzi do przejść elektronów walencyjnych między poziomami energetycznymi. W zakresie UV/VIS efekty absorpcji zachodzą w związkach organicznych, w których występują ugrupowania atomów z wiązaniami wielokrotnymi zawierającymi wolne elektrony .
![Kolor widziany, a długość fali pochłanianego promieniowania max [nm] kolor zaabsorbowany kolor obserwowany 380 Kolor widziany, a długość fali pochłanianego promieniowania max [nm] kolor zaabsorbowany kolor obserwowany 380](http://slidetodoc.com/presentation_image_h/c190838b7309cf38700f33abaeeac457/image-8.jpg)
Kolor widziany, a długość fali pochłanianego promieniowania max [nm] kolor zaabsorbowany kolor obserwowany 380 -420 fioletowy żółtozielony 420 -440 fioletowoniebieski żółty 440 -470 niebieski pomarańczowy 470 -500 niebieskozielony czerwony 500 -520 zielony purpurowy 520 -550 żółto-zielony fioletowy 550 -580 żółty fioletowoniebieski 580 -620 pomarańczowy niebieski 620 -680 czerwony zielononiebieski 680 -780 czerwony zielony
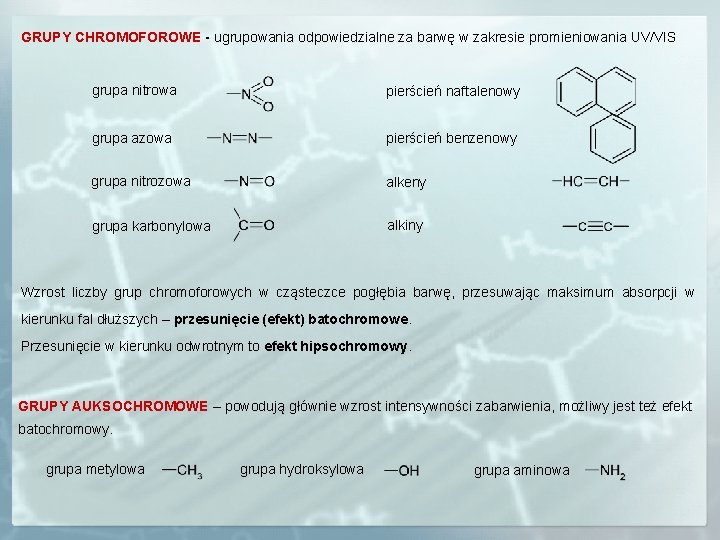
GRUPY CHROMOFOROWE - ugrupowania odpowiedzialne za barwę w zakresie promieniowania UV/VIS grupa nitrowa pierścień naftalenowy grupa azowa pierścień benzenowy grupa nitrozowa alkeny grupa karbonylowa alkiny Wzrost liczby grup chromoforowych w cząsteczce pogłębia barwę, przesuwając maksimum absorpcji w kierunku fal dłuższych – przesunięcie (efekt) batochromowe. Przesunięcie w kierunku odwrotnym to efekt hipsochromowy. GRUPY AUKSOCHROMOWE – powodują głównie wzrost intensywności zabarwienia, możliwy jest też efekt batochromowy. grupa metylowa grupa hydroksylowa grupa aminowa
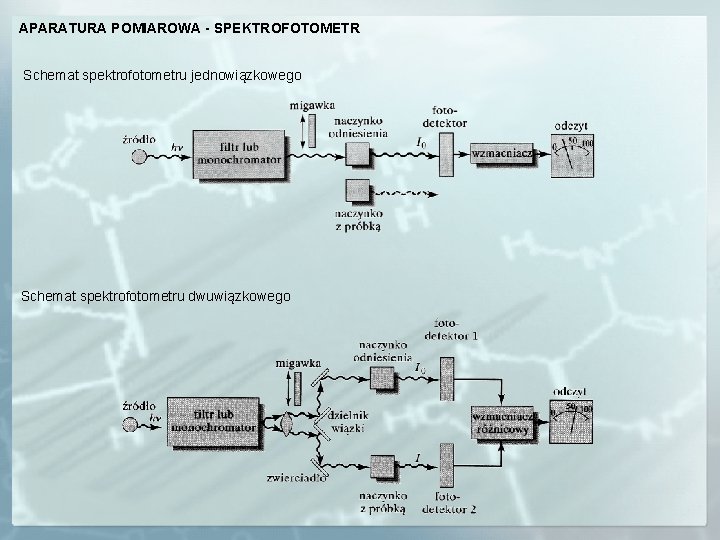
APARATURA POMIAROWA - SPEKTROFOTOMETR Schemat spektrofotometru jednowiązkowego Schemat spektrofotometru dwuwiązkowego
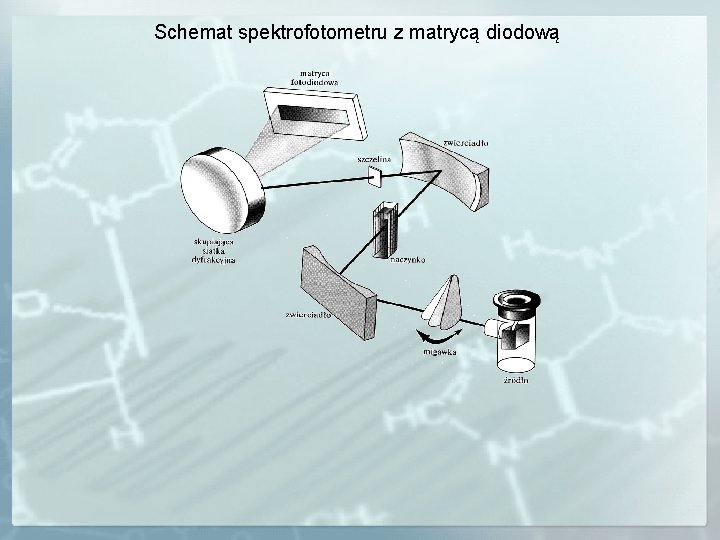
Schemat spektrofotometru z matrycą diodową
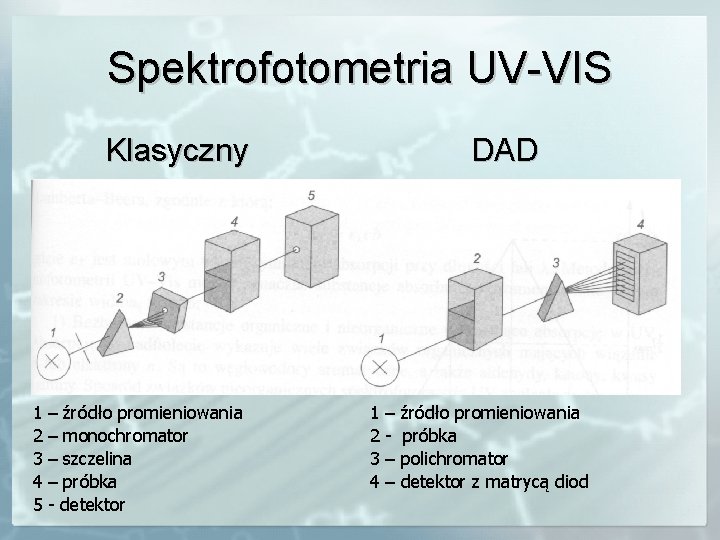
Spektrofotometria UV-VIS Klasyczny DAD 1 2 3 4 5 – źródło promieniowania – monochromator – szczelina – próbka - detektor 1 2 3 4 – – – źródło promieniowania próbka polichromator detektor z matrycą diod

Z padającej na warstwę roztworu równoległej wiązki promieniowania monochromatycznego część ulega: absorpcji, odbiciu, rozproszeniu. b Io It Ir Io – natężenie promieniowania padającego, It – natężenie promieniowania po przejściu przez warstwę absorbującą, Ir – natężenie promieniowania rozproszonego, b – grubość warstwy pochłaniającej,
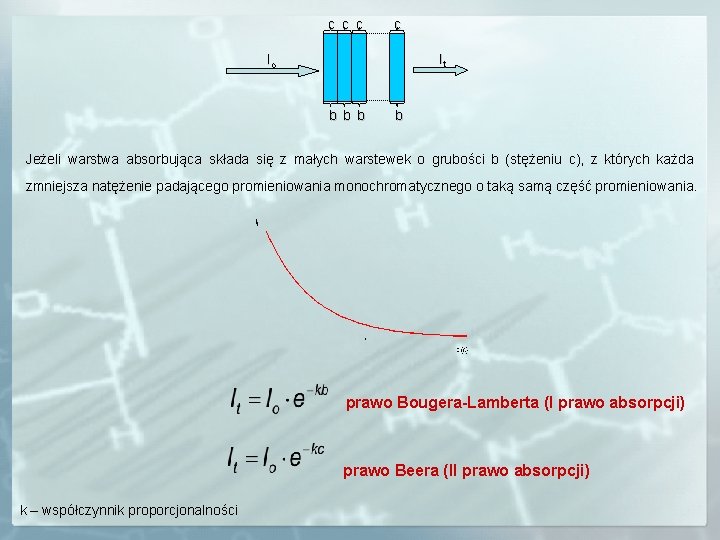
c c It Io b b Jeżeli warstwa absorbująca składa się z małych warstewek o grubości b (stężeniu c), z których każda zmniejsza natężenie padającego promieniowania monochromatycznego o taką samą część promieniowania. prawo Bougera-Lamberta (I prawo absorpcji) prawo Beera (II prawo absorpcji) k – współczynnik proporcjonalności

Prawo Bougera-Lamberta-Beera Natężenie promieniowania monochromatycznego przechodzącego przez ośrodek absorbujący jest wprost proporcjonalne do natężenia promieniowania padającego i maleje wykładniczo wraz z liniowym wzrostem grubości warstwy absorbującej i stężenia. k’ – współczynnik proporcjonalności wyrażający absorbancję jaką wykazuje roztwór przy jednostkowej grubości warstwy pochłaniającej i jednostkowym stężeniu. T transmitancja A absorbancja

dla stężenia c wyrażonego w mol·l-1 k’ = e molowy współczynnik absorpcji Jest liczbową miarą czułości metod spektrofotometrycznych Czułość metody spektrofotometrycznej = d. A/dc Absorbancja zależy od: stężenia substancji, grubości warstwy pochłaniającej, molowego współczynnika absorpcji Molowy współczynnik absorpcji zależy od: rodzaju substancji, długości fali przy której wykonuje się pomiary, Absorpcja – zjawisko fizyczne polegające na pochłanianiu promieniowania lub substancji w całej objętości absorbentu Absorbancja – wielkość fizykochemiczna (bezwymiarowa) Adsorpcja – powierzchniowe zagęszczanie substancji na granicy dwóch faz
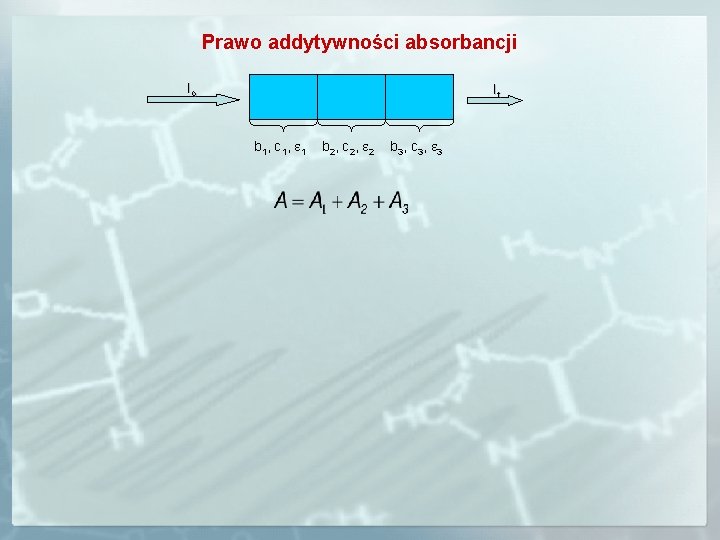
Prawo addytywności absorbancji Io It b 1, c 1, e 1 b 2, c 2, e 2 b 3, c 3, e 3
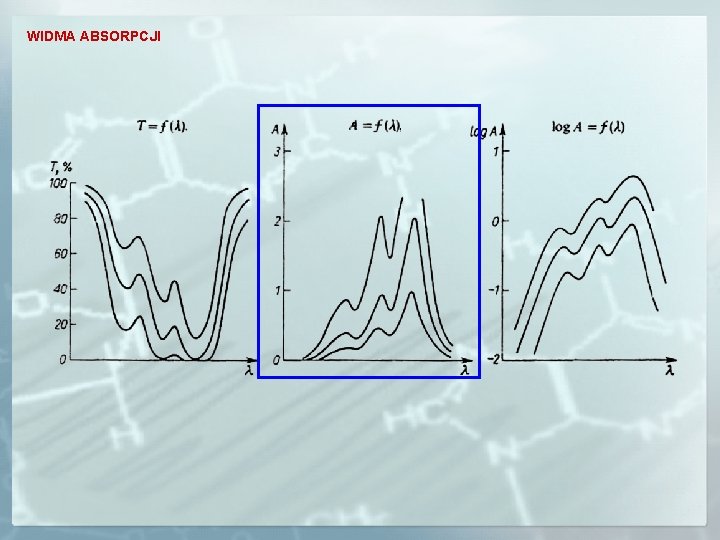
WIDMA ABSORPCJI
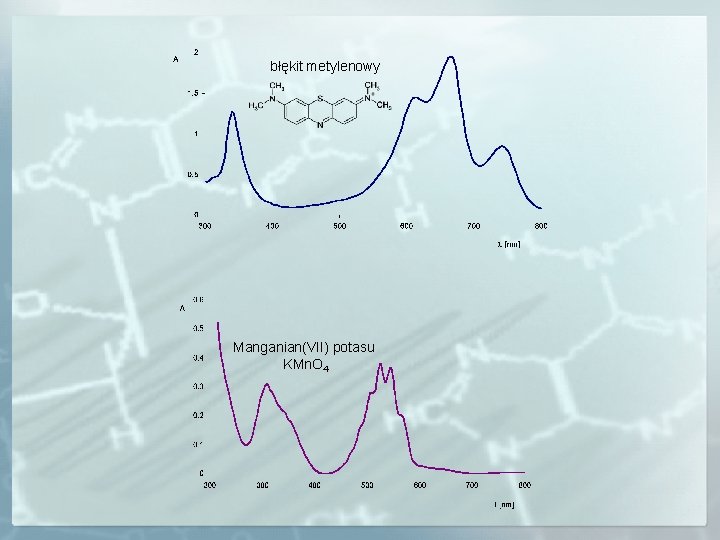
błękit metylenowy Manganian(VII) potasu KMn. O 4

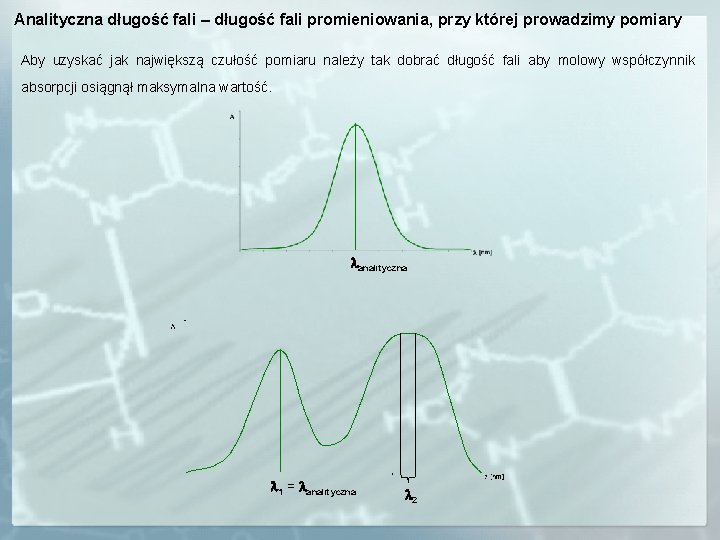
Analityczna długość fali – długość fali promieniowania, przy której prowadzimy pomiary Aby uzyskać jak największą czułość pomiaru należy tak dobrać długość fali aby molowy współczynnik absorpcji osiągnął maksymalna wartość. analityczna 1 = analityczna 2
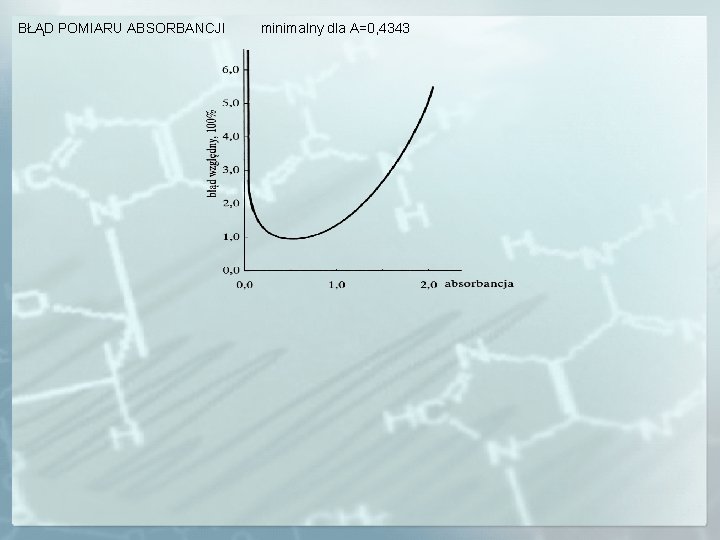
BŁĄD POMIARU ABSORBANCJI minimalny dla A=0, 4343
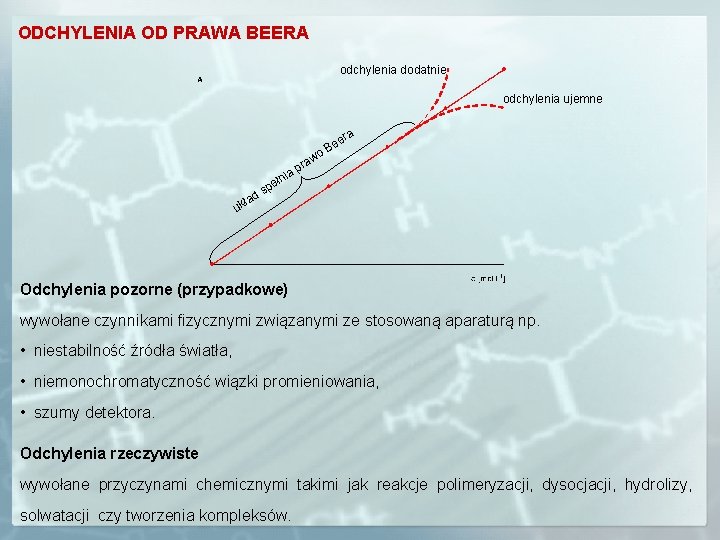
ODCHYLENIA OD PRAWA BEERA odchylenia dodatnie odchylenia ujemne ra e Be o raw p ia ełn uk p d s ła Odchylenia pozorne (przypadkowe) wywołane czynnikami fizycznymi związanymi ze stosowaną aparaturą np. • niestabilność źródła światła, • niemonochromatyczność wiązki promieniowania, • szumy detektora. Odchylenia rzeczywiste wywołane przyczynami chemicznymi takimi jak reakcje polimeryzacji, dysocjacji, hydrolizy, solwatacji czy tworzenia kompleksów.
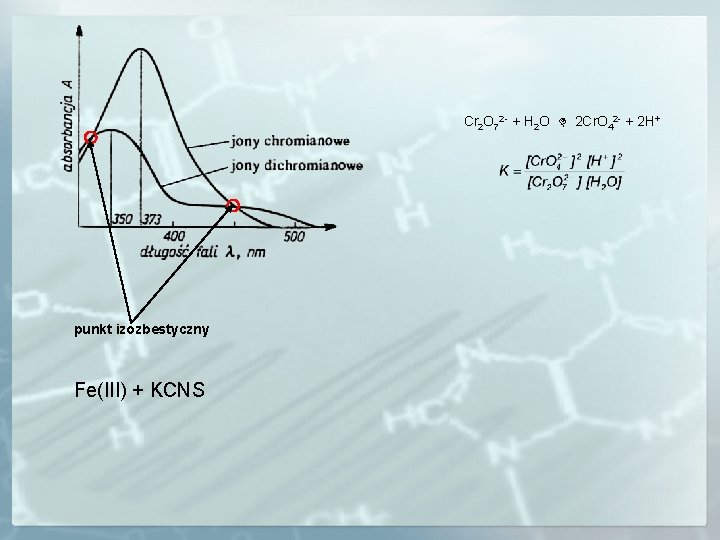
Cr 2 O 72 - + H 2 O 2 Cr. O 42 - + 2 H+ punkt izozbestyczny Fe(III) + KCNS
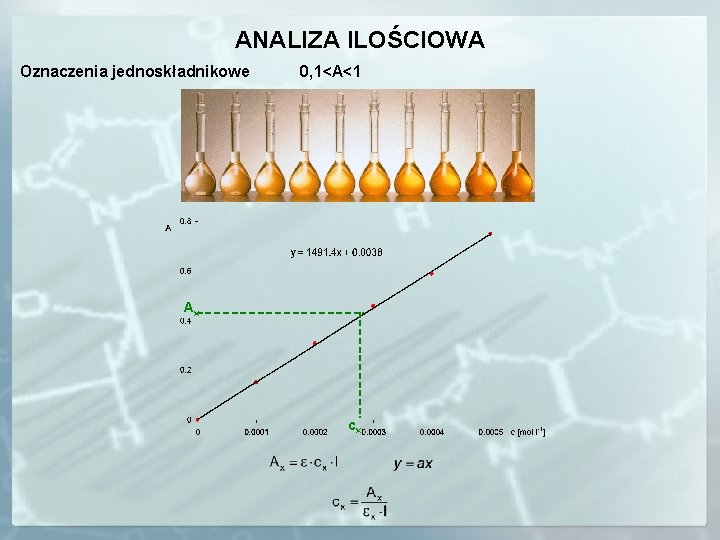
ANALIZA ILOŚCIOWA Oznaczenia jednoskładnikowe 0, 1<A<1 Ax cx

ANALIZA ILOŚCIOWA • Metoda prostej wzorcowej • Metoda dodatku wzorca Ax = k c x A 1 = k c 1
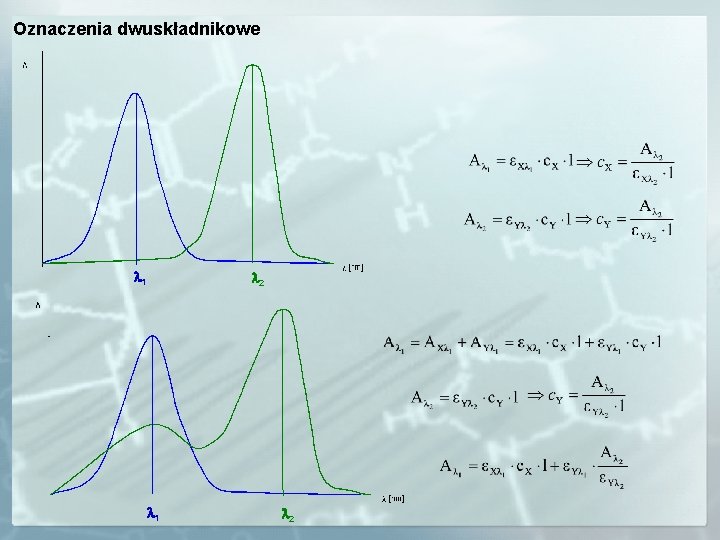
Oznaczenia dwuskładnikowe 1 2
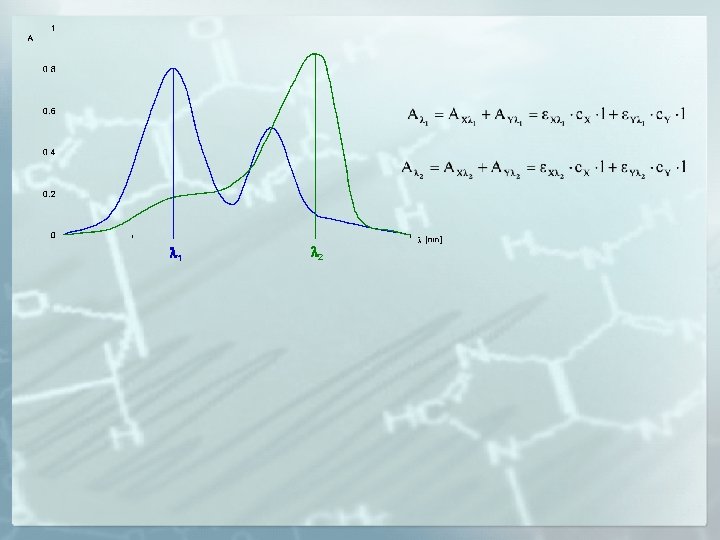
1 2
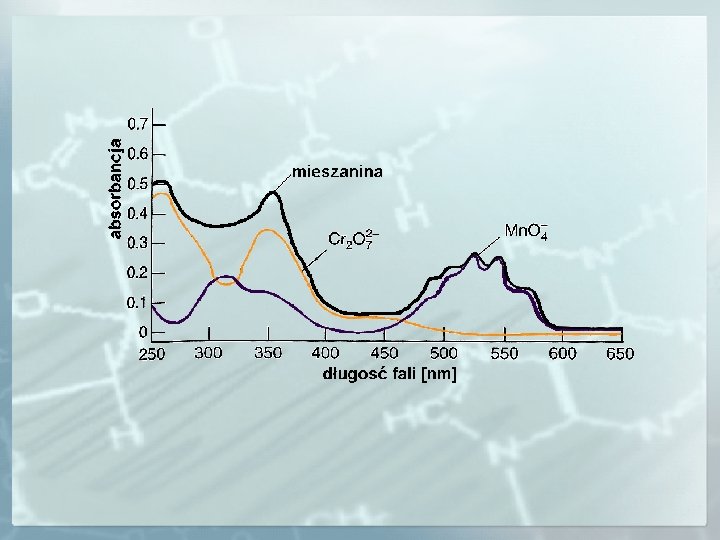
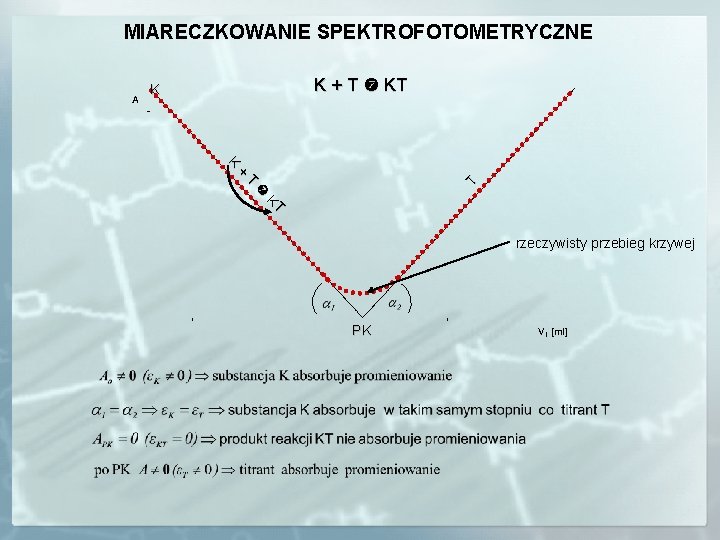
MIARECZKOWANIE SPEKTROFOTOMETRYCZNE K + T KT K T T K T + K rzeczywisty przebieg krzywej PK
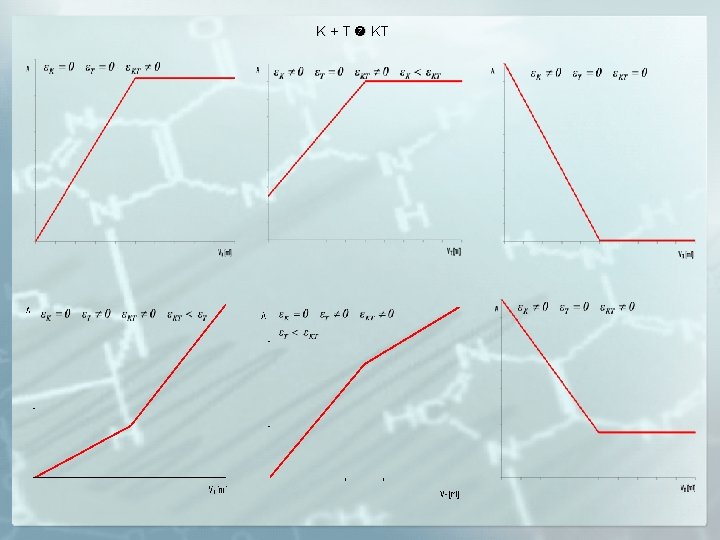
K + T KT
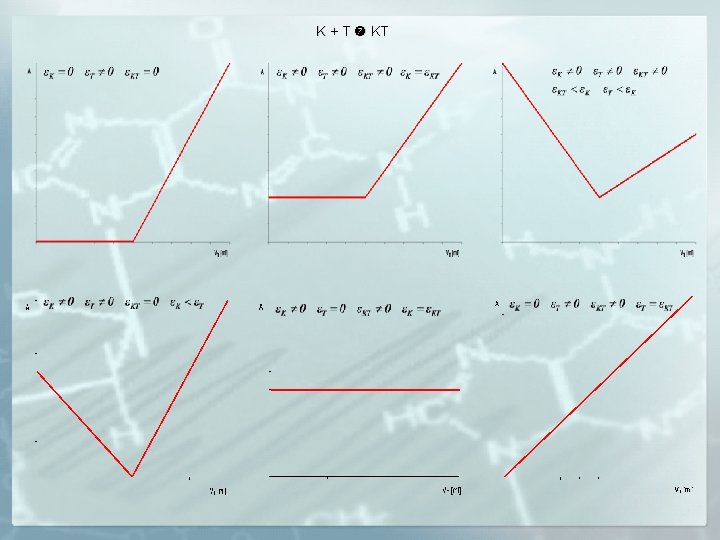
K + T KT
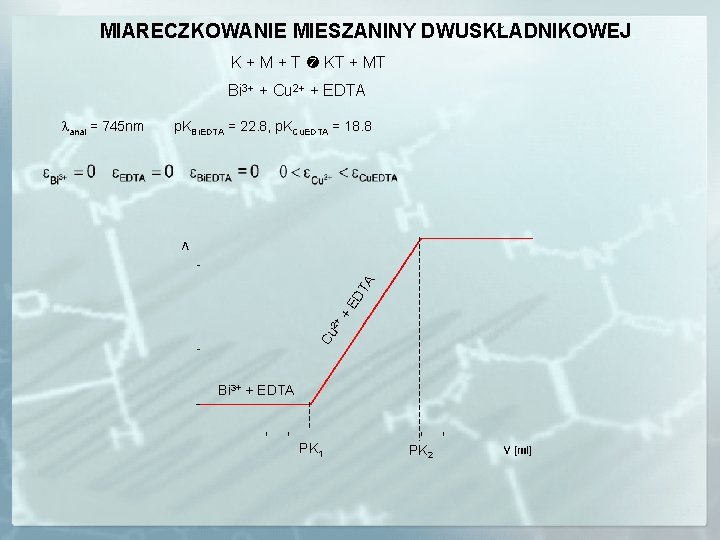
MIARECZKOWANIE MIESZANINY DWUSKŁADNIKOWEJ K + M + T KT + MT Bi 3+ + Cu 2+ + EDTA 2+ + ED TA p. KBi. EDTA = 22. 8, p. KCu. EDTA = 18. 8 Cu lanal = 745 nm Bi 3+ + EDTA PK 1 PK 2
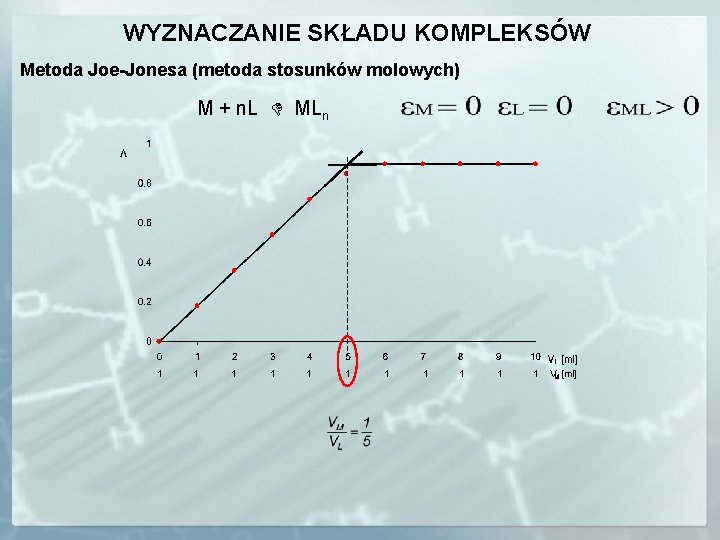
WYZNACZANIE SKŁADU KOMPLEKSÓW Metoda Joe-Jonesa (metoda stosunków molowych) M + n. L MLn 1 1 1 VM [ml]
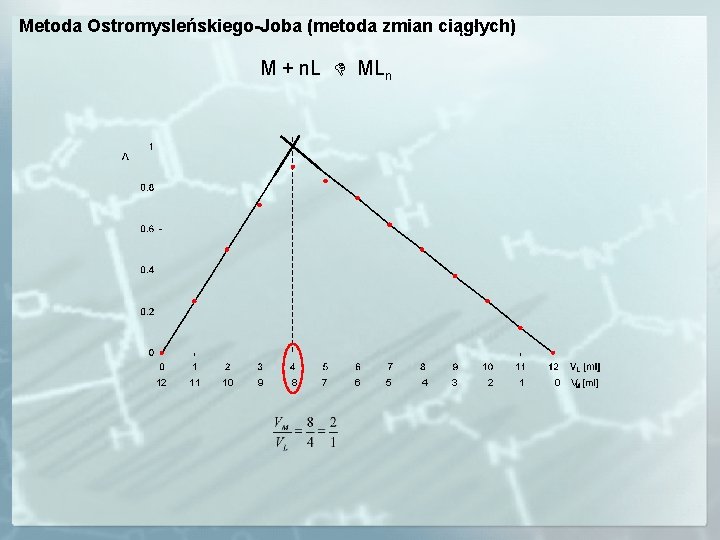
Metoda Ostromysleńskiego-Joba (metoda zmian ciągłych) M + n. L MLn 12 11 10 9 8 7 6 5 4 3 2 1 0 VM [ml]

Spektrofotometryczne wyznaczanie stałej dysocjacji Związek barwny o charakterze słabego kwasu dysocjuje na jony zgodnie z równaniem: HIn H+ + In. Stan równowagi reakcji można opisać stałą równowagi zgodnie z równaniem: Przy odpowiednio niskim p. H w roztworze istnieje tylko forma HIn, a przy odpowiedni wysokim forma In-. Dla odpowiedniego p. H: [In. H] = [In-]
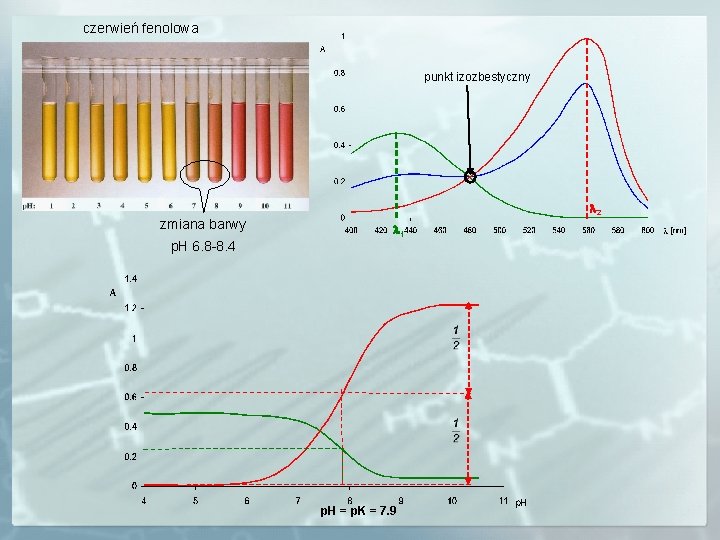
czerwień fenolowa punkt izozbestyczny zmiana barwy p. H 6. 8 -8. 4 2 1 p. H = p. K = 7. 9

Zastosowania spektrofotometrii UV-VIS • oznaczanie kationów i anionów • oznaczanie związków organicznych • wstępna identyfikacja związków na podstawie widma UV-VIS • badanie równowag reakcji chemicznych -wyznaczanie stałych dysocjacji - wyznaczanie składu i stałych trwałości związków kompleksowych • detektor spektrofotometryczny w HPLC

Zalety spektrofotometrii UV-VIS • Dostępna i tania aparatura • Prostota pomiarów • Szeroki zakres zastosowań • Dobra czułość (najmniejsza różnica stężeń badanej substancji, jaką można określić za pomocą danej metody ) • Duża precyzja oznaczeń (RSD: 0, 5 -5%) • Dobra selektywność oznaczeń • Możliwość jednoczesnego oznaczania dwóch a nawet trzech substancji w mieszaninie

SPEKTROFLUORYMETRIA Zasadą metody są pomiary natężenia promieniowania fluorescencyjnego emitowanego po wzbudzeniu substancji oznaczanej. Natężenie tego promieniowania jest wprost proporcjonalne do stężenia substancji oznaczanej
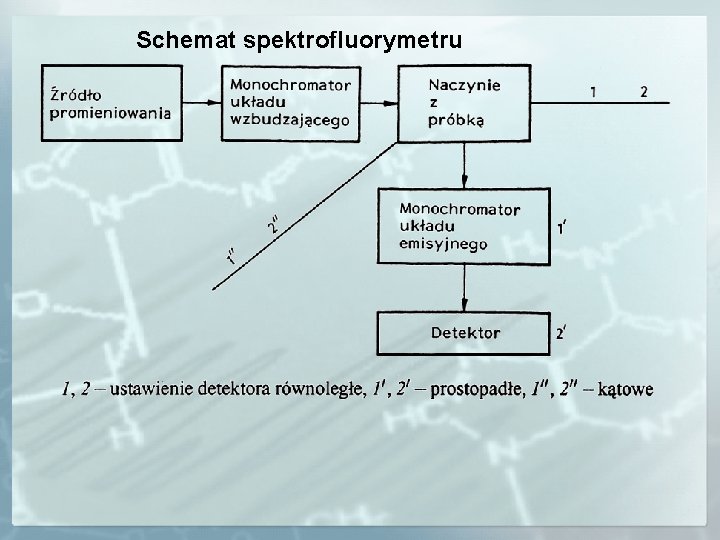
Schemat spektrofluorymetru

Zastosowania spektrofluorymetrii • oznaczanie kationów, anionów i związków organicznych w niższych stężeniach niż spektrofotometrycznie. • detektor spektrofluorymetryczny w HPLC

Pytania egzaminacyjne 1. Narysować i omówić schemat spektrofotometru jednowiązkowego, dwuwiązkowego, DAD. 2. Które z praw absorpcji światła spełnione jest w najszerszym zakresie a które z najmniejszym zakresie? Uzasadnić odpowiedź. 3. Jak wyznaczyć molowy współczynnik absorpcji? 4. Odchylenia od praw absorpcji światła. 5. Jak wykonać analizę mieszaniny dwuskładnikowej metodą spektrofotometryczną? 6. Narysować krzywe miareczkowań spektrofotometrycznych w różnych przypadkach absorbancji analitu, titranta i produktu reakcji. 7. Narysować i omówić krzywe przy wyznaczaniu składu kompleksu w różnych przypadkach.

. 8. Opisać spektrofotometryczne oznaczanie metodą prostej wzorcowej, metodą dodatku wzorca. 9. Podać definicje: analitycznej długości fali, absorbancji, absorpcji, transmitancji, monochromatora, molowego współczynnika absorpcji. 10. Spektrofotometryczne wyznaczanie stałej dysocjacji. 11. Opisać różnice pomiędzy spektrofotometrią i spektrofluorymetrią. 12. Wykorzystanie spektrofotometrii UV-VIS w chemii. 13. Podział metod spektroskopowych
- Slides: 44