UVGrnr blge spektroskopisi elektronik spektroskopi Spektroskopi spektrometri yntemin

UV-Görünür bölge spektroskopisi (elektronik spektroskopi) Spektroskopi (spektrometri): yöntemin adı Spektrometre : cihazın adı Işını filtreler ile dalga boylarına ayıran ve analiz eden aletler kolorimetre veya fotometre olarak adlandırılır. Işını monokromatör ile dalga boylarına ayıran ve analiz eden aletlere spektrofotometre denir. 1

UV-GÖR Spektroskopisi: UV ve görünür bölgedeki ışınların absorpsiyonuna dayanan spektroskopik bir yöntemdir. 10 - 350 nm arasındaki ışımaları kapsayan bölge UV bölgesi 350 - 800 nm arası görünür bölge 10 - 200 nm arasu vakum UV bölgesi 200 - 800 arası UV-GÖR bölge 2

400 - 800 arası UV-GÖR bölge Violet: Indigo: 420 - 440 nm Blue: 440 - 490 nm Green: 490 - 570 nm Yellow: 570 - 585 nm Orange: 585 - 620 nm Red: 380 - 420 nm 620 - 780 nm 3

Işığın absorplanması Belli bir yoğunluktaki (şiddet) ışın demeti çok sayıda atom ve moleküllerin bulunduğu bir ortama gönderilirse ışığın bir miktarı geçerken bir kısmı da madde tarafından tutulur ve şiddetinde (parlaklığında) azalma meydana gelir. Bu olaya absorpsiyon denir.

Absorpsiyon kanunları I / I 0 oranı T = Geçirgenlik (Transmitans) 100 T = (%T) % Transmitans log T = log I / I 0 -1 ile çarpılırsa -log I / I 0 = log I 0 / I = A (Absorbans) A = -log T Absorbans ile derişim arasında A = c l eşitliği vardır ve bu eşitlik Lambert-Beer kanunu olarak bilinir. 5

Labbert – Beer kanunu A= cl : (sabit): molar absorptivite katsayısı, madde ve dalga boyuna göre değişir. c : derişim (molarite) l : cm olarak uzunluk 6

UV-Görünür Bölge Spektrofotometreleri 7
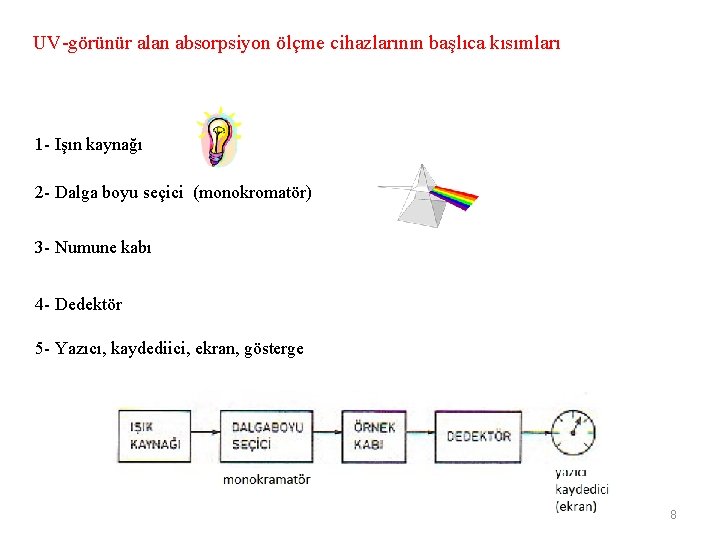
UV-görünür alan absorpsiyon ölçme cihazlarının başlıca kısımları 1 - Işın kaynağı 2 - Dalga boyu seçici (monokromatör) 3 - Numune kabı 4 - Dedektör 5 - Yazıcı, kaydediici, ekran, gösterge 8


Işık Kaynakları 1 - Yeterli güçte ışın demetleri oluşturmalı 2 -Yaydığı ışın şiddeti belirli bir sürede sabit kalmalı 3 - istenilen dalga boyunda ışın yayabilmeli

UV-GÖR spektrofotometrelerinde kullanılan ışık kaynakları H 2 lambası D 2 lambası W lamba W-halojen lamba Xe Lambalar

H 2 lambası
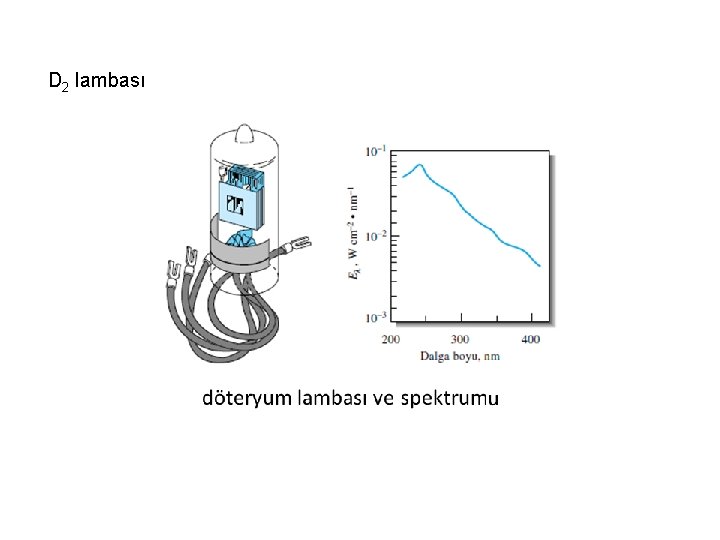
D 2 lambası
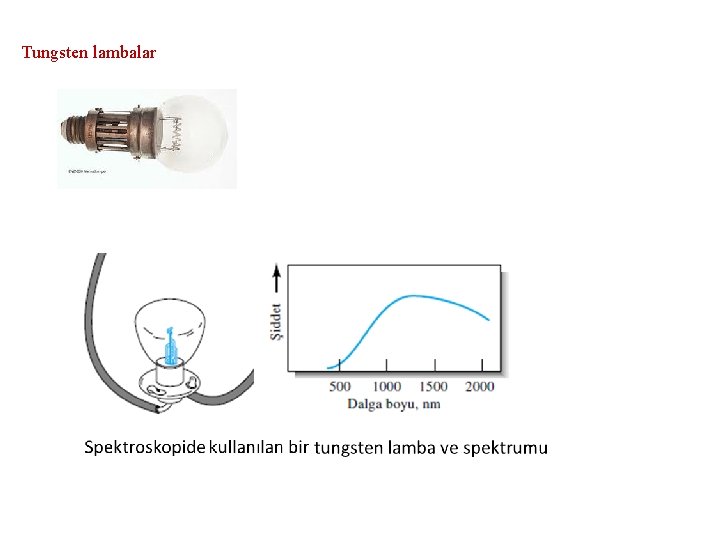
Tungsten lambalar

Tungsten halojen lambalar Tungsten flamanın bulunduğu kuvartz bir kap içinde çok az miktarda iyot vardır. Ömrü normal tungsten lambadan iki kat daha fazladır. 15

Ksenon ark Lambaları Ksenon atmosferinden akım geçişi ile şiddetli ışıma meydana gelir. Spektrum 250 -600 nm aralığı boyunca süreklidir 500 nm civarında şiddetli pik oluşturur 16

• Dalga boyu seçiciler (monokramatör) • Dalga boyu seçicisinden çıkan ışınların tek dalga boylu olması beklenir. • Ancak hiçbir dalga boyu ayırıcısı bunu tam olarak yerine getiremez. • Belli bir dalga boyu aralığı (bant) oluştururlar. • Bandın inceliği cihazın performansına bağlıdır. • Dalga boyu seçiciler • Filtreler ve monokromatörler olarak iki başlıkta incelenir.

• Filtreler: • Filtreler, sürekli ışın veren bir kaynağın yaydığı ışınlardan belli bir ışıma bandındaki diğer dalga boylarını absorplayarak çalışır. Absorpsiyon filtrelerinde etkin bant genişliği 30 -250 nm aralığındadır. • Absorpsiyona duyarlı çalışan filtreler GB de kullanılır. Genelde renkli camdırlar. • Bunun dışında girişim filtreleri, UV, GB ve IR bölgelerde kullanılır. Girişim filtreleri çok dar ışın bandı elde etmek için optik girişimden yararlanır. Filtreler basit sağlam ve ucuzdur.

• Monokromatörler • Yapılarında mercekler, pencereler, optik ağ veya prizmalar bulunan ve geniş bir dalga boyu aralığındaki ışık kaynağını dalga boylarına ayıran (monokromatik ışın) cihazlardır. • Monokromatörler spektral taramaları yapabilmek için tasarlanmıştır. • 200 - 800 nm gibi • Prizmalı monokromatörler • Optik ağlı monokromatörler
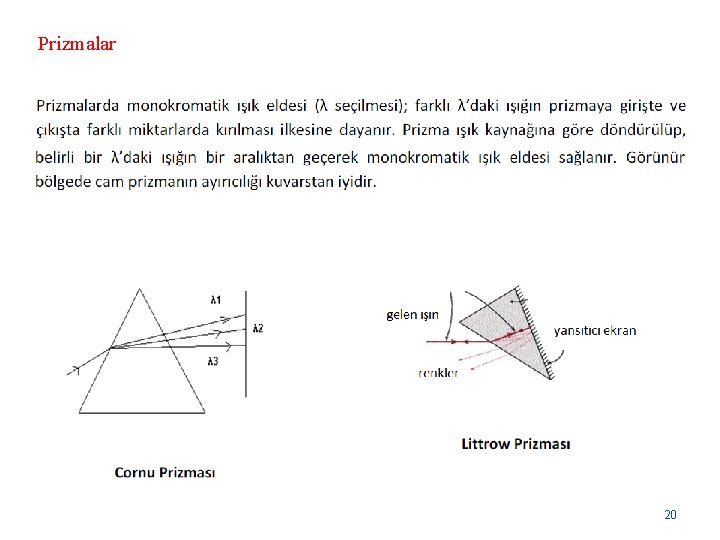
Prizmalar 20
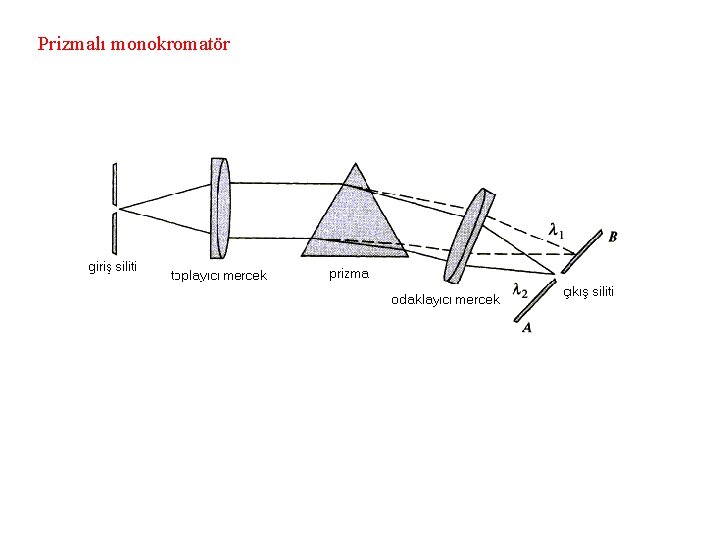
Prizmalı monokromatör

Optik ağlar (grating, ızgara): ışığın kırınım ve girişim ilkesine göre çalışırlar Geçirgen optik ağlar Yansıtmalı optik ağlar Geçirgen optik ağlar : Düz bir cam veya geçirgen düz bir levha üzerine eşit olarak çizilen geçirgen olmayan çizgilerden oluşur. Geçirgen ve geçirgen olmayan aralıkların birbirine eşit ve birkaç cm boyunca çizilmiş olması gerekir. İyi optik ağlar cm’de 6000’e yakın çizgi içerir. 22
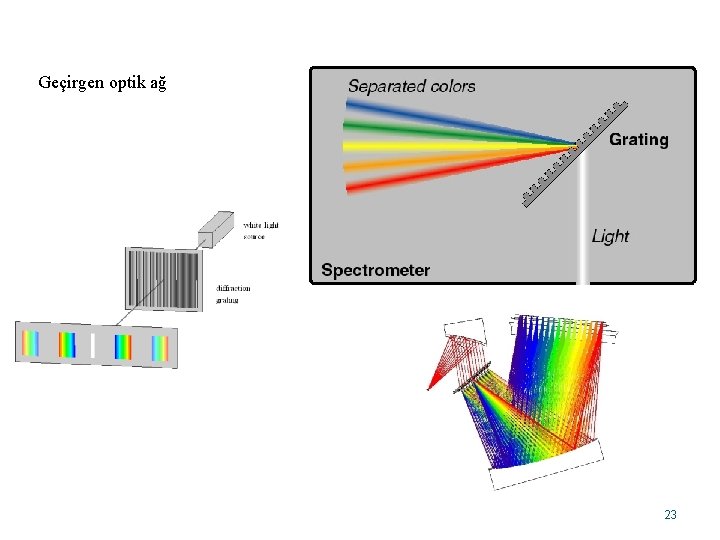
Geçirgen optik ağ 23
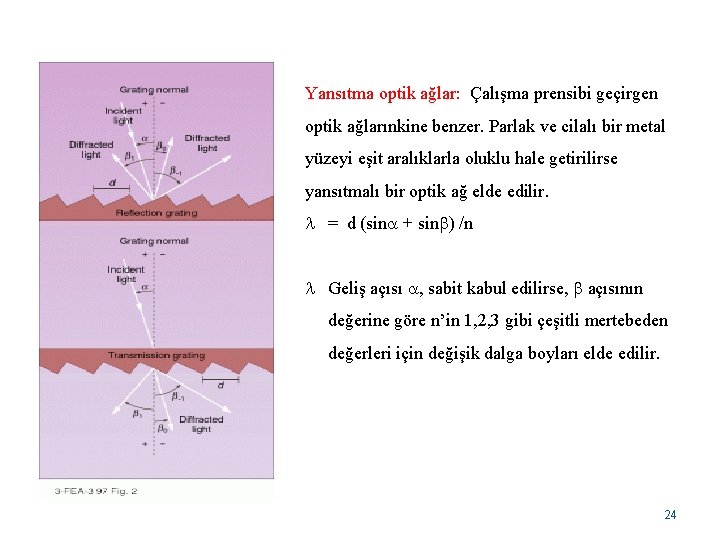
Yansıtma optik ağlar: Çalışma prensibi geçirgen optik ağlarınkine benzer. Parlak ve cilalı bir metal yüzeyi eşit aralıklarla oluklu hale getirilirse yansıtmalı bir optik ağ elde edilir. = d (sin + sin ) /n Geliş açısı , sabit kabul edilirse, açısının değerine göre n’in 1, 2, 3 gibi çeşitli mertebeden değerleri için değişik dalga boyları elde edilir. 24
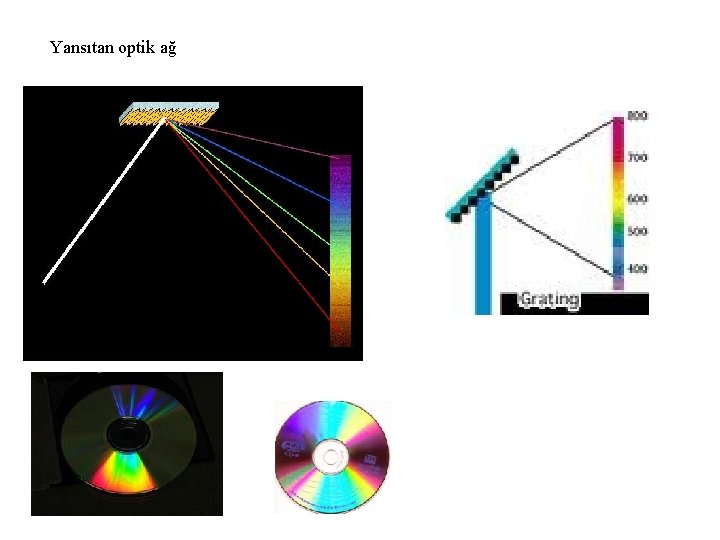
Yansıtan optik ağ
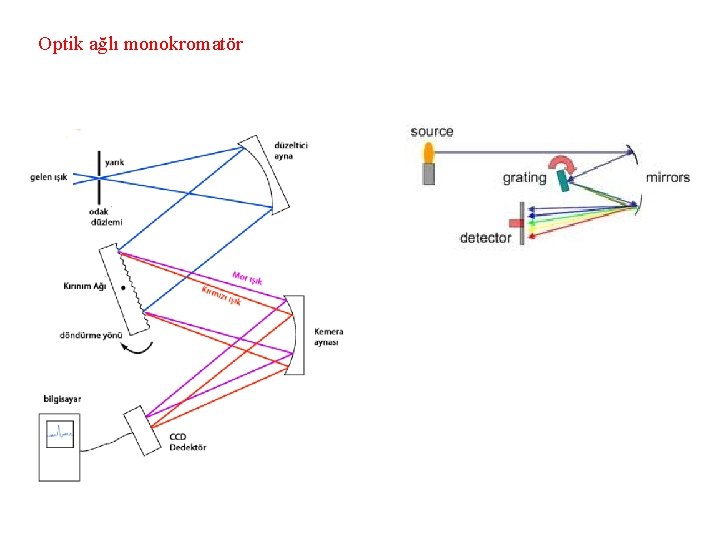
Optik ağlı monokromatör

• Numune kapları hücre veya küvet olarak adlandırılır. Çalışılan dalga boyu aralığı için geçirgen olmalıdır. • Cam küvetler 350 nm altındaki ışığı absorplayacağı için UV bölgedeki çalışmalarda kuvars veya erimiş silis küvet kullanılır.
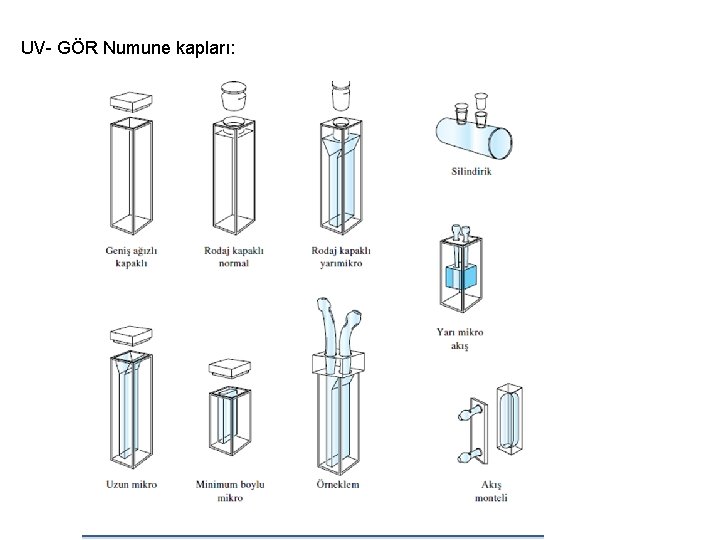
UV- GÖR Numune kapları:

• Dedektörler: • Dedektör genel anlamda herhangi bir fiziksel olgunun varlığını gösteren cihazlardır. Elektromanyetik veya radyoaktif ışınların varlığını gösteren fotoğraf filmleri; kütle farklarını gösteren terazi ibresi, termometrelerdeki civa seviyesi, bilinen dedektörlerdir. • İnsan gözü de bir dedektör olarak düşünülebilir. • Göz GB ışınlarını bir elektrik sinyaline dönüştürür ve bu sinyal optik sinirdeki nöronlar zinciri ile beyne iletilir. • Işık enerjisini elektrik enerjisine çeviren cihazlardır.

İdeal bir dedektörün özellikleri Yüksek duyarlılığa sahip olmalı Sinyal / Gürültü (S/N) oranının yüksek olmalı Geniş dalga boyu aralığında sabit ve orantılı cevap vermeli Hızlı cevap vermeli Işın gelmediğinde çıkış sinyali 0 olmalı.

Gürültü: Analitik cihazlardan elde edilen sinyal, kontrolü mümkün olmayan pek çok değişkenin etkisiyle rastgele şekilde dalgalanır. Cihazın duyarlığını azaltan bu dalgalanmalara gürültü denir.

• Foton dedektörleri, ışın fotonlarının aktif bir yüzeye çarparak elektron koparması ya da yüzeydeki elektronları uyararak yüzeyi iletken hale getirmesi esasına dayanır. Yaygın olarak 5 tip foton dedektörü kullanılır. • Fotovoltaik hücreler • Fototüpler • Fotoçoğaltıcılar • Silisyumlu fotodiyotlar • Yük aktarım düzenekleri
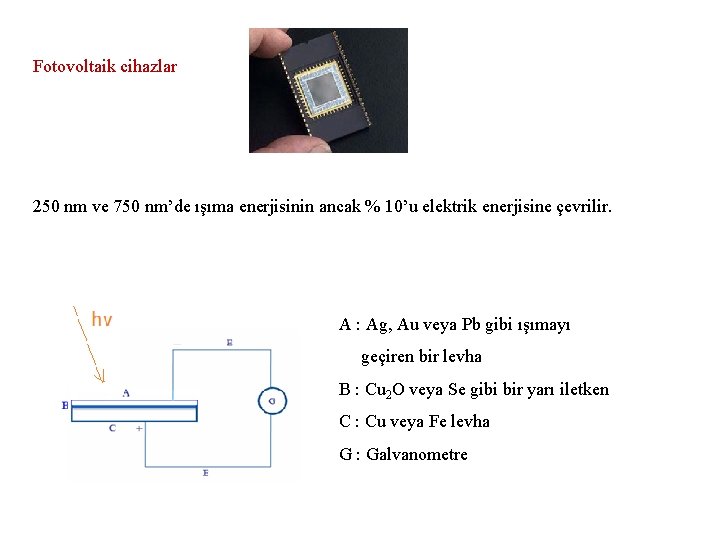
Fotovoltaik cihazlar 250 nm ve 750 nm’de ışıma enerjisinin ancak % 10’u elektrik enerjisine çevrilir. A : Ag, Au veya Pb gibi ışımayı geçiren bir levha B : Cu 2 O veya Se gibi bir yarı iletken C : Cu veya Fe levha G : Galvanometre

Şekildeki sistemde birbiri üzerine yerleştirilmiş üç tabaka vardır. A : Ag, Au veya Pb gibi ışımayı geçiren bir levha, B : Cu 2 O veya Se gibi bir yarı iletken, C : Cu veya Fe levha. A tabakasına ışın geldiğinde B ye geçer ve buradan e koparır. Kopan e lar A üzerinde birikir. Böylece A negatif C pozitif elektrik yüklü olur. A ile C tabakası bir iletken tel ile birleştirildiğinde e lar A dan C ye akarak devreyi tamanlar. Sonuçta ışın şiddetine göre devreden akım geçer.
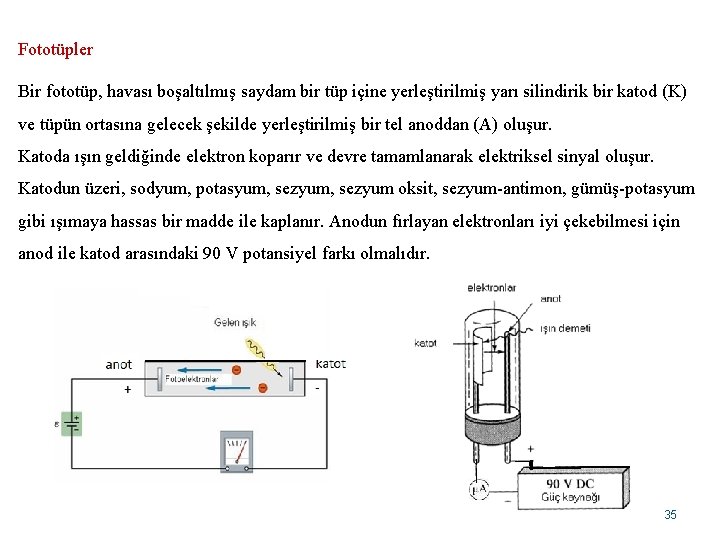
Fototüpler Bir fototüp, havası boşaltılmış saydam bir tüp içine yerleştirilmiş yarı silindirik bir katod (K) ve tüpün ortasına gelecek şekilde yerleştirilmiş bir tel anoddan (A) oluşur. Katoda ışın geldiğinde elektron koparır ve devre tamamlanarak elektriksel sinyal oluşur. Katodun üzeri, sodyum, potasyum, sezyum oksit, sezyum-antimon, gümüş-potasyum gibi ışımaya hassas bir madde ile kaplanır. Anodun fırlayan elektronları iyi çekebilmesi için anod ile katod arasındaki 90 V potansiyel farkı olmalıdır. 35
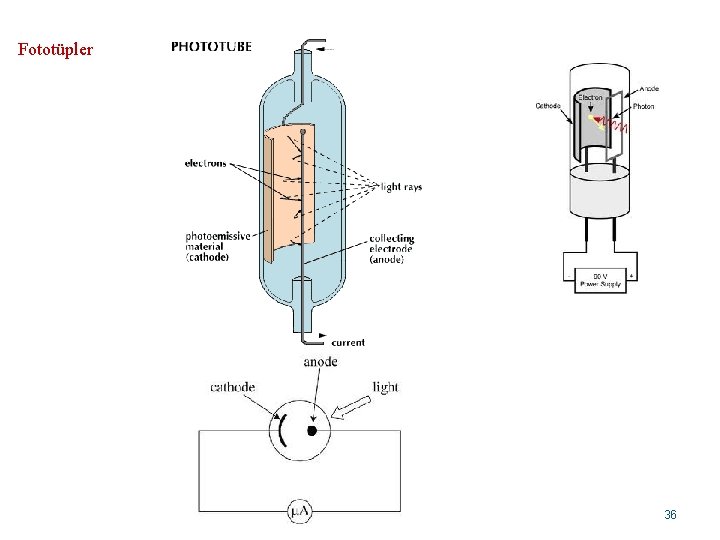
Fototüpler 36
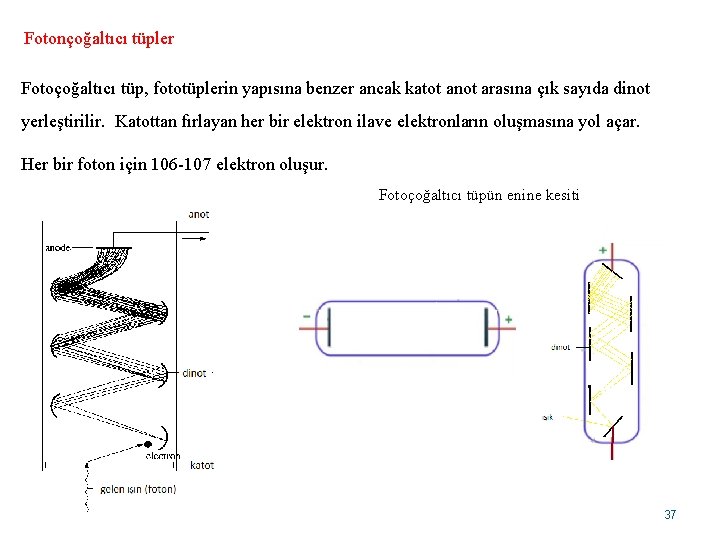
Fotonçoğaltıcı tüpler Fotoçoğaltıcı tüp, fototüplerin yapısına benzer ancak katot anot arasına çık sayıda dinot yerleştirilir. Katottan fırlayan her bir elektron ilave elektronların oluşmasına yol açar. Her bir foton için 106 -107 elektron oluşur. Fotoçoğaltıcı tüpün enine kesiti 37
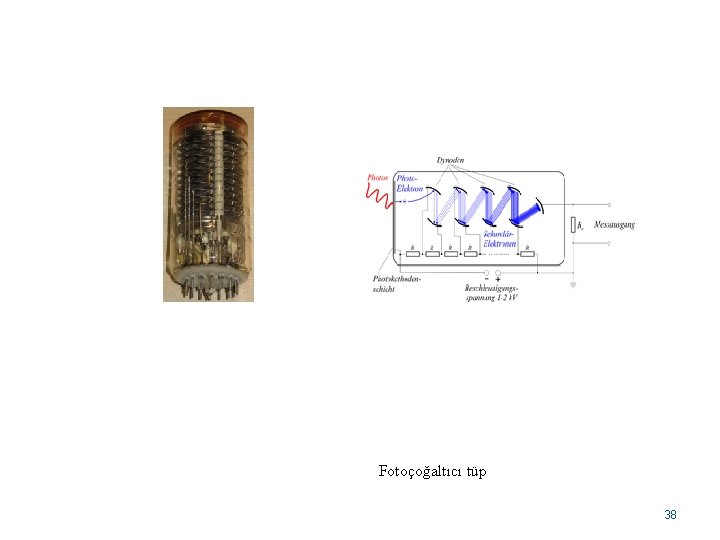
Fotoçoğaltıcı tüp 38
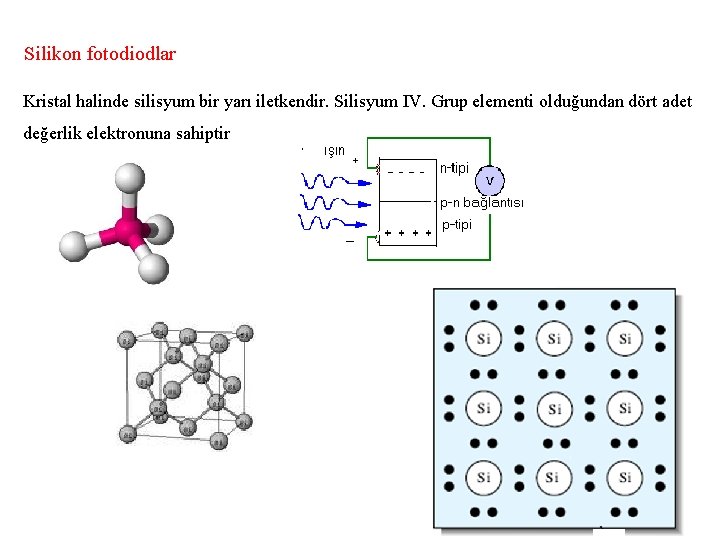
Silikon fotodiodlar Kristal halinde silisyum bir yarı iletkendir. Silisyum IV. Grup elementi olduğundan dört adet değerlik elektronuna sahiptir 39
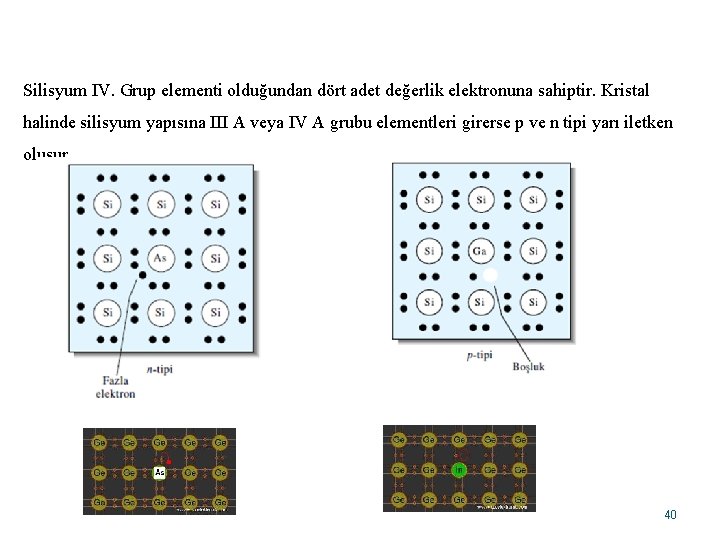
Silisyum IV. Grup elementi olduğundan dört adet değerlik elektronuna sahiptir. Kristal halinde silisyum yapısına III A veya IV A grubu elementleri girerse p ve n tipi yarı iletken oluşur 40
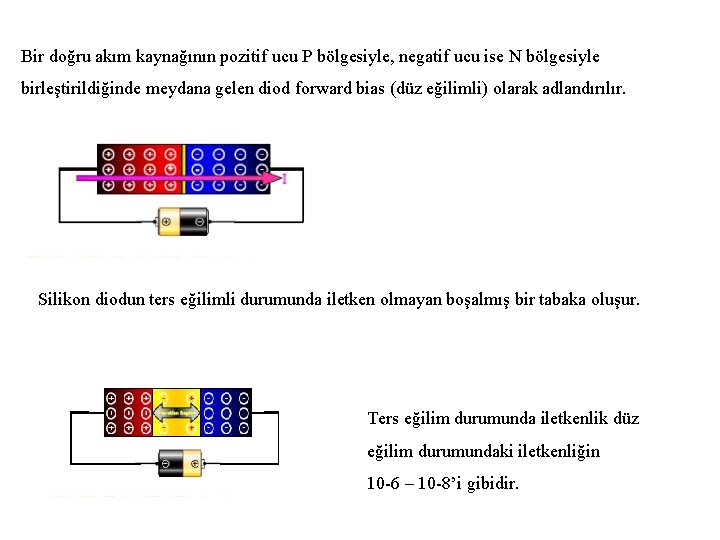
Bir doğru akım kaynağının pozitif ucu P bölgesiyle, negatif ucu ise N bölgesiyle birleştirildiğinde meydana gelen diod forward bias (düz eğilimli) olarak adlandırılır. Silikon diodun ters eğilimli durumunda iletken olmayan boşalmış bir tabaka oluşur. Ters eğilim durumunda iletkenlik düz eğilim durumundaki iletkenliğin 10 -6 – 10 -8’i gibidir.
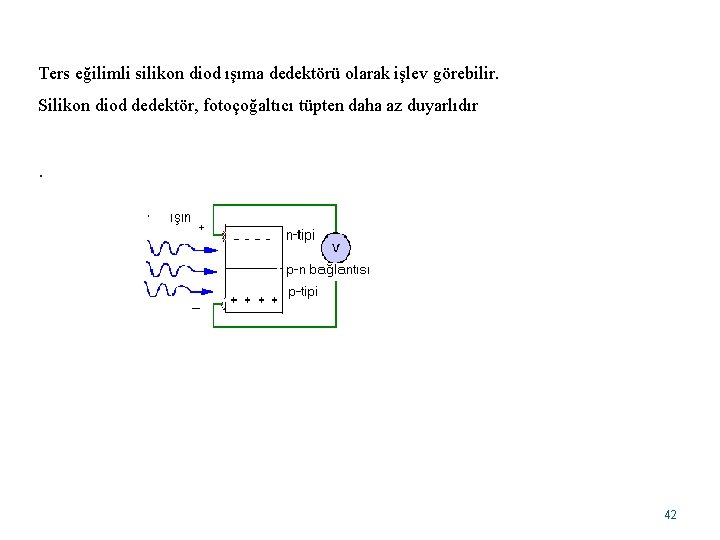
Ters eğilimli silikon diod ışıma dedektörü olarak işlev görebilir. Silikon diod dedektör, fotoçoğaltıcı tüpten daha az duyarlıdır . 42
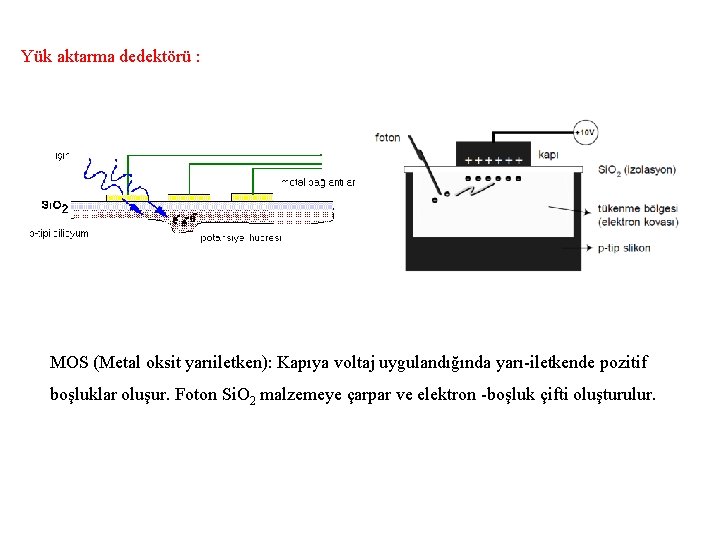
Yük aktarma dedektörü : MOS (Metal oksit yarıiletken): Kapıya voltaj uygulandığında yarı-iletkende pozitif boşluklar oluşur. Foton Si. O 2 malzemeye çarpar ve elektron -boşluk çifti oluşturulur.

UV ve Görünür Bölge Spektrofotometre çeşitleri Normal UV-görünür bölge cihazları 200 -900 nm arasında çalışır. N 2 ve O 2 molekülleri 160 ve 200 nm’de absorpsiyon yaptıkları için 200 nm altındaki dalga boylarında vakumlu UV cihazları kullanılır. UV ve görünür bölgede kullanılan spektrofotometreler 1 - Tek ışıma demetli spektrofotometreler 2 - Çift ışıma demetli spektrofotometreler 44
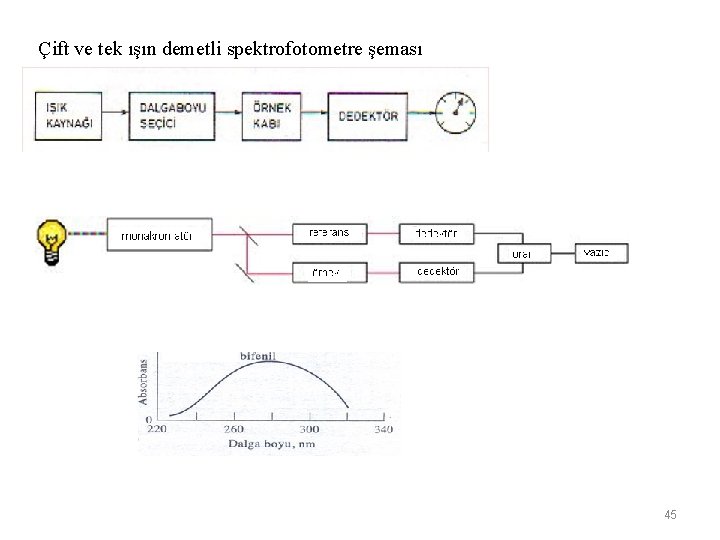
Çift ve tek ışın demetli spektrofotometre şeması 45

UV-GÖR bölge spektrumu UV-Gör spektrofotometresi ile spektrum almak için saf örneğin çözeltisi hazırlanır ve cihaza yerleştirilir. Cihazda, örnek üzerine değişik dalga boyunda ışınlar gönderilerek bu ışınların absorplanma miktarı ölçülür. Dalga boyuna karşı absorbans grafiği oluşturulur. Bu grafiğe maddenin UV-GÖR spektrumu denir. Spektrumlar farklı şekilde de çizilebilir Dalga boyuna karşı molar absorbtivite (є), geçirgenlik (T), % geçirgenlik (%T) Log A, türev spektrumları vs. 46


Atom ve molekülerin spektrumları (atomik ve moleküler spektrumlar) Atomik spektrumlar: Çizgi spektrumu Moleküler spektrumlar: Bant spektrumu

Atomlarda enerji düzeyleri Atomlarda sadece elektronların yörüngesinden kaynaklanan enerji düzeyleri vardır. Geçiş enerjisi iki elektronik seviye farkına eşittir. E = hν Etoplam = Eelektronik
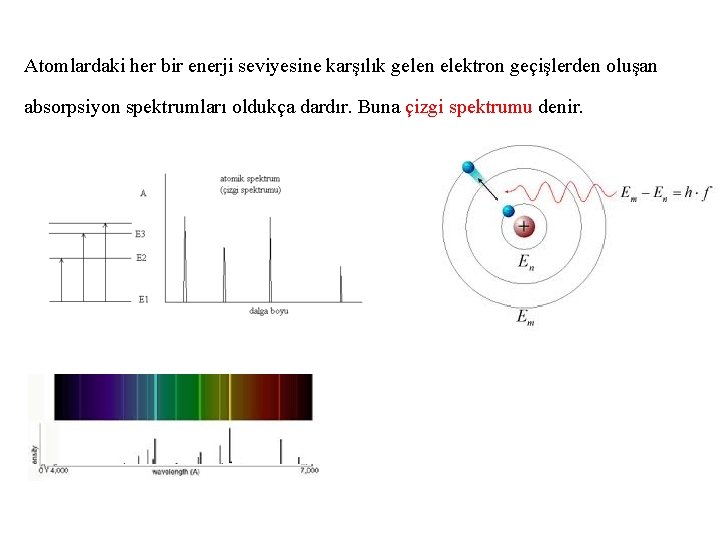
Atomlardaki her bir enerji seviyesine karşılık gelen elektron geçişlerden oluşan absorpsiyon spektrumları oldukça dardır. Buna çizgi spektrumu denir.

Moleküllerdeki enerji düzeyleri Moleküllerde elektronik enerji düzeylerine ek olarak dönme ve titreşim enerji düzeyleri de vardır. Bu geçişler sırasında bir molekülün toplam enerjisi, Etoplam = Eelektronik + Etitreşim + Edönme eşitliği ile verilir.
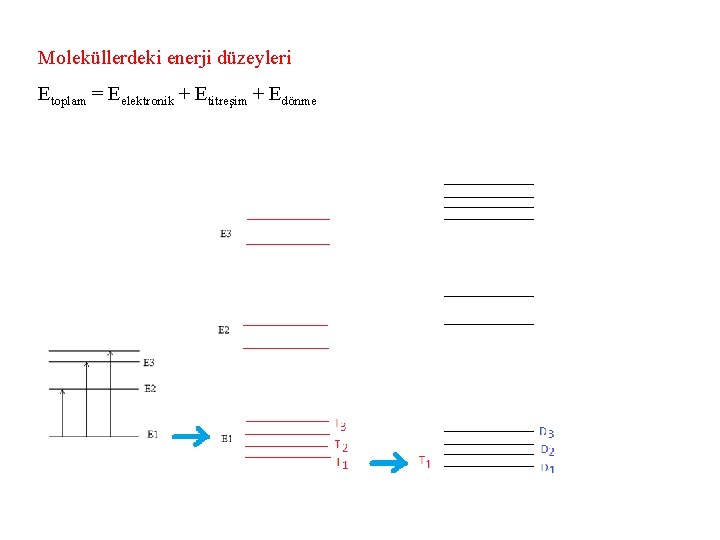
Moleküllerdeki enerji düzeyleri Etoplam = Eelektronik + Etitreşim + Edönme
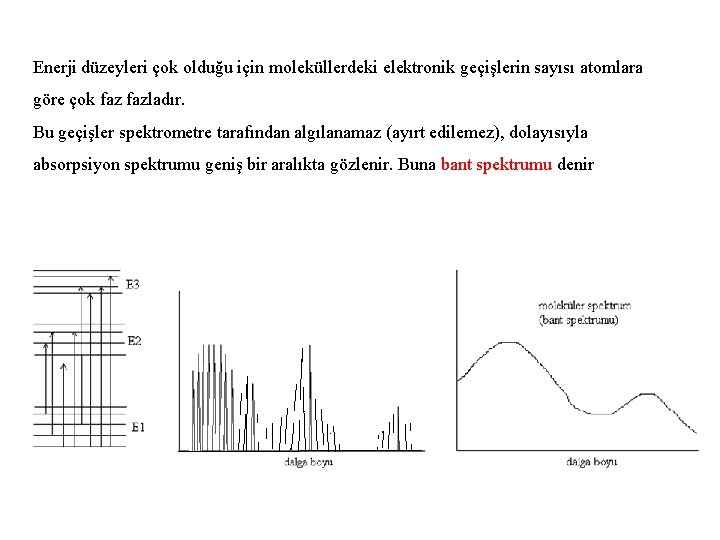
Enerji düzeyleri çok olduğu için moleküllerdeki elektronik geçişlerin sayısı atomlara göre çok fazladır. Bu geçişler spektrometre tarafından algılanamaz (ayırt edilemez), dolayısıyla absorpsiyon spektrumu geniş bir aralıkta gözlenir. Buna bant spektrumu denir
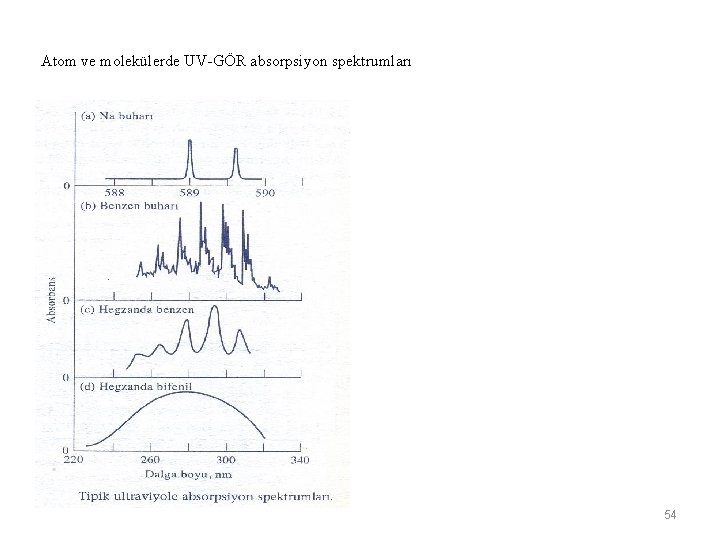
Atom ve molekülerde UV-GÖR absorpsiyon spektrumları 54

Elektronik geçişler ve kimyasal bağlar Hem organik hem de anorganik maddeler UV ve görünür bölgede absorpsiyon yaparlar. Organik maddelerin ışın absorpsiyonu molekül orbital (MO) teorisine göre Anorganik maddelerinki ışın absorpsiyonu ise kristal alan teorisine göre açıklanır.
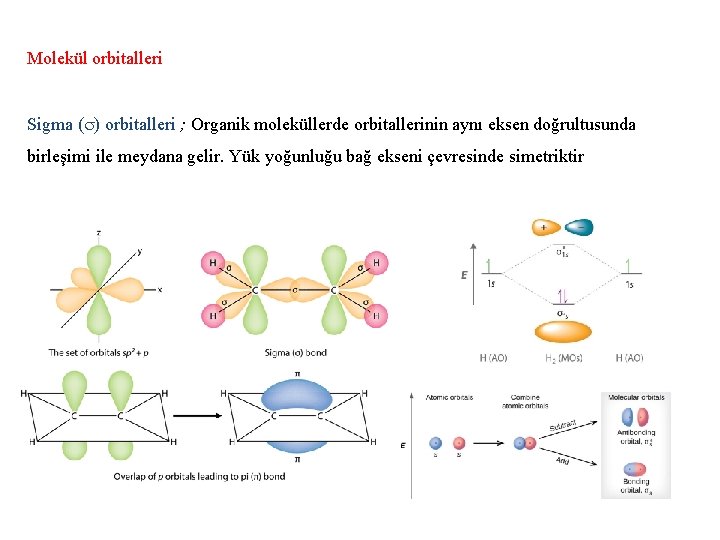
Molekül orbitalleri Sigma ( ) orbitalleri ; Organik moleküllerde orbitallerinin aynı eksen doğrultusunda birleşimi ile meydana gelir. Yük yoğunluğu bağ ekseni çevresinde simetriktir .
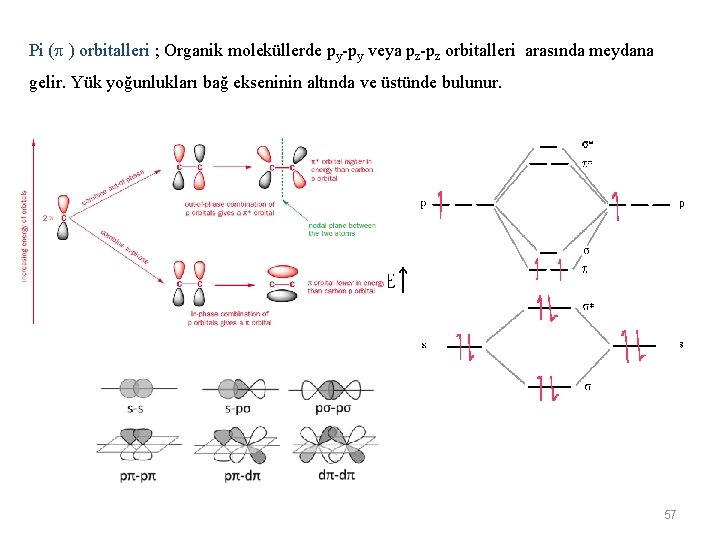
Pi ( ) orbitalleri ; Organik moleküllerde py-py veya pz-pz orbitalleri arasında meydana gelir. Yük yoğunlukları bağ ekseninin altında ve üstünde bulunur. 57
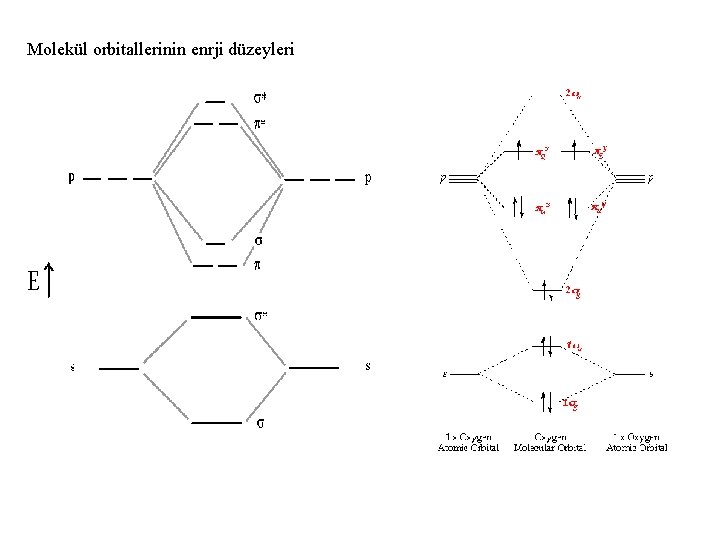
Molekül orbitallerinin enrji düzeyleri
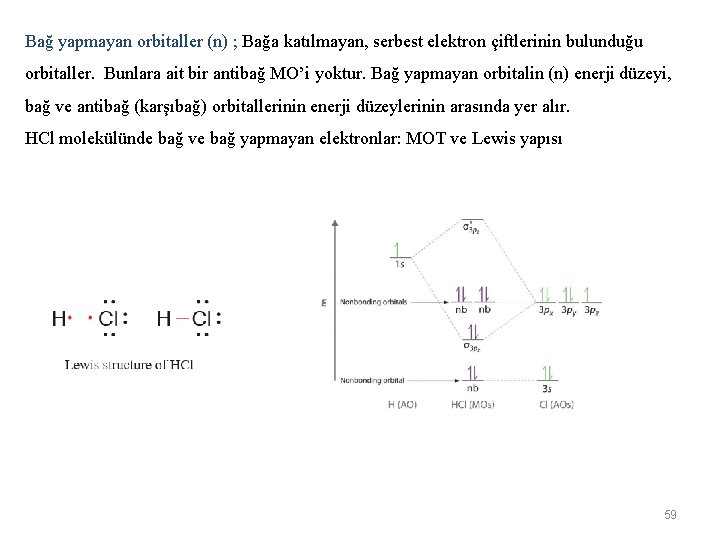
Bağ yapmayan orbitaller (n) ; Bağa katılmayan, serbest elektron çiftlerinin bulunduğu orbitaller. Bunlara ait bir antibağ MO’i yoktur. Bağ yapmayan orbitalin (n) enerji düzeyi, bağ ve antibağ (karşıbağ) orbitallerinin enerji düzeylerinin arasında yer alır. HCl molekülünde bağ ve bağ yapmayan elektronlar: MOT ve Lewis yapısı n 59
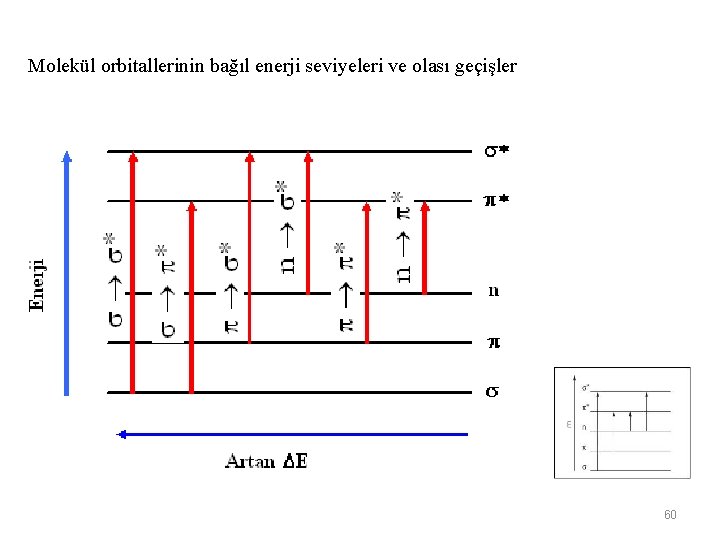
Molekül orbitallerinin bağıl enerji seviyeleri ve olası geçişler 60

Bu 6 geçişten en çok rastlananları ve yapı tayinlerinde kullanılanları; * * n * → * Geçişleri: Vakum UV bölgesinde, bağ orbitalindeki bir elektronun ışın absorplayarak anti bağ orbitaline uyarılması ile gerçekleşir 61
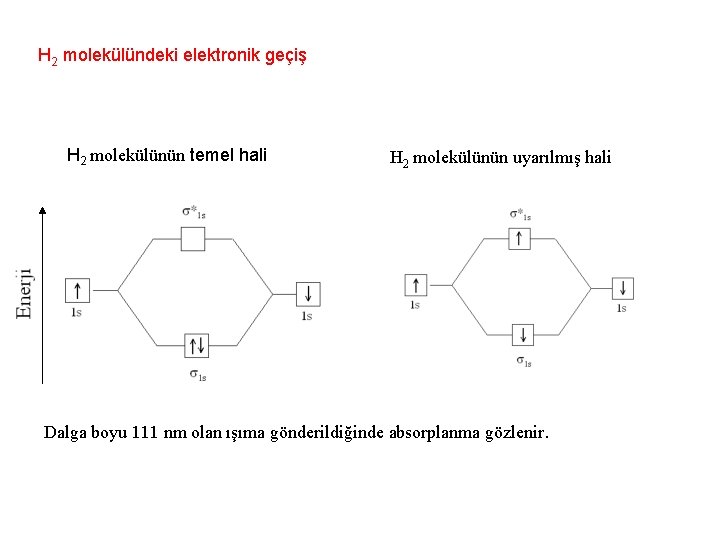
H 2 molekülündeki elektronik geçiş H 2 molekülünün temel hali H 2 molekülünün uyarılmış hali Dalga boyu 111 nm olan ışıma gönderildiğinde absorplanma gözlenir.
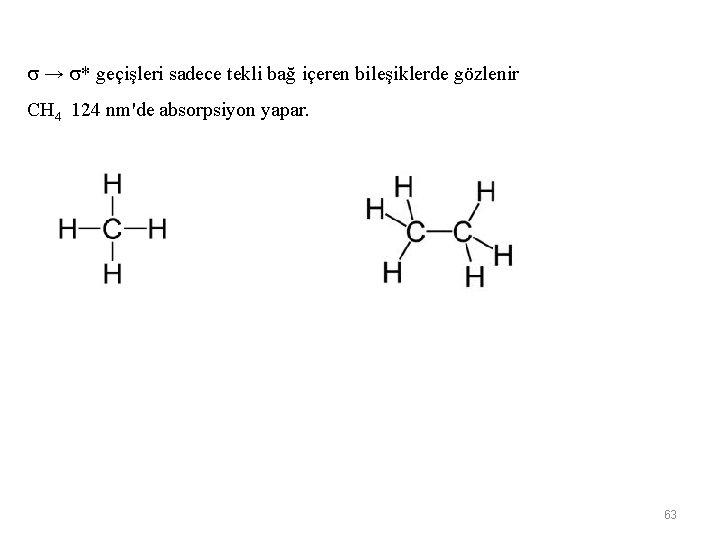
→ * geçişleri sadece tekli bağ içeren bileşiklerde gözlenir CH 4 124 nm'de absorpsiyon yapar. 63

n → * Geçişleri: 160 -250 nm aralığında ortaklanmamış elektron çiftleri içeren bileşiklerde gözlenir. ε→ düşük veya orta şiddetlidir ve çoğunlukla 100 -3000 L cm-1 mol-1 aralığında yer alır. ε değerinin büyüklüğü pikin şiddetini gösterir 64
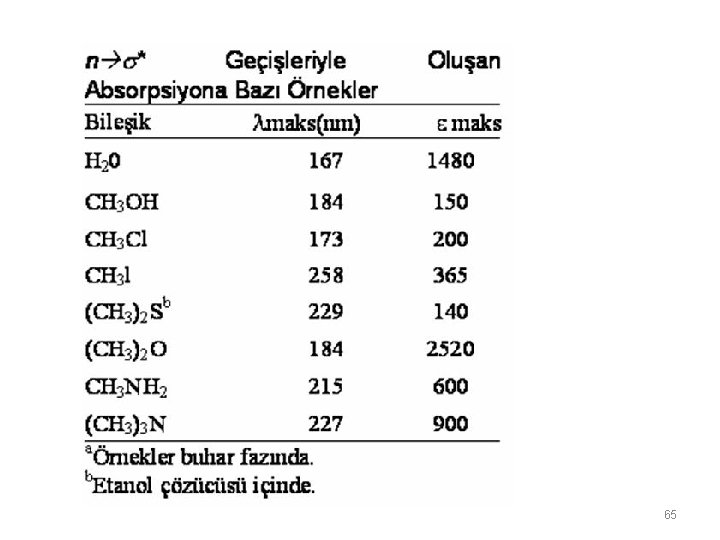
65
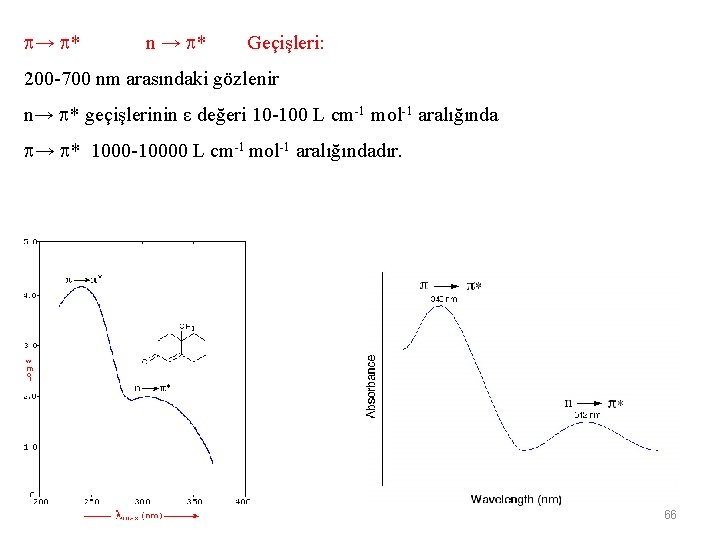
→ * n → * Geçişleri: 200 -700 nm arasındaki gözlenir n→ * geçişlerinin ε değeri 10 -100 L cm-1 mol-1 aralığında → * 1000 -10000 L cm-1 mol-1 aralığındadır. 66

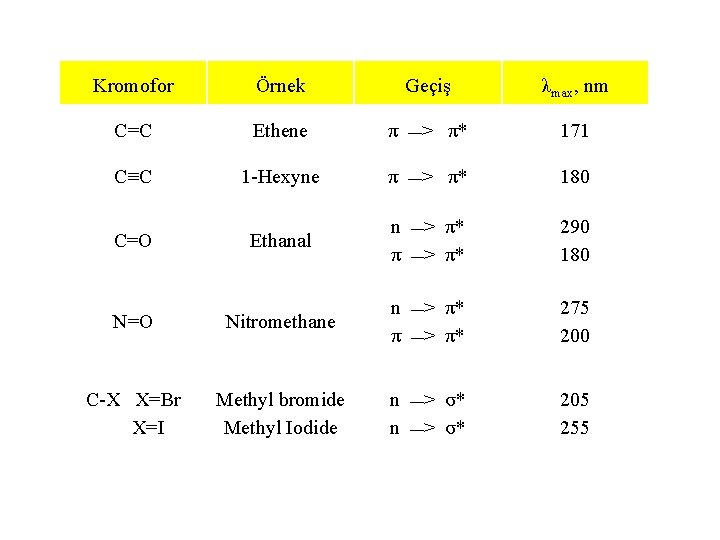
Kromofor Örnek C=C Ethene π __> π* 171 C≡C 1 -Hexyne π __> π* 180 Ethanal n π __> π* 290 180 N=O Nitromethane n π __> π* 275 200 C-X X=Br X=I Methyl bromide Methyl Iodide n n __> 205 255 C=O Geçiş σ* __> σ* λmax, nm

Kromofor grup: GÖR bölgede (400 -800 nm) ışık absorpsiyonu yapan C=0, -NO 2, -NO, C=C, -CHO kromofor gruplar denir. Bu aralıkta absorpsiyon yapan maddeler absorpladıkları rengin tamamlayıcısı olan renkte görünürler 69

Oksokrom grup: -NH 2, -OH, –SH ve -Cl gibi gruplar kendileri renkli olmayan ancak absorpsiyon maksimum dalga boyunu uzun veya kısa dalga boyuna kaydıran gruplardır. Oksokrom grup yada diğer etkilerle absorpsiyonunun uzun dalga boyuna kaymasına (kırmızıya kayma) batokromik etki denir. Oksokrom grup yada diğer etkilerle absorpsiyonunun kısa dalga boyuna kaymasına da (maviye kayma) hipsokromik etki denir. Absorpsiyon şiddetinin artmasına hiperkromik etki azalmasına ise hipokromik etki denir. 70


C = O grubunun absorbsiyon dalgaboyunun sübstitüentlere göre değişimi 72

Elektronik geçişleri değiştiren etkenler Konjügatif etki Rezonans etkisi İndüktif etki Çevre etkisi 73
Konjügatif etki Konjüge durumda en az iki çift bağ içeren moleküllerde görülür. Konjügasyon elektronlarının delokalizasyonunu arttırır. Delokalizasyon arttıkça * geçiş enerjisi küçülür. -C=C-C=C-C=C- 74
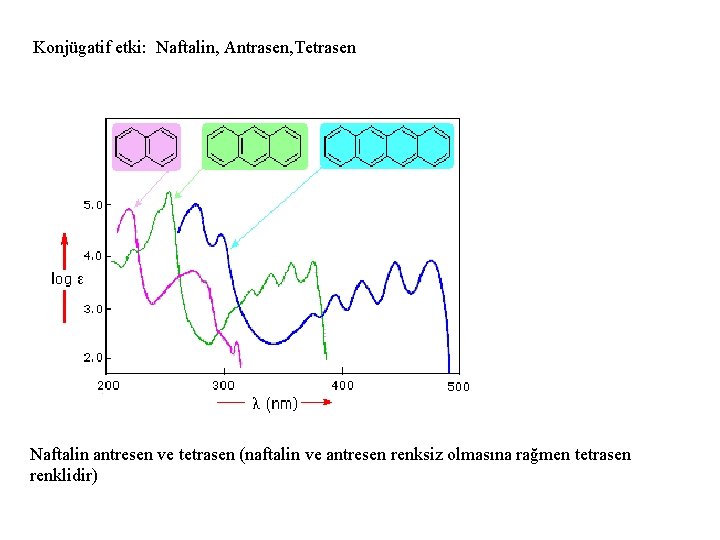
Konjügatif etki: Naftalin, Antrasen, Tetrasen Naftalin antresen ve tetrasen (naftalin ve antresen renksiz olmasına rağmen tetrasen renklidir)

Rezonans etkisi Ortaklanmamış elektron çiftlerinden ileri gelen bir etkidir. Asit klorürleri, amidler ve esterlerde görülür Cl, N, O gibi elektronegatif elementlerin serbest elektron çiftleri karbonil çifte bağıyla rezonansa girer ve geçiş enerjisini yükseltir. 76

İndüktif etki Elektronegatif bir elementin bağ elektronlarını çekme etkisinin maddenin öteki bağlarını da etkilemesi olayıdır. Karbonil karbonuna bağlı olan elektronegatif X atomu C X bağının elektronlarını kendine çeker. C’un elektronegativitesi ve çifte bağın var olma olasılığı artar. Geçiş enerjisi büyür. 77

Çevre etkisi Çözücü etkisi ve sterik etkiler olmak üzere iki çeşittir. Çözücü etkisi Çözücünün polarlığının artması ile * geçişi uzun dalgaboyuna (batokromik etki), n * geçişi kısa dalgaboyuna (hipsokromik etki) Polar olmayan çözücü E 1 > E 2 Polar çözücü E 4 > E 3 78
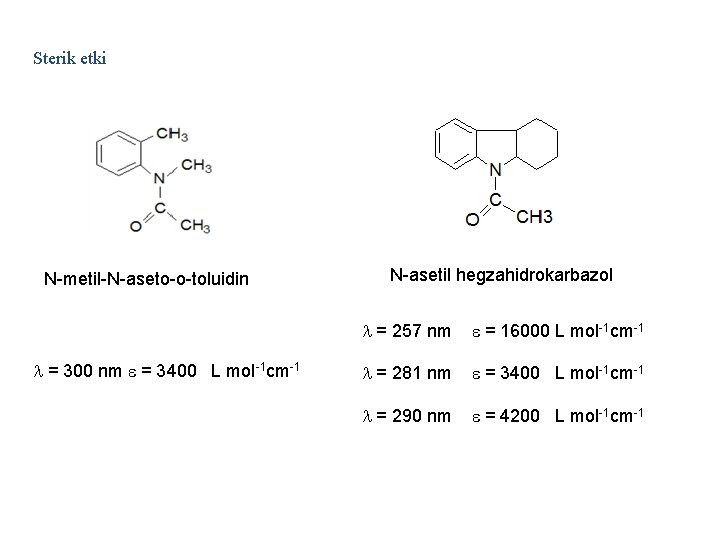
Sterik etki N-metil-N-aseto-o-toluidin = 300 nm = 3400 L mol-1 cm-1 N-asetil hegzahidrokarbazol = 257 nm = 16000 L mol-1 cm-1 = 281 nm = 3400 L mol-1 cm-1 = 290 nm = 4200 L mol-1 cm-1
Bir molekülde orbitallerinin artması molekülü düzlemsel yapıda olmaya zorlar. Difenil Orto pozisyonunda büyük alkil grupları bağlanırsa sterik etki nedeniyle düzlemsellikten sapmalar olur. Absorpsiyon dalga boyu ve değişir.

Anorganik maddelerin ışığı absorplaması: Na, K, Ca, Al gibi elementleri içeren anorganik maddeler 200 nm’in altında absorpsiyon yapar. Çoğu geçiş metali iyonları, spektrumun UV veya GB’de absorpsiyon gösterirler. Geçiş metallerinin spektral özellikleri, 3 d ve 4 d orbitallerinin çeşitli enerji seviyeleri arasındaki elektronik geçişlerden kaynaklanır. 81

Metal komplekslerinde elektronik geçişler Kompleks (koordinasyon bileşiği): Elektron boşluğu olan merkez atomu (M) veya iyonu ile üzerinde e- çifti bulunan iyon veya moleküllerin (L, ligant) koordine kovalent bağ yaparak oluşturduğu bileşiklerdir. M + n. L ==== MLn [Co(H 2 O)6]3+ Hekza aquakobalt(III) [Ag(NH 3)2]+ Diammingümüş(I) [Co(NH 3)6]Br 2 Hekzaminkobalt(II) bromür [Co(en)3)]2(SO 4)3 Tris(etilendiamin)kobalt(III) sülfat

Metal komplekslerinde elektronik geçişler d d geçişleri f f geçişleri Yük transfer (yük aktarım) geçişleri Metalden liganda yük transferleri Liganttan metale yük transferleri
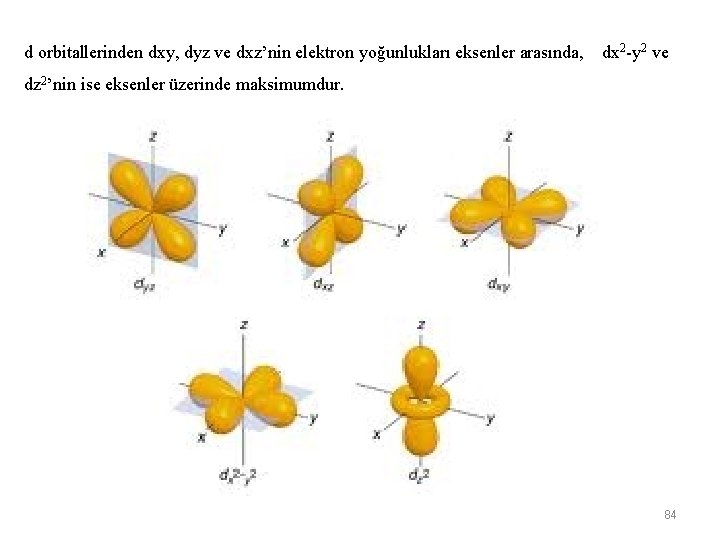
d orbitallerinden dxy, dyz ve dxz’nin elektron yoğunlukları eksenler arasında, dx 2 -y 2 ve dz 2’nin ise eksenler üzerinde maksimumdur. 84
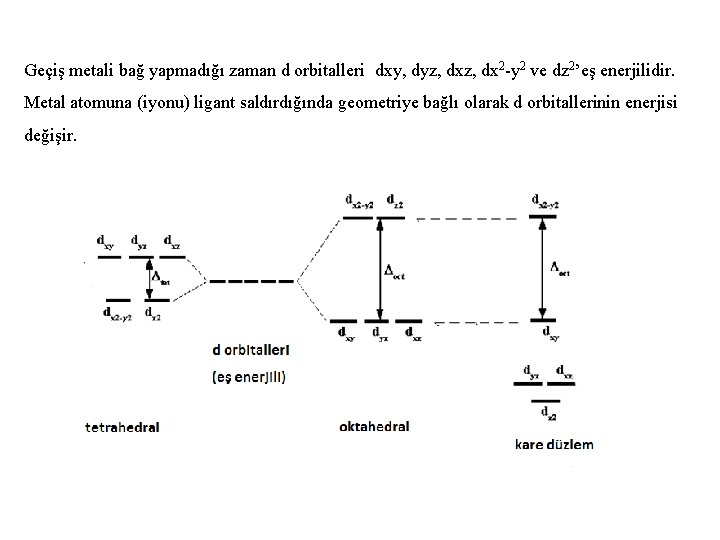
Geçiş metali bağ yapmadığı zaman d orbitalleri dxy, dyz, dx 2 -y 2 ve dz 2’eş enerjilidir. Metal atomuna (iyonu) ligant saldırdığında geometriye bağlı olarak d orbitallerinin enerjisi değişir.
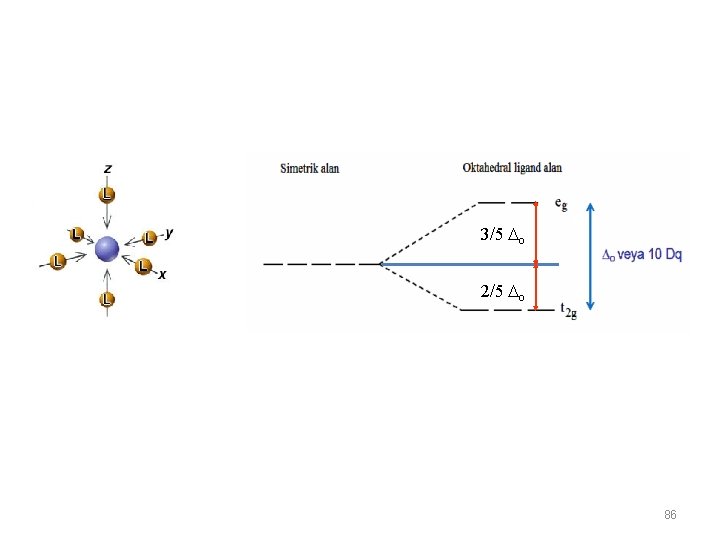
3/5 o 2/5 o 86
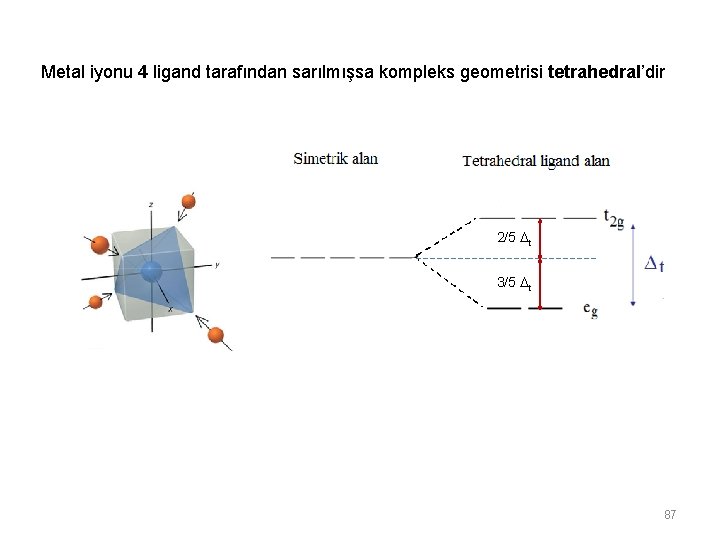
Metal iyonu 4 ligand tarafından sarılmışsa kompleks geometrisi tetrahedral’dir 2/5 t 3/5 t 87

d 0 ve d 10 yapısında d-d geçişleri olmaz ve rennksiz olması beklenir Zn 2+ d 10 iyonu renksiz Ti. F 4 d 0 iyonu beyaz Ti. Cl 4 d 0 iyonu beyaz Ti. Br 4 d 0 iyonu turuncu Ti. I 4 d 0 iyonu koyu kahve [Cr 2 O 7]- Cr(VI) d 0 koyu mor [Mn. O 4]- Mn(VII) d 0 turuncu [Cu(Me. CN)4]+ Cu(I) d 10 renksiz [Cu(phen)2]+ Cu(I) d 10 koyu turuncu

Yük transfer (aktarma) geçişleri Molar absorptiviteleri çok yüksektir ( maks> 10000) Yük aktarım absorpsiyonu olabilmesi için bileşenlerinden birinin elektron verici diğerinin ise elektron alıcı olması gerekir. Metalden liganta Fe(II) (o-fenontrolin) Liganttan metale Fe. SCN 2+ 89

Analitik Uygulamalar 1 -Yapı analizi UV-Gör spektroskopisi ile yapı analiz yapmak için saf örneğin çözeltisi hazırlanır ve spektrumu kaydedilir. Bu spektrum literatürdeki belli grupların spektrumlar ile karşılaştırılır. 90

UV/GB spektrumlarından yararlanarak maddenin yapısı ile ilgili bazı ipuçları elde edilebilir. 200 -210 nm’den daha büyük dalgaboylarında absorpsiyon yoksa, a) Konjuge gruplar b) C=O grupları c) Yüksek derecede sübstitüe olmuş C=C d) Halojenler ve tek bağlı oksijen hariç ortaklanmamış elektron çifti içeren başka bir atom olmadığı sonucuna varılabilir. 91 91

Madde spektrumunda 200 -300 nm arasında şiddetli bir absorpsiyon ( = 10 000 -20 000 L mol-1 cm-1) varsa, konjuge durumda en az iki kromofor grup var demektir. 300 nm üzerindeki şiddetli absorpsiyon ise daha ileri giden bir konjügasyonun varlığını gösterir. 92

Maddede 270 -400 nm’de görülen zayıf bir absorpsiyon ( = 10 -200 L mol-1 cm-1) N atomu yoksa, aldehid veya keton gruplarından birinin, N atomu varsa, C=N, N=N veya NO 2 gruplarından birinin varlığını gösterir. Spektrumda, 200 -280 nm arasında orta şiddette ( =5 000 -16 000 L mol-1 cm-1), 250 -300 nm arasında daha zayıfça ( =200 -5 000 L mol-1 cm-1), birer band görülen madde büyük olasılıkla sübstitüe olmuş bir benzen halkasıdır. 93
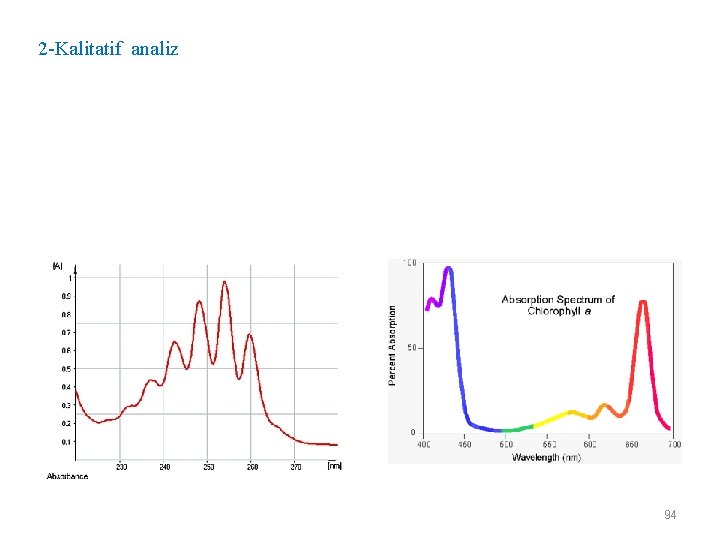
2 -Kalitatif analiz UV-Gör spektroskopisi ile kalitatif analiz yapmak için saf örneğin çözeltisi hazırlanır ve spektrumu kaydedilir. Bu spektrum standart maddenin spektrumu veya literatürdeki spektrumlar ile karşılaştırılır. Benzenin spektrumu 94
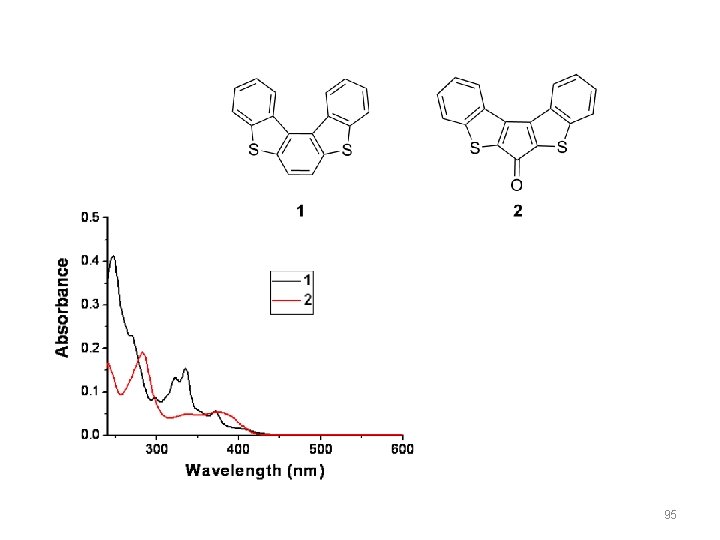
95

3 -Kantitatif Analiz Çözelti haline getirilen örneğin absorbansı ölçülür. Bu değer standart çözeltilerin absorbansı ile karşılaştırılarak derişimi bulunur. A=ϵlc Bunun için önce çalışma dalga boyu seçilir. -maksimum dalga boyu tercih edilir -girişimler dikkate alınır -pikin geniş olduğu dalga boyu seçilmelidir 96
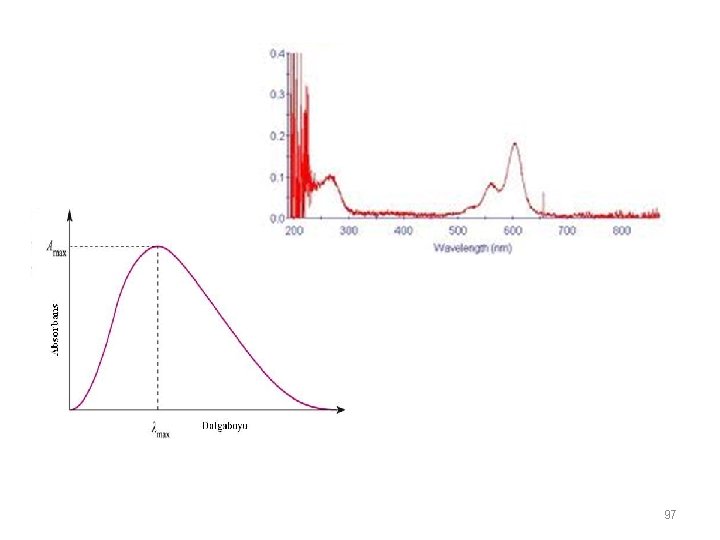
97
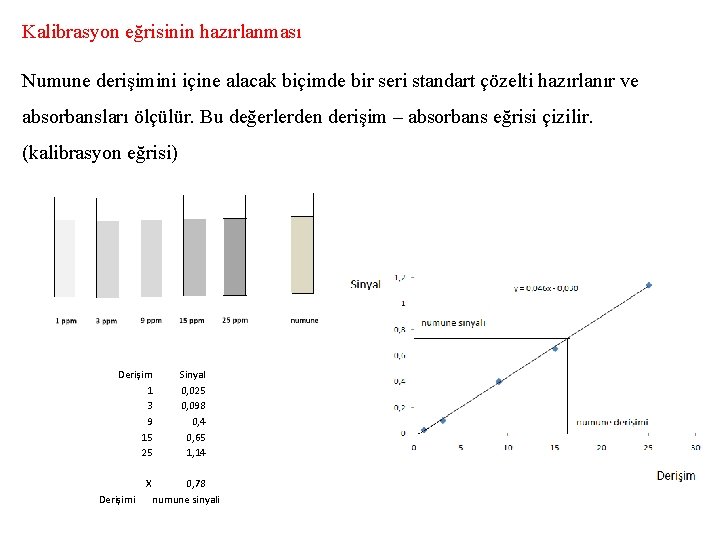
Kalibrasyon eğrisinin hazırlanması Numune derişimini içine alacak biçimde bir seri standart çözelti hazırlanır ve absorbansları ölçülür. Bu değerlerden derişim – absorbans eğrisi çizilir. (kalibrasyon eğrisi) Derişim 1 3 9 15 25 X Derişimi Sinyal 0, 025 0, 098 0, 4 0, 65 1, 14 0, 78 numune sinyali
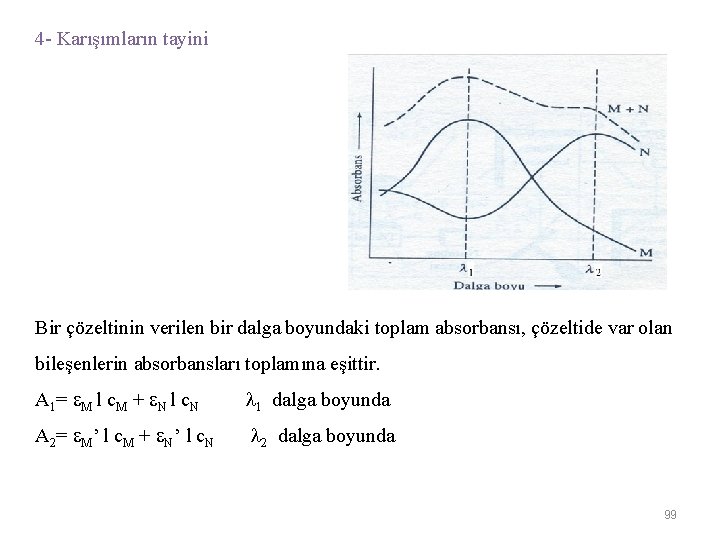
4 - Karışımların tayini Bir çözeltinin verilen bir dalga boyundaki toplam absorbansı, çözeltide var olan bileşenlerin absorbansları toplamına eşittir. A 1 = M l c M + N l c N 1 dalga boyunda A 2= M’ l c. M + N’ l c. N 2 dalga boyunda 99
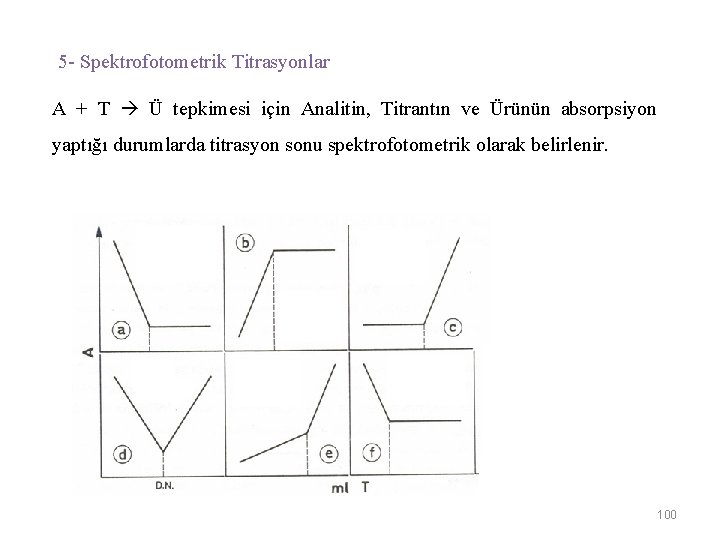
5 - Spektrofotometrik Titrasyonlar A + T Ü tepkimesi için Analitin, Titrantın ve Ürünün absorpsiyon yaptığı durumlarda titrasyon sonu spektrofotometrik olarak belirlenir. 100

6 - Komplekslerin stokiyometrilerinin belirlenmesi 1 -Job veya Sürekli Değişim Yöntemi 2 -Mol oranları yöntemi 3 -Eğim oranları yöntemi 101

7 -Zayıf asitlerin Ka’larının bulunması Asit çözeltisinin değişik p. H değerlerinde absorbansı ölçülür ve p. H / A grafiği çizilir. 102
- Slides: 102