CHROMATOGRAFIA PODZIA METOD I ICH ZASTOSOWANIE KLASYFIKACJA METOD

















- Slides: 21

CHROMATOGRAFIA PODZIAŁ METOD I ICH ZASTOSOWANIE

KLASYFIKACJA METOD CHROMATOGRAFICZNYCH Rodzaj metody Chromatografia cieczowa (LC) Chromatografia bibułowa (PC) Format Chromatografia cienkowarstwowa (TLC) Wysokosprawna chromatografia cieczowa (HPLC) Chromatografia nadkrytyczna (SFC) Chromatografia gazowa (GC) Chromatografia gaz-ciecz (GLC) Chromatografia gaz-ciało stałe (GSC) Technika planarna podział (adsorpcja, wymiana jonowa, wykluczenie) adsorpcja (podział, wymiana jonowa, wykluczenie) kolumnowa adsorpcja (podział, wymiana jonowa, wykluczenie) podział kolumnowa adsorpcja

Chromatografia bibułowa (PC) Format – planarna Mechanizm sorpcji (technika) – podział (również adsorpcja, wymiana jonowa, wykluczenie). Nośnik – bibuła Faza stacjonarna – ciekła – woda zawarta w higroskopijnej bibule. Faza ruchoma – rozpuszczalnik organiczny lub mieszanina. Rozpuszczalnik używany jest do rozwijania chromatogramu i do kondycjonowania bibuły przez jej nasycenie parami Komory do chromatografii bibułowej – różne naczynia o kształtach prostopadłościennych, cylindrycznych, a nawet próbówki. Nanoszenie próbki – podlega zasadom ogólnym chromatografii. Próbki nanoszone są w postaci roztworów w rozpuszczalnikach łatwo lotnych. Substancja rozdzielana przenoszona jest wraz z fazą ruchomą, ulegając podziałowi pomiędzy dwie niemieszające się ciecze: eluent i wodę związana z bibułą. Identyfikacja – porównanie z wzorcem chromatografowanym równocześnie

Chromatografia bibułowa – stosowane metody zależne od rodzaju przepływu eluentu po powierzchni bibuły: • Metoda wstępująca – brzeg bibuły zawieszonej linią startową do dołu zanurzony jest w pojemniku z rozpuszczalnikiem. • Metoda zstępująca lub spływowa – brzeg bibuły zawieszonej linią startową do góry zanurzony jest w korytku z rozpuszczalnikiem podwieszonym u góry komory chromatograficznej. Stosowane są paski lub arkusze bibuły prostokątne lub kwadratowe. Nie ma możliwości stosowania metody zwijania bibuły ze względu na sposób pobierania rozpuszczalnika. • Metoda pierścieniowa – bibuła leży poziomo, a rozpuszczalnik doprowadzany jest do punktu centralnego chromatogramu, gdzie naniesiony został roztwór mieszaniny. Bibuła ma w tym przypadku kształt krążków. • Metoda dwuwymiarowa lub dwukierunkowa – stosowana w przypadku niewystarczającego rozdzielenia składników po pierwszym rozwinięciu chromatogramu. Rozpuszczalnik migruje w dwóch kierunkach prostopadłych. Zwykle stosowane są też dwa różne rozpuszczalniki. Zwiększa to możliwość precyzyjnej identyfikacji. Arkusze bibuły są tu kwadratowe. • Metoda elektrochromatografii – rozpuszczalnik porusza się w polu elektrycznym do 400 V. Jest to przypadek połączenia chromatografii z elektroforezą. Stosowany wyłącznie do rozdziału ulegających jonizacji lub silnie polarnych.

Chromatografia cienkowarstwowa (TLC) Format – planarna Mechanizm sorpcji – podział, adsorpcja, wymiana jonowa, wykluczenie. Nośnik – płytki szklane, aluminiowe, plastikowe. Faza stacjonarna – drobnoziarniste sorbenty stałe o wielkości ziarna 10 -30 µm– żel krzemionkowy, celuloza, żywice jonowymienne, tlenek glinu, ziemia okrzemkowa, selektory chiralne. Grubość warstwy sorbentu 0, 2 -2, 5 mm. Może zawierać nierozpuszczalny odczynnik fluorescencyjny Faza ruchoma – pojedyncze rozpuszczalniki lub ich mieszaniny o różnej polarności – od niepolarnych węglowodorów do polarnych alkoholi, wody oraz rozpuszczalników kwasowych i zasadowych. Rozpuszczalnik porusza się dzięki siłom kapilarnym. Komory elucyjne – różne naczynia o kształtach prostopadłościennych lub cylindrycznych. Szczelnie zamknięte i wypełnione parami fazy ruchomej. Nanoszenie próbki – podlega zasadom ogólnym chromatografii. Substancja rozdzielana przenoszona jest wraz z fazą ruchomą przez płaskie złoże fazy stacjonarnej metodą pionową (wstępującą) lub horyzontalną. Identyfikacja – spryskiwanie odczynnikiem wywołującym reakcję barwną lub wskaźnikiem fluorescencyjnym dla obserwacji w świetle UV.

Fazy stacjonarne (sorbenty) w chromatografii cienkowarstwowej. Charakterystyka i zastosowanie Sorbent Mechanizm sorpcji Rozdzielane substancje Żel krzemionkowy (NP) adsorpcja aminokwasy, alkaloidy, witaminy Krzemionka modyfikowana węglowodorami (RP) Celuloza sproszkowana Tlenek glinu Ziemia okrzemkowa Celuloza jonowymienna Żel Sephadex β-cyklodekstryny zmodyfikowany podział związki niepolarne. podział, stereoadsorpcja węglowodany, aminokwasy, nukleotydy adsorpcja węglowodory, alkaloidy, barwniki, lipidy, jony met. podział cukry, kwasy tłuszczowe wymiana jonowa kwasy nukleinowe, nukleotydy, jony metali, halogenki wykluczenie polimery, białka, kompleksy metali stereoadsorpcja mieszaniny enancjomerów

Wykrywanie rozdzielonych składników (analiza jakościowa) • Wizualizacja przy pomocy odczynników chromogennych tworzącymi połączenia barwne ze wszystkimi lub niektórymi substancjami rozdzielanymi. • Oświetlanie promieniami UV (254, 315 i 370 nm) • Utlenianie i zwęglanie kwasem siarkowym (spryskiwanie) • Działanie par jodu - wiele substancji zabarwia się na brązowo • Skanowanie densytometryczne – pomiar natężenia promieniowania odbitego od powierzchni po naświetleniu jej promieniowaniem UV/VIS. Powstają piki wskazujące na obecność substancji absorbującej. • Wykrywanie substancji znakowanych wskaźnikami promieniotwórczymi (klisza fotograficzna, liczenie scyntylacji, skanowanie licznikiem Geigera-Müllera

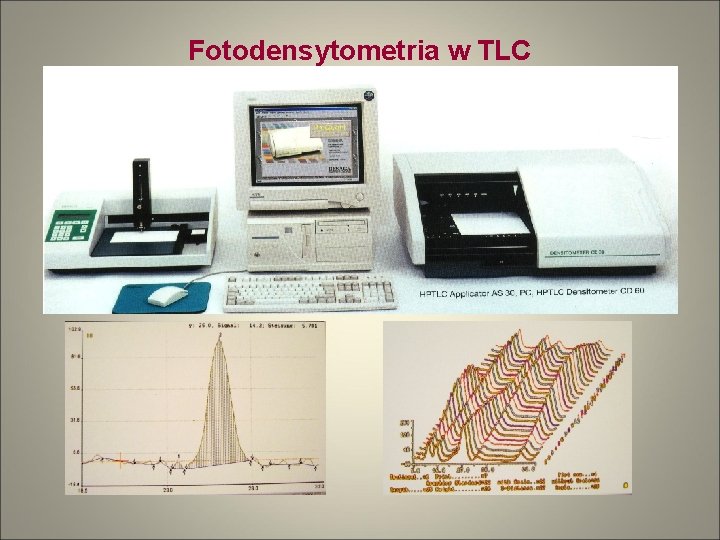
Oznaczenie składu mieszaniny (analiza ilościowa) • Metody bezpośrednie – poprzez pomiar powierzchni plamki. Do pomiaru używa się planimetru. Uwzględniana jest grubość warstwy sorbentu i aktywność substancji. Również nanoszone są na tę samą płytkę substancje wzorcowe w znanej ilości. • Fotodensytometria – w oznaczeniu stosowany jest pomiar światła odbitego lub przepuszczonego – głównie UV/VIS, analizowany w aparacie rejestrującym. Pomiar wysokości piku lub pola powierzchni pod pikiem. • Fluorymetria – pomiar natężenia światła emitowanego przez substancje fluoryzujące. • Oznaczenie pośrednie w eluatach – sorbent z powierzchni płytki zawierający plamkę ekstrahowany jest rozpuszczalnikiem a roztwór badany poddaje się analizie instrumentalnej (NMR, IR, UV lub innej).

Fotodensytometria w TLC

Inne procedury TLC Dwuwymiarowa TLC – stosowana dla pełnego rozdzielenia substancji o podobnych właściwościach chemicznych. Pojedynczą próbkę rozwija się po naniesieniu w polu startowym umieszczonym w rogu płytki. Składniki są częściowo rozdzielone wzdłuż jednego boku płytki. Chromatogram po wysuszeniu i obróceniu o 90 o rozwijany jest ponownie z użyciem fazy ruchomej o innym składzie. Otrzymuje się dwuwymiarową mapę składników. Wysokosprawna chromatografia cienkowarstwowa (HPTLC). Oznaczenie prowadzone jest według reguł klasycznej TLC. Stosowane są płytki pokryte cieńszą warstwą (0, 1 mm grubości) bardzo drobnoziarnistego sorbentu (średnia wielkość ziarna 5 µm). Zwiększa się czułość i rozdzielczość. Odczyty chromatogramów prowadzone są przy pomocy densytometru.

Porównanie metod TLC z GC i HPLC Zalety: - Możliwość chromatografowania wielu próbek równocześnie, np. w celu natychmiastowego i bezpośredniego porównania z wzorcem; - Możliwość zastosowania wszystkich mechanizmów sorpcji; - Podstawowa technika jest tania, wszechstronna i szybka; - Możliwość wykrycia wszystkich substancji rozdzielanych, łącznie z tymi, które nie migrują z punktu startu. Wady: - Ograniczona powtarzalność wyników; - Zmiany w składzie fazy ruchomej w czasie rozwijania chromatogramu; - Wzrastające rozmycie plamki (poszerzenia pasma) powodowane zmniejszeniem szybkości fazy ruchomej wraz z pokonywaną odległością.

Chromatografia gazowa (GC) Format – kolumnowa Mechanizm sorpcji (technika) – podział (gaz-ciecz GLC), adsorpcja (gaz-ciało stałe GSC). Wymywanie w kolejności rosnącej temp. wrzenia. Nośnik – ściana kolumny, drobnoziarniste ciało stałe. Faza stacjonarna – wysokowrzące ciecze, oleje, woski, stałe drobnoziarniste adsorbenty. Kolumny – długie, wąskie rurki kapilarne (otwarte) z fazą stacjonarną pokrywającą ściany lub krótkie rurki o większej średnicy, wypełnione sorbentem (kolumny pakowane). Faza ruchoma – obojętny gaz oczyszczany w absorbentach, a dostarczany z butli przez zawory regulujące ciśnienie i przepływ. Azot stosowany do kolumny pakowanej, hel w kolumnach kapilarnych. Dozowanie próbki – gazowe, ciekłe lub stałe – wprowadzane przez dozownik (mikrostrzykawka, zawór) do fazy ruchomej na szczycie kolumny w postaci roztworu 0, 5 -20µL. Rozpuszczalnik zostaje usunięty. Regulacja temperatury – kolumny znajdują się w termostatowanych piecach. Temperatura rozdziału jest stała lub regulowana (wzrastająca w czasie rozdziału. Temperatura elucji 50 -350 o. C. Identyfikacja – substancje rozdzielane wykrywane są w fazie ruchomej w kolejności elucji przez detektory. Detektor generuje sygnał elektryczny. Chromatogram stanowi wykres zależności stężenia od czasu retencji.

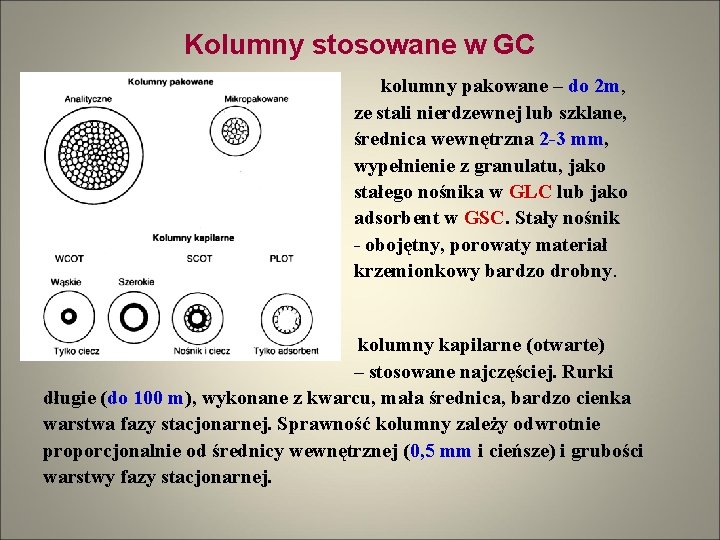
Kolumny stosowane w GC kolumny pakowane – do 2 m, ze stali nierdzewnej lub szklane, średnica wewnętrzna 2 -3 mm, wypełnienie z granulatu, jako stałego nośnika w GLC lub jako adsorbent w GSC. Stały nośnik - obojętny, porowaty materiał krzemionkowy bardzo drobny. kolumny kapilarne (otwarte) – stosowane najczęściej. Rurki długie (do 100 m), wykonane z kwarcu, mała średnica, bardzo cienka warstwa fazy stacjonarnej. Sprawność kolumny zależy odwrotnie proporcjonalnie od średnicy wewnętrznej (0, 5 mm i cieńsze) i grubości warstwy fazy stacjonarnej.

Fazy stacjonarne stosowane w GC Ciekłe fazy stacjonarne – wysokowrzące ciecze, oleje lub woski często o strukturze polimerowej. Niepolarne mają charakter węglowodorowy lub są dialkilowanymi siloksanami bez polarnych grup funkcyjnych. Polarne zawierają grupy funkcyjne: –CN; –CO; –OH, mają charakter poliestrowy – pochodne poli(dimetylosiloksanu) lub poli(glikolu etylenowego). Faza stacjonarna związana i usieciowana – krzemionkowa powierzchnia kolumny może być pokryta chemicznie związaną warstwą molekularną fazy stacjonarnej. Faza ta może być usieciowana przez wytworzenie wewnętrznych wiązań węgiel-węgiel dzięki ogrzewaniu w obecności nadtlenków. Pożądane właściwości nieruchomej fazy ciekłej – mała lotność (temperatura wrzenia o 100 o wyższa od temperatury oznaczenia); stabilność termiczna; odporność chemiczna; charakterystyka rozpuszczalnika (powinowactwo)

Detektory stosowane w GC Płomieniowo-jonizacyjny – najczęściej stosowany do badania węglowodorów, detektor uniwersalny. Wymywana substancja ulega pirolizie w płomieniu powietrzno-wodorowym tworząc jony i elektrony. Detekcja związana jest z pomiarem prądu wytworzonego przez te nośniki (zwiększenie przewodności elektrycznej płomienia). Odmiana – termojonowy selektywny dla związków azotu i fosforu. Termokonduktometryczny – cieplno-przewodnościowy detektor uniwersalny – katarometr. Ogrzewane źródło – drut platynowy, złoty lub wolframowy zmienia oporność w zależności od temperatury zmieniającej się wraz ze zmianą przewodności cieplnej gazu przepływającego. Wychwytu elektronów – czuły i selektywny dla związków organicznych z elektroujemnymi grupami funkcyjnymi. Bardzo funkcjonalny. Promieniotwórczy emiter powoduje jonizację gazu nośnego i wyrzucenie elektronów. Natężenie prądu maleje pod wpływem czynników zdolnych do wychwytu elektronów. Spektrometr mas – cząsteczki próbki ulegają jonizacji w źródle jonów. Mierzony jest stosunek masy do ładunku jonów powstających.

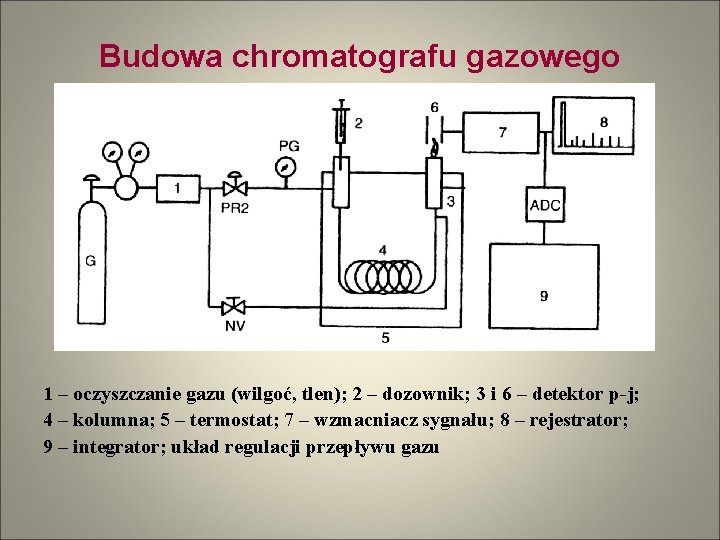
Budowa chromatografu gazowego 1 – oczyszczanie gazu (wilgoć, tlen); 2 – dozownik; 3 i 6 – detektor p-j; 4 – kolumna; 5 – termostat; 7 – wzmacniacz sygnału; 8 – rejestrator; 9 – integrator; układ regulacji przepływu gazu

Wysokosprawna chromatografia cieczowa (HPLC) Format – kolumnowa Mechanizm sorpcji (technika) – podział, adsorpcja, wymiana jonowa, wykluczenie, powinowactwa i chiralna. Składniki rozdzielają się na podstawie szybkości migracji zależnej od powinowactwa do faz. Nośnik – ściana kolumny, drobnoziarniste ciało stałe. Faza stacjonarna – modyfikowana krzemionka, niemodyfikowana krzemionka, żywice polimerowe, żele. Kolumny – proste rurki ze stali nierdzewnej (dł. 5 -25 cm, śr. 4, 5 -10 mm) wypełnione fazą stacjonarną drobnoziarnistą lub polimerem. Faza ruchoma – jeden rozpuszczalnik lub ich mieszanina (do czterech składników). Organiczne rozpuszczalniki niepolarne do wodnych roztworów buforowych. Dostarczane po przejściu przez system odgazowania, filtracji i mieszania na szczyt kolumny pompą stałoprzepływową. Dozowanie próbki – ciekłe próbki i roztwory wprowadzane przez dozownik (zawór) do fazy ruchomej na szczycie kolumny. Identyfikacja – substancje rozdzielane wykrywane są w fazie ruchomej w kolejności wypływu przez detektor – zależność stężenia od czasu. Detektory – absorpcyjny; fluorescencyjny; elektrochemiczny, FTIR; spektrometr mas; refraktometryczny; konduktometryczny

Fazy stacjonarne (sorbenty) w chromatografii HPLC. Charakterystyka i zastosowanie Faza stacjonarna Mechanizm sorpcji Charakterystyka Niemodyfikowana krzemionka adsorpcja NP polarna, uniwersalna Krzemionka modyfikowana z węglowodorami C 2 -C 18 zmodyfikowany podział niepolarne, uniwersalne RP K. z grupami aminopropylowymi zmodyfikowany podział polarna do rozdziału NP lub RP węglowodanów K. z grupami sulfonowymiana kationowa K. z czwartorzędowymi grupami amoniowymiana anionowa K. o regulowanej porowatości wykluczenie uniwersalna K. z α, β, γ-cyklodekstryną selektywność chiralna kosztowna, nietrwała Usieciowane kopolimery styren/diwinylobenzen podział, wykluczenie, wymiana jonowa niepolarna, niemodyfikowana jest trwała Inne, specjalne powinowactwo ograniczona pojemność i p. H 2, 5 -7, 5

Detektory systemu HPLC Spektrometryczny UV-VIS - jest najszerzej stosowany. Dokonuje pomiaru absorbancji rozdzielanych składników (w zakresie nadfioletu i światła widzialnego 200 -870 nm) zawierających grupy chromoforowe. Odmiany – fotometr z filtrami; spektrofotometr o zmiennej długości fali (wykres dwuwymiarowy); typu photodiode array wyposażony w dwa lub więcej szeregi fotodiod (wykres trójwymiarowy) Fluorymetryczny – reaguje selektywnie na substancje fluoryzujące. Jest bardziej selektywny i czuły od spektrometrycznego. Refraktometryczny – najbardziej uniwersalne. Pomiar zmiany współczynnika załamania światła fazy ruchomej (różnicowy). Mniej czuły od spektrometrycznego, cenny w przypadku rozdzielania związków nasyconych (cukry, alkany). Elektrochemiczny – pomiar przewodności dla substancji jonowych lub prądu w reakcji elektrochemicznego utlenienia lub redukcji. Spektrometr mas – możliwość identyfikacji wszystkich substancji. Wymaga usunięcia rozpuszczalnika i przeprowadzenia próbki w stan gazowy.

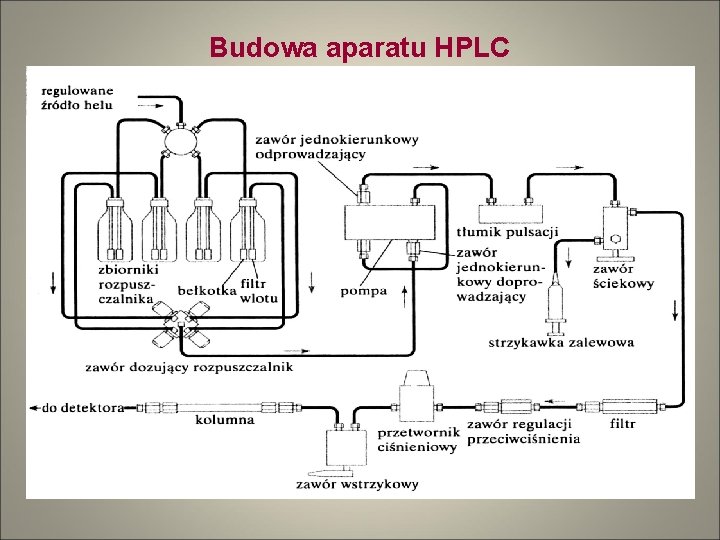
Budowa aparatu HPLC

Odmiany HPLC Chromatografia adsorpcyjna – w normalnym lub odwróconym układzie faz. Substancje rozdzielane konkurują o dostęp do grup silanolowych f. stacjonarnej i wymywane są z kolumny w kolejności wzrastającej polarności. Chromatografia podziałowa zmodyfikowana (chromatografia z fazą związaną (BPC). – faza stacjonarna to modyfikowana chemicznie krzemionka. Rodzaj związanego czynnika modyfikującego decyduje o zastosowaniu. Również chromatografia powinowactwa. Chromatografia jonowymienna (IEC) – do rozdzielania substancji jonowych na kopolimerach usieciowanych z mobilnymi jonami. Chromatografia jonowa (CI) – cienka warstwa jonowymienna umieszczona na powierzchni porowatej. Faza ruchoma – roztwory elektrolitów. Chromatografia wykluczenia – zależnego od wielkości cząsteczek. Faza stacjonarna – usieciowany kopolimer. Rzeczywistemu rozdzieleniu ulegają tylko cząstki o wymiarach pośrednich porów. Chromatografia chiralna – chiralne fazy stacjonarne (cyklodekstryny związane z krzemionką) rozdzielają enancjomery związków.