EQUILBRIO QUMICO PROCESSOS REVERSVEIS So processos que reagentes

EQUILÍBRIO QUÍMICO
PROCESSOS REVERSÍVEIS São processos que reagentes e produtos são consumidos e produzidos ao mesmo tempo ÁGUA Os reagentes e produtos das reações reversíveis são separados por uma dupla seta H 2 O ( l ) H 2 O (v) PROF. AGAMENON ROBERTO
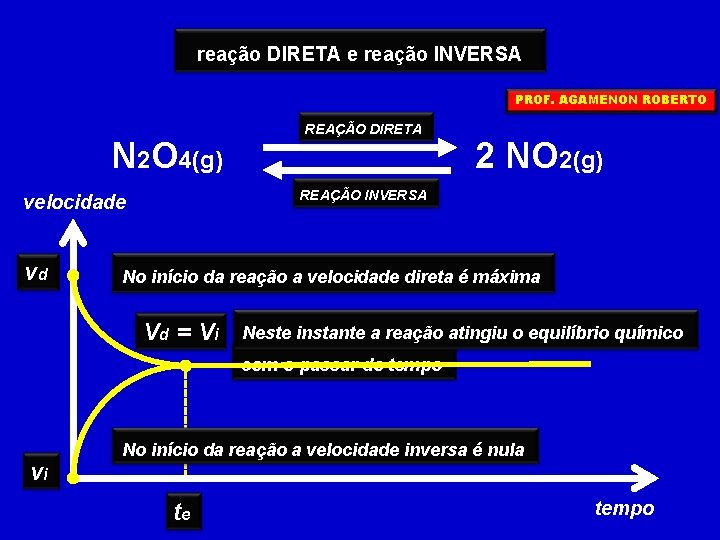
reação DIRETA e reação INVERSA PROF. AGAMENON ROBERTO N 2 O 4(g) 2 NO 2(g) REAÇÃO INVERSA velocidade vd REAÇÃO DIRETA No início da reação a velocidade direta é máxima Vd = V i Neste instante a reação atingiu o equilíbrio químico com o passar do tempo vi No início da reação a velocidade inversa é nula te tempo
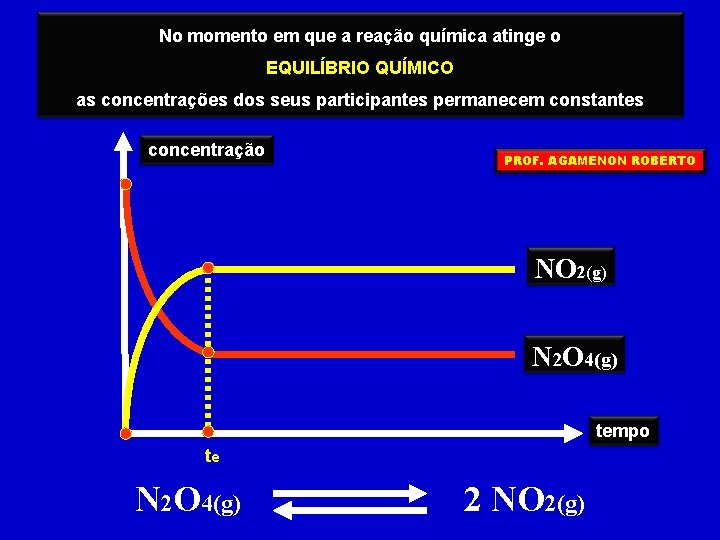
No momento em que a reação química atinge o EQUILÍBRIO QUÍMICO as concentrações dos seus participantes permanecem constantes concentração PROF. AGAMENON ROBERTO NO 2(g) N 2 O 4(g) tempo te N 2 O 4(g) 2 NO 2(g)
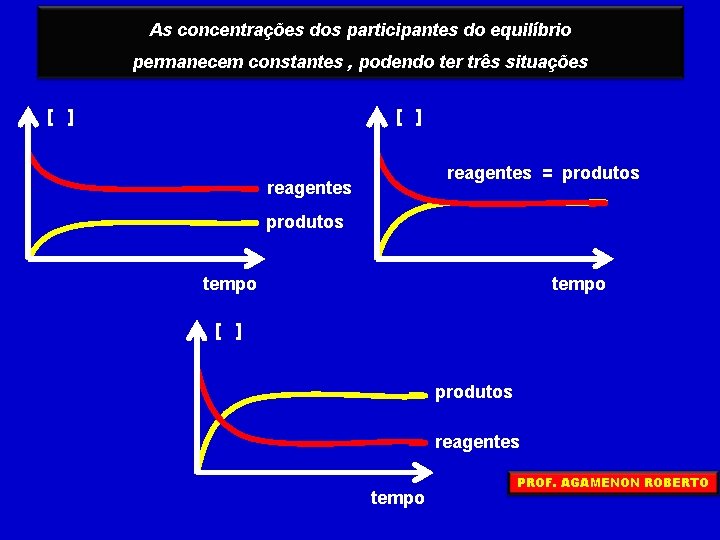
As concentrações dos participantes do equilíbrio permanecem constantes , podendo ter três situações [ ] reagentes = produtos reagentes produtos tempo [ ] produtos reagentes tempo PROF. AGAMENON ROBERTO

01) Sobre equilíbrio químico: 0 0 Uma reação é reversível quando se processa simultaneamente nos dois sentidos. 1 1 Uma reação reversível atinge o equilíbrio quando as velocidades das reações direta e inversa se igualam. 2 2 O equilíbrio das reações é dinâmico 3 3 Ao atingir o estado de equilíbrio, a concentração de cada substância do sistema permanece constante. 4 4 Todas as reações reversíveis caminham espontaneamente para o estado de equilíbrio. PROF. AGAMENON ROBERTO

CONSTANTE DE EQUILÍBRIO EM TERMOS DE CONCENTRAÇÃO MOLAR Vamos considerar uma reação reversível genérica a A+ b. B 1 c C+ d. D 2 PROF. AGAMENON ROBERTO No equilíbrio teremos: K 1. [ A ] a. [ B V ]b 1 = V K 22. [ C ]C. [ D ]d Isolando-se as constantes K 1 [ C ]C. [ D ] d KC = K 2 [ A ]a. [ B ] b

I. O valor de KC depende da reação considerada e da temperatura. II. O valor de KC independe das concentrações iniciais dos reagentes III. A constante de equilíbrio é tratada como um número puro, isto é, sem unidades IV. Líquidos e sólidos puros, que não fazem parte da solução, não constam da expressão da constante de equilíbrio PROF. AGAMENON ROBERTO

N 2(g) + 3 H 2(g) Kc = 2 H 2 O( g ) Kc = 2 NH 3 (g) [NH 3]2 [N 2]. [H 2]3 2 H 2(g) + O 2(g) [H 2]2. [O 2] [H 2 O]2 PROF. AGAMENON ROBERTO

01) Na equação abaixo, após atingir o equilíbrio químico, podemos concluir a respeito da constante de equilíbrio que: 1 a A+ b. B c C+ d. D 2 a) Quanto maior for o valor de Kc, menor será o rendimento da reação direta. b) Kc independe da temperatura. c) Se as velocidades das reações direta e inversa forem iguais, então K 2 = 0. d) Kc depende das molaridades iniciais dos reagentes. e) Quanto maior for o valor de Kc, maior será a concentração dos produtos. PROF. AGAMENON ROBERTO

02) (Covest – 98) Medidas de concentração para o sistema abaixo, em equilíbrio, a uma certa temperatura forneceram os seguintes resultados: [ H 2 ] = 0, 10 mol/L H 2 ( g ) + I 2 ( g ) 2 HI ( g ) [ I 2 ] = 0, 20 mol/L [ HI ] = 1, 0 mol/L Determine a constante de equilíbrio da reação nestas condições. Kc = [HI]2 [H 2]. [I 2] = (1, 0)2 0, 1. 0, 2 = 1, 0 0, 02 KC = 50 PROF. AGAMENON ROBERTO
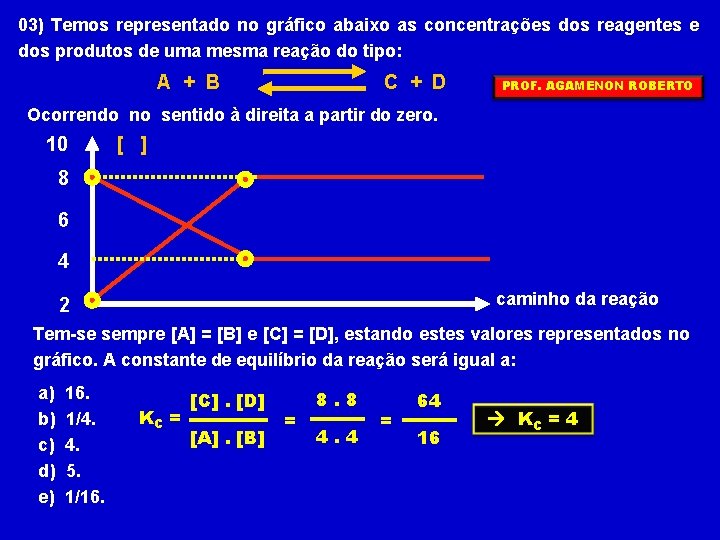
03) Temos representado no gráfico abaixo as concentrações dos reagentes e dos produtos de uma mesma reação do tipo: A + B C + D PROF. AGAMENON ROBERTO Ocorrendo no sentido à direita a partir do zero. 10 [ ] 8 6 4 caminho da reação 2 Tem-se sempre [A] = [B] e [C] = [D], estando estes valores representados no gráfico. A constante de equilíbrio da reação será igual a: a) b) c) d) e) 16. 1/4. 4. 5. 1/16. KC = [C]. [D] [A]. [B] = 8. 8 4. 4 = 64 16 KC = 4

04) Foram colocados em um recipiente fechado, de capacidade 2, 0 L, 6, 5 mol de CO e 5 mol de NO 2. À 200°C o equilíbrio foi atingido e verificou-se que haviam sido formados 3, 5 mol de CO 2. PROF. AGAMENON ROBERTO Podemos dizer que o valor de Kc para o equilíbrio dessa reação é: a) 4, 23. CO + NO 2 b) 3, 84. c) 2, 72. início 6, 5 d) 1, 96. reage / produz 3, 5 equilíbrio 3, 0 e) 3, 72. [ CO 2 ] = [ NO ] [ CO ] [ NO 2 ] = = = 3, 5 2, 0 3, 0 2, 0 1, 5 2, 0 = 1, 75 M CO 2 + NO 5, 0 0, 0 3, 5 1, 5 3, 5 KC = [ CO 2 ] [ CO ] = 1, 75 M KC = 1, 50 M KC = = 0, 75 M 1, 75 x x 3, 0625 1, 125 [ NO ] x x [ NO 2 ] 1, 75 0, 75 KC = 2, 72

05) Em um recipiente de 400 m. L são colocados 2 mols de PCl 5 gasoso a uma determinada temperatura. Esse gás se decompõem segundo a reação química abaixo, e, o equilíbrio foi alcançado quando 20% do pentacloreto de fósforo reagiram (% em mols). A constante de equilíbrio, Kc, nessas condições, vale: a) 4, 0. PCl 5 PCl 3 início 2, 0 0, 0 d) 0, 25. reage / produz 0, 4 e) 0, 025. equilíbrio 1, 6 0, 4 b) 1, 0. c) 0, 5. Reage : n = 0, 2 x 2 = 0, 4 mol [ PCl 3 ] [ Cl 2 ] [ PCl 5 ] = 0, 4 = 1, 6 0, 4 KC = [ PCl 3 ] x [ Cl 2 ] [ PCl 5 ] = 1, 0 M = 4, 0 M KC = + 1, 0 4, 0 KC = 0, 25 Cl 2 = 1, 0 x 1, 0 4, 0 PROF. AGAMENON ROBERTO

Considere um sistema em equilíbrio químico, com as substâncias A, B, C e D. A + B C + D Se, por algum motivo, houver modificação em uma das velocidades, teremos mudanças nas concentrações das substâncias Esta modificação em uma das velocidades ocasiona o que denominamos de DESLOCAMENTO DO EQUILÍBRIO que será no sentido da MAIOR VELOCIDADE PROF. AGAMENON ROBERTO
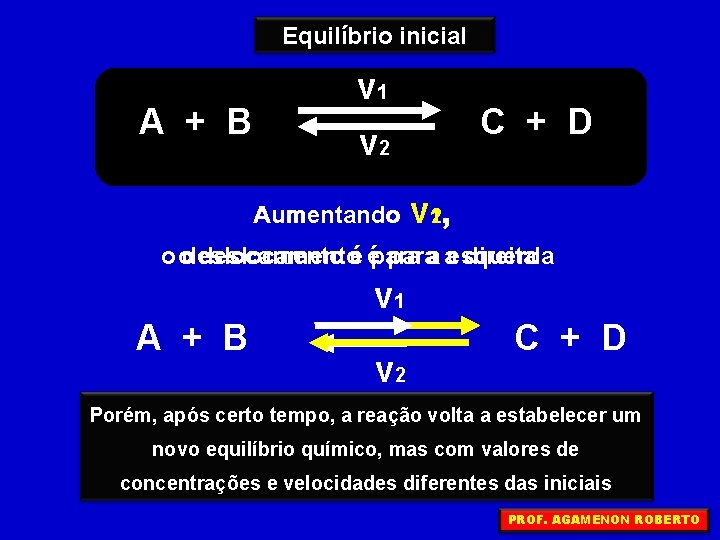
Equilíbrio inicial A + B v 1 C + D v 2 Aumentando v 12, o odeslocamentoé éparaa aesquerda direita v 1 A + B v 2 C + D Porém, após certo tempo, a reação volta a estabelecer um novo equilíbrio químico, mas com valores de concentrações e velocidades diferentes das iniciais PROF. AGAMENON ROBERTO

O químico Henri Louis Le Chatelier propôs um princípio que afirma: “Quando um sistema em equilíbrio sofre algum tipo de perturbação externa, ele se deslocará no sentido de minimizar essa perturbação, a fim de atingir novamente uma situação de equilíbrio” PROF. AGAMENON ROBERTO
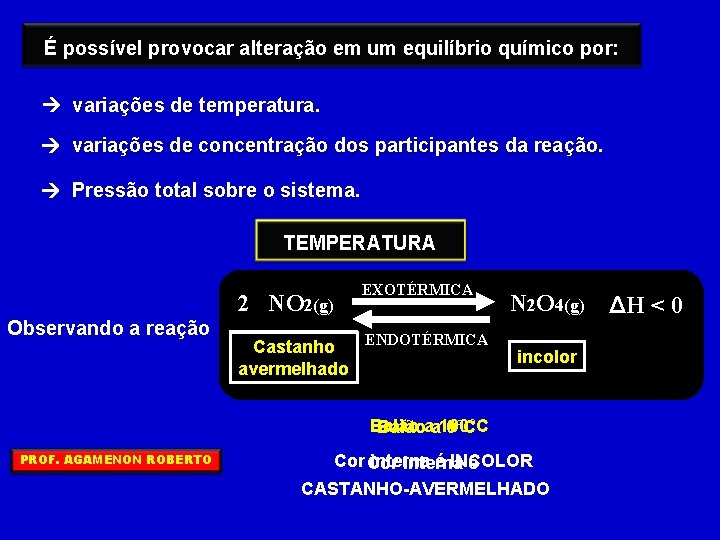
É possível provocar alteração em um equilíbrio químico por: variações de temperatura. variações de concentração dos participantes da reação. Pressão total sobre o sistema. TEMPERATURA 2 NO 2(g) Observando a reação EXOTÉRMICA ENDOTÉRMICA Castanho avermelhado N 2 O 4(g) incolor Balãoaa 100°C PROF. AGAMENON ROBERTO Cor interna é INCOLOR interna é CASTANHO-AVERMELHADO ΔH < 0

Podemos observar que o aumento da temperatura favorece a reação que é ENDOTÉRMICA, e a redução da temperatura favorece a reação que é EXOTÉRMICA Podemos generalizar dizendo que um(a). . . AUMENTO DE TEMPERATURA desloca o equilíbrio no SENTIDO ENDOTÉRMICO DIMINUIÇÃO DE TEMPERATURA desloca o equilíbrio no SENTIDO EXOTÉRMICO PROF. AGAMENON ROBERTO
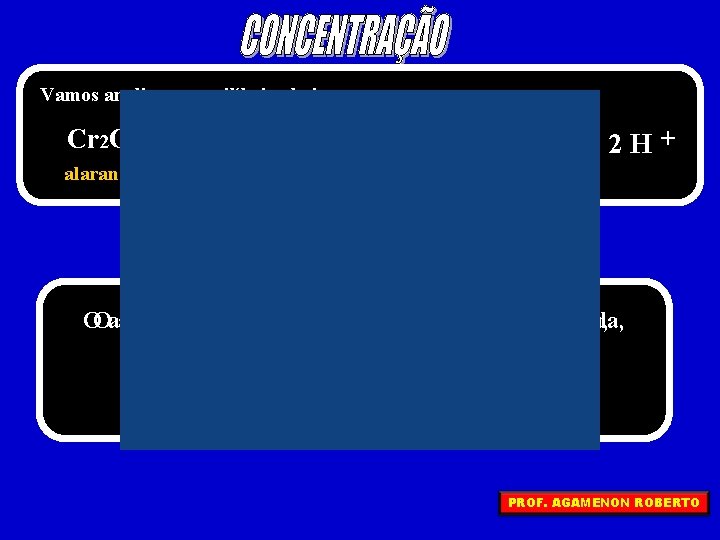
Vamos analisar o equilíbrio abaixo: Cr 2 O 7 2– alaranjada + H 2 O 1 2 2 Cr. O 4 2– + 2 H+ amarela OOacréscimode deum uma ácido basedeixaaasoluçãoalaranjada, amarela, deslocando ooequilíbrioparaaaesquerda direita PROF. AGAMENON ROBERTO

Podemos generalizar afirmando que um(a). . . AUMENTO DE CONCENTRAÇÃO desloca o equilíbrio no SENTIDO OPOSTO da espécie química adicionada DIMINUIÇÃO DE CONCENTRAÇÃO desloca o equilíbrio no mesmo MESMO SENTIDO da espécie retirada PROF. AGAMENON ROBERTO
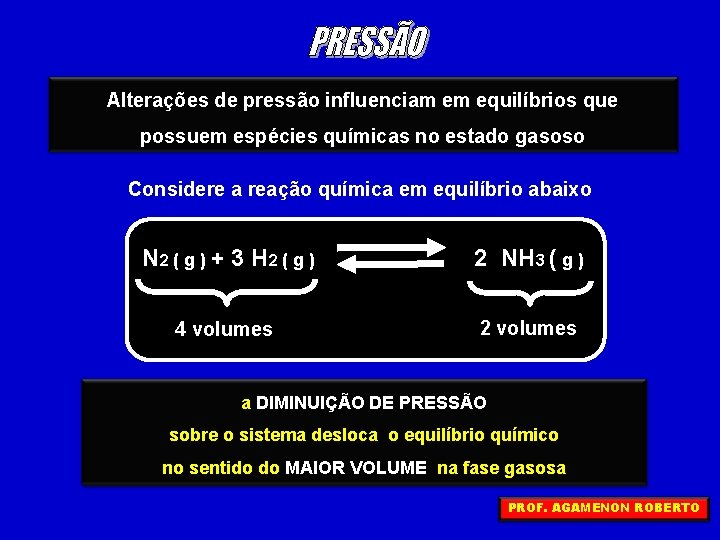
Alterações de pressão influenciam em equilíbrios que possuem espécies químicas no estado gasoso Considere a reação química em equilíbrio abaixo N 2 ( g ) + 3 H 2 ( g ) 2 NH 3 ( g ) 4 volumes 2 volumes ao. DIMINUIÇÃO DEPRESSÃO AUMENTO DE sobre o sistema desloca o equilíbrio químico no sentido do do MENOR MAIOR VOLUME no VOLUME na nafasegasosa PROF. AGAMENON ROBERTO

01) Considere a reação em equilíbrio químico: N 2 (g) + O 2 (g) 2 NO (g) É possível deslocá-lo para a direita: a) Retirando o N 2 existente. b) Removendo o NO formado. c) Introduzindo um catalisador. d) Diminuindo a pressão, à temperatura constante. e) Aumentando a pressão, à temperatura constante. PROF. AGAMENON ROBERTO

02) Temos o equilíbrio: CO( g ) + H 2 O( g ) CO 2( g ) + H 2( g ) Queremos aumentar a concentração de CO 2(g) nesse equilíbrio. Para isso ocorrer, devemos: a) Aumentar a pressão sobre o sistema. b) Diminuir a pressão sobre o sistema. c) Adicionar H 2(g) ao sistema. d) Retirar H 2 O(g) do sistema. e) Adicionar CO(g) ao sistema. PROF. AGAMENON ROBERTO

03) O equilíbrio gasoso representado pela equação : N 2( g ) + O 2( g ) 2 NO( g ) – 88 kj É deslocado no sentido de formação de NO(g), se : a) a pressão for abaixada. b) N 2 for retirado. c) a temperatura for aumentada. d) for adicionado um catalisador sólido ao sistema. e) o volume do recipiente for diminuído. PROF. AGAMENON ROBERTO

04) Nitrogênio e hidrogênio reagem para formar amônia segundo a equação: N 2( g ) + 3 H 2( g ) 2 NH 3( g ) + 22 kcal Se a mistura dos três gases estiver em equilíbrio, qual o efeito, em cada situação, sobre a quantidade de amônia, se provocar I. Compressão da mistura. aumenta II. Aumento de temperatura. diminui III. Introdução de hidrogênio. aumenta a) aumenta, aumenta. b) diminui, aumenta, diminui. c) aumenta, diminui. d) diminui, aumenta. e) aumenta, diminui, aumenta. PROF. AGAMENON ROBERTO

É o caso especial de equilíbrio químico em que aparecem íons Cr 2 O 7 2– + H 2 O 2 Cr. O 4 2– + 2 H+ Nos equilíbrios iônicos, também são definidos um grau de ionização ( a ) e uma constante de equilíbrio ( Ki ) PROF. AGAMENON ROBERTO
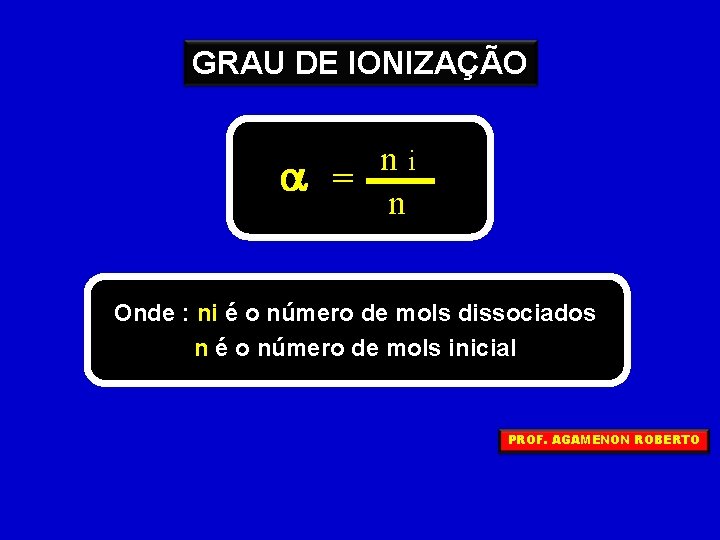
GRAU DE IONIZAÇÃO a ni = n Onde : ni é o número de mols dissociados n é o número de mols inicial PROF. AGAMENON ROBERTO
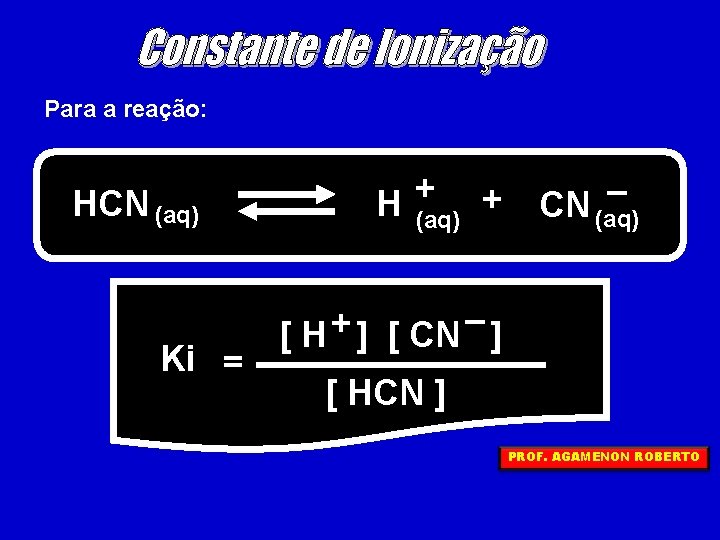
Para a reação: HCN (aq) Ki = + H (aq) + – CN (aq) – + [ H ] [ CN ] [ HCN ] PROF. AGAMENON ROBERTO
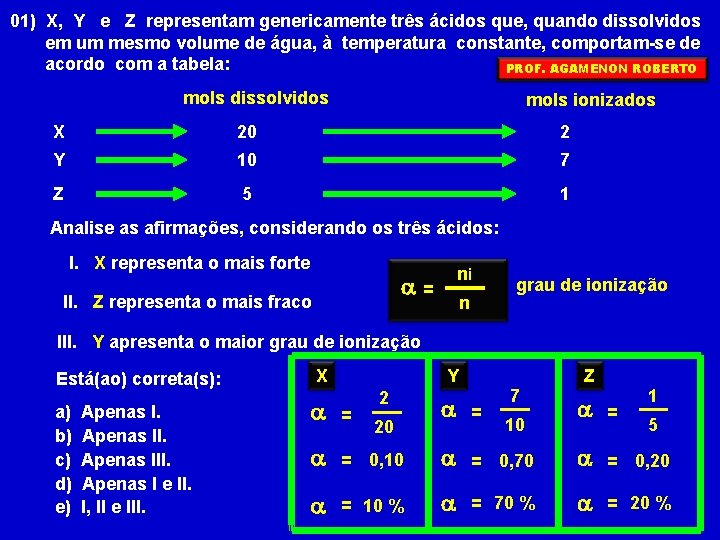
01) X, Y e Z representam genericamente três ácidos que, quando dissolvidos em um mesmo volume de água, à temperatura constante, comportam-se de acordo com a tabela: PROF. AGAMENON ROBERTO mols dissolvidos mols ionizados X 20 2 Y 10 7 Z 5 1 Analise as afirmações, considerando os três ácidos: I. X representa o mais forte ni a= II. Z representa o mais fraco n grau de ionização III. Y apresenta o maior grau de ionização Está(ao) correta(s): X a) b) c) d) e) a = a a Apenas III. Apenas I e II. I, II e III. Y 2 Z a = = 0, 10 a = 10 % a 20 7 1 a = = 0, 70 a = 0, 20 = 70 % a = 20 % 10 5

H+ + H 3 C – COO – 02) (FUVEST-SP) A reação H 3 C – COOH Ka = 1, 8 x 10– 5 tem Dada amostra de vinagre foi diluída com água até se obter uma solução de [H+] = 1, 0 x 10 – 3 mol/L Nesta solução as concentrações em mol/L de CH 3 COO – e de CH 3 COOH são, respectivamente, da ordem de: a) 3 x 10 – 1 e 5 x 10 [ H+] = 1, 0 x 10 – 3 – 10. b) 3 x 10 – 1 e 5 x 10 – 2. [ CH 3 COO – ] = 1, 0 x 10 c) 1 x 10 – 3 e 5 x 10 – 5. d) 1 x 10 – 3 e 5 x 10 – 12. e) 1 x 10 1, 8 x 10 – 5 = – 3 e 5 x 10 [ CH 3 COO – ] [ CH 3 COOH ] 1, 0 x 10 – 3 [ CH 3 COOH ] = Ki = – 2. [ H+ ] – 3 x 1, 0 x 10 – 3 [ CH 3 COOH ] 1, 0 x 10 – 3 x 1, 0 x 10 – 3 1, 8 x 10 – 5 PROF. AGAMENON ROBERTO = 5, 0 x 10 – 2

É uma lei que relaciona o grau de ionização com o volume (diluição) da solução Ki = m α 2 para solução de grau 1– α de ionização pequeno Ki = m α 2 PROF. AGAMENON ROBERTO
![DEMONSTRAÇÃO DA FÓRMULA HA Para a reação: início equilíbrio Ki = [ H+ ] DEMONSTRAÇÃO DA FÓRMULA HA Para a reação: início equilíbrio Ki = [ H+ ]](http://slidetodoc.com/presentation_image/04c120a76f848fc9fbc8e0eacc6c8f99/image-33.jpg)
DEMONSTRAÇÃO DA FÓRMULA HA Para a reação: início equilíbrio Ki = [ H+ ] ] mα 1 – α – (aq) 0, 0 ni = nα nα nα n –– n α nα nα n(1 – α ) nα nα V V V = nα x V nα V n(1– α) 2 A + 0, 0 [ A– ] [ HCN ] Ki = (aq) n reage / produz [ H + (aq) PROF. AGAMENON ROBERTO = n α V x V n(1 – α ) V para solução de grau de ionização pequeno Ki = m α 2
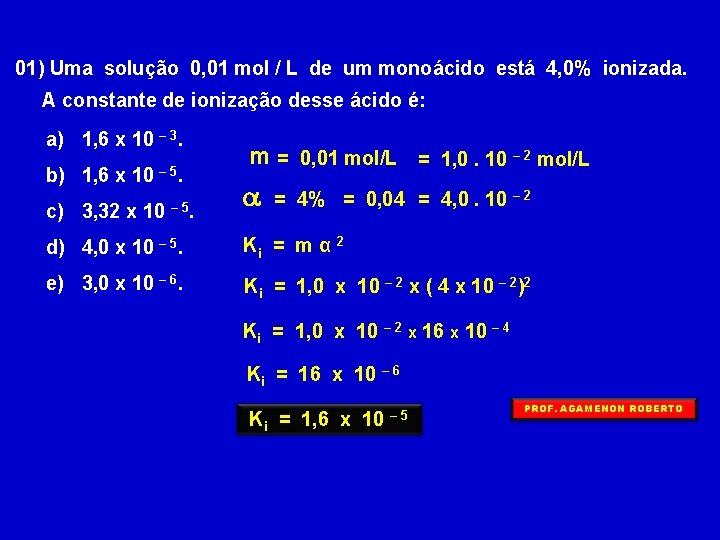
01) Uma solução 0, 01 mol / L de um monoácido está 4, 0% ionizada. A constante de ionização desse ácido é: a) 1, 6 x 10 – 3. b) 1, 6 x 10 – 5. c) 3, 32 x 10 – 5. m = 0, 01 mol/L = 1, 0. 10 – 2 mol/L a = 4% = 0, 04 = 4, 0. 10 – 2 d) 4, 0 x 10 – 5. Ki = m α 2 e) 3, 0 x 10 – 6. Ki = 1, 0 x 10 – 2 x ( 4 x 10 – 2)2 Ki = 1, 0 x 10 – 2 x 16 x 10 – 4 Ki = 16 x 10 – 6 Ki = 1, 6 x 10 – 5 PROF. AGAMENON ROBERTO

02) A constante de ionização de um ácido HX, que se encontra 0, 001% dissociado, vale 10 – 11. A molaridade desse ácido, nessas condições é : – 11 a) 10 α = 0, 001% = 0, 00001 = 1, 0 x 10 – 5 b) 0, 001 Ki = 10 – 11 c) 10 – 5 d) 0, 10. e) 1, 00. PROF. AGAMENON ROBERTO m = ? Ki = m α 2 10 – 11 = m x ( 1, 0 x 10 – 5)2 10 – 11 = m x 10 – 10 10 – 11 m = 10 – 10 m = 10 – 1 m = 0, 10 mol/L

03) O grau de dissociação iônica do hidróxido de amônio em solução 2 mol/L é 0, 283% a 20°C. A constante de ionização da base, nesta temperatura, é igual a: a) 1, 6 x 10 – 5 α = 0, 283% = 0, 00283 = 2, 83. 10 – 3 b) 1, 0 x 10 – 3 m = 2 mol/L c) 4, 0 x 10 – 3 Ki = ? d) 4, 0 x 10 – 2 e) 1, 6 x 10 – 1 Ki = m α 2 Ki = 2, 0 x Ki = 2 x 8 ( 2, 83 x 10 – 3)2 x 10 – 6 Ki = 16 x 10 – 6 Ki = 1, 6 x 10 – 5 PROF. AGAMENON ROBERTO

04) (FAMECA – SP) Qual o valor de “Ka” para o HCN, sabendo-se que o ácido em solução 0, 10 mol/L encontra-se 0, 006% ionizado? a) 1, 2 x 10 – 4. b) 3, 6 x 10 – 10. c) 3, 6 x 10 – 8. d) 3, 6 x 10 – 5. e) 6, 0 x 10 – 5. Ka = ? m = 0, 10 mol/L α = 0, 006% = 0, 00006 = 6. 10 – 5 Ki = m α 2 Ki = 1, 0 x 10 – 1 ( 6 x 10 – 5)2 Ki = 1 x 10 – 1 x 36 x 10 – 10 Ki = 36 x 10 – 11 Ki = 3, 6 x 10 – 10 PROF. AGAMENON ROBERTO

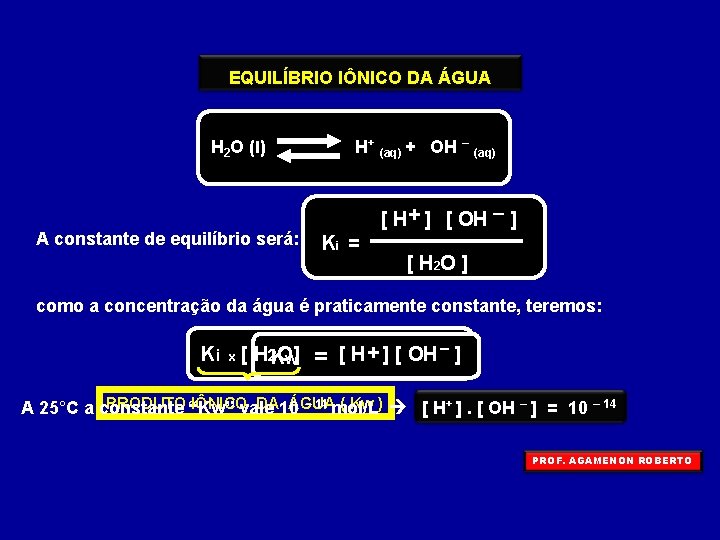
EQUILÍBRIO IÔNICO DA ÁGUA H 2 O (l) A constante de equilíbrio será: H+ (aq) + OH – (aq) [ H + ] [ OH – ] Ki = [ H 2 O ] como a concentração da água é praticamente constante, teremos: Ki x [ H 2 KO] w = [ H + ] [ OH – ] – 14 mol/L PRODUTO “Kw” IÔNICO DA 10 ÁGUA ( Kw ) [ H+ ]. [ OH – ] = 10 – 14 A 25°C a constante vale PROF. AGAMENON ROBERTO

1) Um alvejante de roupas, do tipo “ água de lavadeira “, apresenta [OH – ] aproximadamente igual a 1, 0. 10 – 4 mol/L. Nessas condições, a concentração de H+ será da ordem de: a) 10 – 2 [ OH – ] = 10 – 4 M b) 10 – 3 [H+ ] = ? c) 10 – 10 d) 10 – 14 e) zero. Kw = 10 – 14 M [H+]. [OH – ] = 10 – 14 [H+]. 10 – 4 = 10 – 14 [H + ] = [H+ ] 10 10 = 10 – 14 – 10 mol/L PROF. AGAMENON ROBERTO

02) Qual das expressões abaixo é conhecida como “produto iônico da água, KW”? a) Kw = [H 2][O 2]. b) Kw = [H+] / [OH – ]. c) Kw = [H+][OH – ]. d) Kw = [H 2 O]. e) Kw = [2 H][O 2]. PROF. AGAMENON ROBERTO
![Em água pura a concentração hidrogeniônica [H + ] é igual à concentração hidroxiliônica Em água pura a concentração hidrogeniônica [H + ] é igual à concentração hidroxiliônica](http://slidetodoc.com/presentation_image/04c120a76f848fc9fbc8e0eacc6c8f99/image-42.jpg)
Em água pura a concentração hidrogeniônica [H + ] é igual à concentração hidroxiliônica [OH – ], isto é, a 25°C, observa-se que: – [H + ] = [OH ] = 10 – 7 Nestas condições dizemos que a solução é “ NEUTRA “ PROF. AGAMENON ROBERTO
![As soluções em que [H+ ] > [OH – ] terão características ÁCIDAS nestas As soluções em que [H+ ] > [OH – ] terão características ÁCIDAS nestas](http://slidetodoc.com/presentation_image/04c120a76f848fc9fbc8e0eacc6c8f99/image-43.jpg)
As soluções em que [H+ ] > [OH – ] terão características ÁCIDAS nestas soluções teremos [ H+] > 10 – 7 mol/L [OH – ] < 10 – 7 mol/L PROF. AGAMENON ROBERTO
![As soluções em que [H+ ] < [OH – ] terão características BÁSICAS nestas As soluções em que [H+ ] < [OH – ] terão características BÁSICAS nestas](http://slidetodoc.com/presentation_image/04c120a76f848fc9fbc8e0eacc6c8f99/image-44.jpg)
As soluções em que [H+ ] < [OH – ] terão características BÁSICAS nestas soluções teremos [ H+] < 10 – 7 mol/L [OH – ] > 10 – 7 mol/L PROF. AGAMENON ROBERTO
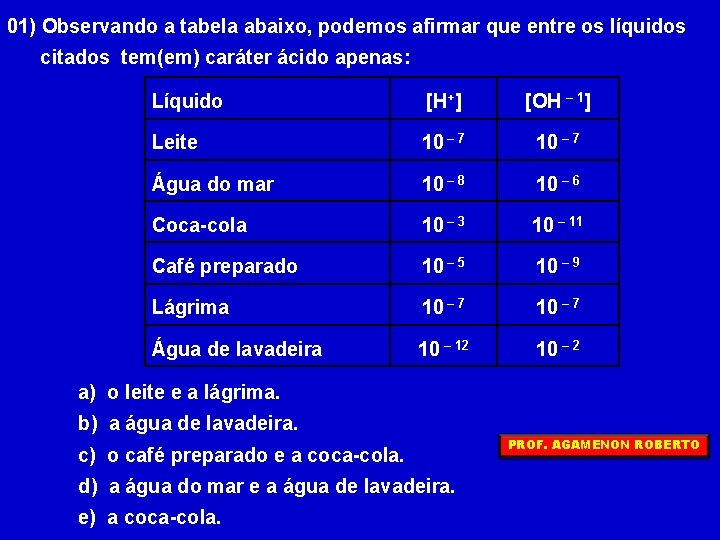
01) Observando a tabela abaixo, podemos afirmar que entre os líquidos citados tem(em) caráter ácido apenas: Líquido [H+] [OH – 1] Leite 10 – 7 Água do mar 10 – 8 10 – 6 Coca-cola 10 – 3 10 – 11 Café preparado 10 – 5 10 – 9 Lágrima 10 – 7 Água de lavadeira 10 – 12 10 – 2 a) o leite e a lágrima. b) a água de lavadeira. c) o café preparado e a coca-cola. d) a água do mar e a água de lavadeira. e) a coca-cola. PROF. AGAMENON ROBERTO

02) (Covest-90) O leite azeda pela transformação da lactose em ácido lático, por ação bacteriana. Conseqüentemente apresenta. . . I) aumento da concentração dos íons hidrogênio. II) aumento da concentração dos íons oxidrilas. III) diminuição da concentração dos íons hidrogênios. IV) diminuição da concentração dos íons oxidrilas. Assinale o item a seguir que melhor representa o processo. a) I e III. b) II e IV. c) I e II. d) II. e) I e IV. PROF. AGAMENON ROBERTO
![03) Misturando-se 100 m. L de suco de laranja, cuja [H +] = 0, 03) Misturando-se 100 m. L de suco de laranja, cuja [H +] = 0,](http://slidetodoc.com/presentation_image/04c120a76f848fc9fbc8e0eacc6c8f99/image-47.jpg)
03) Misturando-se 100 m. L de suco de laranja, cuja [H +] = 0, 6 mol/L, com 200 m. L de suco de laranja, cuja [H +] = 0, 3 mol/L, não se obtém: Vf a) uma solução onde [H +] = 0, 4 mol/L. b) uma solução completamente neutra. c) uma solução de acidez intermediária. d) uma solução menos ácida do que a de [H +] = 0, 6 mol/L. e) uma solução mais ácida do que a de [H +] = 0, 3 mol/L. V 1 = 100 m. L V 2 = 200 m. L Vf = 300 m. L [H+ ]1 = 0, 6 mol/L [H + ]2 = 0, 3 mol/L [H + ]f = ? mol/L x [H + ]f = V 1 x [H + ]1 + V 2 x [H + ]2 300 x [H + ]f = 100 x 0, 6 + 200 x 0, 3 PROF. AGAMENON ROBERTO 300 x [H + ]f = 60 + 60 [H + ]f = 120 : 300 [H + ]f = 0, 4 mol/L

04) Observando a tabela abaixo, podemos afirmar que entre os líquidos citados tem(êm) caráter ácido apenas: Líquido [ H+ ] [ OH – ] Leite 10 – 7 Água do mar 10 – 8 10 – 6 Coca-cola 10 – 3 10 – 11 Café preparado 10 – 5 10 Lágrima 10 – 7 Água de lavadeira 10 – 12 10 – 2 a) b) c) d) e) O leite e a lágrima. A água de lavadeira. O café preparado e a coca-cola. A água do mar e a água de lavadeira. A coca-cola. – 9 PROF. AGAMENON ROBERTO

Como os valores das concentrações hidrogeniônica e oxidriliônica são pequenos, é comum representá-las na forma de logaritmos e, surgiram os conceitos de p. H e p. OH + p. H = – log [ H ] p. OH = – log [ OH – ] PROF. AGAMENON ROBERTO

Na temperatura de 25°C PROF. AGAMENON ROBERTO Em soluções neutras p. H = p. OH = 7 Em soluções ácidas p. H < 7 e p. OH > 7 Em soluções básicas p. H > 7 e p. OH < 7

Podemos demonstrar que, a 25°C, e em uma mesma solução p. H + p. OH = 14 PROF. AGAMENON ROBERTO

01) A concentração dos íons H+ de uma solução é igual a 0, 0001. O p. H desta solução é: a) 1. [ H + ] = 0, 0001 mol/L = 10 – 4 mol/L b) 2. p. H = – log [H+] c) 4. p. H = – log 10 – 4 d) 10. p. H = – (– 4). log 10 e) 14. p. H = 4 PROF. AGAMENON ROBERTO

02) A concentração hidrogeniônica de uma solução é de 3, 45 x 10 – 11 íons – g/L. O p. H desta solução vale: Dado: log 3, 45 = 0, 54 a) 11. [ H + ] = 3, 45 x 10 – 11 íons – g/L b) 3. p. H = – log [H+] c) 3, 54. d) 5, 4. e) 10, 46. p. H = – log ( 3, 45 x 10 – 11 ) p. H = – [ log 3, 45 + log 10 ] p. H = – [ 0, 54 – 11 ] p. H = 11 – 0, 54 p. H = 10, 46 PROF. AGAMENON ROBERTO

03) Considere os sistemas numerados (25°C) 1 Vinagre p. H = 3, 0 2 Leite p. H = 6, 8 3 Clara de ovos p. H = 8, 0 4 Sal de frutas p. H = 8, 5 5 Saliva p. H = 6, 0 PROF. AGAMENON ROBERTO A respeito desses sistemas, NÃO podemos afirmar: a) São de caráter básico os sistemas 3 e 4. b) O de maior acidez é o número 1. c) O de número 5 é mais ácido que o de número 2. d) O de número 1 é duas vezes mais ácido que o de número 5. e) O de menor acidez é o sal de frutas. “ 1 “ tem p. H = 3 [ H+] = 10 – 3 “ 5 “ tem p. H = 6 [ H+] = 10 – 6 = 10 3 o 1 é 1000 vezes mais ácido do que 5, então é FALSO
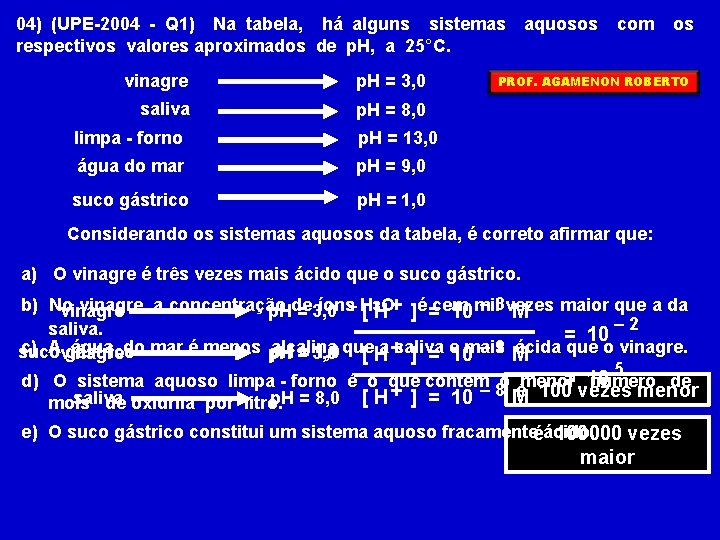
04) (UPE-2004 - Q 1) Na tabela, há alguns sistemas respectivos valores aproximados de p. H, a 25°C. vinagre p. H = 3, 0 saliva p. H = 8, 0 limpa - forno p. H = 13, 0 água do mar p. H = 9, 0 suco gástrico p. H = 1, 0 aquosos com os PROF. AGAMENON ROBERTO Considerando os sistemas aquosos da tabela, é correto afirmar que: a) O vinagre é três vezes mais ácido que o suco gástrico. – 3 vezes b) No vinagre, a concentração íons+ H maior que a da vinagre p. Hde = 3, 0 [ 3 HO+ ]é =cem 10 mil M – 2 saliva. = 10 c) Avinagre água do mar é menos p. H alcalina ácida que o vinagre. 1 M – 3 suco gástrico p. H 1, 0 que == 3, 0 [ Ha +saliva ] = e 10 mais 5 = 10 d) O sistema aquoso limpa - forno é o que contém– 8 o émenor número de saliva p. H = 8, 0 [ H + ] = 10 M 100 vezes menor mols de oxidrila por litro. e) O suco gástrico constitui um sistema aquoso fracamenteéácido. 100000 vezes maior

05) (Covest-2003) As características ácidas e básicas de soluções aquosas são importantes para outras áreas além da “Química”, como, por exemplo, a Saúde Pública, a Biologia, a Ecologia, e Materiais. Estas características das soluções aquosas são quantificadas pelo p. H, cuja escala é definida em termos da constante de ionização da água (K w) a uma dada temperatura. Por exemplo, a 25 C a constante de ionização da água é 10– 14 e a 63 C é 10– 13. Sobre o p. H de soluções aquosas a 63 C julgue os itens abaixo: PROF. AGAMENON ROBERTO 0 0 p. H + p. OH = 13. 1 1 Água pura (neutra) apresenta p. H igual a 6, 5. 2 2 Água pura (neutra) apresenta p. H igual a 7, 0. 3 3 Uma solução com p. H igual a 6, 7 é ácida. 4 4 A concentração de íons hidroxila na água pura (neutra) é igual 10– 7 mol/L. 0 63ºC Kw = 10 – 13 ácida 6, 5 neutra básica 13

06)(Covest – 2004) Sabendo-se que, a 25°C, o cafezinho tem p. H = 5, 0, o suco de tomate apresenta p. H = 4, 2, a água sanitária p. H = 11, 5 e o leite, p. H = 6, 4, pode-se afirmar que, nesta temperatura: a) o cafezinho e a água sanitária apresentam propriedades básicas. b) o cafezinho e o leite apresentam propriedades básicas. c) a água sanitária apresenta propriedades básicas. d) o suco de tomate e a água sanitária apresentam propriedades PROF. AGAMENON ROBERTO ácidas. e) apenas o suco de tomate apresenta propriedades ácidas. 0 25ºC Kw = 10 – 14 ácida 7, 0 básica 14 neutra Cafezinho: p. H = 5, 0 Propriedades ácidas Suco de tomate: p. H = 4, 2 Propriedades ácidas Água sanitária: p. H = 11, 5 Propriedades básicas Leite: p. H = 6, 4 Propriedades ácidas

07)(Covest – 2007) O p. H de fluidos em partes distintas do corpo humano tem valores diferentes, apropriados para cada tipo de função que o fluido exerce no organismo. O p. H da saliva é de 6, 5; o do sangue é 7, 5 e, no estômago, o p. H está na faixa de 1, 6 a 1, 8. O esmalte dos dentes é formado, principalmente por um mineral de composição Ca 10(PO 4)6(OH)2. Após as refeições, ocorre diminuição do p. H bucal. O p. H do sangue é mantido aproximadamente constante pelo seguinte equilíbrio químico, envolvendo o íon bicarbonato: PROF. AGAMENON ROBERTO Com base nestas informações avalie as seguintes proposições: 0 0 A concentração de íons H+ é maior na saliva que no sangue. 1 1 A concentração de H+ no estômago é maior que 10 – 2 mol/L. 2 2 3 3 Um aumento na acidez da saliva pode resultar em ataque ao esmalte dos dentes. O bicarbonato pode ser usado para elevar o p. H do estômago. 4 4 A adição de uma base em um meio contendo acido carbônico, íons Hidrogênio e bicarbonato causará deslocamento do equilíbrio mostrado no enunciado da questão no sentido da formação dos reagentes.

08) (Fuvest – SP) À temperatura ambiente, o p. H de um certo refrigerante, saturado com gás carbônico, quando em garrafa fechada, vale 4. Ao abrir-se a garrafa, ocorre escape de gás carbônico. Qual deve ser o valor do p. H do refrigerante depois de a garrafa ser aberta? a) p. H = 4. b) 0 < p. H < 4. c) 4 < p. H < 7. d) p. H = 7. e) 7 < p. H < 14. PROF. AGAMENON ROBERTO

HIDRÓLISE SALINA É o processo em que a água reage com o cátion ou o ânion de um sal Este processo é reversível, devendo ser analisado seguindo os princípios do equilíbrio químico PROF. AGAMENON ROBERTO

Os casos fundamentais são: Hidrólise de um sal de ácido forte e base fraca. Hidrólise de um sal de ácido fraco e base forte. Hidrólise de um sal de ácido e base ambos fracos. Hidrólise de um sal de ácido e base ambos fortes. PROF. AGAMENON ROBERTO
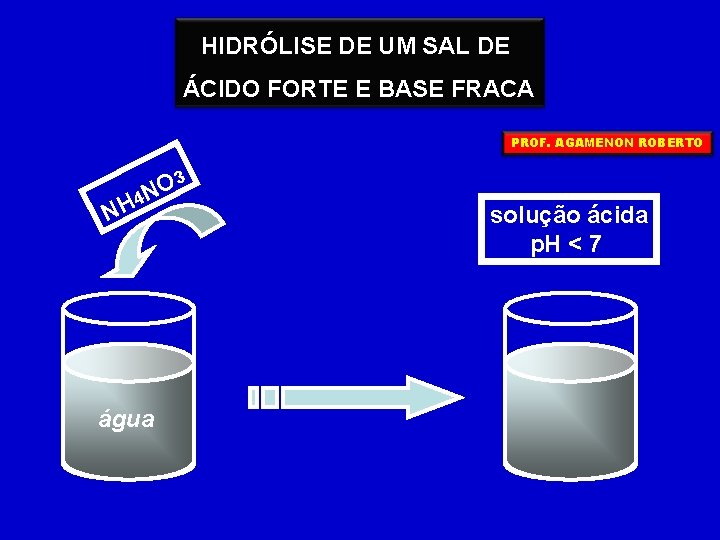
HIDRÓLISE DE UM SAL DE ÁCIDO FORTE E BASE FRACA PROF. AGAMENON ROBERTO 4 H N 3 O N água solução ácida p. H < 7
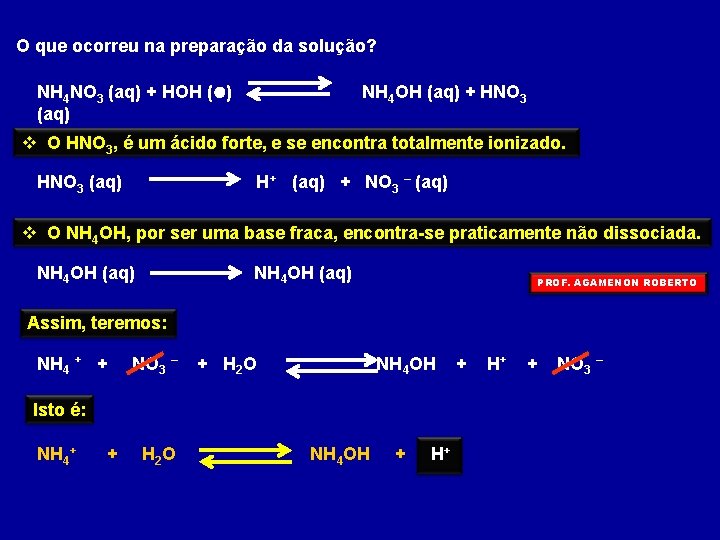
O que ocorreu na preparação da solução? NH 4 NO 3 (aq) + HOH (l) (aq) NH 4 OH (aq) + HNO 3 O HNO 3, é um ácido forte, e se encontra totalmente ionizado. HNO 3 (aq) H+ (aq) + NO 3 – (aq) O NH 4 OH, por ser uma base fraca, encontra-se praticamente não dissociada. NH 4 OH (aq) PROF. AGAMENON ROBERTO Assim, teremos: NH 4 + + NO 3 – + H 2 O NH 4 OH Isto é: NH 4+ + H 2 O NH 4 OH + H+ + NO 3 –
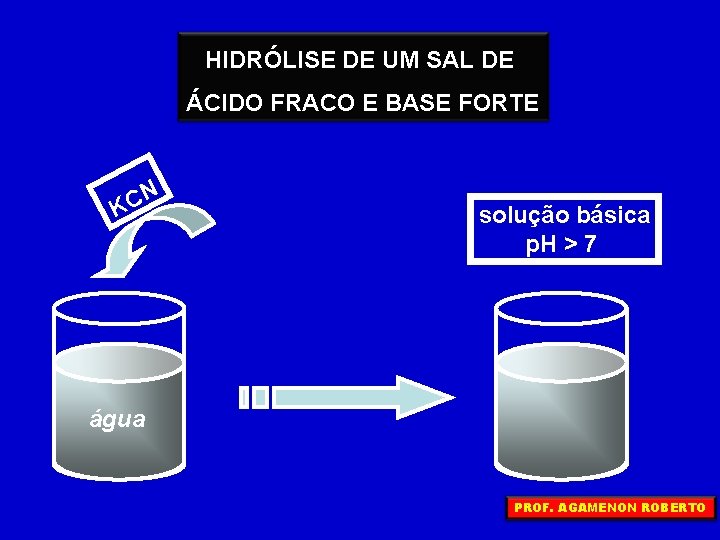
HIDRÓLISE DE UM SAL DE ÁCIDO FRACO E BASE FORTE N C K solução básica p. H > 7 água PROF. AGAMENON ROBERTO
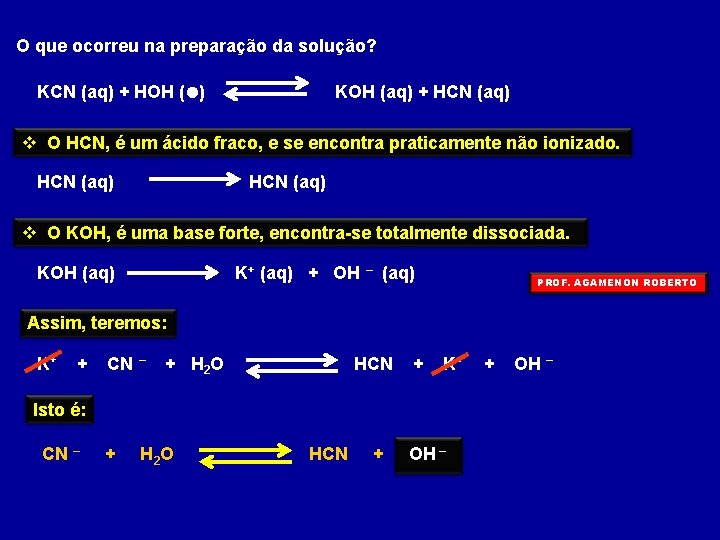
O que ocorreu na preparação da solução? KCN (aq) + HOH (l) KOH (aq) + HCN (aq) O HCN, é um ácido fraco, e se encontra praticamente não ionizado. HCN (aq) O KOH, é uma base forte, encontra-se totalmente dissociada. KOH (aq) K+ (aq) + OH – (aq) PROF. AGAMENON ROBERTO Assim, teremos: K+ + CN – + H 2 O HCN + K+ Isto é: CN – + H 2 O HCN + OH –
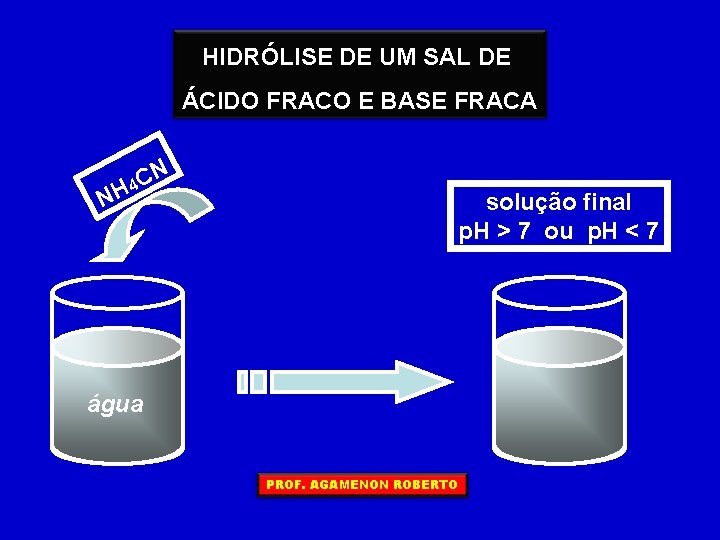
HIDRÓLISE DE UM SAL DE ÁCIDO FRACO E BASE FRACA NH N 4 C solução final p. H > 7 ou p. H < 7 água PROF. AGAMENON ROBERTO

O que ocorreu na preparação da solução? NH 4 CN (aq) + HOH (l) NH 4 OH (aq) + HCN (aq) O HCN, é um ácido fraco, e se encontra praticamente não ionizado. HCN (aq) O NH 4 OH, por ser uma base fraca, encontra-se praticamente não dissociada. NH 4 OH (aq) PROF. AGAMENON ROBERTO A solução final pode ser ligeiramente ácida ou ligeiramente básica; isto depende da constante (Ka e Kb) de ambos Neste caso: Ka = 4, 9 x 10 – 10 e Kb = 1, 8 x 10 – 5, isto é, Kb é maior que Ka; então a solução será ligeiramente básica
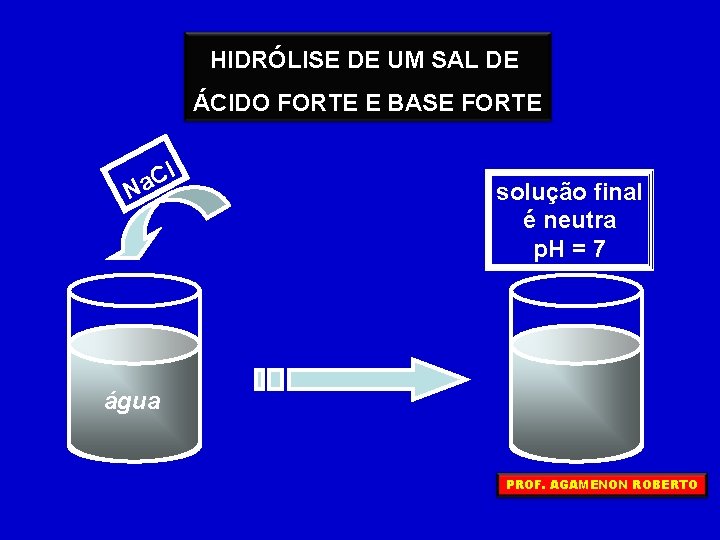
HIDRÓLISE DE UM SAL DE ÁCIDO FORTE E BASE FORTE l C a N solução final é neutra p. H = 7 água PROF. AGAMENON ROBERTO
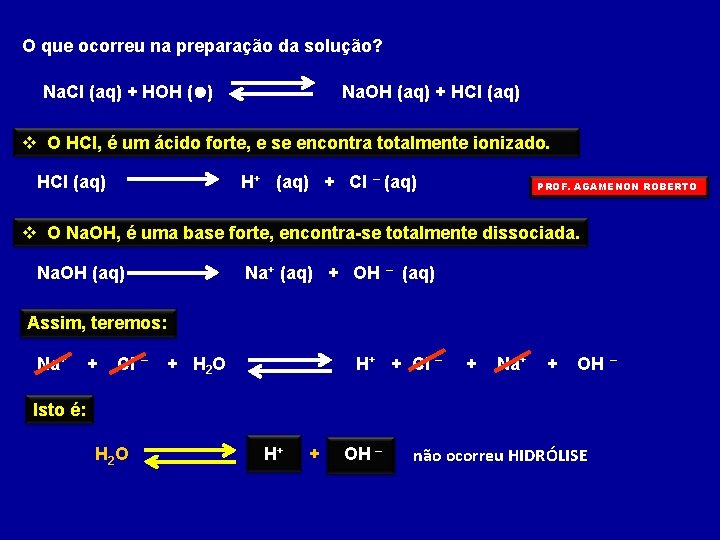
O que ocorreu na preparação da solução? Na. Cl (aq) + HOH (l) Na. OH (aq) + HCl (aq) O HCl, é um ácido forte, e se encontra totalmente ionizado. HCl (aq) H+ (aq) + Cl – (aq) PROF. AGAMENON ROBERTO O Na. OH, é uma base forte, encontra-se totalmente dissociada. Na. OH (aq) Na+ (aq) + OH – (aq) Assim, teremos: Na+ + Cl – + H 2 O H+ + Cl – + Na+ + OH – Isto é: H 2 O H+ + OH – não ocorreu HIDRÓLISE

01) Solução aquosa ácida é obtida quando se dissolve em água o sal: PROF. AGAMENON ROBERTO a) Na. HCO 3. b) K 2 SO 4. c) KCN. d) KF. e) NH 4 Cl p. Hmetro

02) O p. H resultante da solução do nitrato de potássio (KNO 3) em água será: a) igual a 3, 0. b) igual a 12, 0. c) maior que 7, 0. d) igual ao p. H da água. e) menor que 7, 0. p. Hmetro PROF. AGAMENON ROBERTO

03) (UFPE) O azul de bromotimol é um indicador ácido – base, com faixa de viragem [6, 0 – 7, 6], que apresenta cor amarela em meio ácido e cor azul em meio básico. Considere os seguintes sistemas: I. Água pura. II. CH 3 COOH 1, 0 mol/L. III. NH 4 Cl 1, 0 mol/L. PROF. AGAMENON ROBERTO Indique, na tabela que segue, a coluna contendo as cores desses sistemas depois da adição de azul de bromotimol, respectivamente: a) verde, amarela, azul. b) verde, azul, verde. c) verde, amarelo, verde. d) verde, amarela, amarelo. e) azul, amarelo, azul. p. Hmetro

04) Um sal formado por base forte e ácido fraco hidrolisa ao se dissolver em água, produzindo uma solução básica. Esta é uma característica do: a) Na 2 S. b) Na. Cl. c) (NH 4)2 SO 4. d) KNO 3. e) NH 4 Br. PROF. AGAMENON ROBERTO

É a expressão que exprime o equilíbrio das reações de hidrólise. Para a reação NH 4 + + H 2 O NH 4 OH + H+ A expressão da constante de hidrólise é: Kh = [ NH 4 OH ] [H +] [ NH 4 + ] PROF. AGAMENON ROBERTO

Podemos relacionar a constante de hidrólise (Kh), com a constante de ionização da água e as constantes de ionização e dissociação dos ácidos e das bases pelas expressões: Para a hidrólise do cátion, isto é, para sais formados por ácido forte e base fraca, usamos a relação: PROF. AGAMENON ROBERTO Para a hidrólise do ânion, isto é, para sais formados por ácido fraco e base forte, usamos a relação Ocorrendo a hidrólise do cátion e do ânion, para sais formados por ácido fraco e base fraca, a relação será:

01) (UFPI) Uma solução aquosa de cloreto de amônio 0, 2 mol/L apresenta um grau de hidrólise igual a 0, 5%. Determine o [H +], [OH –], p. H, p. OH e Kh para essa solução e o Kb para o NH 4 OH. PROF. AGAMENON ROBERTO Dado: Kw = 10 – 14, a 25°C. O NH 4 Cl é proveniente do HCl (ácido forte) e do NH 4 OH (base fraca), então ocorre a hidrólise do cátion NH 4+, então: NH 4 início + 0, 2 reage e produz equilíbrio + H 2 O constante 10 – 3 0, 2 mol/L constante [H +] = 10 – 3 mol/L [OH –] = 10 – – 113 mol/L Reage e produz: 0, 2 x 0, 005 = 0, 001 = 10 p. H = - log 10 – 3 p. H = 3 e p. OH = 11 Kh = [NH [H –+3] – 3 X 10 10 4 OH] [NH 4 +–] 1 2 x 10 NH 4 OH + H+ 0, 0 10 – 3 – h 6 == 5 x 10 K Kw– 14 10 Kb Kb = 2 x 10 – 9 = 5 x 10 – 6
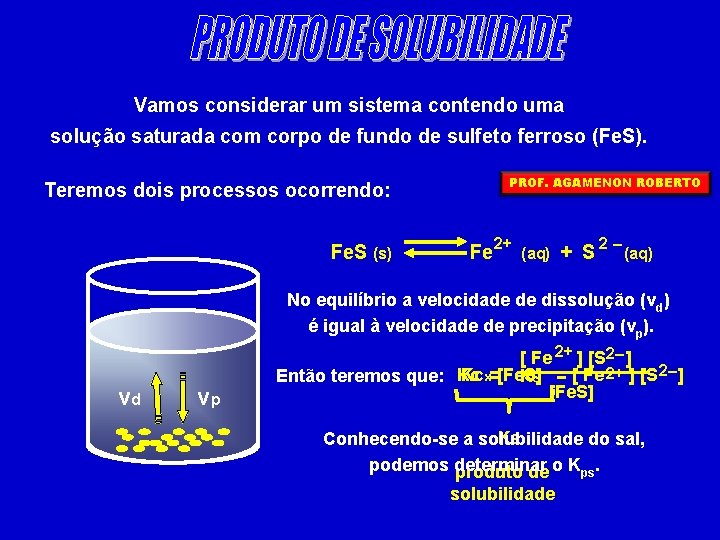
Vamos considerar um sistema contendo uma solução saturada com corpo de fundo de sulfeto ferroso (Fe. S). Teremos dois processos ocorrendo: Fe. S (s) PROF. AGAMENON ROBERTO Fe 2+ (aq) + S 2 – (aq) No equilíbrio a velocidade de dissolução (vd) é igual à velocidade de precipitação (vp). vd vp [ Fe 2+ ] [S 2– ] Kc x=[Fe. S] Então teremos que: Kc KS = [ Fe 2+ ] [S 2– ] [Fe. S] KS Conhecendo-se a solubilidade do sal, podemos determinar produto de o Kps. solubilidade

01) (Fuvest – SP) Em determinada temperatura, a solubilidade do sulfato de prata (Ag 2 SO 4) em água é de 2, 0 x 10 – 2 mol/L. Qual o valor do produto de solubilidade (K ps ) desse sal, à mesma temperatura? Ag 2 SO 4 2 x 10 – 2 mol/L 2 Ag + + 4 x 10 – 2 mol/L SO 4– 2 2 x 10 – 2 mol/L KS = [ Ag+ ] 2 [SO 4 – 2 ] KS = (4 x 10 – 2 )2 x 10 – 2 KS = 16 x 10 – 4 x 2 x 10 – 2 KS = 32 x 10 – 6 KS = 3, 2 x 10 – 5 PROF. AGAMENON ROBERTO

02) A determinada temperatura, a solubilidade do composto XY em água é 2, 0 x 10 – 2 mol/L. O produto de solubilidade (Kps) desse sal à mesma temperatura é: a) 4, 0 x 10 – 4. b) 8, 0 x 10 – 4. c) 6, 4 x 10 – 5. XY X+ A 2, 0. 10 – 2 + Y –B 2, 0. 10 – 2 Kps = [ X+A ] [Y – B ] d) 3, 2 x 10 – 5. e) 8, 0 x 10 – 6. Kps = 2, 0. 10 – 2 Kps = 4, 0. 10 – 4 PROF. AGAMENON ROBERTO

03) (FESO-RJ) A solubilidade de um fosfato de metal alcalino terroso a 25°C é 10 – 4 mol/L. O produto de solubilidade deste sal a 25°C é, aproximadamente, igual a: a) 1, 08 x 10 – 8. Me 3(PO 4)2 b) 1, 08 x 10 – 12. 10 – 4 c) 1, 08 x 10 – 16. d) 1, 08 x 10 – 18. e) 1, 08 x 10 – 2. PROF. AGAMENON ROBERTO 3 Me+ 2 3 x + 2 PO 4– 3 10 – 4 2 x Kps = [ Me+ ] 3 x [ PO 4 – 3 ] 2 Kps = (3 x Kps = 27 10 – 4 )3 x x 10 – 12 Kps = 108 x 10 – 20 Kps = 1, 08 x 10 – 18 x (2 x 10 – 4 ) 2 4 x 10 – 8 10 – 4

04) O carbonato de bário, Ba. CO 3, tem Ks = 1, 6 x 10 – 9, sob 25°C. A solubilidade desse sal, em mol/L, será igual a: a) 4 x 10 – 5. b) 16 x 10 – 5. c) 8 x 10 – 10. d) 4 x 10 – 10. Ba. CO 3 Ba +2 S CO 3– 2 + S – 9 1, 6 x 10 Ks = [Ba S +2 ] S[CO 3 – 2 x e) 32 x 10 – 20. S 2 = 1, 6 x 10 – 9 PROF. AGAMENON ROBERTO S= S = 4 16 x 10 – 10 x 10 – 5 S ]

05) (PUC-SP) Uma solução saturada de base representada por X(OH)2, cuja reação de equilíbrio é PROF. AGAMENON ROBERTO tem p. H = 10 a 25°C. O produto de solubilidade (KPS) do X(OH)2 é: a) 5 x 10 – 13. b) 2 x 10 – 13. p. H = 10 p. OH = 4, então, [OH – ] = 10 – 4 mol/L X(OH)2 X +2 c) 6 x 10 – 1. d) 1 x 10 – 12. e) 3 x 10 – 10. 5 x + 10 – 5 Kps = [ X+2 ] x [ OH – ] 2 Kps = (5 x 10 – 5 ) x ( 10 – 4 ) 2 Kps = 5 x 10 – 5 Kps = 5 x 10 – 13 x 10 – 8 2 OH – 10 – 4
- Slides: 82