EQUILBRIO ENTRE FASES CONDENSADAS EQUILBRIO ENTRE FASES LQUIDAS

EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO ENTRE FASES LÍQUIDAS Uma mistura entre dois líquidos pode ser: - Totalmente miscível para qualquer composição; - Totalmente imiscível para qualquer composição; - Parcialmente miscível dependendo da composição (nosso caso de estudo); Para duas camadas líquidas distintas em equilíbrio: A= Ao A- Ao = 0 (1) Para uma solução ideal: A- Ao = RT lnx. A (2) Portanto a Equação (2) só será satisfeita quando x. A=1 (componente puro), logo uma mistura imiscível entre duas fases líquidas não será uma solução ideal. Logo substâncias que formam soluções ideais são completamente miscíveis entre si.
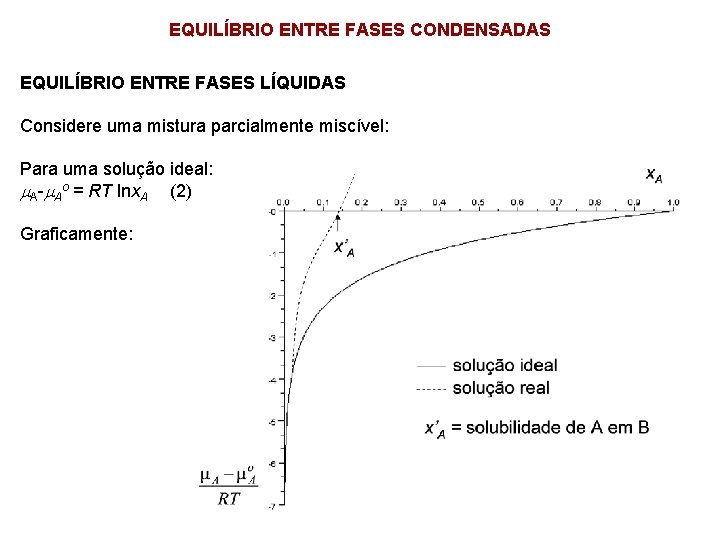
EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO ENTRE FASES LÍQUIDAS Considere uma mistura parcialmente miscível: Para uma solução ideal: A- Ao = RT lnx. A (2) Graficamente:
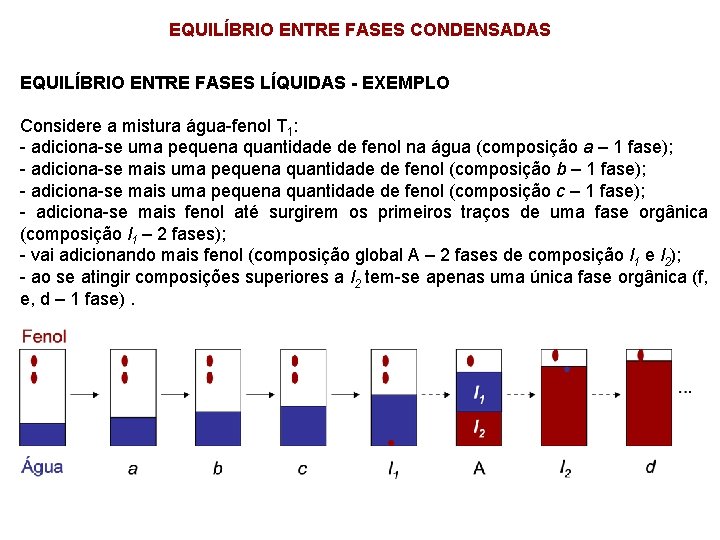
EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO ENTRE FASES LÍQUIDAS - EXEMPLO Considere a mistura água-fenol T 1: - adiciona-se uma pequena quantidade de fenol na água (composição a – 1 fase); - adiciona-se mais uma pequena quantidade de fenol (composição b – 1 fase); - adiciona-se mais uma pequena quantidade de fenol (composição c – 1 fase); - adiciona-se mais fenol até surgirem os primeiros traços de uma fase orgânica (composição l 1 – 2 fases); - vai adicionando mais fenol (composição global A – 2 fases de composição l 1 e l 2); - ao se atingir composições superiores a l 2 tem-se apenas uma única fase orgânica (f, e, d – 1 fase).
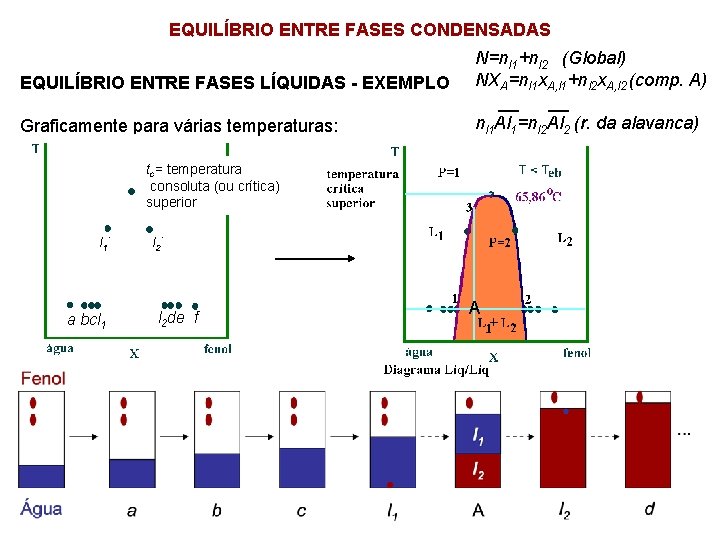
EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO ENTRE FASES LÍQUIDAS - EXEMPLO Graficamente para várias temperaturas: N=nl 1+nl 2 (Global) NXA=nl 1 x. A, l 1+nl 2 x. A, l 2 (comp. A) __ __ nl 1 Al 1=nl 2 Al 2 (r. da alavanca) tc= temperatura consoluta (ou crítica) superior l 1’ a bcl 1 l 2’ l 2 de f A
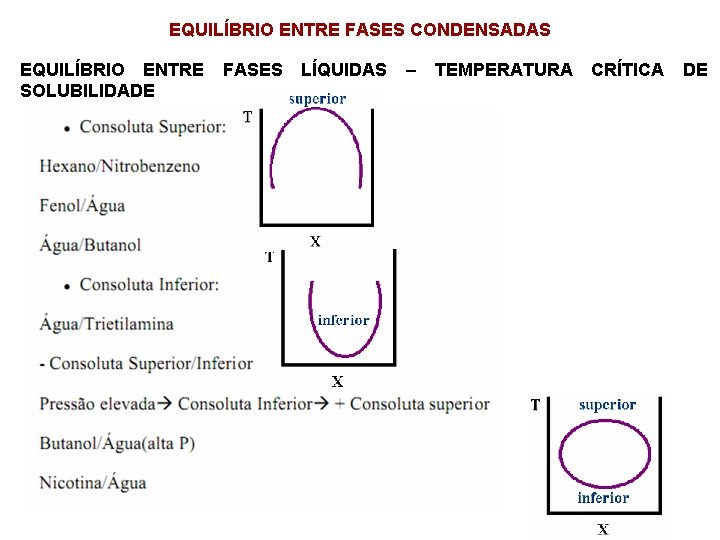
EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO ENTRE SOLUBILIDADE FASES LÍQUIDAS – TEMPERATURA CRÍTICA DE
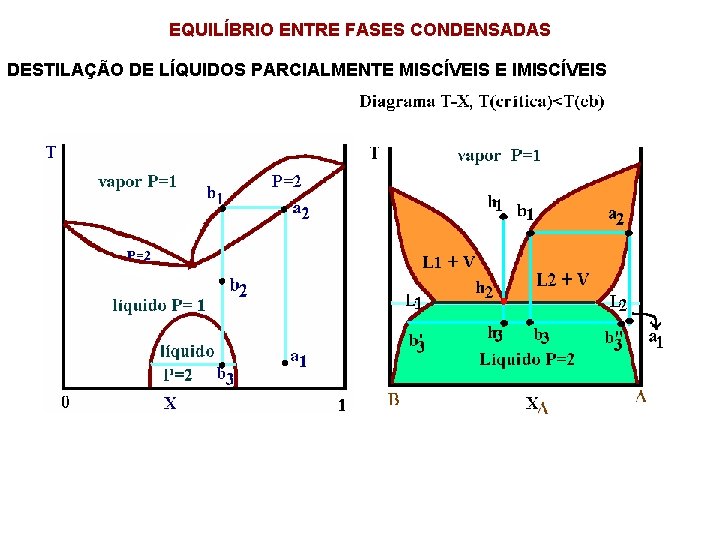
EQUILÍBRIO ENTRE FASES CONDENSADAS DESTILAÇÃO DE LÍQUIDOS PARCIALMENTE MISCÍVEIS E IMISCÍVEIS

EQUILÍBRIO ENTRE FASES CONDENSADAS DESTILAÇÃO DE LÍQUIDOS PARCIALMENTE MISCÍVEIS E IMISCÍVEIS y. A=p. Ao/p y. B=p. Bo/p p=p. Ao+p. Bo A n. A/n. B=y. A/y. B=p. Ao/pbo B m=n. M Equação da Destilação por arraste de vapor Exemplo: Suponha o sistema anilina (A) – água (B) a 98, 4 o. C. A pressão de vapor da anilina nesta temperatura é da ordem de 42 mm. Hg, enquanto que a da água é aproximadamente 718 mm. Hg. A pressão de vapor total é 718+42=760 mm. Hg, de modo que essa mistura ferve a 98, 4 o. C sob 1 atm de pressão. A massa de anilina que destila para cada 100 g de água evaporada é:

EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO SÓLIDO-LÍQUIDO – O DIAGRAMA EUTÉTICO SIMPLES No estudo das propriedades coligativas, obteve-se abaixameto do ponto de solidificação: a seguinte equação para o Curvas líquidus Sólido Eutético Componentes puros Eutético = de fácil fusão.
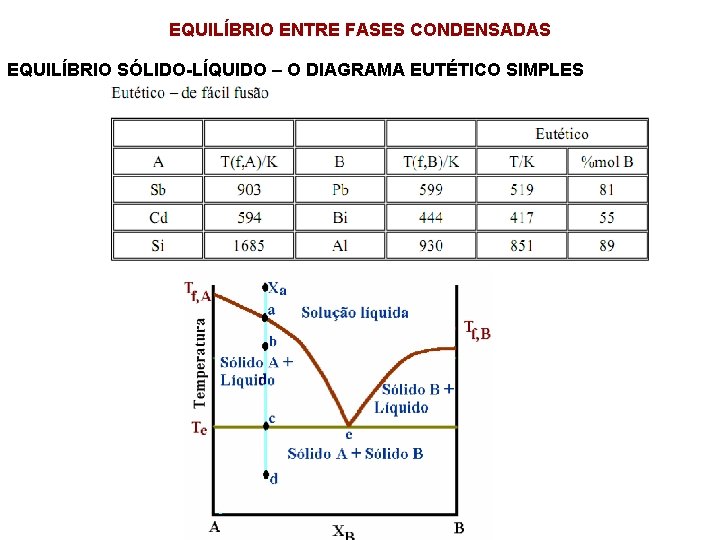
EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO SÓLIDO-LÍQUIDO – O DIAGRAMA EUTÉTICO SIMPLES
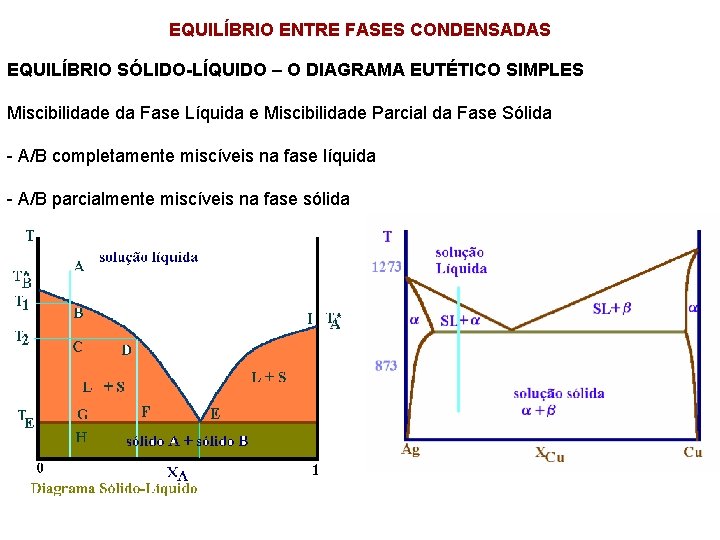
EQUILÍBRIO ENTRE FASES CONDENSADAS EQUILÍBRIO SÓLIDO-LÍQUIDO – O DIAGRAMA EUTÉTICO SIMPLES Miscibilidade da Fase Líquida e Miscibilidade Parcial da Fase Sólida - A/B completamente miscíveis na fase líquida - A/B parcialmente miscíveis na fase sólida
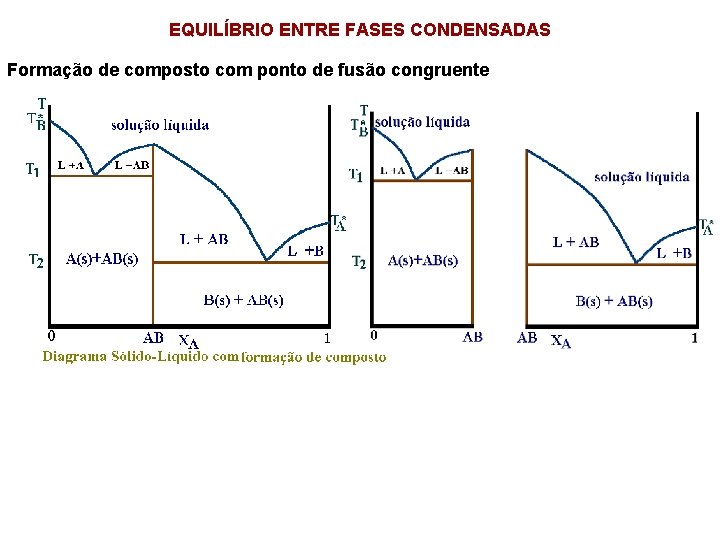
EQUILÍBRIO ENTRE FASES CONDENSADAS Formação de composto com ponto de fusão congruente
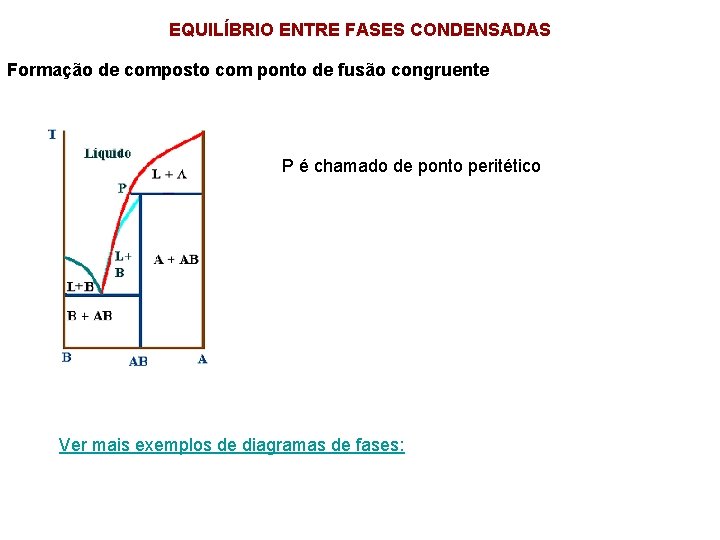
EQUILÍBRIO ENTRE FASES CONDENSADAS Formação de composto com ponto de fusão congruente P é chamado de ponto peritético Ver mais exemplos de diagramas de fases:
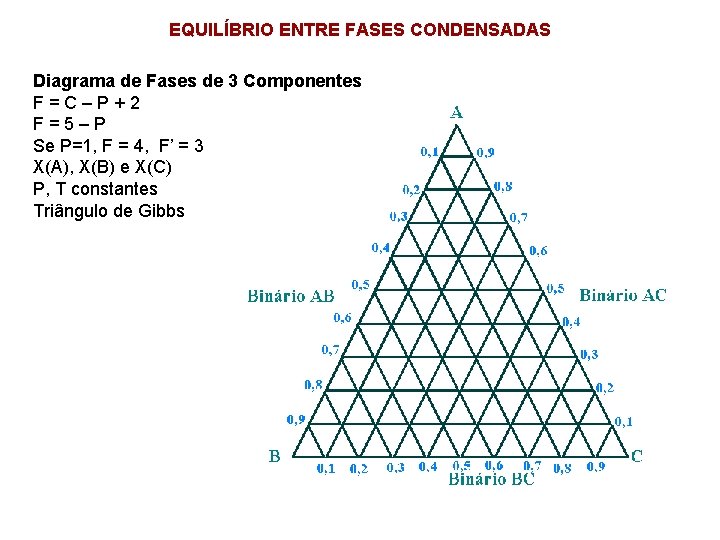
EQUILÍBRIO ENTRE FASES CONDENSADAS Diagrama de Fases de 3 Componentes F=C–P+2 F=5–P Se P=1, F = 4, F’ = 3 X(A), X(B) e X(C) P, T constantes Triângulo de Gibbs
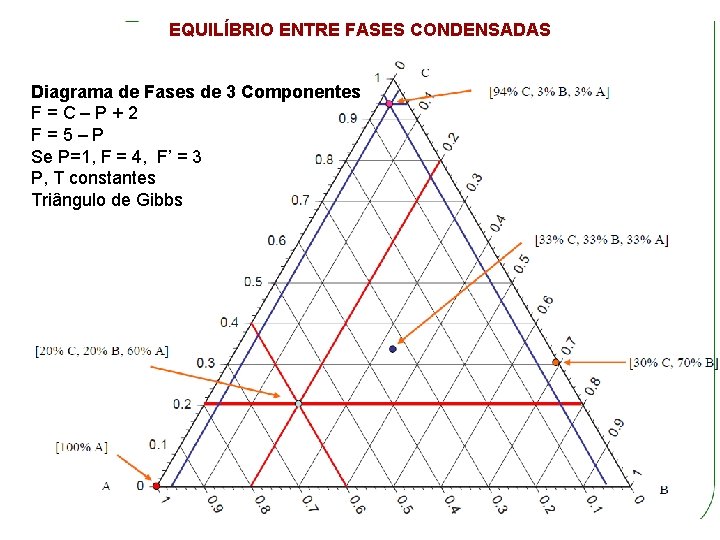
EQUILÍBRIO ENTRE FASES CONDENSADAS Diagrama de Fases de 3 Componentes F=C–P+2 F=5–P Se P=1, F = 4, F’ = 3 P, T constantes Triângulo de Gibbs
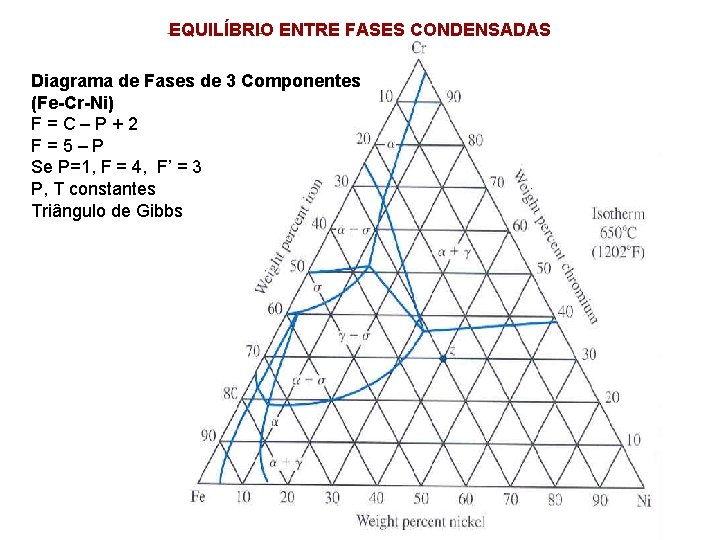
EQUILÍBRIO ENTRE FASES CONDENSADAS Diagrama de Fases de 3 Componentes (Fe-Cr-Ni) F=C–P+2 F=5–P Se P=1, F = 4, F’ = 3 P, T constantes Triângulo de Gibbs
- Slides: 15