EQUILBRIO CIDOBASE EQUILBRIO CIDOBASE Um pouco de histria

EQUILÍBRIO ÁCIDO-BASE

EQUILÍBRIO ÁCIDO-BASE Um pouco de história Na antiguidade, as propriedades organolépticas eram importantes na caracterização de substâncias A palavra ácido vem do latim “acere”, que significa azedo. Produtos que tinham esse sabor, como o vinagre, o leite coalhado e o suco de limão, eram considerados ácidos. O termo “álcalis”, por outro lado, é derivado do Árabe e foi inicialmente empregado para caracterizar substâncias capazes de neutralizar os ácidos. Ex: as cinzas obtidas pela queima de certas plantas (ricas em carbonato de potássio – K 2 CO 3). O termo “base” foi introduzido mais recentemente, no século XVIII, e praticamente substituiu a denominação “álcalis”.
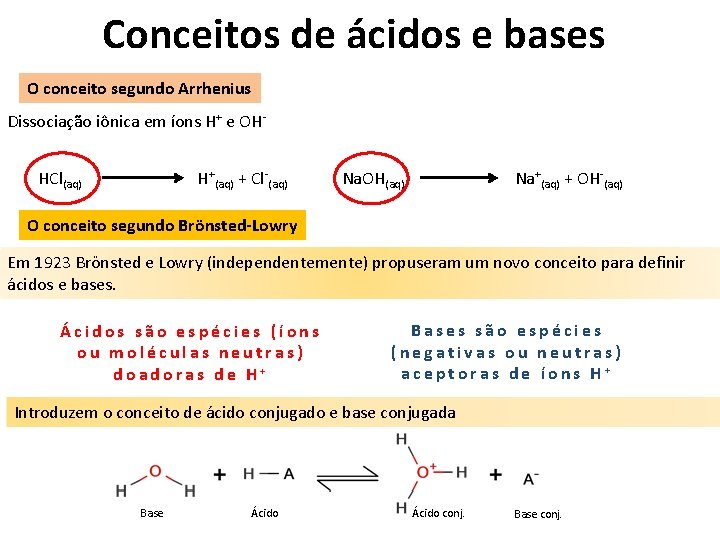
Conceitos de ácidos e bases O conceito segundo Arrhenius Dissociação iônica em íons H+ e OHHCl(aq) H+(aq) + Cl-(aq) Na. OH(aq) Na+(aq) + OH-(aq) O conceito segundo Brönsted-Lowry Em 1923 Brönsted e Lowry (independentemente) propuseram um novo conceito para definir ácidos e bases. Ácidos são espécies (íons ou moléculas neutras) doadoras de H+ Bases são espécies (negativas ou neutras) aceptoras de íons H+ Introduzem o conceito de ácido conjugado e base conjugada Base Ácido conj. Base conj.
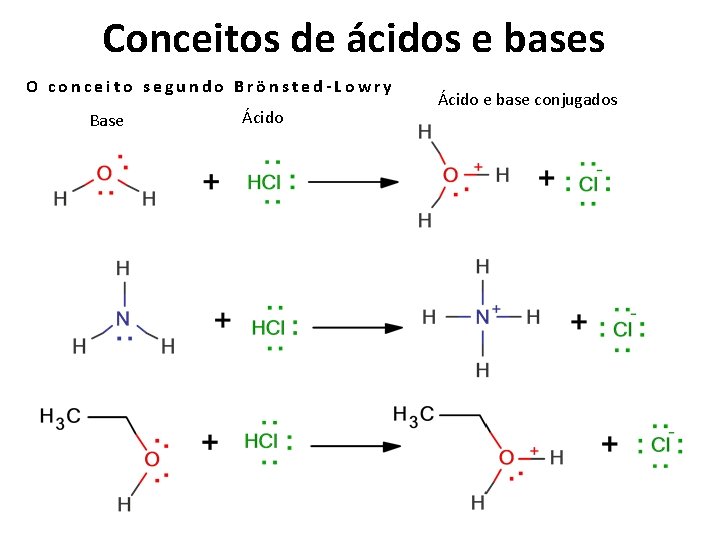
Conceitos de ácidos e bases O conceito segundo Brönsted-Lowry Base Ácido e base conjugados
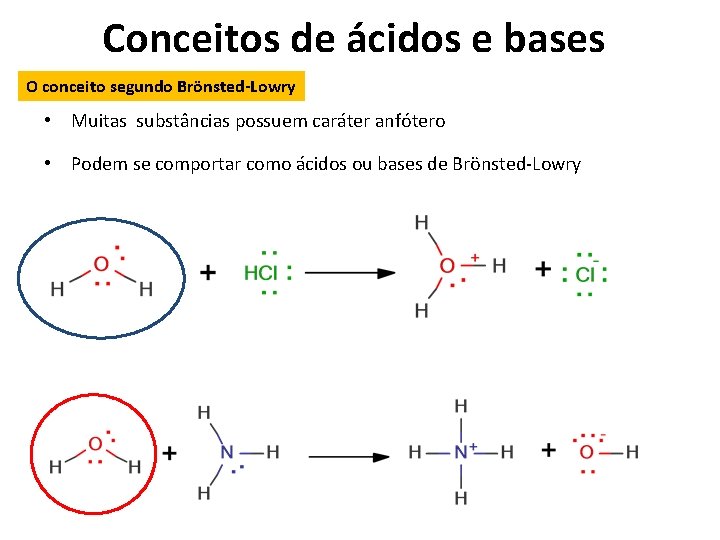
Conceitos de ácidos e bases O conceito segundo Brönsted-Lowry • Muitas substâncias possuem caráter anfótero • Podem se comportar como ácidos ou bases de Brönsted-Lowry
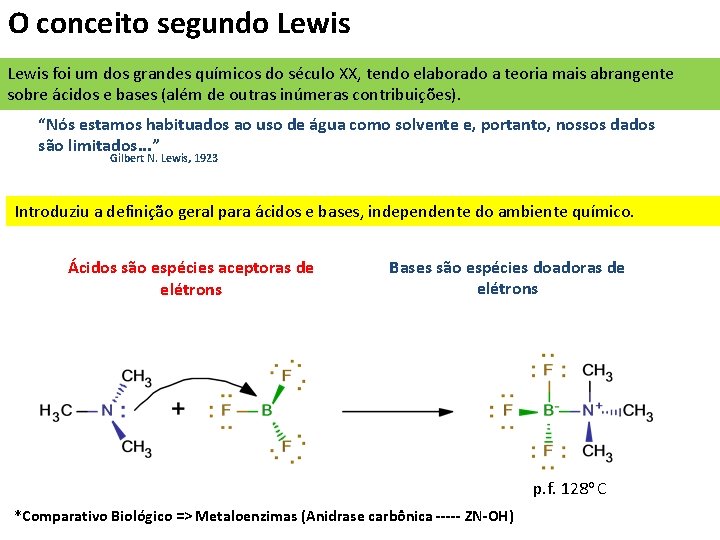
O conceito segundo Lewis foi um dos grandes químicos do século XX, tendo elaborado a teoria mais abrangente sobre ácidos e bases (além de outras inúmeras contribuições). “Nós estamos habituados ao uso de água como solvente e, portanto, nossos dados são limitados. . . ” Gilbert N. Lewis, 1923 Introduziu a definição geral para ácidos e bases, independente do ambiente químico. Ácidos são espécies aceptoras de elétrons Bases são espécies doadoras de elétrons p. f. 128 o C *Comparativo Biológico => Metaloenzimas (Anidrase carbônica ----- ZN-OH)
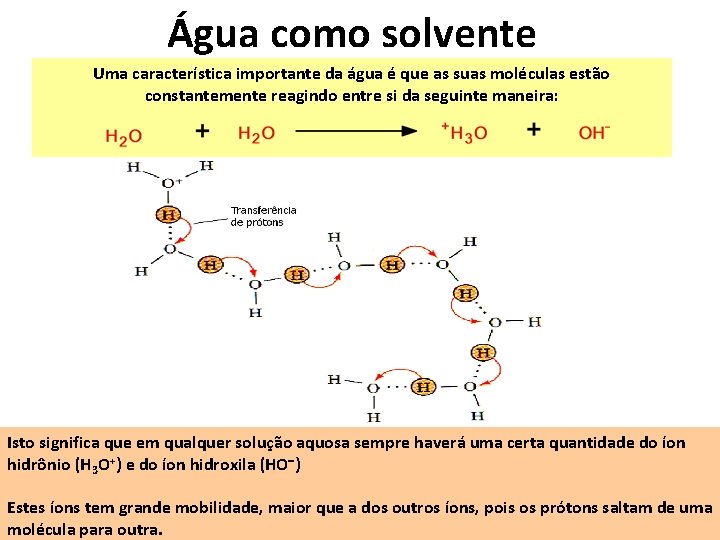
Água como solvente Uma característica importante da água é que as suas moléculas estão constantemente reagindo entre si da seguinte maneira: Isto significa que em qualquer solução aquosa sempre haverá uma certa quantidade do íon hidrônio (H 3 O+) e do íon hidroxila (HO ) Estes íons tem grande mobilidade, maior que a dos outros íons, pois os prótons saltam de uma molécula para outra.
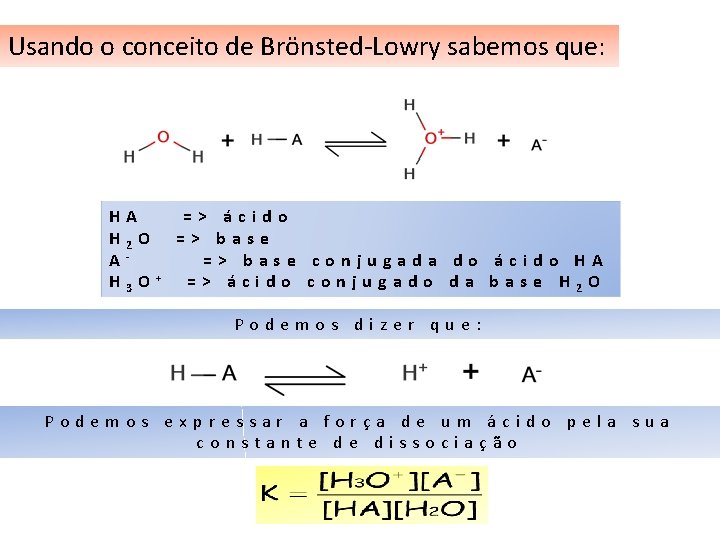
Usando o conceito de Brönsted-Lowry sabemos que: HA H 2 O AH 3 O + => ácido => base conjugada do ácido HA => ácido conjugado da base H 2 O Podemos dizer que: Podemos expressar a força de um ácido pela sua constante de dissociação
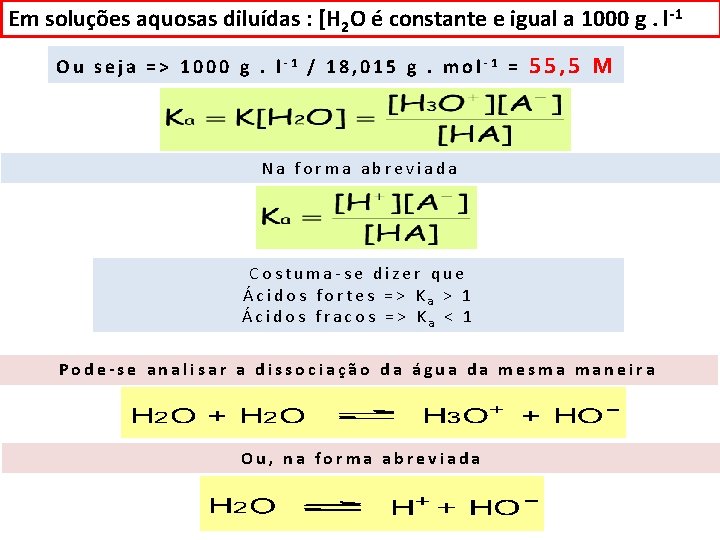
Em soluções aquosas diluídas : [H 2 O é constante e igual a 1000 g. l-1 Ou seja => 1000 g. l-1 / 18, 015 g. mol-1 = 55, 5 M Na forma abreviada Costuma-se dizer que Ácidos fortes => Ka > 1 Ácidos fracos => Ka < 1 Pode-se analisar a dissociação da água da mesma maneira Ou, na forma abreviada


A escala de p. H é prática e costuma ser usada entre 0 e 14 Na água pura p. H = log[H+] = log(10 7)= 7 Também na água pura: p. OH = 14 – p. H = 14 – 7 = 7
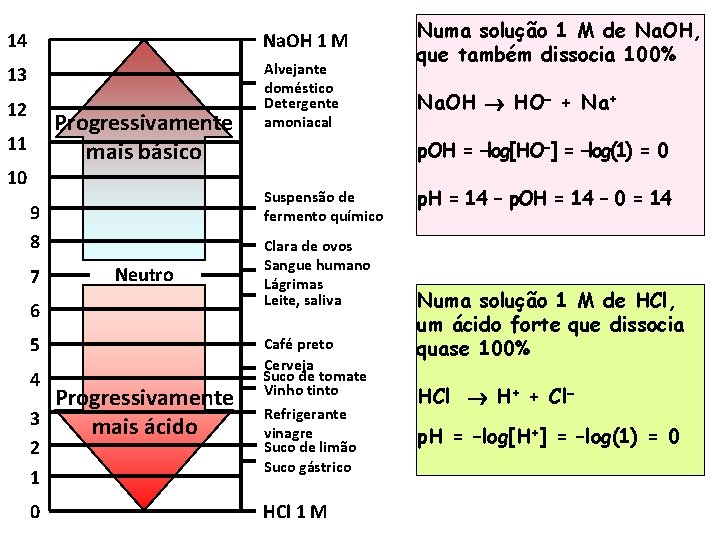
14 Na. OH 1 M 13 Alvejante doméstico Detergente amoniacal 12 Progressivamente mais básico 11 10 7 Neutro 6 5 Clara de ovos Sangue humano Lágrimas Leite, saliva Progressivamente 3 mais ácido Café preto Cerveja Suco de tomate Vinho tinto Refrigerante vinagre Suco de limão Suco gástrico 0 HCl 1 M 4 2 1 Na. OH HO + Na+ p. OH = –log[HO ] = –log(1) = 0 Suspensão de fermento químico 9 8 Numa solução 1 M de Na. OH, que também dissocia 100% p. H = 14 – p. OH = 14 – 0 = 14 Numa solução 1 M de HCl, um ácido forte que dissocia quase 100% HCl H+ + Cl p. H = –log[H+] = –log(1) = 0


Para ácidos e bases fracas ou, rearranjando


ou, rearranjando ou ou ainda
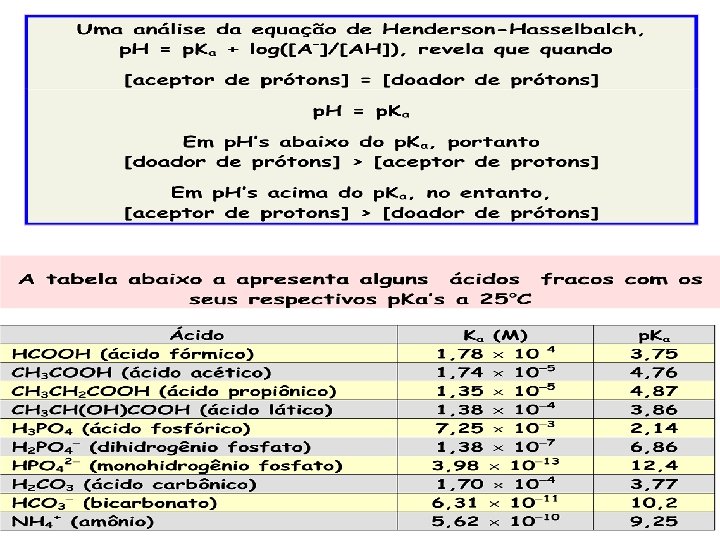

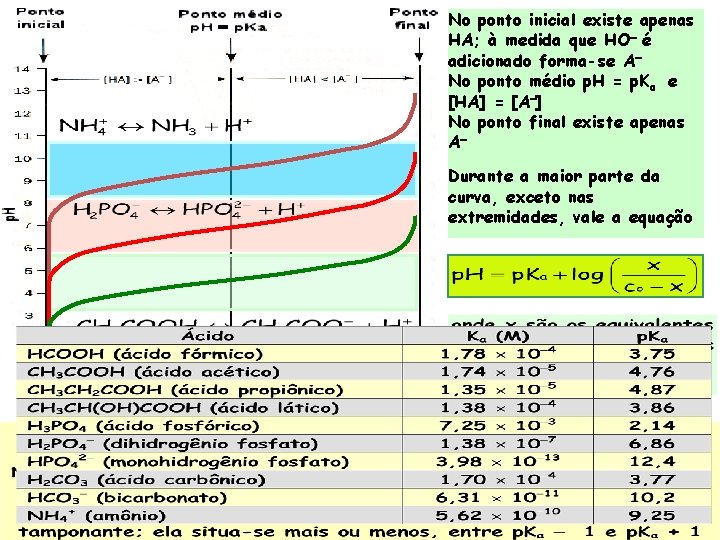
No ponto inicial existe apenas HA; à medida que HO é adicionado forma-se A No ponto médio p. H = p. Ka e [HA] = [A ] No ponto final existe apenas A Durante a maior parte da curva, exceto nas extremidades, vale a equação
- Slides: 21