EQUILBRIO QUMICO 1 2 EQUILBRIO QUMICO O que

EQUILÍBRIO QUÍMICO 1

2 EQUILÍBRIO QUÍMICO • O que é equilíbrio químico? • Quais são os aspectos qualitativos e quantitativos mais importantes?

Propriedades de Um Equilíbrio 3 Sistemas em equilíbrio são: • DIN MICOS (em movimento constante) • REVERSÍVEIS • Podem ser atingidos de qualquer direção Rosa para azul Co(H 2 O)6 Cl 2 Co(H 2 O)4 Cl 2 + 2 H 2 O Azul para rosa Co(H 2 O)4 Cl 2 + 2 H 2 O Co(H 2 O)6 Cl 2

Dinamismo do Equilíbrio 4 • Equilíbrio – dois processos opostos que ocorrem com velocidades iguais, em movimento constante Velocidade da reação direta = Velocidade da reação inversa A Velocidade de cada pessoa é igual à Velocidade da esteira, em sentido oposto Tanto a esteira quanto as pessoas continuam se movendo, mas macroscopicamente o sistema não se altera

Dinamismo do Equilíbrio Velocidade da reação direta = Velocidade da reação inversa i A d B H 2 O(s) H 2 O(l) H 2 O(g) I 2(H 2 O) I 2(CCl 4) Co(H 2 O)4 Cl 2 + 2 H 2 O Co(H 2 O)6 Cl 2 CO(g) + 2 H 2(g) CH 3 OH(g) 5
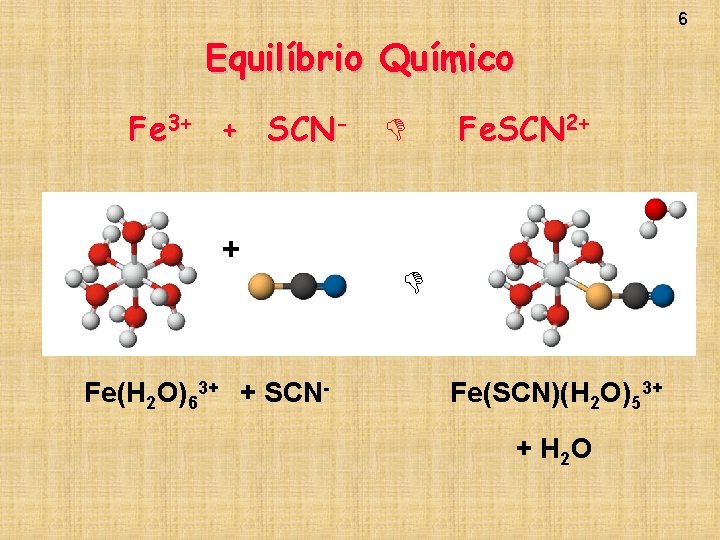
6 Equilíbrio Químico Fe 3+ + SCN- + Fe(H 2 O)63+ + SCN- Fe. SCN 2+ Fe(SCN)(H 2 O)53+ + H 2 O
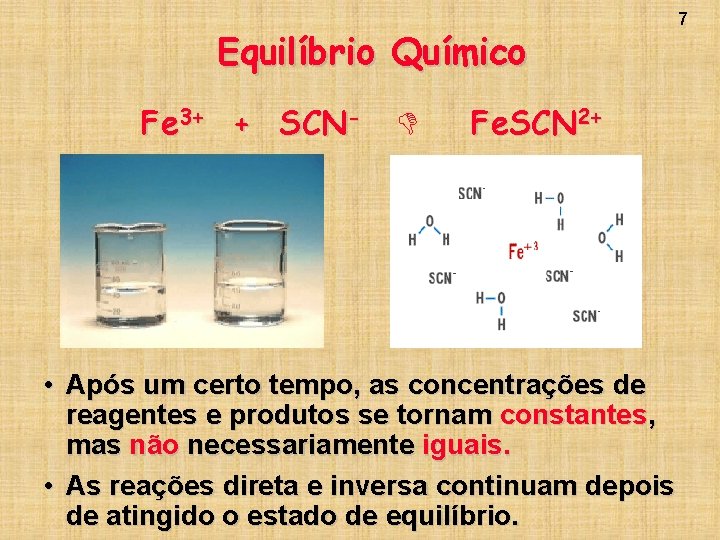
Equilíbrio Químico Fe 3+ + SCN- Fe. SCN 2+ • Após um certo tempo, as concentrações de reagentes e produtos se tornam constantes, mas não necessariamente iguais. • As reações direta e inversa continuam depois de atingido o estado de equilíbrio. 7

8 Exemplos de Equilíbrios Químicos Formação de estalactites e estalagmites Ca. CO 3(s) + H 2 O(liq) + CO 2(g) Ca 2+(aq) + 2 HCO 3 -(aq)

9 Reversibilidade no Equilíbrio Químico • Tecnicamente, todas as reações químicas são um equilíbrio, ou seja, não se completa. Mas quando a concentração de reagentes ou produtos é MUITO BAIXA, diz-se que a reação aconteceu completamente. Exemplo: H+(aq) + OH-(aq) H 2 O(l) H+(aq) + OH-(aq) H 2 O(l)

10 Reversibilidade no Equilíbrio Químico • Teoria das Colisões: Quando 2 moléculas A e B colidem uma com a outra numa orientação apropriada e com suficiente energia, elas podem reagir formando novas moléculas, os produtos C e D. • O diagrama de energia potencial para esta colisão, supostamente exotérmica, pode ser apresentado como:
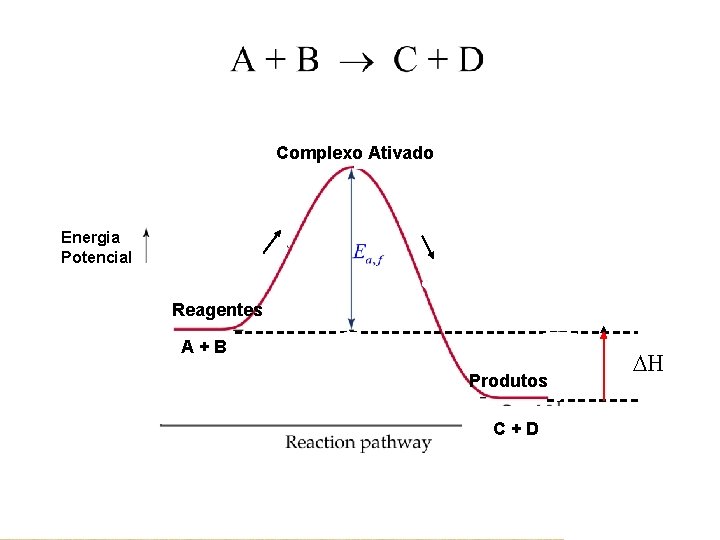
11 Complexo Ativado Energia Potencial Reagentes A+B Produtos C+D DH

12 Reversibilidade no Equilíbrio Químico • A partir de um momento, quantidades significativas de C e D são formadas, e sua concentração começa a aumentar. • Torna-se inevitável que uma molécula de C colida com uma de D. • Se esta colisão ocorrer com energia e orientação adequadas, elas podem reagir e formar novamente as moléculas originais A e B. A+B C+D • Este evento, supostamente endotérmico, apresenta o
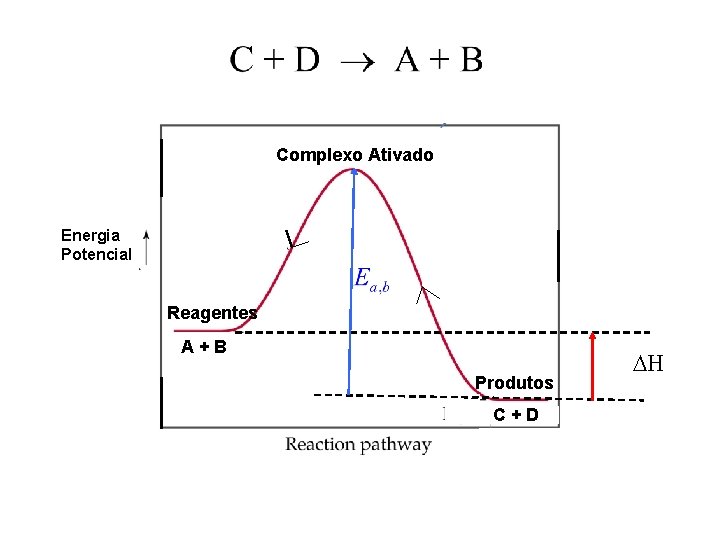
13 Complexo Ativado Energia Potencial Reagentes A+B Produtos C+D DH

14 Reversibilidade no Equilíbrio Químico Qualquer reação que ocorra em extensão significativa tanto nos sentidos direto como inverso é chamada de reação reversível: A+B C+D

Aspectos Quantitativos do Equilíbrio Químico 15 • CONSTANTE DE EQUILÍBRIO Suponha que a reação a seguir ocorra de forma elementar em ambos os sentidos e que inicialmente apenas A e B estejam presentes no vaso de reação. a. A + b. B c. C + d. D

A CONSTANTE DE EQUILÍBRIO A , B Inicialmente, Velocidade da Reação: Velocidade da reação direta Inicialmente C e D não estão presentes, ou seja, não há reação inversa. Há apenas a reação direta: 16

A CONSTANTE DE EQUILÍBRIO Após um certo tempo, a concetração de C e D cresce e a reação inversa começa a acontecer também: A , B, C, D Velocidade da Reação: Velocidade da Reação Inversa Conforme a reação prossegue, as concentrações de A e B caem, ao passo que as de C e D aumentam. As velocidades das reações direta e inversa seguem o seguinte comportamento: 17
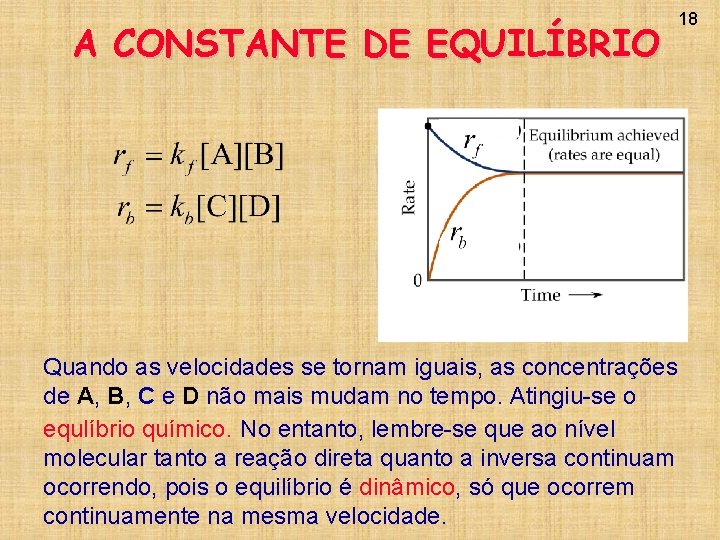
A CONSTANTE DE EQUILÍBRIO Quando as velocidades se tornam iguais, as concentrações de A, B, C e D não mais mudam no tempo. Atingiu-se o equlíbrio químico. No entanto, lembre-se que ao nível molecular tanto a reação direta quanto a inversa continuam ocorrendo, pois o equilíbrio é dinâmico, só que ocorrem continuamente na mesma velocidade. 18

19 A CONSTANTE DE EQUILÍBRIO Para o exemplo realizado na lousa e para uma formulação mais completa, levando-se em conta a lei de ação das massas: Se K é conhecida, pode-se prever as concentrações de reagentes ou produtos.

Determinação de K 2 NOCl(g) 2 NO(g) + Cl 2(g) Coloque 2, 00 mol de NOCl em um frasco de 1, 00 L. No equilíbrio você encontra 0, 66 mol/L de NO. Calcule K. Solução Construa uma tabela de concentrações [NOCl] [NO] [Cl 2] Inicial 2, 00 0 0 Variação Equilíbrio 0, 66 20

Determinação de K 2 NOCl(g) 2 NO(g) + Cl 2(g) Coloque 2, 00 mol de NOCl em um frasco de 1, 00 L. No equilíbrio você encontra 0, 66 mol/L de NO. Calcule K. Solução Construa uma tabela de concentrações [NOCl] [NO] [Cl 2] Inicial 2, 00 0 0 Variação -0, 66 +0, 33 Equilíbrio 1, 34 0, 66 0, 33 21
![Determinação de K 2 NOCl(g) 2 NO(g) + Cl 2(g) [NOCl] [NO] [Cl 2] Determinação de K 2 NOCl(g) 2 NO(g) + Cl 2(g) [NOCl] [NO] [Cl 2]](http://slidetodoc.com/presentation_image_h/e3a625a0f37cdc87b512969d67ace942/image-22.jpg)
Determinação de K 2 NOCl(g) 2 NO(g) + Cl 2(g) [NOCl] [NO] [Cl 2] Inicial 2, 00 0 0 Variação -0, 66 +0, 33 Equilíbrio 1, 34 0, 66 0, 33 22

23 Determinação de K Exemplos Escreva as expressões de constante de equilíbrio para as seguintes reações: Equações Químicas balanceadas

24 Relações Envolvendo a Constante de Equilíbrio • A reversão de uma reação causa a inversão de K. • A multiplicação dos coeficientes por um fator comum eleva a constante de equilíbrio à potencia correspondente. • A divisão dos coeficientes por um fator comum leva à raiz correspondente da constante de equilíbrio.

25 Combinando Expressões de Constante de Equilíbrio N 2 O(g) + ½O 2 2 NO(g) N 2(g) + ½O 2 N 2 O(g) N 2(g) + O 2 2 NO(g) K c= [NO]2 [N 2 O][O 2] = ½ K c= ? Kc(2)= 2, 7 x 10 -18 [N 2 O] = [N 2][O 2]½ Kc(3)= 4, 7 x 10 -31 = [NO]2 [N 2][O 2]½ [N 2][O 2] [N 2 O] = Kc(3) 1 [NO]2 [N 2][O 2] = 1, 7 x 10 -13 Kc(2)

Gases: A constante de Equilíbrio, KP • Misturas de gases são soluções, da mesma forma que os líquidos. • Use KP, baseado nas pressões parciais dos gases. Equações Químicas balanceadas 26

27 Líquidos e Sólidos Puros • As expressões das constantes de equilíbrio não têm termos de concentração para fases líquidas ou sólidas de um determinado componente (isto é, sólidos ou líquidos puros). C(s) + H 2 O(g) CO(g) + H 2(g) [CO][H 2] Kc = e Kp = [H 2 O]2 PCOPH 2 O 2
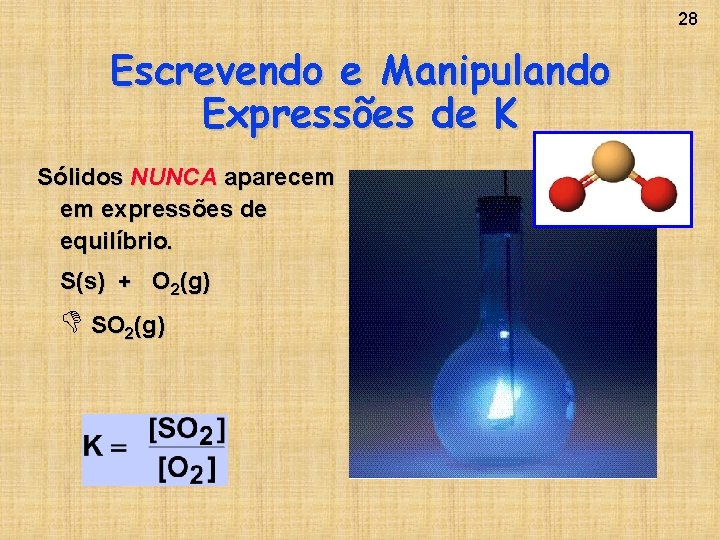
28 Escrevendo e Manipulando Expressões de K Sólidos NUNCA aparecem em expressões de equilíbrio. S(s) + O 2(g) SO 2(g)

29 Queima de Calcário Ca. CO 3(s) Ca. O(s) + CO 2(g) Kc = [CO 2] KP = PCO 2(RT)
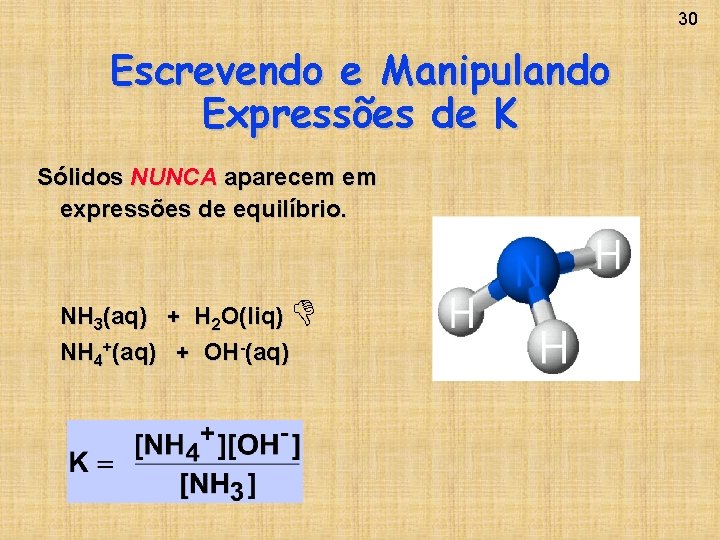
30 Escrevendo e Manipulando Expressões de K Sólidos NUNCA aparecem em expressões de equilíbrio. NH 3(aq) + H 2 O(liq) NH 4+(aq) + OH-(aq)

O Significado de K 1. Podemos dizer se a reação é reagente- ou produto-favorecida. Para N 2(g) + 3 H 2(g) 2 NH 3(g) Conc. de produtos é muito maior que a de reagentes no equilíbrio. A reação é fortemente produto-favorecida. 31
![O Significado de K Para Ag. Cl(s) Ag+(aq) + Cl-(aq) Kc = [Ag+] [Cl-] O Significado de K Para Ag. Cl(s) Ag+(aq) + Cl-(aq) Kc = [Ag+] [Cl-]](http://slidetodoc.com/presentation_image_h/e3a625a0f37cdc87b512969d67ace942/image-32.jpg)
O Significado de K Para Ag. Cl(s) Ag+(aq) + Cl-(aq) Kc = [Ag+] [Cl-] = 1, 8 x 10 -5 Conc. de produtos é muito menor que a de reagentes no equilíbrio. A reação é fortemente reagente- favorecida. 32
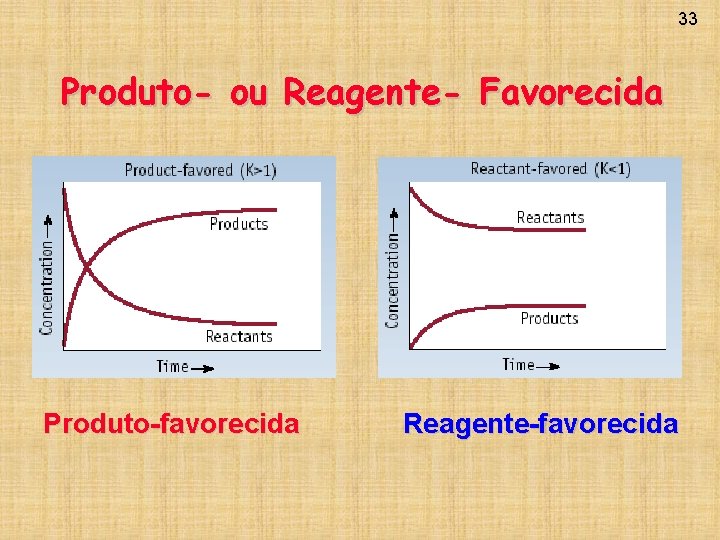
33 Produto- ou Reagente- Favorecida Produto-favorecida Reagente-favorecida
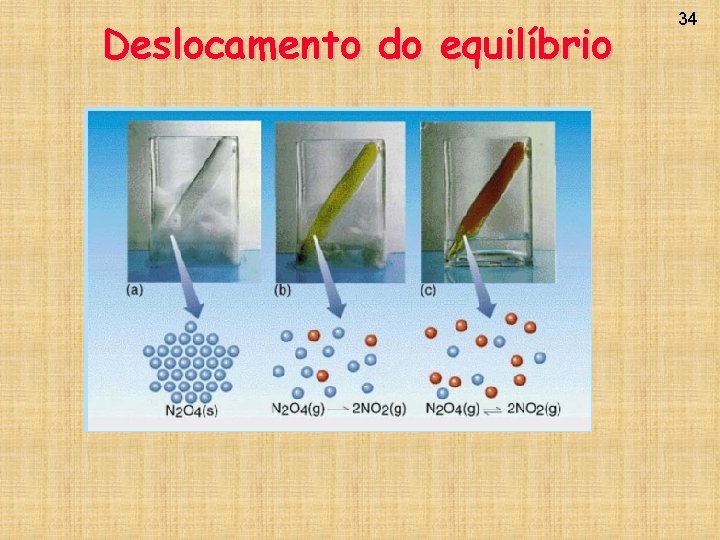
Deslocamento do equilíbrio 34
- Slides: 34