Equilbrio Qumico AB CD u REVERSIBILIDADE Reaes que

Equilíbrio Químico A+B C+D u REVERSIBILIDADE Reações que se desenvolvem ao mesmo tempo, em direções opostas. Ou seja, reagentes e produtos são consumidos e formados ao mesmo tempo. u EQUILÍBRIO QUÍMICO – condições: Sistema fechado e temperatura e pressão constantes
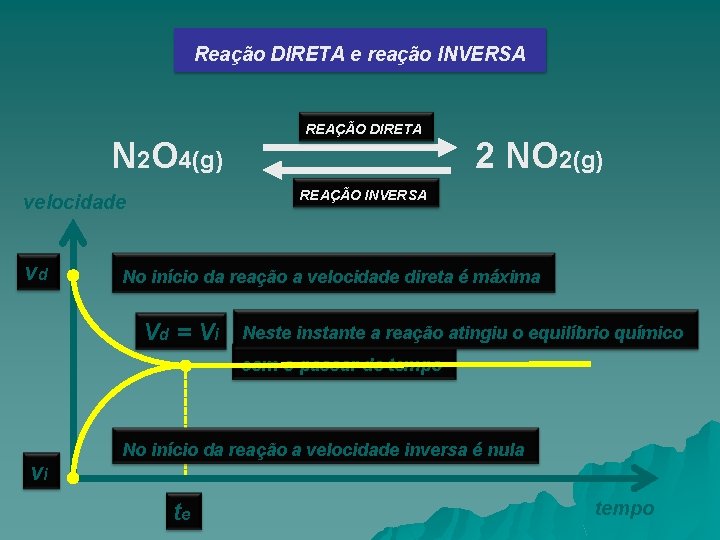
Reação DIRETA e reação INVERSA N 2 O 4(g) 2 NO 2(g) REAÇÃO INVERSA velocidade vd REAÇÃO DIRETA No início da reação a velocidade direta é máxima Vd = V i Neste instante a reação atingiu o equilíbrio químico com o passar do tempo vi No início da reação a velocidade inversa é nula te tempo

V 1 = V 2

u No equilíbrio químico. . . 1 a. A + b. B c. C + d. D 2 V 1 = V 2 K 1. [ A ]a. [ B ]b = K 2. [ C ]c. [ D ]d K 1 = [ C ] c. [ D ]d = kc K 2 [ A ]a. [ B ]b

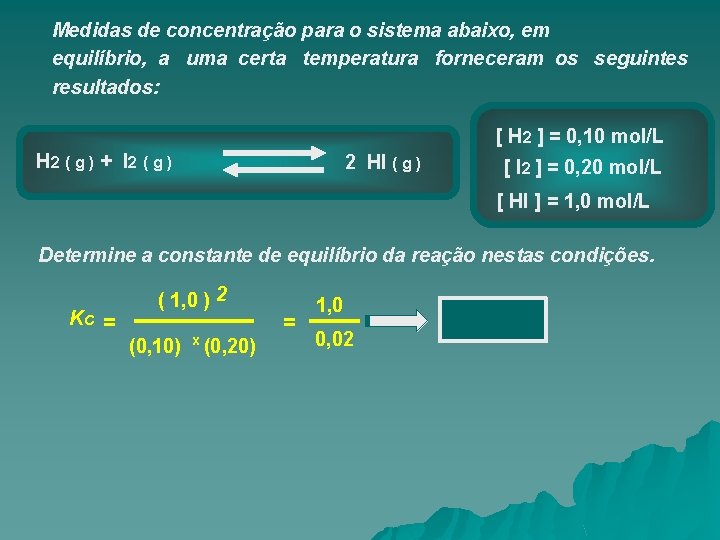
Medidas de concentração para o sistema abaixo, em equilíbrio, a uma certa temperatura forneceram os seguintes resultados: [ H 2 ] = 0, 10 mol/L H 2 ( g ) + I 2 ( g ) 2 HI ( g ) [ I 2 ] = 0, 20 mol/L [ HI ] = 1, 0 mol/L Determine a constante de equilíbrio da reação nestas condições. KC = ( 1, 0 ) 2 (0, 10) x (0, 20) = 1, 0 0, 02 KC = 50

04) Foram colocados em um recipiente fechado, de capacidade 2, 0 L, 6, 5 mol de CO e 5 mol de NO 2. À 200°C o equilíbrio foi atingido e verificou-se que haviam sido formados 3, 5 mol de CO 2. Podemos dizer que o valor de Kc para o equilíbrio dessa reação é: a) 4, 23. CO + NO 2 b) 3, 84. c) 2, 72. início 6, 5 d) 1, 96. reage / produz 3, 5 equilíbrio 3, 0 e) 3, 72. [ CO 2 ] [ NO ] [ CO ] [ NO 2 ] = = 3, 5 2, 0 3, 0 2, 0 1, 5 2, 0 = 1, 75 M CO 2 + NO 5, 0 0, 0 3, 5 1, 5 3, 5 KC = [ CO 2 ] [ CO ] = 1, 75 M KC = 1, 50 M KC = = 0, 75 M 1, 75 x x 3, 0625 1, 125 [ NO ] x x [ NO 2 ] 1, 75 0, 75 KC = 2, 72

1. 888

2 NO 2(g) Castanho avermelhado EXOTÉRMICA ENDOTÉRMICA N 2 O 4(g) incolor ΔH < 0

Vamos analisar o equilíbrio abaixo: Cr 2 O 7 2– alaranjada + H 2 O 1 2 2 Cr. O 4 amarela 2– + 2 H+

Consideremos o efeito da variação de concentração na mistura em equilíbrio cloro e água. A equação de equilíbrio é: Cl 2 + 2 H 2 O HOCl + H 3 O+ + Cl- Esquerda Direita Esquerda

Podemos generalizar afirmando que um(a). . . AUMENTO DE CONCENTRAÇÃO desloca o equilíbrio no SENTIDO OPOSTO da espécie química adicionada DIMINUIÇÃO DE CONCENTRAÇÃO desloca o equilíbrio no mesmo MESMO SENTIDO da espécie química retirada

N 2 ( g ) + 3 H 2 ( g ) 2 NH 3 ( g ) 4 volumes 2 volumes A reação em equilíbrio, ocorre a variação do n. moles de reagentes e produtos, ou seja variação de volume. Um aumento de pressão desloca o equilíbrio para o lado de menor volume (menor n. moles) para diminuir o efeito do aumento da pressão. Aumento de volume diminui a pressão total desloca para o maior número de moléculas Redução de volume aumenta a pressão total desloca para o menor número de moléculas

Exemplo: N 2(g) + 3 H 2(g) 1 mol 3 mols 2 NH 3(g) 2 mols O lado esquerdo da reação representa 4 mols de gás combinando-se para dar 2 mols no lado direito. Um aumento na pressão total do sistema desloca o equilíbrio para a direita. Exemplo: N 2(g) + O 2(g) 2 NO(g) 1 mol 1 mol 2 mols

Considere a reação em equilíbrio químico: N 2 (g) + O 2 (g) 2 NO (g) É possível deslocá-lo para a direita: a) Retirando o N 2 existente. b) Removendo o NO formado. c) Introduzindo um catalisador. d) Diminuindo a pressão, à temperatura constante. e) Aumentando a pressão, à temperatura constante.

O equilíbrio gasoso representado pela equação : N 2( g ) + O 2( g ) 2 NO( g ) – 88 kj É deslocado no sentido de formação de NO(g), se : a) a pressão for abaixada. b) N 2 for retirado. c) a temperatura for aumentada. d) for adicionado um catalisador sólido ao sistema. e) o volume do recipiente for diminuído.

Referências – Equilíbrio Químico u Agamenon Roberto
- Slides: 17