Equilbrio Qumico Profa Karen 1 Conceito de equilbrio

Equilíbrio Químico Profa. Karen 1

Conceito de equilíbrio Um equilíbrio químico é a situação em que a proporção entre as quantidades de reagentes e produtos em uma reação química se mantém constante ao longo do tempo. 2

Teoricamente, toda a reação química ocorre nos dois sentidos: Reagentes produtos Produtos reagentes e Contudo, em certas reações, como a de combustão, virtualmente 100% dos reagentes são convertidos em produtos, e não se observa o contrário ocorrer (ou pelo menos não em escala mensurável); tais reações são chamadas de irreversíveis. 3

Há também uma série de reações nas quais logo que certa quantidade de produto(s) é formada, este(s) torna(m) a dar origem ao(s) reagente(s); essas reações possuem o nome de reversíveis. O conceito de equilíbrio químico praticamente restringe-se às reações reversíveis. 4

5

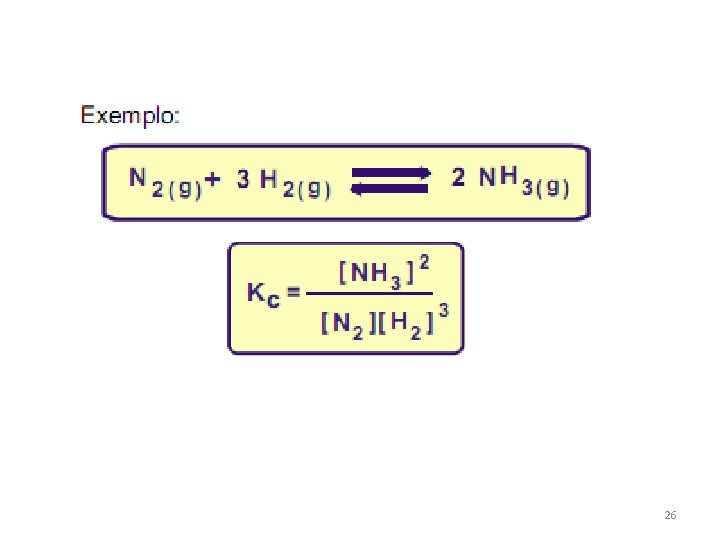
Reversibilidade de reações químicas Um exemplo de reação reversível é a da produção da amônia (NH 3), a partir do gás hidrogênio (H 2) e do gás nitrogênio (N 2) — que faz parte do Processo de Haber: N 2(g) + 3 H 2(g) 2 NH 3(g) Note-se que a seta dupla ( ) significa que a reação ocorre nos dois sentidos, e que o subscrito (g) indica que a substância se encontra na fase gasosa. 6

• Considere o N 2 O 4 congelado e incolor. À temperatura ambiente, ele se decompõe em NO 2 marrom: N 2 O 4(g) 2 NO 2(g). • Em um determinado momento, a cor pára de se alterar e temos a mistura de N 2 O 4 e NO 2. • Equilíbrio químico é o ponto em que as concentrações de todas as espécies são constantes. 7

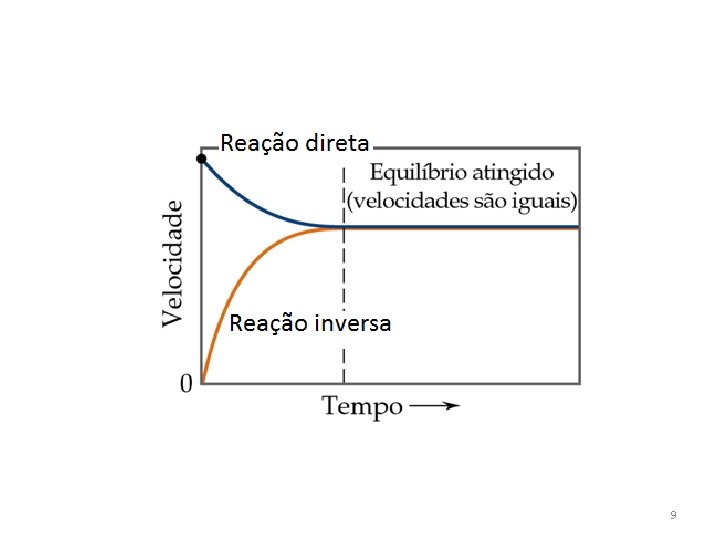
Para um sistema qualquer representado por: A + B V 1 V 2 C +D A rapidez varia a partir do inicio da reação até atingir a situação de equlibrio. O gráfico a seguir mostra essa variação. 8
9
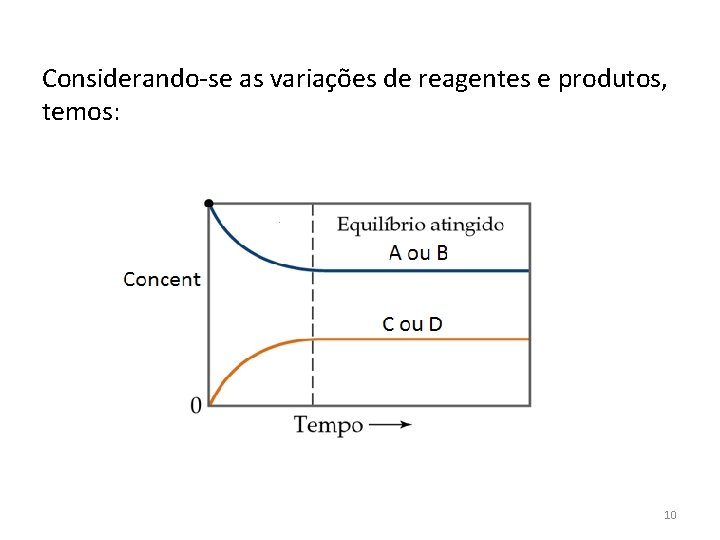
Considerando-se as variações de reagentes e produtos, temos: 10

Deve-se salientar que quando uma reação atinge o equilíbrio ela não para. Ela continua se processando, porém tanto a reação direta como a inversa ocorrem à mesma velocidade, e desse jeito a proporção entre os reagentes e os produtos não variam. Por outras palavras, estamos na presença de um equilíbrio dinâmico. 11

• No equilíbrio, tanto de N 2 O 4 reage para formar NO 2 quanto de NO 2 reage para formar outra vez N 2 O 4: • A seta dupla significa que o processo é dinâmico. • Considere Reação direta: A B Velocidade = k[A] Reação inversa: B A Velocidade = k[B] • No equilíbrio VA = VB = k[A] = k[B]. 12

• Para um equilíbrio escrevemos: A+ B C + D • À medida que a reação progride – [A] e [B] diminuem para uma constante, – [C] e [D] aumentam de zero para uma constante. – Quando [A], [B] e [C], [D] são constantes, o equilíbrio é alcançado. – k[A] diminui para uma constante, – k[B] aumenta de zero para uma constante. – Quando k[A] = k[B], o equilíbrio é alcançado. 13

Equilíbrio Homogêneo e Heterogêneo Quando todas as substâncias envolvidas no equilíbrio se encontram no mesmo estado físico diz-se que temos um equilíbrio homogêneo, que é o caso de todos os equilíbrios apresentados aqui até então. N 2(g) + 3 H 2(g) 2 NH 3(g) 14

Analogamente, os equilíbrios onde estão envolvidas mais de uma fase são chamados de equilíbrios heterogêneos, como o seguinte: Ni(s) + 4 CO(g) Ni(CO)4(g) Note-se que o subscrito (s) significa que a espécie se encontra no estado sólido. Equilíbrios heterogêneos, como este, frequentemente apresentam ao menos um sólido ou um líquido. 15
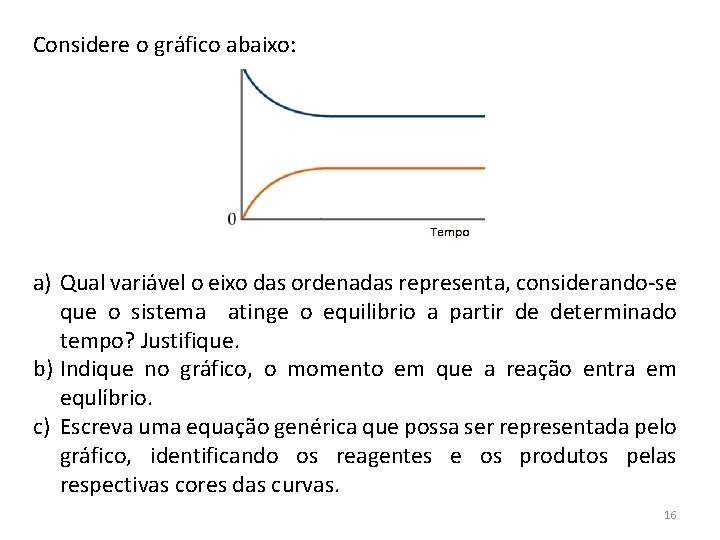
Considere o gráfico abaixo: a) Qual variável o eixo das ordenadas representa, considerando-se que o sistema atinge o equilibrio a partir de determinado tempo? Justifique. b) Indique no gráfico, o momento em que a reação entra em equlíbrio. c) Escreva uma equação genérica que possa ser representada pelo gráfico, identificando os reagentes e os produtos pelas respectivas cores das curvas. 16

Quando uma reação química exotérmica atinge o equilíbrio, são válidas todas as afirmativas abaixo, exceto: a) As velocidades da reação nos sentidos direto e inverso se igualam. b) A energia de ativação é a mesma nos sentidos direto e inverso. c) A reação ocorre com liberação de calor. d) As concentrações de reagentes e produtos permanecem inalteradas. e) A reação inversa é endotérmica 17

Represente, por meio de gráfico, a rapidez da reação direta e da reação inversa até atingir o estado de equilíbrio para a reação: 2 SO 2 (g) + O 2 (g) ↔ 2 SO 3 (g) 18

Considere a reação entre nitrogênio e hidrogênio: (v 1 e v 2 são as velocidades das reações direta e inversa) Quando se estabelece o equilíbrio químico é possível afirmar que: a) b) c) d) e) [N 2] = [H 2]. [NH 3] = constante. [N 2] = [NH 3]. v 2 > v 1 > v 2. 19

Constantes de equilíbrio As constantes de equilíbrio, representadas por K, são determinadas a partir de dados experimentais. Por conta da análise de uma grande quantidade de dados, chegou-se a uma expressão genérica para todos os equilíbrios: K = [produtos]/[reagentes] 20

Constantes de equilíbrio (Kc) As constantes de equilíbrio determinadas com base nas concentrações em mol/L, são representadas por Kc. 21

22
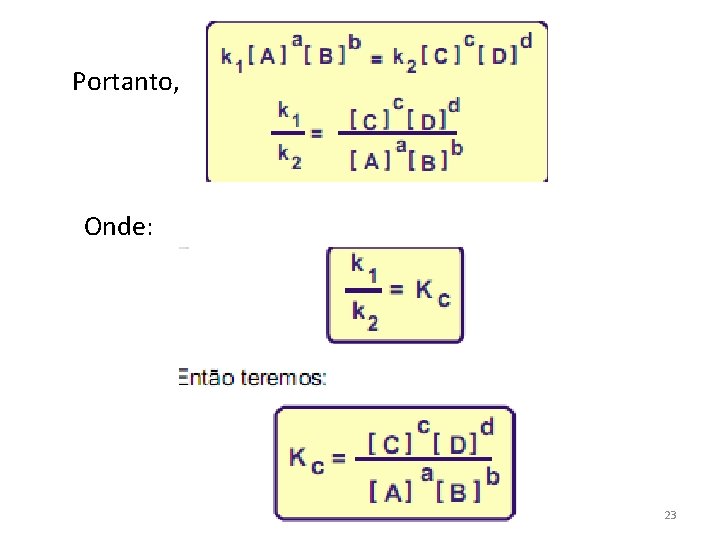
Portanto, Onde: 23

24

25
26

A constante de equilíbrio • Para uma reação geral a expressão d. A constante de equilíbrio para tudo em solução é onde Keq é A constante de equilíbrio. 27

Escreva a expressão da constante de equilíbrio para as equações abaixos: a) 2 NO (g) + Cl 2 (g) ↔ 2 NOCl (g) b) Fe(s) + Cu 2+ (aq) ↔ Fe 2+ (aq) + Cu (s) c) CO 2 (g) + Ca(OH)2 (aq) ↔ Ca. CO 3 (s) + H 2 O (l) 28
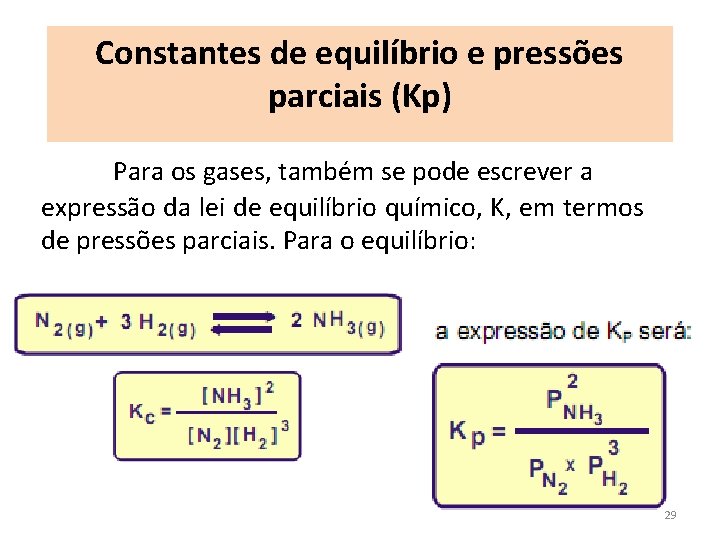
Constantes de equilíbrio e pressões parciais (Kp) Para os gases, também se pode escrever a expressão da lei de equilíbrio químico, K, em termos de pressões parciais. Para o equilíbrio: 29

Para expressar a lei de equilíbrio em termos das pressões parciais, basta que apenas uma das espécies do equilíbrio esteja no estado gasoso. Escreva a expressão da constante de equlíbrio Kp para as seguintes reações: a) H 2 (g) + I 2 (g) ↔ 2 HI (g) b) Ca. CO 3 (s) ↔ Ca. O (s) + CO 2 (g) 30

A constante de equilíbrio Ordem de grandeza das constantes de equilíbrio • A constante de equilíbrio, K, é a razão entre produtos e reagentes. • Conseqüentemente, quanto maior for K, mais produtos estarão presentes no equilíbrio. • De modo inverso, quanto menor for K, mais reagentes estarão presentes no equilíbrio. 31

A constante de equilíbrio Ordem de grandeza das constantes de equilíbrio • Se K >> 1, então os produtos predominam no equilíbrio encontra-se à direita. • Se K << 1, então os reagentes predominam no equilíbrio encontra-se à esquerda. 32

A constante de equilíbrio O sentido da equação química e Keq • Um equilíbrio pode ser abordado a partir de qualquer sentido. • Sentido direto: • temos: 33
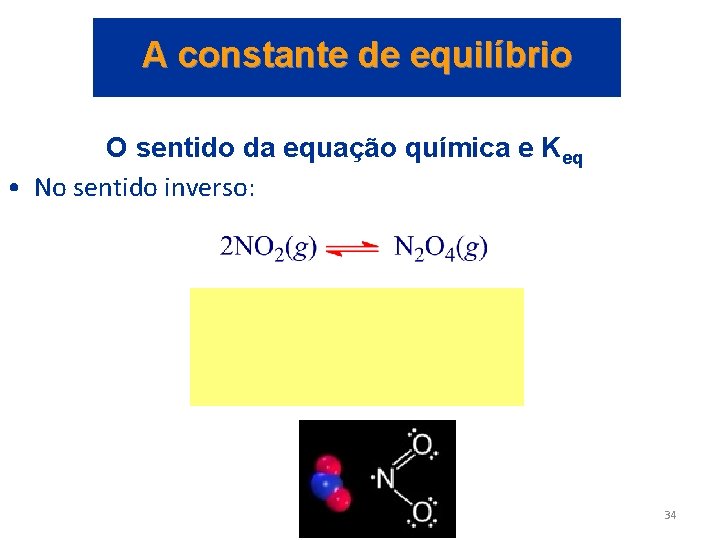
A constante de equilíbrio O sentido da equação química e Keq • No sentido inverso: 34

A constante de equilíbrio Outras maneiras de manipular as equações químicas e os valores de Keq • A reação tem o qual é o quadrado da constante de equilíbrio para 35

A constante de equilíbrio Outras maneiras de se trabalhar as equações químicas e os valores de Keq • A constante de equilíbrio para o sentido inverso é o inverso daquela para o sentido direto. N 2 O 4 (g) 2 NO 2(g) Direto: Kc = (PNO 2 )2/ (PN 2 O 4)= 6, 46 (a 100 o. C) Inverso: Kc= (PN 2 O 4 )/(PNO 2 )2= 1/6, 46 = 0, 155 (a 100 o. C) 36

• Quando uma reação é multiplicada por um número, a constante de equilíbrio é elevada àquela potência. N 2 O 4 (g) 2 NO 2(g) Kc = (PNO 2 )2/ (PN 2 O 4)= 6, 46 (a 100 o. C) 2 N 2 O 4 (g) 4 NO 2(g) Kc = (PNO 2 )4/ (PN 2 O 4)2= (6, 46)2 = 41, 7 (a 100 o. C) 37

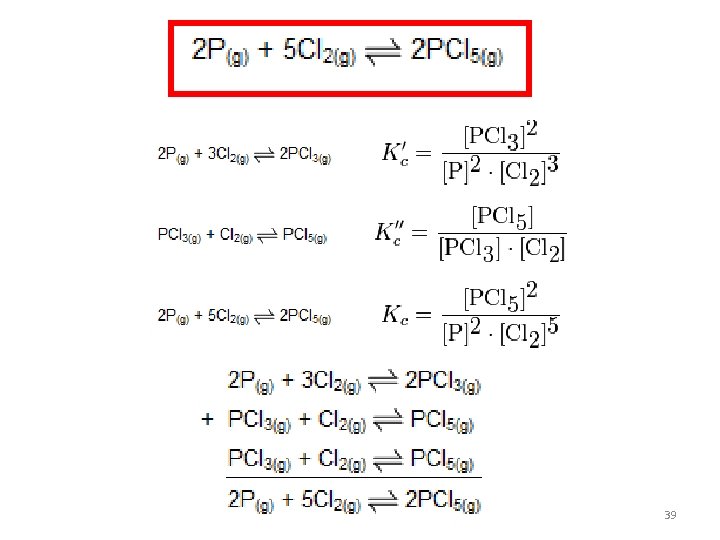
Constante para a soma de reações Se uma reação química pode ser expressa pela soma de duas ou mais reações (ou etapas individuais), então: Kc da reação global será a multiplicação das constantes de cada uma das reações individuais. 38
39

40

Em determinadas condições de T e P, existe 0, 5 mol/L de N 2 O 4 em equilíbrio com 2 mol/L de NO 2, segundo a equação: N 2 O 4 (g) 2 NO 2 (g). Qual o valor da constante (Kc ) desse equilíbrio nessas condições e indique o sentido da reação. 41
- Slides: 41