EQUILBRIO QUMICO INTRODUO CARACTERSTICAS DO EQUILBRIO ANLISE GRFICA

EQUILÍBRIO QUÍMICO -INTRODUÇÃO -CARACTERÍSTICAS DO EQUILÍBRIO -ANÁLISE GRÁFICA DO EQUILÍBRIO -CONSTANTE DE EQUILÍBRIO -PRINCÍPIO DE LE CHATELIER -DESLOCAMENTO DO EQUILÍBRIO -EXERCÍCIOS

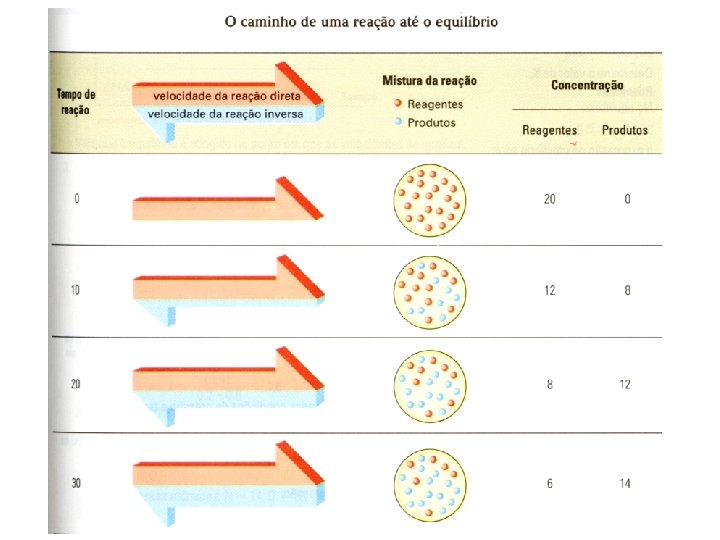
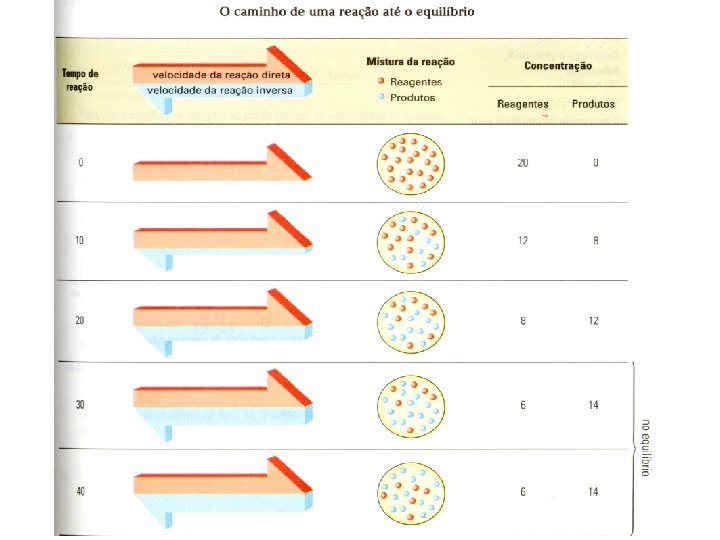
A+B C+D

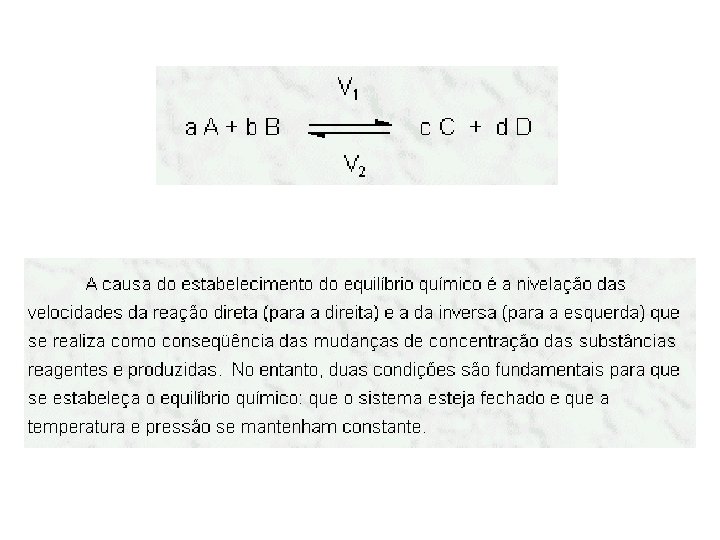

V 1 = V 2 O que existe, na verdade, são duas reações opostas que ocorrem com a mesma velocidade.

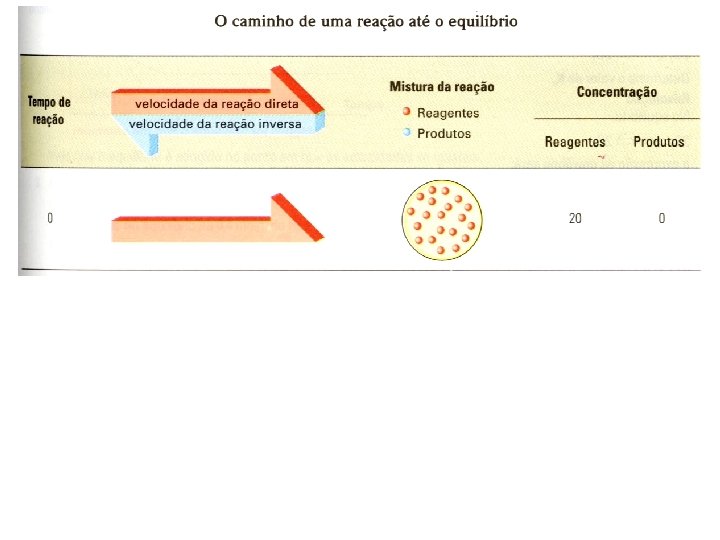
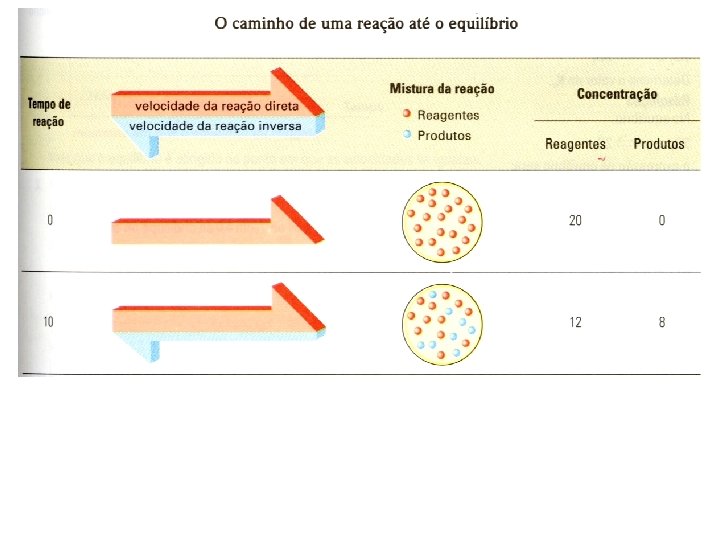
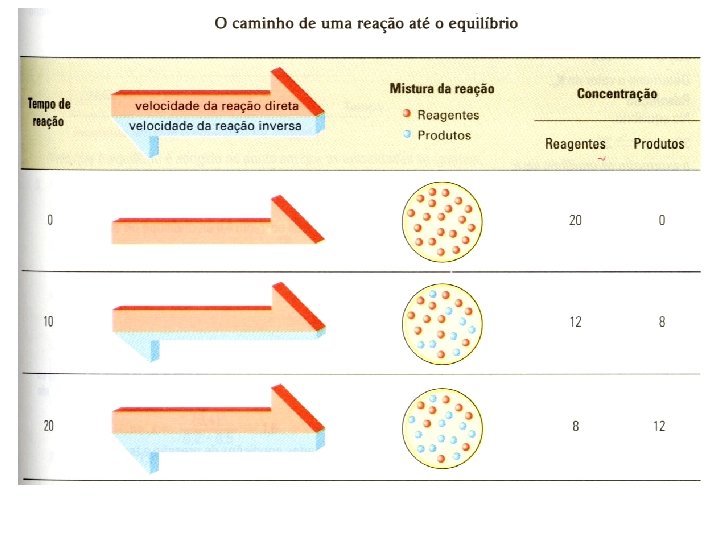

![(c) [Produtos] X Tempo (c) [Produtos] X Tempo](http://slidetodoc.com/presentation_image_h/a74d375127f8bfa9ffc8687b5ae0a4dc/image-13.jpg)
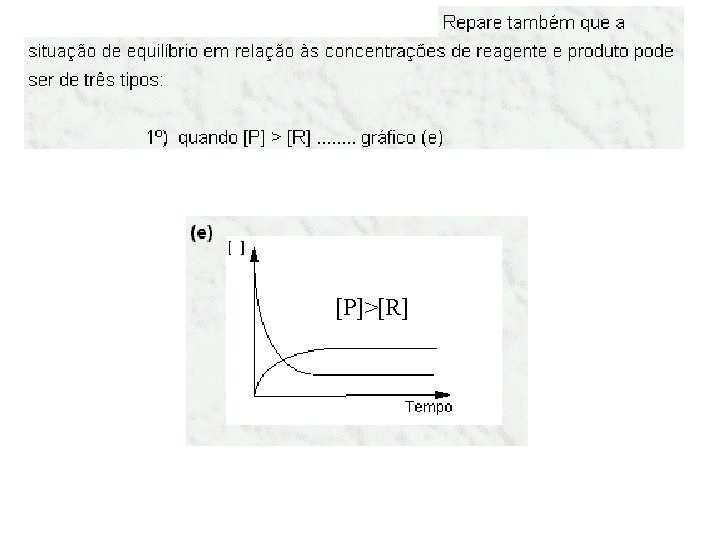
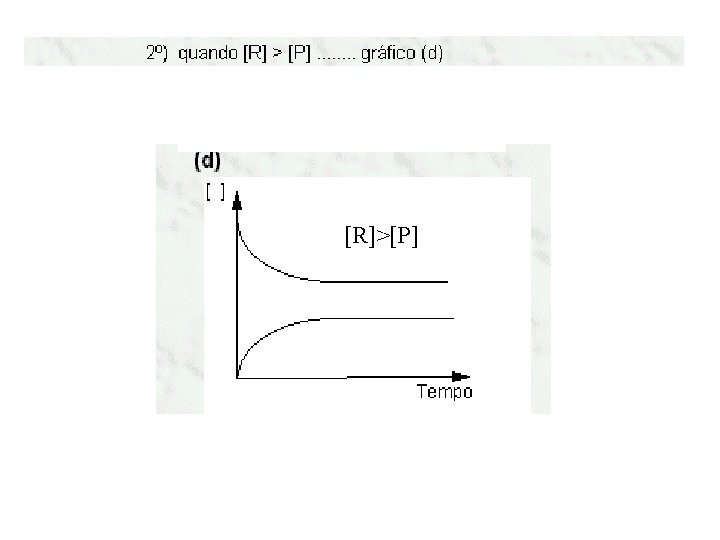
(c) [Produtos] X Tempo
![(c) [Produtos] X Tempo (c) [Produtos] X Tempo](http://slidetodoc.com/presentation_image_h/a74d375127f8bfa9ffc8687b5ae0a4dc/image-14.jpg)
(c) [Produtos] X Tempo
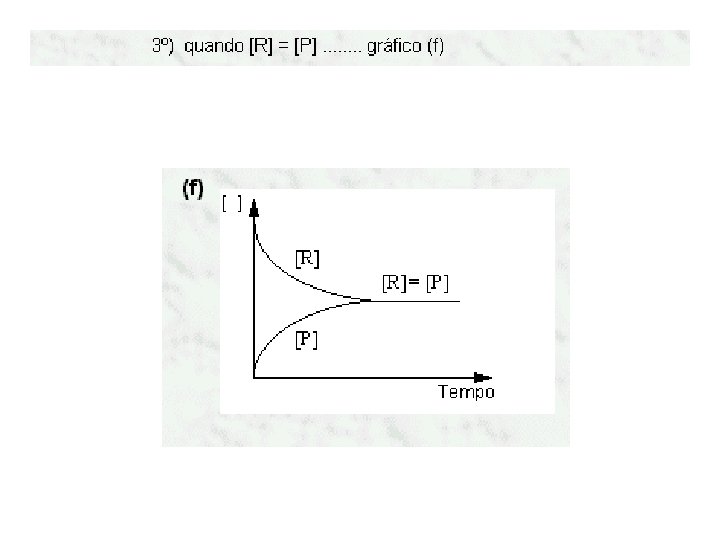
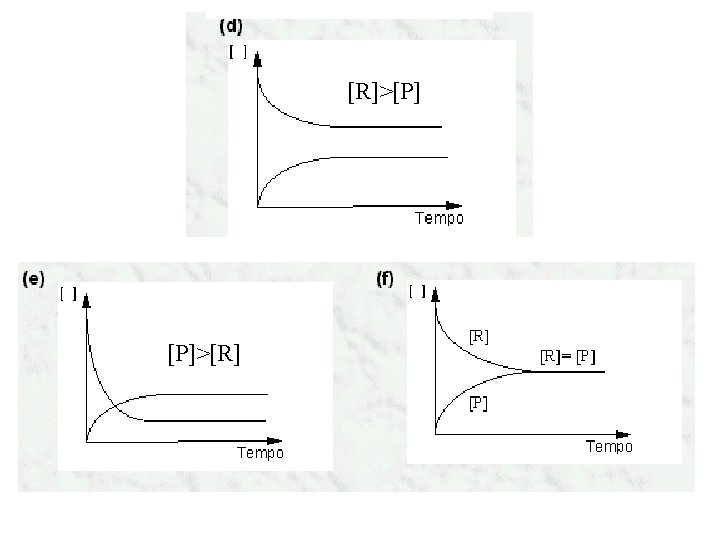




1. 888

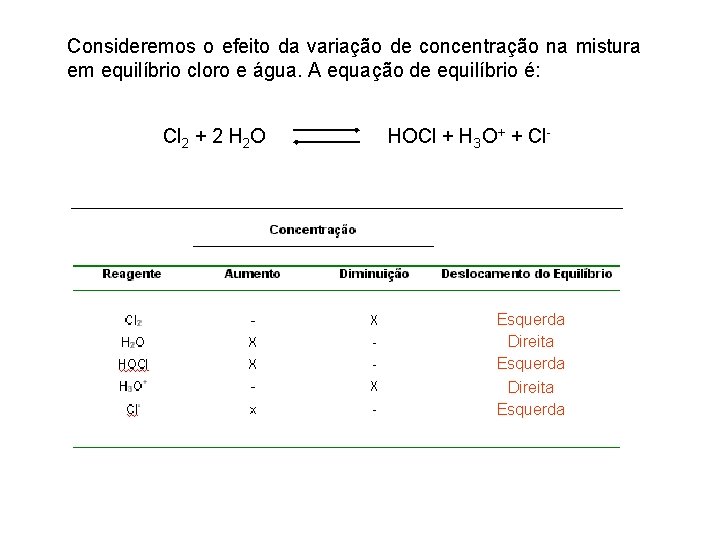
Consideremos o efeito da variação de concentração na mistura em equilíbrio cloro e água. A equação de equilíbrio é: Cl 2 + 2 H 2 O HOCl + H 3 O+ + Cl- Esquerda Direita Esquerda


Exemplo: N 2(g) + 3 H 2(g) 1 mol 3 mols 2 NH 3(g) 2 mols O lado esquerdo da reação representa 4 mols de gás combinando-se para dar 2 mols no lado direito. Um aumento na pressão total do sistema desloca o equilíbrio para a direita. Exemplo: N 2(g) + O 2(g) 2 NO(g) 1 mol 1 mol 2 mols


O calor pode ser considerado um reagente em reações endotérmicas ou um produto em reações exotérmicas. Portanto, a temperatura é análoga à concentração, ao se aplicar o Princípio de Le Chatelier aos efeitos do calor em uma reação química. Exemplo 1: C(s) + CO 2(g) + calor 2 CO(g) A reação é endotérmica e, como pode ser visto, o equilíbrio desloca-se para a direita em temperaturas mais elevadas. Exemplo 2: PCl 3(l) + Cl 2(g) PCl 5(s) + 88 k. J Neste caso a reação é exotérmica. O calor fará com que o produto PCl 5, se decomponha, regenerando o PCl 3 e o Cl 2. Portanto, o calor desloca o equilíbrio para a esquerda.

Keq varia com a temperatura Exemplos: N 2 + 3 H 2 2 NH 3 t°C Keq 200 0, 4 300 4. 10 -3 400 2. 10 -4
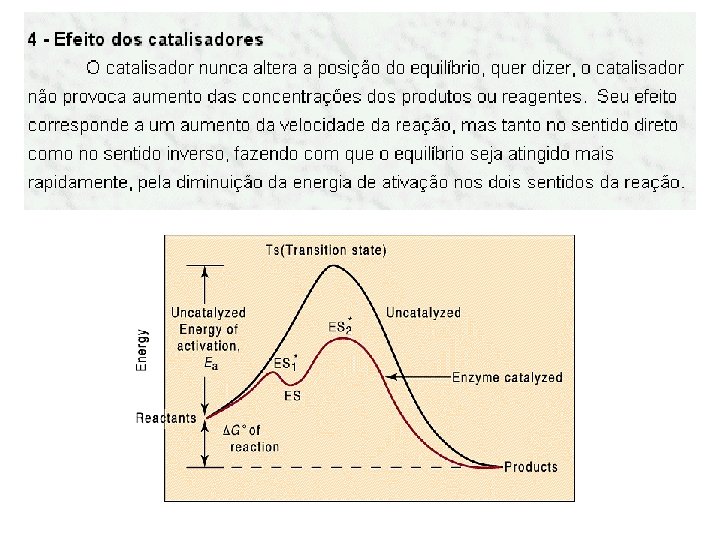

1) Escrever a expressão da constante de equilíbrio (Keq) para as seguintes reações genéricas de equilíbrios homogêneos: a) 2 A + 3 B C + 4 D b) X 2 Y + M

2) Em determinadas condições de pressão e temperatura, um frasco fechado contém 0, 4 mol/L de O 3(g) em equilíbrio com 0, 2 mol/L de O 2(g), de acordo com a seguinte equação: 3 O 2 2 O 3 Determine o valor de Keq.
- Slides: 32