EQUILBRIO EM FASE AQUOSA Equilbrio cido e base

EQUILÍBRIO EM FASE AQUOSA Equilíbrio ácido e base Equilíbrio de solubilidade
Equilíbrio químico - acido e base: • Arrhenius Ácido: substância que aumenta a concentração do íon hidrônio, H 3 O+, em solução aquosa. HCl + H 2 O →H 3 O+ + Cl- ou HCl + H 2 O →H+ + Cl. Base: substância que aumenta a concentração do íon hidróxido, OH-, em água. Na. OH + H 2 O →OH- + Na+
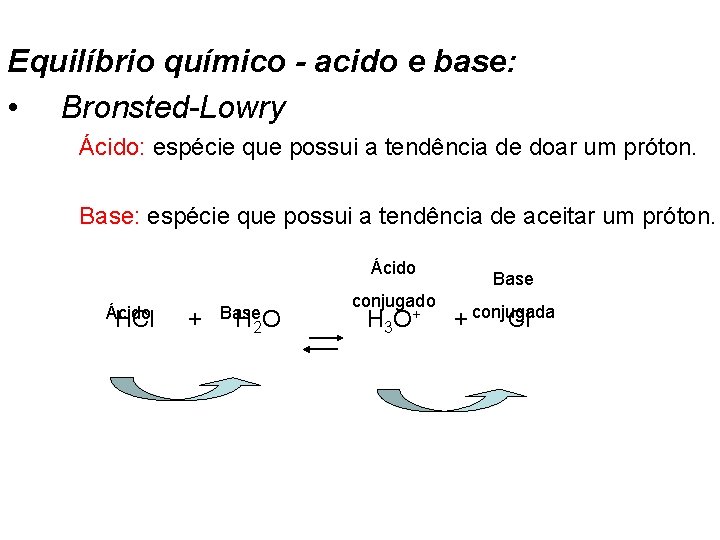
Equilíbrio químico - acido e base: • Bronsted-Lowry Ácido: espécie que possui a tendência de doar um próton. Base: espécie que possui a tendência de aceitar um próton. Ácido Base conjugado conjugada Ácido Base HCl + H O H O+ + Cl 2 3

AUTO-IONIZAÇÃO DA ÁGUA • Bronsted-Lowry: uma mesma substância pode ser considerada como ácido e com base. • Água pode agir com doadora e aceptora de prótons e assim é chamada de anfiprótica H 2 O + H 2 O H 3 O+ + OHÁcido Base conjugado conjugada • Reação de auto-protólise ou auto-ionização • Kw = [H 3 O+][OH-]
![Kw = [H 3 O+][OH-] Kw: constante do produto iônico da água Kw = Kw = [H 3 O+][OH-] Kw: constante do produto iônico da água Kw =](http://slidetodoc.com/presentation_image_h/c856f13c23f42e306949ed4e97d5c42e/image-5.jpg)
Kw = [H 3 O+][OH-] Kw: constante do produto iônico da água Kw = 1, 00 x 10 -14, à 25 o. C [H 3 O+][OH-] = 1, 00 x 10 -14
![Solução neutra: [H 3 O+]=[OH-] [H 3 O+]2 = 1, 00 x 10 -14 Solução neutra: [H 3 O+]=[OH-] [H 3 O+]2 = 1, 00 x 10 -14](http://slidetodoc.com/presentation_image_h/c856f13c23f42e306949ed4e97d5c42e/image-6.jpg)
Solução neutra: [H 3 O+]=[OH-] [H 3 O+]2 = 1, 00 x 10 -14 [H 3 O+] = 1, 00 x 10 -7 Assim as concentração de [H 3 O+] é 1, 00 x 10 -7 M e de [OH-] é 1, 00 x 10 -7 M.
![Acido forte: dissocia-se totalmente em água HCl H+ + Cl- [H+] = CHCl Base Acido forte: dissocia-se totalmente em água HCl H+ + Cl- [H+] = CHCl Base](http://slidetodoc.com/presentation_image_h/c856f13c23f42e306949ed4e97d5c42e/image-7.jpg)
Acido forte: dissocia-se totalmente em água HCl H+ + Cl- [H+] = CHCl Base forte: dissocia-se totalmente em água Na. OH Na+ + OH[OH-] = CNa. OH Exemplo: Quais as molaridades de H 3 O+ e OH- numa solução 0, 2 M de HCl preparada em água?
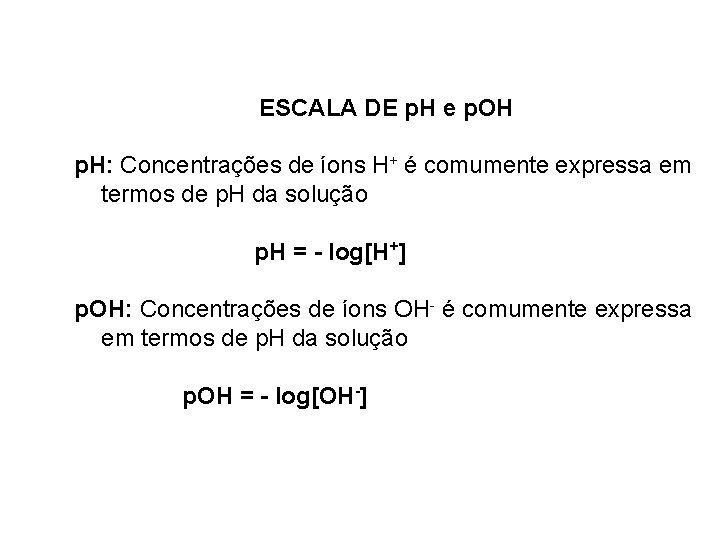
ESCALA DE p. H e p. OH p. H: Concentrações de íons H+ é comumente expressa em termos de p. H da solução p. H = - log[H+] p. OH: Concentrações de íons OH- é comumente expressa em termos de p. H da solução p. OH = - log[OH-]
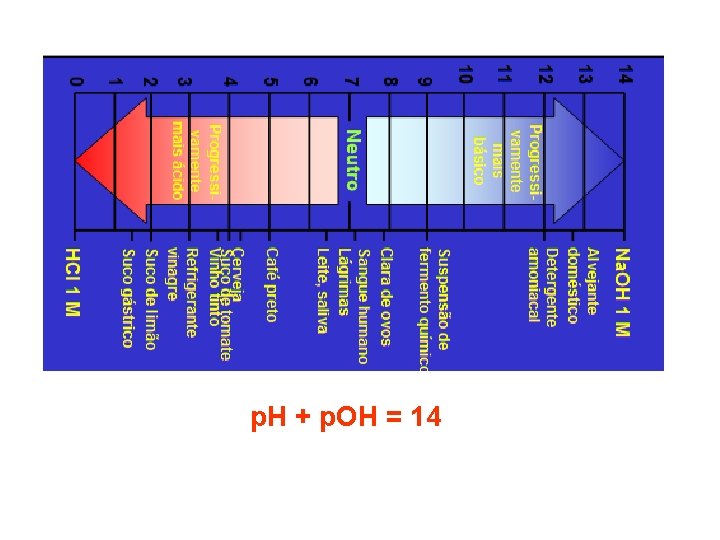
p. H + p. OH = 14
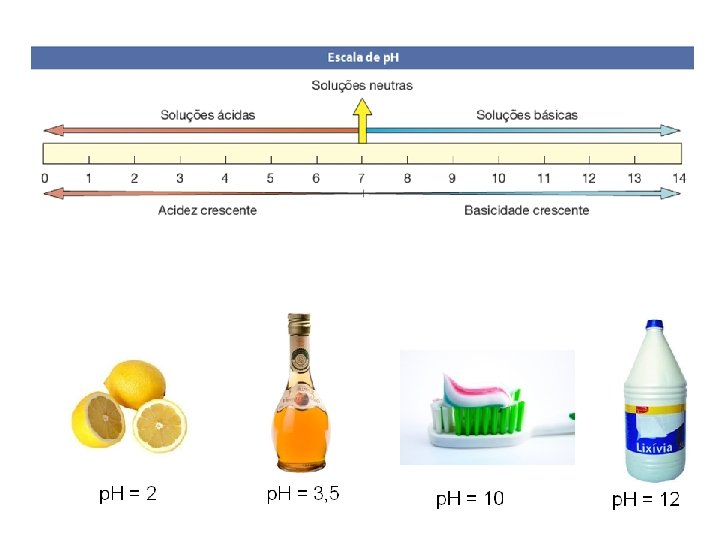
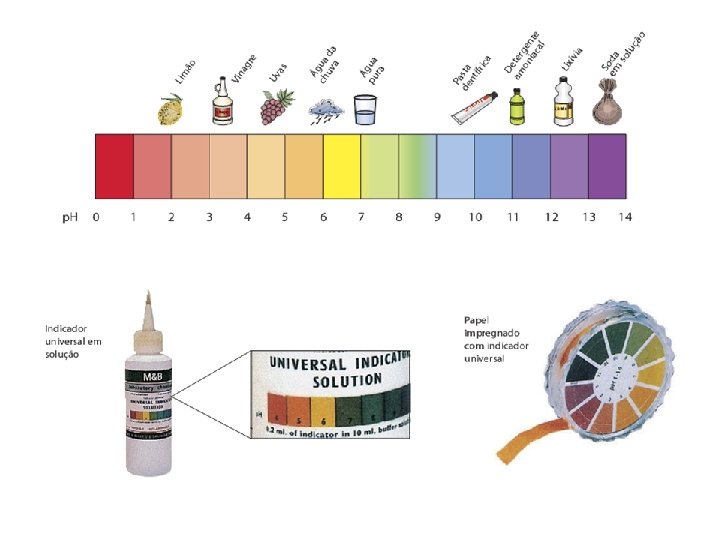

Soluções ácidas: Sabor azedo (p. H<7, 0)

Soluções básicas: escorregadia ao tato (p. H>7, 0)

Soluções neutras: Sabor azedo (p. H=7, 0)
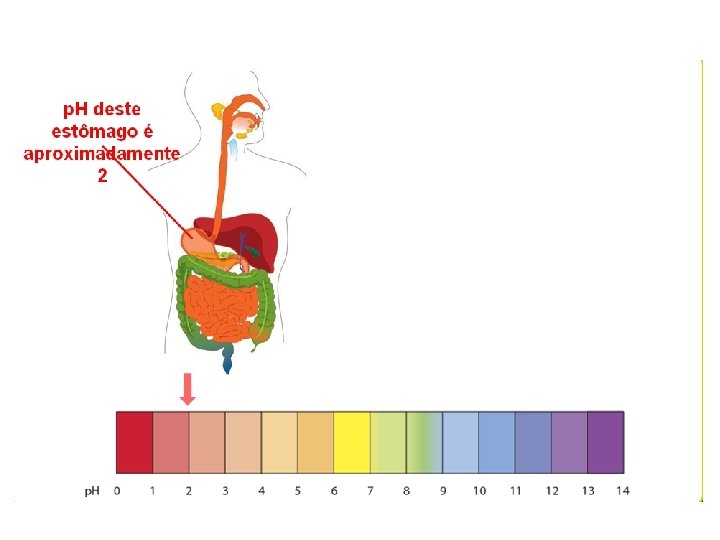


p. H - solo • Indica se o solo é fértil ou não, • 0< p. H<14 • Ideal para agricultura: 5, 5 < p. H < 5, 8 ideal • Varia de acordo com sua composição (rochas), concentração de sais, metais, ácidos, bases e substâncias orgânicas • p. H de um solo pode ser modificado através do uso de substâncias alcalinas como o calcário

Chuva ácida p. H < 5, 6 Origem: da presença de gases NO 2, SO 2, CO 2

p. Hmetros: medir a concentração hidrogeniônica

DISSOCIAÇÃO DE ÁCIDOS E BASES FRACAS v Ácidos e as bases fracas que não se dissociam totalmente em solução aquosa. v Equilíbrio entre as espécies não dissociadas e seus íons correspondentes

Constante de ionização ou dissociação para qualquer ácido fraco: HA + H 2 O 100% H 3 O+ + A- Dissocia-se apenas 0, 1 % 0, 05% Ka = [H 3 O+][A-] [HA] Ka: constante de ionização dos ácidos p. Ka = -log Ka

Constante de ionização ou dissociação para qualquer base fraca: B + H 2 O 100% BH+ + OH- Dissocia-se apenas 0, 1 % 0, 05% Kb = [BH +][OH-] [B] Kb: constante de ionização das bases p. Kb = -log Kb
![RELAÇÃO ENTRE Ka e Kb Ka x Kb = [H 3 O+] [OH-] Ka RELAÇÃO ENTRE Ka e Kb Ka x Kb = [H 3 O+] [OH-] Ka](http://slidetodoc.com/presentation_image_h/c856f13c23f42e306949ed4e97d5c42e/image-23.jpg)
RELAÇÃO ENTRE Ka e Kb Ka x Kb = [H 3 O+] [OH-] Ka x Kb = Kw p. Ka + p. Kb = p. Kw

Exemplo: Um estudante preparou uma solução de ácido acético 0, 50 M e mediu o p. H desta solução, encontrando-o igual a 2, 88. Calcule o Ka para o ácido acético?

DISSOCIAÇÃO DE ELETRÓLITOS POLIPRÓTICOS Ácido poliprótico: é um composto que pode doar mais de um próton Exemplo: Ácido sulfúrico (H 2 SO 4) e ácido carbônico (H 2 CO 3): podem doar dois prótons Ácido fosfórico (H 3 PO 4): podem doar três prótons
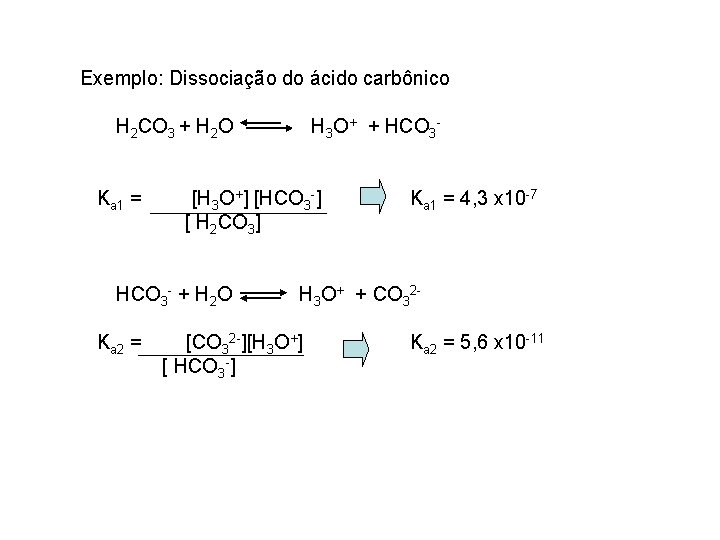
Exemplo: Dissociação do ácido carbônico H 2 CO 3 + H 2 O H 3 O+ + HCO 3 - Ka 1 = [H 3 O+] [HCO 3 -] [ H 2 CO 3] Ka 1 = 4, 3 x 10 -7 HCO 3 - + H 2 O H 3 O+ + CO 32 - Ka 2 = [CO 32 -][H 3 O+] [ HCO 3 -] Ka 2 = 5, 6 x 10 -11

SOLUÇÃO TAMPÃO Ø p. H permanece constante quando ácido e bases fortes são adicionados Ø Solução constituída de mistura de um ácido fraco com uma base conjugada ou de uma base com o ácido conjugado Exemplos: § Solução tampão ácida: solução de ácido acético (H 3 CCOOH) e acetato de sódio (H 3 CCOONa) § Solução tampão básica: solução de amônia (NH 3) e cloreto de amônia (NH 4 Cl)

p. H = 4, 74 SOLUÇÃO TAMPÃO CH 3 COOH/ CH 3 COONa consegue manter o p. H constante após a adição de HCl e de Na. OH
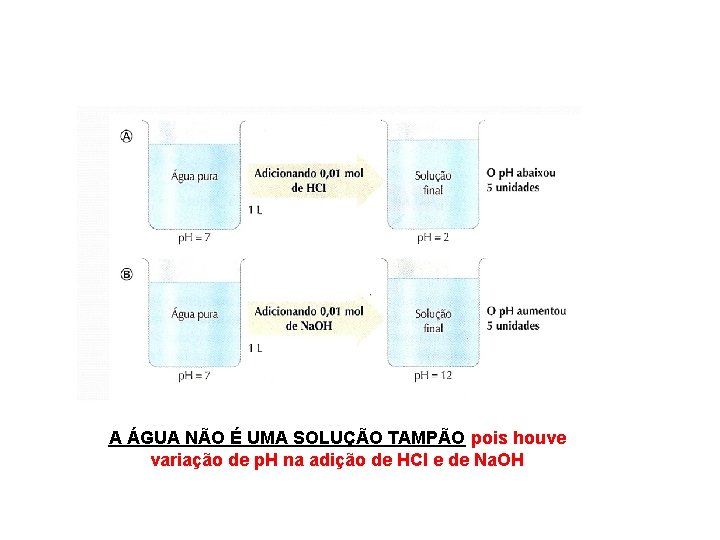
A ÁGUA NÃO É UMA SOLUÇÃO TAMPÃO pois houve variação de p. H na adição de HCl e de Na. OH

Equação de Henderson-Hasselbalch Determinação do p. H de um tampão ácido é dada pela equação: p. H = p. Ka + log [sal] [ácido] § Solução tampão ácida: solução de ácido acético (H 3 CCOOH) e acetato de sódio (H 3 CCOONa) p. H = p. Ka + log [H 3 CCOONa] [H 3 CCOOH] Tampão ácido: p. H<7
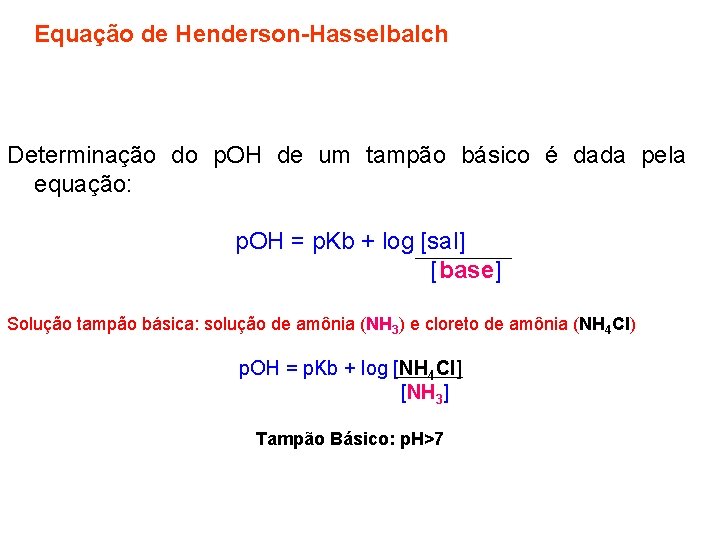
Equação de Henderson-Hasselbalch Determinação do p. OH de um tampão básico é dada pela equação: p. OH = p. Kb + log [sal] [base] Solução tampão básica: solução de amônia (NH 3) e cloreto de amônia (NH 4 Cl) p. OH = p. Kb + log [NH 4 Cl] [NH 3] Tampão Básico: p. H>7

p. H de soluções de sais Se medirmos o p. H de uma solução de sal, em geral não encontramos o valor “neutro” do p. H = 7 Exemplo 1: uma solução 0, 3 M de acetato de sódio tem p. H ~ 9, 0 !! ácido fraco e base forte Exemplo 2: Por outro lado, uma solução 0, 15 M de NH 4 Cl (aq) tem p. H ~ 5, 0 !! ácido forte e base fraca É descrito como o fenômeno de hidrólise
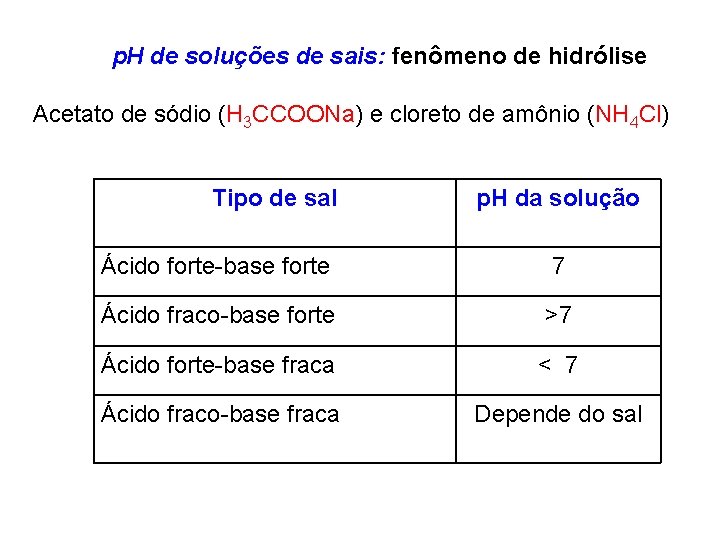
p. H de soluções de sais: fenômeno de hidrólise Acetato de sódio (H 3 CCOONa) e cloreto de amônio (NH 4 Cl) Tipo de sal p. H da solução Ácido forte-base forte 7 Ácido fraco-base forte >7 Ácido forte-base fraca < 7 Ácido fraco-base fraca Depende do sal
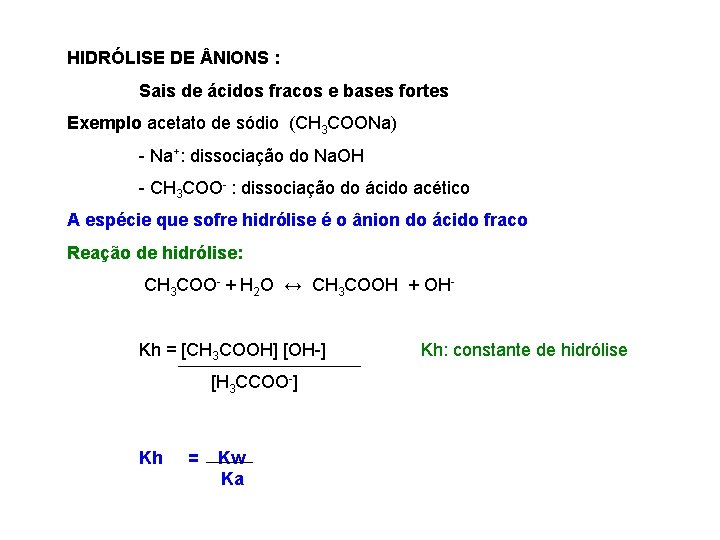
HIDRÓLISE DE NIONS : Sais de ácidos fracos e bases fortes Exemplo acetato de sódio (CH 3 COONa) - Na+: dissociação do Na. OH - CH 3 COO- : dissociação do ácido acético A espécie que sofre hidrólise é o ânion do ácido fraco Reação de hidrólise: CH 3 COO- + H 2 O ↔ CH 3 COOH + OH- Kh = [CH 3 COOH] [OH-] Kh: constante de hidrólise [H 3 CCOO-] Kh = Kw Ka

HIDRÓLISE DE CÁTIONS : Sais de ácidos fortes e bases fracas Exemplo cloreto de amônia (NH 4 Cl ) - NH 4+ : dissociação da amônia (NH 3) - Cl- : dissociação do ácido clorídrico (HCl) A espécie que sofre hidrólise é o cátion da base fraca Reação de hidrólise: NH 4+ + H 2 O ↔ NH 3 + H 3 O+ Kh = [NH 3] [H 3 O+] Kh: constante de hidrólise [NH 4+ ] Kh = Kw Kb

SAIS DE ÁCIDOS FRACOS E BASES FRACAS HIDRÓLISE DE CÁTION E DE NION: v Soluções deste tipo sal podem ser ácidas, neutras ou básicas: v Cátion e o ânion do sal sofrem hidrólise. Se Ka = Kb então p. H da solução neutro Acetato de amônio – CH 3 COONH 4 Ka = 1, 8 x 10 -5 ácido acético - Kb = 1, 8 x 10 -5 amônia (NH 3) Kh-ânion = Kw igual a Kh-cátion = Kw Ka K b

HIDRÓLISE DE CÁTION E DE NION: SAIS DE ÁCIDOS FRACOS E BASES FRACAS cianeto de amônia –NH 4 CN Ka = 4, 9 x 10 -10 ácido cianídrico - Kb = 1, 8 x 10 -5 amônia (NH 3) Kh-ânion = Kw Kh-cátion = Kw Ka K b Kh-ânion = 2, 0 x 10 -5 Kh-cátion = 5, 6 x 10 -10 Kh-ânion > Kh-cátion – p. H da solução é básico

HIDRÓLISE DE CÁTION E DE NION: SAIS DE ÁCIDOS FRACOS E BASES FRACAS fluoreto de amônia – NH 4 F Ka = 6, 7 x 10 -4 ácido fluorídrico - Kb = 1, 8 x 10 -5 amônia (NH 3) Kh-ânion = Kw Kh-cátion = Kw Ka K b Kh-ânion = 1, 5 x 10 -11 Kh-cátion = 5, 6 x 10 -10 Kh-ânion < Kh-cátion – p. H da solução é ácido

METODOLOGIA DE DETERMINAÇÃO DE p. H Equipamento: p. Hmetro Procedimento: 1. Ligar o p. Hmetro e esperar 5 minutos para estabilização; 2. Verificar os níveis de eletrólitos (solução de KCl e Hg 2 Cl 2) dentro do eletrodos. 3. Calibrar o p. Hmetro com tampões 7 e 4 (para soluções ácidas) ou 7 e 10 (para soluções básicas).

METODOLOGIA DE DETERMINAÇÃO DE p. H 4. Acertar as temperaturas. 5. Usar água destilada para lavar o eletrodo, antes de fazer qualquer medida e secar com papel higiênico. 6. Determiar o p. H da amostra fazendo a leitura com precisao de 0, 01 unidades de p. H.

DETERMINAÇÃO DE p. H EM DIFERENTES TIPOS DE AMOSTRAS v- Leitura direta em produtos líquidos como água, sucos, vinhos e bebidas em geral, e que não contenham CO 2; v. Bebidas com gás carbônico, como refrigerante, devem ser submetidas a agitação mecânica ou a vácuo antes de se tomar a medida de p. H, pois o CO 2 pode formar o ácido carbônico e abaixar o p. H;

DETERMINAÇÃO DE p. H EM DIFERENTES TIPOS DE AMOSTRAS v- Bebidas com polpa em suspensão devem ser agitadas para misturar a polpa decantada e medir o p. H imediatamente, antes da polpa se separar novamente, ou utilizar um agitador magnético para conseguir um resultado homogêneo, já que a polpa e o líquido pode ter p. Hs diferentes.

DETERMINAÇÃO DE p. H EM DIFERENTES TIPOS DE AMOSTRAS v- Em produtos sólidos e secos, como farinhas, pão, macarrão e biscoito, é preparado um extrato em suspensão de 10 g do produto em 100 m. L de água, e toma-se o p. H do líquido sobrenadante após a decantação.

DETERMINAÇÃO DE p. H EM DIFERENTES TIPOS DE AMOSTRAS v- Produtos sólidos, mas com bastante umidade, como queijo fresco, devem ser macerados e homogeneizados, e os eletrodos são enfiados dentro da massa da amostra em pelo menos três lugares diferentes para se tirar uma medida média do p. H.






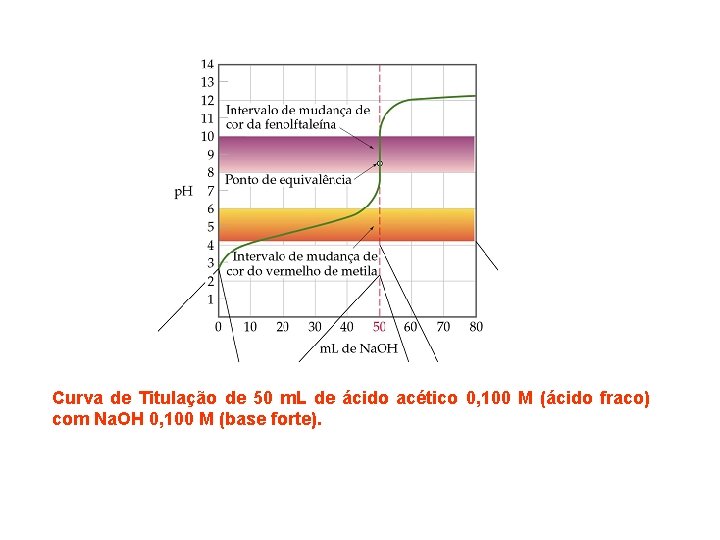
Curva de Titulação de 50 m. L de ácido acético 0, 100 M (ácido fraco) com Na. OH 0, 100 M (base forte).

TITULAÇÕES ÁCIDO – BASE- NEUTRALIZAÇÃO ANÁLISE TITRIMÉTRICA OU VOLUMETRIA Procedimento de análise que é usado para se determinar a quantidade de um ácido pela adição de uma quantidade equivalente de uma base, ou vice-versa. Substâncias participantes de reação de titulação Titulante: substância adicionada ao titulado numa titulação e que tem concentração conhecida – solução reagente - bureta. Titulado: solução que reage com titulante e queremos determinar a concentração. Indicador: substância que é muda a cor quando passa de meio ácido para básico e vice-versa.
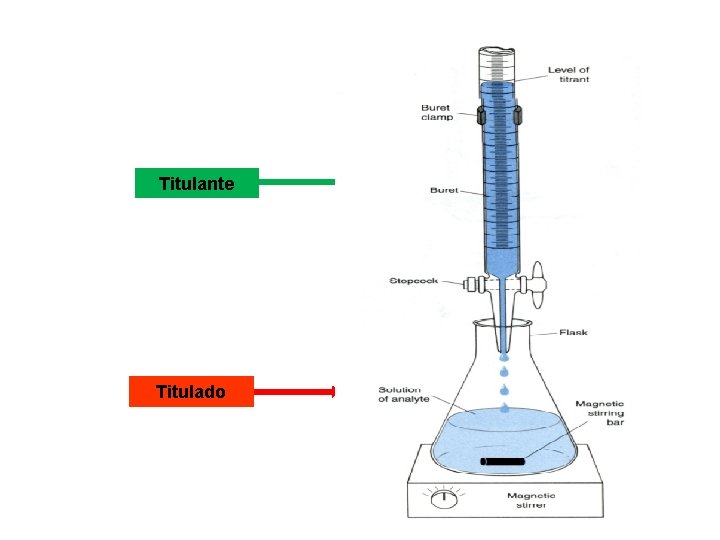
Titulante Titulado
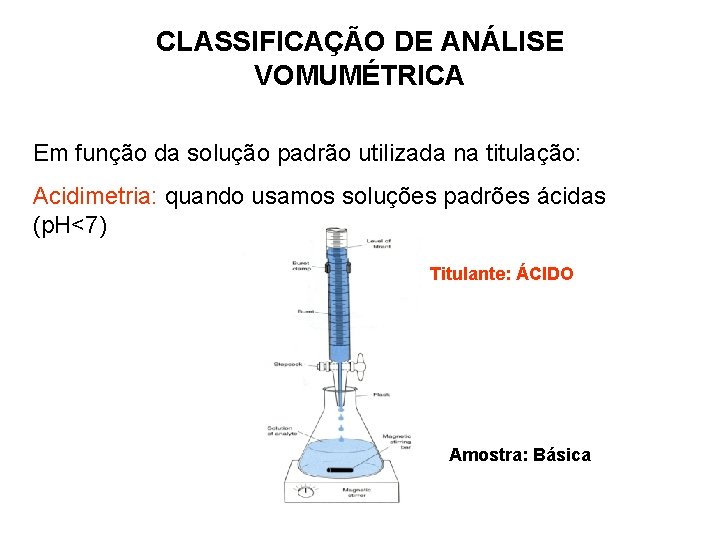
CLASSIFICAÇÃO DE ANÁLISE VOMUMÉTRICA Em função da solução padrão utilizada na titulação: Acidimetria: quando usamos soluções padrões ácidas (p. H<7) Titulante: ÁCIDO Amostra: Básica
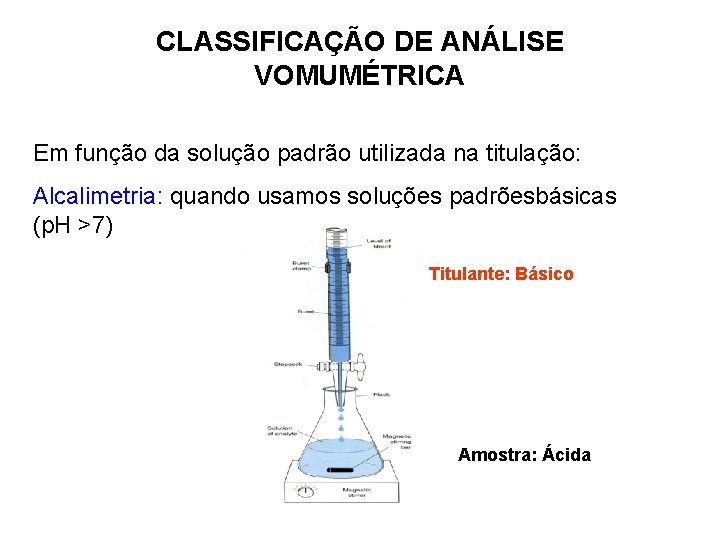
CLASSIFICAÇÃO DE ANÁLISE VOMUMÉTRICA Em função da solução padrão utilizada na titulação: Alcalimetria: quando usamos soluções padrõesbásicas (p. H >7) Titulante: Básico Amostra: Ácida

Titulações: - Ácido forte – base forte - Ácido fraco – base forte - Ácido forte – base fraca v. Calcula-se a quantidade de analito através da quantidade de titulante adicionado


Ponto de Equivalência Ponto da titulação em que a quantidade da solução padrão adicionada é quimicamente equivalente à substância com o qual reage. número de moles do H+ = número de moles do OH- Determinação da quantidade de ácido que é quimicamente equivalente a quantidade de base

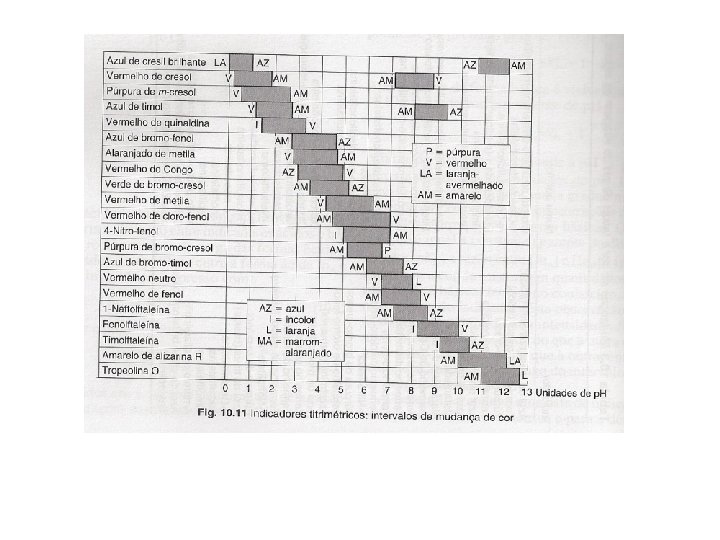
INDICADORES ÁCIDO-BASE • Determinação do ponto de equivalência • Modificam a cor quando passam de meio ácido para meio básico • Ácidos ou bases orgânicas fracas, solúvel em água
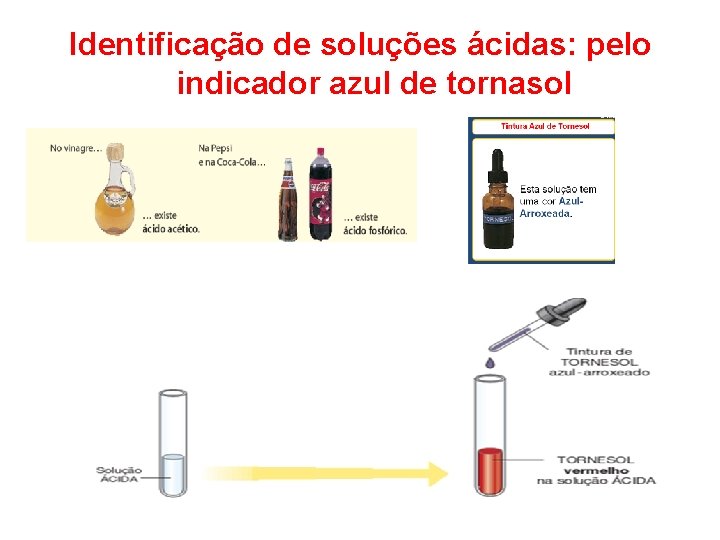
Identificação de soluções ácidas: pelo indicador azul de tornasol
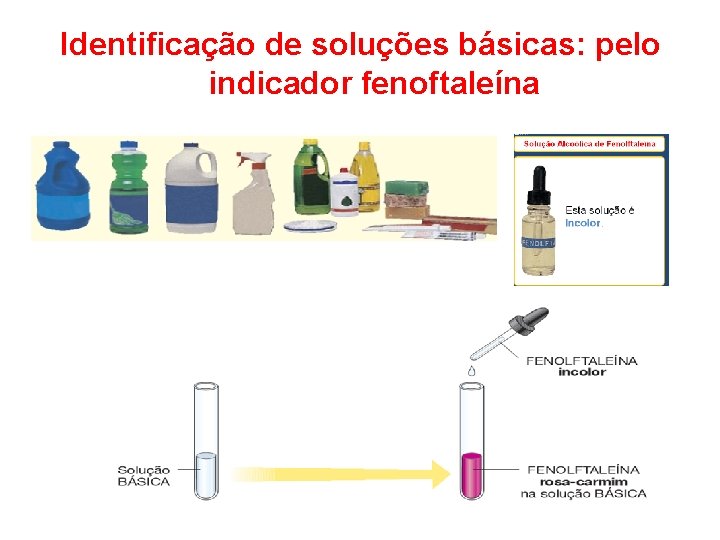
Identificação de soluções básicas: pelo indicador fenoftaleína
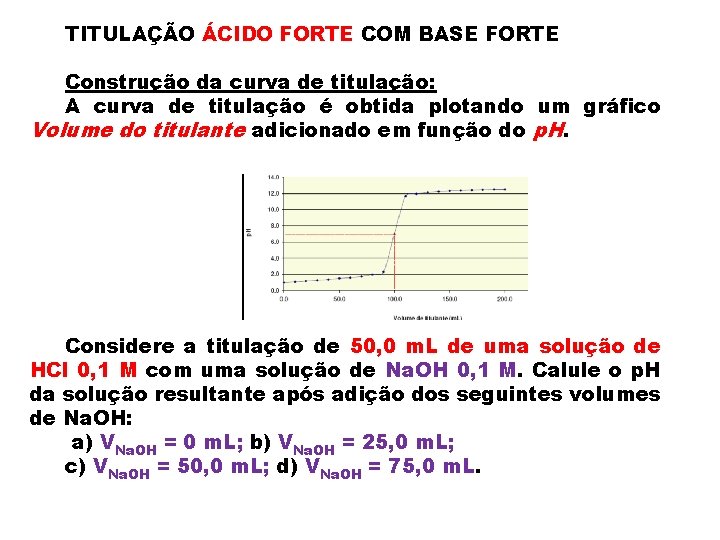
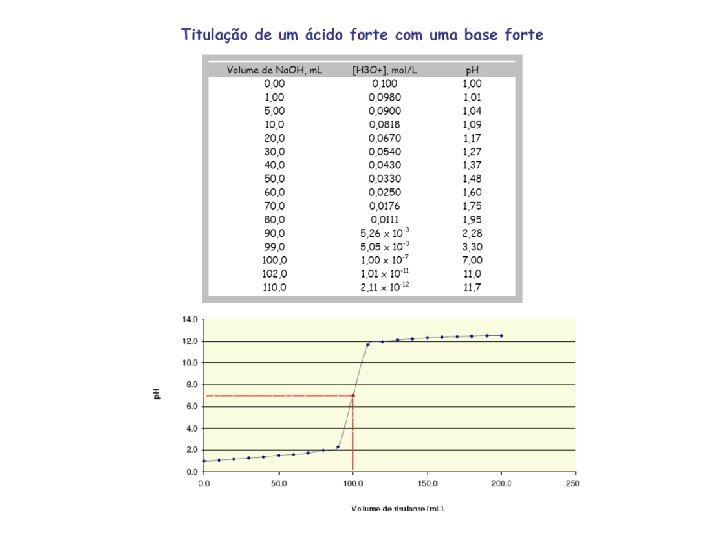
TITULAÇÃO ÁCIDO FORTE COM BASE FORTE Construção da curva de titulação: A curva de titulação é obtida plotando um gráfico Volume do titulante adicionado em função do p. H. Considere a titulação de 50, 0 m. L de uma solução de HCl 0, 1 M com uma solução de Na. OH 0, 1 M. Calule o p. H da solução resultante após adição dos seguintes volumes de Na. OH: a) VNa. OH = 0 m. L; b) VNa. OH = 25, 0 m. L; c) VNa. OH = 50, 0 m. L; d) VNa. OH = 75, 0 m. L.

CURVA DE TITULAÇÃO: ÁCIDO FORTE COM BASE FORTE Cálculo do p. H: a. VNa. OH = 0 m. L Neste caso no erlenmeyer tem apenas 50, 0 m. L de uma solução de HCl 0, 1 M [H+] = CHCl [H+] = 0, 1 M p. H = -log[H+] assim p. H = 1

CURVA DE TITULAÇÃO: ÁCIDO FORTE COM BASE FORTE Cálculo do p. H: b) VNa. OH = 25, 0 m. L (ANTES DO PONTO DE EQUIVALÊNCIA) Neste caso no erlenmeyer temos excesso de HCl 0, 1 M e assim o p. H da solução resultante será: [H+] = CHCl (EXCESSO) p. H = 1, 48

CURVA DE TITULAÇÃO: ÁCIDO FORTE COM BASE FORTE Cálculo do p. H: c) VNa. OH = 50, 0 m. L (NO PONTO DE EQUIVALÊNCIA) Neste caso no erlenmeyer temos que de [HCl] IGUAL a [Na. OH] e assim o p. H da solução resultante será: Os ions [H+] e [OH-] vem apenas da dissociação da água [H+] x [OH-] = 1, 0 x 10 -14 [H+] = 1, 0 x 10 -7 p. H = 7

CURVA DE TITULAÇÃO: ÁCIDO FORTE COM BASE FORTE Cálculo do p. H: VNa. OH = 75, 0 m. L (APÓS DO PONTO DE EQUIVALÊNCIA) Neste caso no erlenmeyer temos excesso de Na. OH 0, 1 M e assim o p. OH da solução resultante será: [OH-] = CNa. OH (EXCESSO) p. OH = 1, 70 e p. H = 12, 30

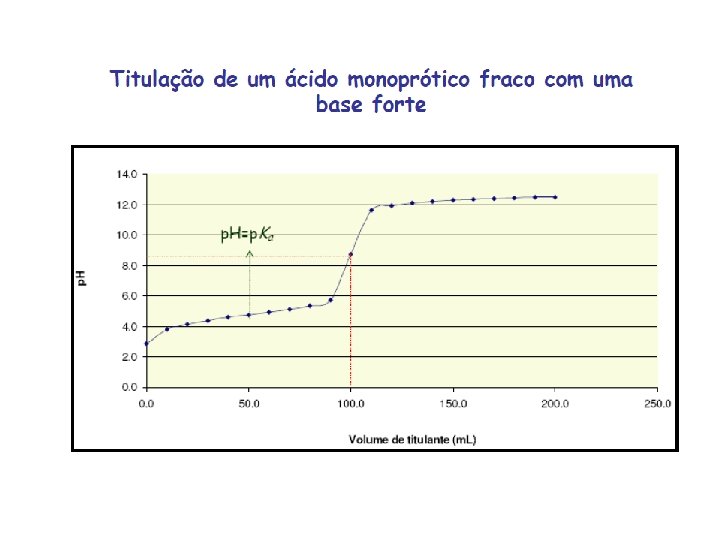
TITULAÇÃO ÁCIDO FRACO COM BASE FORTE Considere a titulação de 50, 0 m. L de uma solução de H 3 CCOOH 0, 1 M com uma solução de Na. OH 0, 1 M. Calule o p. H da solução resultante após adição dos seguintes volumes de Na. OH: a) VNa. OH = 0 m. L; b) VNa. OH = 25, 0 m. L; c) VNa. OH = 50, 0 m. L; d) VNa. OH = 75, 0 m. L.

CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE Cálculo do p. H: a) VNa. OH = 0 m. L Neste caso no erlenmeyer tem apenas 50, 0 m. L de uma solução de H 3 CCOOH 0, 1 M HC 2 H 3 O 2 + H 2 O →C 2 H 3 O 2 - + H+ Ka = [C 2 H 3 O 2 - ] x [H+] [HC 2 H 3 O 2] [H+]2 = Ka x [HC 2 H 3 O 2] p. H = 2, 87

CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE Cálculo do p. H: a) VNa. OH = 25, 0 m. L (ANTES DO PONTO DE EQUIVALÊNCIA) Neste caso no erlenmeyer temos excesso de H 3 CCOOH 0, 1 M e assim o p. H da solução resultante será: [H+] = CH 3 CCOOH (EXCESSO) HC 2 H 3 O 2 + H 2 O →C 2 H 3 O 2 - + H+ Ka = [C 2 H 3 O 2 - ] x [H+] [HC 2 H 3 O 2]
![CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE [H+] = Ka x [HC 2 CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE [H+] = Ka x [HC 2](http://slidetodoc.com/presentation_image_h/c856f13c23f42e306949ed4e97d5c42e/image-72.jpg)
CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE [H+] = Ka x [HC 2 H 3 O 2] [C 2 H 3 O 2 - ] p. H = 4, 75

CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE Cálculo do p. H: c) VNa. OH = 50, 0 m. L (NO PONTO DE EQUIVALÊNCIA) O cálculo do p. H neste ponto consiste na determinação do p. H de um sal de ácido fraco e base forte (SAL). C 2 H 3 O 2 - + H 2 O → HC 2 H 3 O 2 + OHKh = [HC 2 H 3 O 2] x [OH-] [C 2 H 3 O 2 - ] Kh = Kw Ka [OH-]2 = Kh x [HC 2 H 3 O 2 -] p. OH= 5, 28 e p. H = 8, 72

CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE Cálculo do p. H: VNa. OH = 75, 0 m. L (APÓS O PONTO DE EQUIVALÊNCIA) Neste caso no erlenmeyer temos excesso de Na. OH 0, 1 M e assim o p. H da solução resultante será: [OH-] = CNa. OH (EXCESSO) p. OH = 1, 70 e p. H = 12, 30

TITULAÇÃO BASE FRACA COM ÁCIDO FORTE Considere a titulação de 50, 0 m. L de uma solução de NH 4 OH 0, 1 M com uma solução de H 3 CCOOH 0, 1 M. Calcule o p. H da solução resultante após adição dos seguintes volumes de HCl 0, 1 M: a) VHCl = 0 m. L; b) V HCl = 25, 0 m. L; c) V HCl = 50, 0 m. L; d) V HCl = 75, 0 m. L.

CURVA DE TITULAÇÃO: BASE FRACA COM ÁCIDO FORTE Cálculo do p. H: a) VHCl= 0 m. L Neste caso no erlenmeyer tem apenas 50, 0 m. L de uma solução de NH 4 OH 0, 1 M NH 4 OH + H 2 O → NH 4+ + OH- Kb = [NH 4+] x [OH-] [NH 4 OH] [OH+]2 = Kb x [HC 2 H 3 O 2] p. OH = 2, 87 p. H = 11, 13

CURVA DE TITULAÇÃO: BASE FRACA COM ÁCIDO FORTE Cálculo do p. H: b) VHCl= 25, 0 m. L (ANTES DO PONTO DE EQUIVALÊNCIA) Neste caso no erlenmeyer temos excesso de NH 4 OH 0, 1 M e assim o p. H da solução resultante será: NH 4 OH + H 2 O → NH 4+ + OH- Kb = [NH 4+] x [OH-] [NH 4 OH] = VNH 4 OH x MNH 4 OH - VHCl x MHCl VNH 4 OH + VHCl
![CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE Cálculo do p. H: [NH 4+] CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE Cálculo do p. H: [NH 4+]](http://slidetodoc.com/presentation_image_h/c856f13c23f42e306949ed4e97d5c42e/image-79.jpg)
CURVA DE TITULAÇÃO: ÁCIDO FRACO COM BASE FORTE Cálculo do p. H: [NH 4+] = VHCl x MHCl VNH 4 OH + VHC Kb = [NH 4+] x [OH-] [NH 4 OH] l [OH-] = Kb x [NH 4 OH] [NH 4+ ] p. OH = 4, 75 p. H = 9, 25

CURVA DE TITULAÇÃO: BASE FRACA COM ÁCIDO FORTE Cálculo do p. H: c) VHCl= 50, 0 m. L (NO PONTO DE EQUIVALÊNCIA) O cálculo do p. H neste ponto consiste na determinação do p. H de um sal de ácido fraco e base forte (SAL). NH 4+ + H 2 O → NH 3 + H+ Kh = [NH 3] x [H+] [NH 4+ ] = V NH 4 OH x M NH 4 OH VNH 4 OH + VHCl p. H= 5, 28 Kh = Kw Kb [H+]2 = Kh x [NH 4+ ]

CURVA DE TITULAÇÃO: BASE FRACA COM ÁCIDO FORTE Cálculo do p. H: d) VHCl= 75, 0 m. L (APÓS O PONTO DE EQUIVALÊNCIA) Neste caso no erlenmeyer temos excesso de HCl 0, 1 M e assim o p. H da solução resultante será: [H+] = CHCl (EXCESSO) [H+] = VHCl x MHCl - VNH 4 OH x MNH 4 OH VNH 4 OH + VHCl p. H= 1, 70
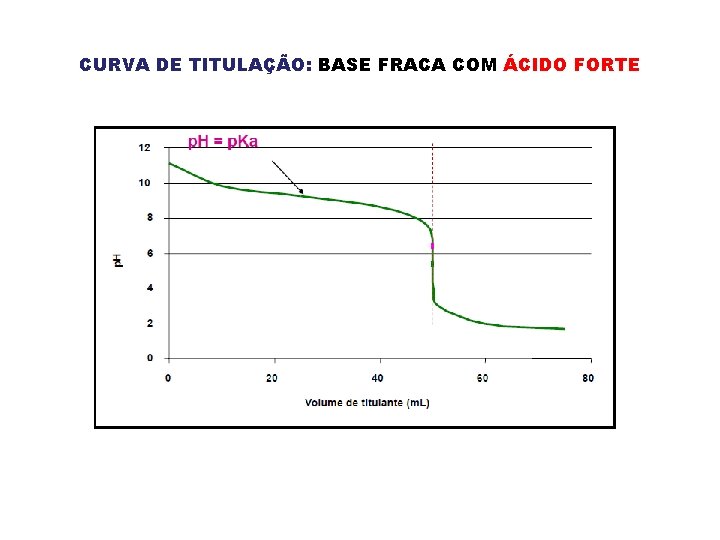
CURVA DE TITULAÇÃO: BASE FRACA COM ÁCIDO FORTE

APLICAÇÕES DA VOLUMETRIA DE NEUTRALIZAÇÃO • Determinação de acidez em vinagre, bebida alcoólica; • Determinação de teor de nitrogênio (Kjeldahl) : alimentos, solo, adubo e planta • Determinação de nitratos e fosfato • Índice de saponificação de óleos e gorduras • Determinação da pureza da vitamina C

APLICAÇÕES DA VOLUMETRIA DE NEUTRALIZAÇÃO • Determinação de acidez em vinagre e em bebida alcóolica • Cálculo: Acidez total (g/100 g de ácido acético) = (Vo x M x PM)/(10 x V) Onde: Volume gasto na titulação de hidróxido de sódio, em m. L M: Molaridade da solução de hidróxido de sódio PM: Peso molecular do ácido acético (60) V: Volume total da amostra

Determinação de teor de nitrogênio (Kjeldahl) Fundamento: O nitrogênio da amostra é deslocado e transformado em sal de amônio (mineralização ou digestão). A seguir, em meio alcalino (adição de Na. OH 40%) e aquecimento desloca-se o NH 3, recebendo-o em ácido bórico com solução indicadora, vermelho de metila + verde de bromocresol, (destilação por arraste a vapor). Por titulação com ácido clorídrico (0, 1 N), determina-se a quantidade de amônio que reagiu com ácido bórico.

Determinação de teor de nitrogênio (Kjeldahl): Cálculo da concentração de nitrogênio

Extratores de Kjeldahl
- Slides: 87