9 Reacciones oxidacinreduccin Qumica 1 S Grado Biologa

9. Reacciones oxidación-reducción Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción

Contenidos • Conceptos básicos. – Estado de oxidación; oxidación y reducción; semirreacción; ajuste de reacciones redox; valoraciones redox • Electroquímica. • Serie electromotriz: semirreacciones y potenciales de electrodo. • Aplicaciones. • Reacciones espontáneas: pilas. • Fuerza electromotriz y energía libre. • Efecto de la concentración sobre el voltaje: Ecuación de Nernst. Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 2

Bibliografía recomendada • Petrucci: Química General, 8ª edición. R. H. Petrucci, W. S. Harwood, F. G. Herring, (Prentice Hall, Madrid, 2003). – Secciones 3. 4, 5. 5, 21. 1, 21. 2, 21. 3, 21. 4 Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 3

Conceptos básicos Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción

Estado de oxidación • Estado de oxidación (o número de oxidación) de un átomo en una molécula – Es un número que se le asigna y que indica de modo aproximado la estructura electrónica de ese átomo en esa molécula – Regla general de asignación de estados de oxidación (e. o. ): • se imagina la situación límite (no real) de que los electrones de un enlace se hayan transferido completamente al átomo más electronegativo del enlace • el estado de oxidación de cada átomo es la carga que tiene tras esta operación mental – e. o. positivo: el átomo pierde total o parcialmente electrones en la molécula respecto al átomo aislado neutro – e. o. negativo: el átomo gana total o parcialmente electrones en la molécula respecto al átomo aislado neutro [Lectura: Petrucci 3. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 5

Estado de oxidación • Reglas básicas de asignación de estados de oxidación: – Los e. o. de los átomos en sus compuestos de determinan aplicando las reglas siguientes, en orden, hasta donde sea necesario: 1. El e. o. de un átomo individual sin combinar químicamente con otros elementos es 0 2. La suma de los e. o. de todos los átomos de una molécula neutra es 0; la de todos los átomos de un ión es la carga del ión 3. En sus compuestos, los metales alcalinos (Grupo 1) tienen e. o. +1 y los alcalinotérreos (Grupo 2) tienen e. o. +2 4. En sus compuestos, el e. o. del F es -1 5. En sus compuestos, el e. o. del H es +1 6. En sus compuestos, el e. o. del O es -2 7. En sus compuestos binarios con metales, los elemetos del Grupo 17 (F, Cl, . . . ) tienen e. o. -1, los del Grupo 16 (O, S, . . . ) tienen e. o. -2, y los del Grupo 15 (N, P, . . . ) tienen e. o. -3 [Lectura: Petrucci 3. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 6

Estado de oxidación Ejemplos: Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 7

Oxidación, reducción y reacción de oxidación-reducción o redox • Oxidación: – aumento del e. o. o pérdida de electrones • Reducción: – disminución del e. o. o ganancia de electrones • Reacción redox o de oxidación-reducción: – reacción de transferencia de electrones, en la que algunos elementos se oxidan y otros se reducen • Oxidante: – reactivo que gana electrones y se reduce • Reductor: – reactivo que cede electrones y se oxida [Lectura: Petrucci 5. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 8

Oxidación, reducción y reacción de oxidación-reducción o redox gana electrones y se reduce de +3 a 0 pierde electrones y se oxida de +2 a +4 es el oxidante es el reductor se reduce a se oxida a gana electrones y se reduce de +1 a 0 pierde electrones y se oxida de 0 a +2 es el oxidante es el reductor se reduce a se oxida a [Lectura: Petrucci 5. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 9

Oxidación, reducción y reacción de oxidación-reducción o redox : (coenzima de función metabólica) dinucleótido de nicotinamida-adenina : forma oxidada del : forma reducida del gana electrones y se reduce de +1 a -1 pierde electrones y se oxida de -2 a 0 es el oxidante es el reductor se reduce a se oxida a [Lectura: Petrucci 5. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 10

Semirreacciones • Semirreacciones de reducción y de oxidación: – cada una de las dos partes en que se separa una reacción redox y en las que se aíslan la reducción (ganancia de e-) y la oxidación (pérdida de e-) Reacción redox global semirreacción de reducción semirreacción de oxidación [Lectura: Petrucci 5. 4] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 11

Ajustes de reacciones redox • Método del ión-electrón 1. Descomponer los compuestos en sus iones –los que se formarían en disolución acuosa-. 2. Identificar elementos que cambian su número de oxidación y escribir semirreacciones iónicas de oxidación y de reducción. 3. Ajustar las semirreacciones como si éstas tuviesen lugar en medio ácido, con la ayuda de H+ y de H 2 O. 1. 2. 3. 4. Ajustar los átomos que no sean H ni O los O, utilizando H 2 O los H, utilizando H+ la carga utilizando e- 4. Sumar las semirreacciones ponderadas de modo que se equilibre el número de electrones. 1. Los H+ y H 2 O auxiliares se eliminarán automáticamente en este paso. 5. Completar la reacción con los compuestos o iones que no participan en las oxidaciones y reducciones. 6. Obtener los compuestos que se habían disociado en iones en el paso 1. a partir de esos mismos iones [Lectura: Petrucci 5. 5] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 12

Ajustes de reacciones redox globales Ejemplo: 1. 2+3. 3. 2 3. 3 3. 4 4. Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 13
![Ajustes de reacciones redox globales 5. 6. [Recomendación: Petrucci ejemplo 5. 6] Química (1 Ajustes de reacciones redox globales 5. 6. [Recomendación: Petrucci ejemplo 5. 6] Química (1](http://slidetodoc.com/presentation_image_h/b96de997b227e0ef94f7d8ce7980a38b/image-14.jpg)
Ajustes de reacciones redox globales 5. 6. [Recomendación: Petrucci ejemplo 5. 6] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 14

Valoraciones redox • Determinación de la concentración de un reactivo en una disolución por medio de una reacción redox (ajustada) – El punto de equivalencia se determina por un cambio brusco: cambio de color, aparición de precipitado, . . . – Ejemplo: Valoración redox de Mn. O 4 - (permanganato) con HSO 3(bisfulfito) en medio ácido violeta incoloro Problema: desconocida Valorante: conocido conocida Se añaden gotas de un ácido fuerte, p. ej. Se determina el punto de equivalencia por cambio de color: de violeta a incoloro. Se mide Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 15

Electroquímica Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción
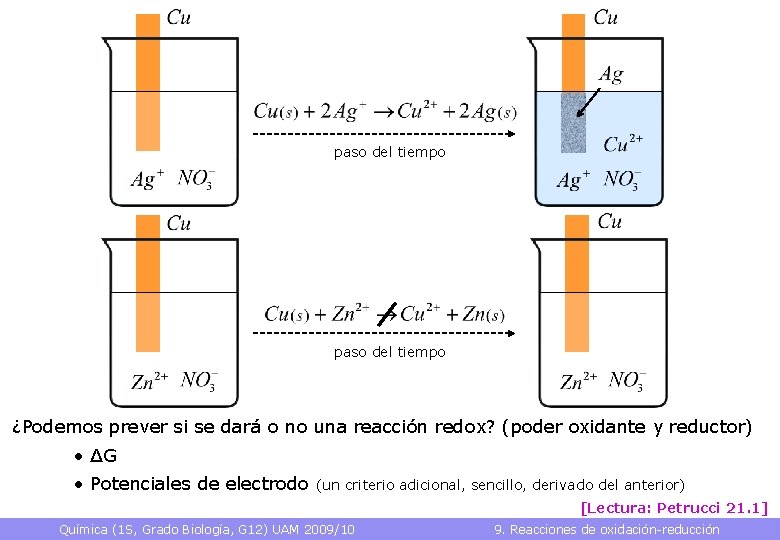
paso del tiempo ¿Podemos prever si se dará o no una reacción redox? (poder oxidante y reductor) • ΔG • Potenciales de electrodo (un criterio adicional, sencillo, derivado del anterior) [Lectura: Petrucci 21. 1] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 17

Semicélulas electroquímicas ¿Podemos separar las semirreacciones de oxidación y de reducción? reducción: oxidación: electrodo de semicélula [Lectura: Petrucci 21. 1] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 18
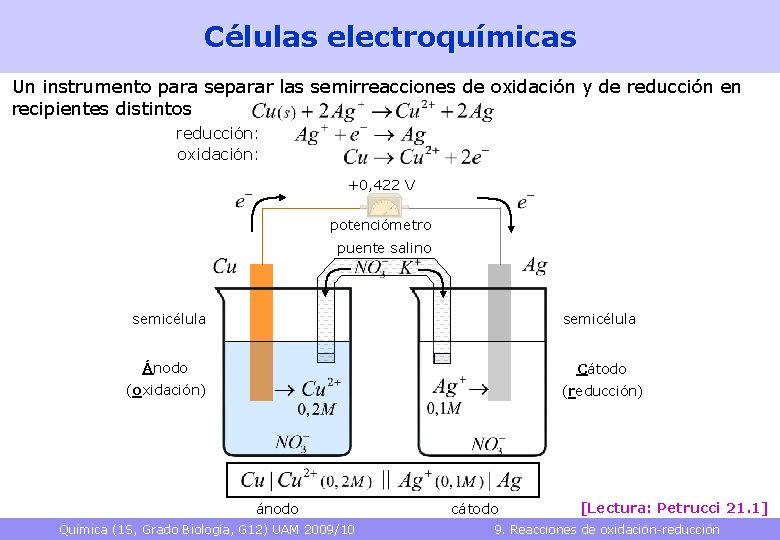
Células electroquímicas Un instrumento para separar las semirreacciones de oxidación y de reducción en recipientes distintos reducción: oxidación: +0, 422 V potenciómetro puente salino semicélula Ánodo Cátodo (oxidación) (reducción) ánodo Química (1 S, Grado Biología, G 12) UAM 2009/10 cátodo [Lectura: Petrucci 21. 1] 9. Reacciones de oxidación-reducción 19
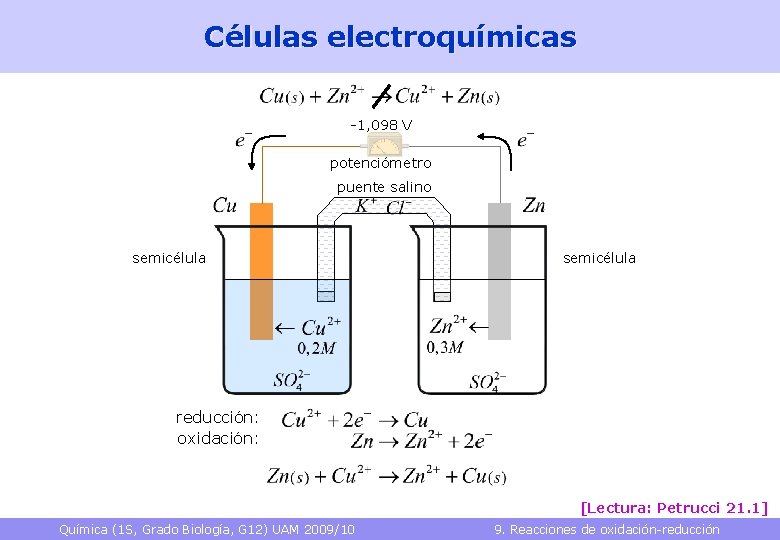
Células electroquímicas -1, 098 V potenciómetro puente salino semicélula reducción: oxidación: [Lectura: Petrucci 21. 1] Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 20
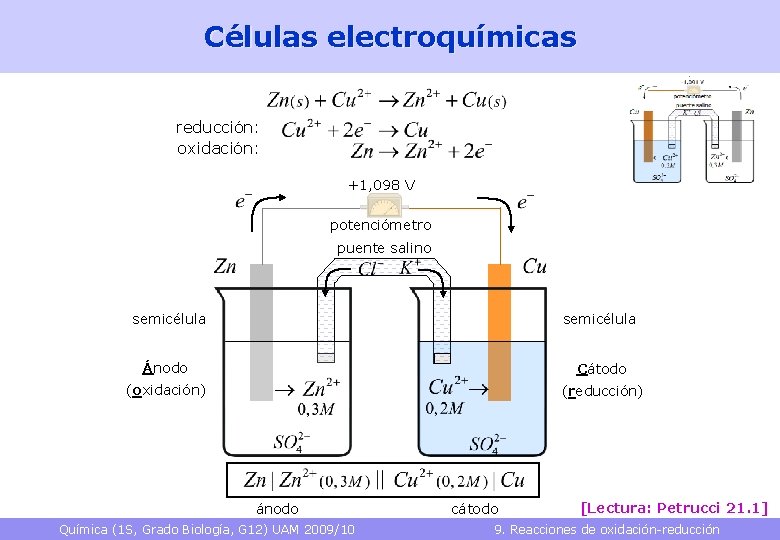
Células electroquímicas reducción: oxidación: +1, 098 V potenciómetro puente salino semicélula Ánodo Cátodo (oxidación) (reducción) ánodo Química (1 S, Grado Biología, G 12) UAM 2009/10 cátodo [Lectura: Petrucci 21. 1] 9. Reacciones de oxidación-reducción 21

Células electroquímicas Ejemplo: El aluminio metálico desplaza al ions zinc(II) de sus disoluciones acuosas. a) Escribe las semirreacciones de reducción y oxidación y la ecuación global. b) ¿Cuál es la notación de la célula electroquímica en la que tiene lugar esa reacción? reducción: oxidación: global: célula electroquímica: Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 22

Potenciales de electrodo Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción

Potenciales de electrodo (escala internacional) • El voltaje medido en una célula electroquímica es la diferencia de potencial entre sus electrodos, o fuerza electromotriz FEM. – Una dif. de potencial de 1 V indica que se realiza un trabajo de 1 J por cada 1 C de carga que pasa por el circuito eléctrico; o que hay suministrar una energía de 1 J para que pase 1 C de carga (según el convenio de signos) • Podríamos calcular FEM de células electroquímicas hipotéticas si conociésemos los potenciales de sus electrodos, por resta. • No existe una escala absoluta de potenciales de electrodo. • Se define una escala arbitraria de potenciales de electrodo, por convenio internacional, por medio de: 1) asignar potencial cero a un electrodo concreto, el electrodo estándar de hidrógeno, y 2) elegir el signo de la FEM de modo que a mayor valor del potencial mayor tendencia a reducirse (poder oxidante). Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 24

Potenciales de electrodo (escala internacional) 1) Electrodo de referencia: electrodo estándar de hidrógeno (EEH) 2) (signo de los) Potenciales de reducción electrodo en el que hay oxidación 3) Potencial de reducción de una semicélula cualquiera (un electrodo): • • Se construye una célula con ella y con un EEH y se mide el voltaje Se observa si este electrodo actúa de ánodo o de cátodo si en la semicélula hay reducción (cátodo): si en la semicélula hay oxidación (ánodo): Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 25

Potenciales de electrodo (escala internacional) • Un potencial de reducción >0 indica una mayor capacidad para reducirse que el EEH – en el electrodo habrá una reducción y en el EEH una oxidación – cuanto más positivo el potencial de reducción, mayor poder oxidante – cuanto más arriba en la escala de potenciales de reducción, mayor poder oxidante • Un potencial de reducción <0 indica una menor capacidad para reducirse que el EEH – en el electrodo habrá una oxidación y en el EEH una reducción – cuanto más abajo en la escala de potenciales de reducción, menor poder oxidante, o mayor poder reductor • Sólo se tabulan los potenciales de electrodos en condiciones estándar a 298 K: – potenciales estándar de electrodo, o de reducción, a 298 K Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 26
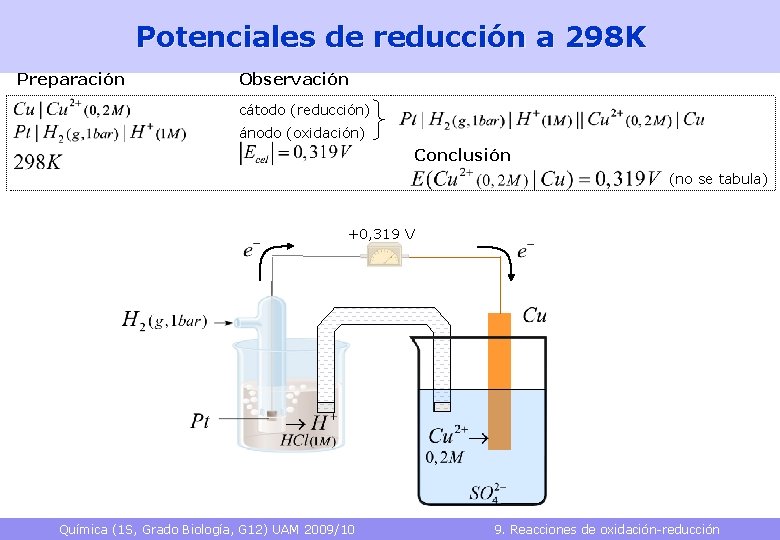
Potenciales de reducción a 298 K Preparación Observación cátodo (reducción) ánodo (oxidación) Conclusión (no se tabula) +0, 319 V Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 27

Potenciales de reducción a 298 K Preparación Observación cátodo (reducción) ánodo (oxidación) Conclusión (no se tabula) cátodo (reducción) ánodo (oxidación) Conclusión (SE TABULA) Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 28
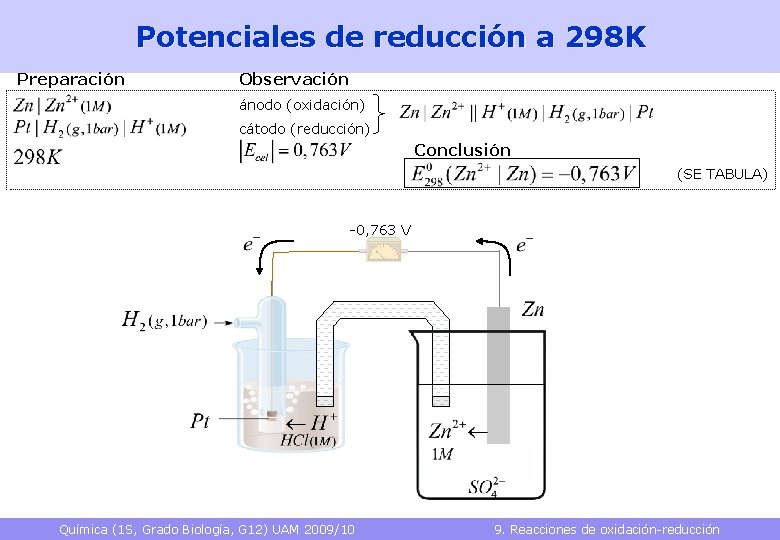
Potenciales de reducción a 298 K Preparación Observación ánodo (oxidación) cátodo (reducción) Conclusión (SE TABULA) -0, 763 V Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 29

poder reductor (tendencia a oxidarse) poder oxidante (tendencia a reducirse) Potenciales estándar de reducción a 298 K http: //www. uam. es/departamentos/ciencias/quimica/aimp/luis/Docencia/QB/Otro_material/Potenciales_estandar_reduccion. htm Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 31

Potenciales estándar de reducción a 298 K Electrodo Semirreacción de reducción Ej. : La batería de zinc-cloro tiene como reacción neta: Zn(s)+Cl 2(g) Zn. Cl 2(ac). ¿Cuánto vale el voltaje o FEM de la pila voltaica estándar a 298 K? Ej. : Semirreacciones, reacción global y voltaje de las pilas estándar cobre-plata y cobre-zinc a 298 K? Red: Ox: Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 32

Relaciones Ecel-ΔG-Keq Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción

Relación Ecel-ΔG • -ΔG es el trabajo que se puede obtener de un proceso a P y T constantes. (Cuando la energía interna se convierte en trabajo, es necesario convertir parte de ella en calor. ) • La carga que circula por una célula electroquímica en la que se transfieren n mol de e-, es: • El trabajo eléctrico que realiza una pila es: • Luego: • Reacción (a P, T ctes) espontánea si ; es decir, si Si una reacción redox tiene Ecel>0 en unas condiciones de concentraciones y temperatura dadas, es espontánea en esas condiciones. Si tiene Ecel<0, la reacción inversa es espontánea en esas condiciones. Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 34
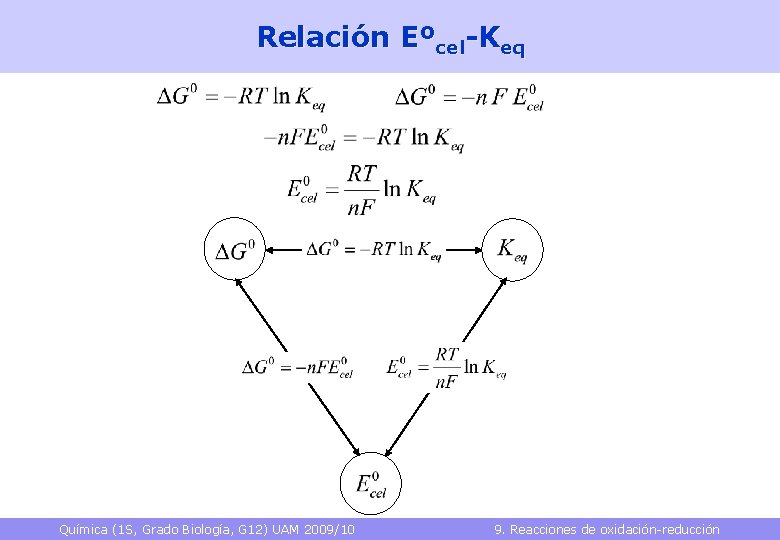
Relación Eºcel-Keq Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 35

Efecto de las concentraciones sobre los potenciales Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción

Ecuación de Nernst Los voltajes de las células electroquímicas de las diapositivas 19 y 21 no coinciden con las diferencias entre los potenciales de reducción estándar (diap. 31). ¿Cómo cambian los potenciales con las concentraciones? Ecuación de Nernst Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 37

Ecuación de Nernst Los voltajes de las células electroquímicas de las diapositivas 19 y 21 no coinciden con las diferencias entre los potenciales de reducción estándar (diap. 27) a 298 K. Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 38
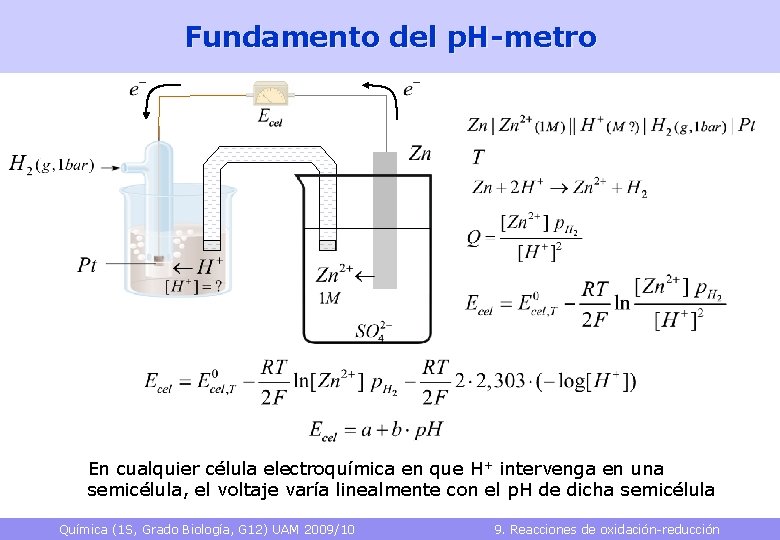
Fundamento del p. H-metro En cualquier célula electroquímica en que H+ intervenga en una semicélula, el voltaje varía linealmente con el p. H de dicha semicélula Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 39
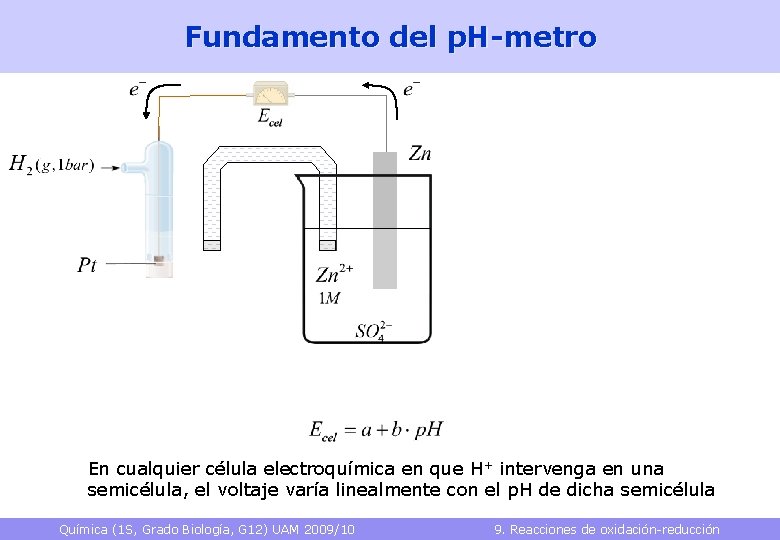
Fundamento del p. H-metro En cualquier célula electroquímica en que H+ intervenga en una semicélula, el voltaje varía linealmente con el p. H de dicha semicélula Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 40
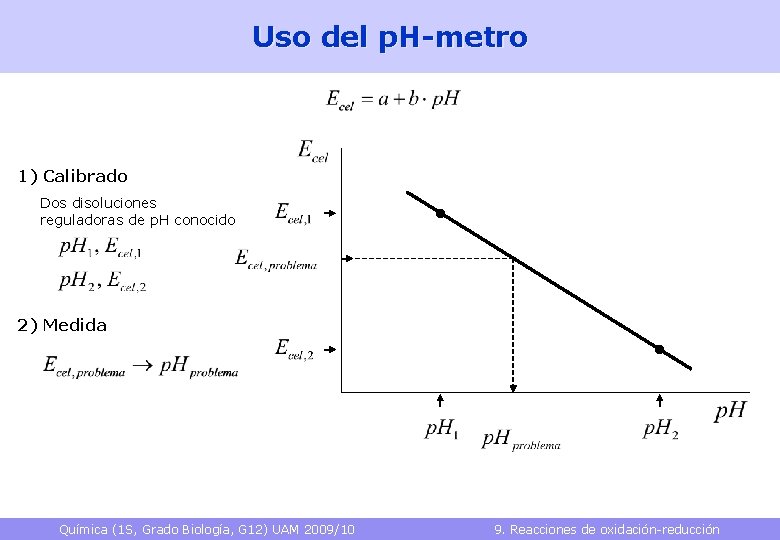
Uso del p. H-metro 1) Calibrado Dos disoluciones reguladoras de p. H conocido 2) Medida Química (1 S, Grado Biología, G 12) UAM 2009/10 9. Reacciones de oxidación-reducción 41
- Slides: 40