OXIDACINREDUCCIN Fernando Carrillo rea de Qumica Inorgnica UCLM











- Slides: 20

OXIDACIÓN-REDUCCIÓN Fernando Carrillo Área de Química Inorgánica UCLM

OXIDACIÓN-REDUCCIÓN TRANSFERENCIA DE ELECTRONES ENTRE ESPECIES QUÍMICAS Ø No existen electrones libres Ø Reductor: cede electrones se oxida Ø Oxidante: acepta electrones se reduce

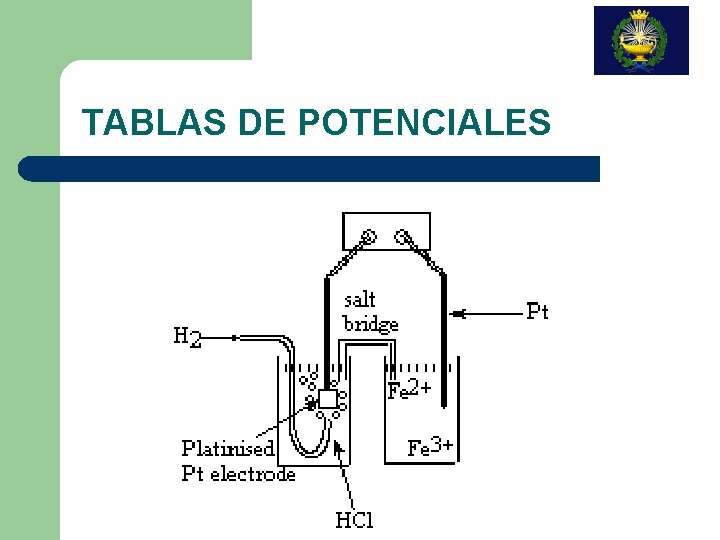
TABLAS DE POTENCIALES Recogen semirreacciones redox Reacción redox: combinación de semirreacciones de oxidación y reducción (de manera formal) e. o. I e. o. 0 2 H+(aq) + 2 ee. o. 0 H 2(g) REDUCCIÓN e. o. II Zn(s) Zn 2+(aq) + 2 e- OXIDACIÓN Zn(s) + 2 H+(aq) Zn 2+(aq) + H 2(g) REDOX Par redox: H+/H 2 Zn 2+/Zn forma ox. / forma red.

TABLAS DE POTENCIALES CONVENIO: SE TABULAN SEMIRREACCIONES DE REDUCCIÓN, DE TAL FORMA QUE UNA REACCIÓN REDOX SE PUEDE EXPRESAR COMO LA DIFERENCIA DE DOS SEMIRREACCIONES DE REDUCCIÓN , DESPUÉS DE IGUALAR EL NÚMERO DE ELECTRONES INTERCAMBIADOS 2 H+(aq) + 2 e- - H 2(g) Zn 2+(aq) + 2 e- Zn(s) + 2 H+(aq) Zn 2+(aq) + H 2(g) REDOX

TABLAS DE POTENCIALES EN TÉRMINOS DE DGo - Ox 1 + ne- Red 1 DGo 1 Ox 2 + ne- Red 2 DGo 2 Ox 1 + Red 2 Red 1 + Ox 2 DGo. T= DGo 1 - DGo 2

TABLAS DE POTENCIALES POR CONVENIO 2 H+(aq) + 2 e- H 2(g) DGo= 0 p(H 2)= 1 atm p. H = 0 (1 M) Por la relación con esta semirreacción (electrodo de hidrógeno) se mide el resto.

TABLAS DE POTENCIALES

TABLAS DE POTENCIALES SE TABULAN SEMIRREACCIONES DE REDUCCIÓN CON SUS POTENCIALES DE REDUCCIÓN. 2 H+(aq) + 2 e- - Zn 2+(aq) + 2 e- Zn(s) + 2 H+(aq) H 2(g) Zn(s) Eo= 0 V a cualquier T Eo=-0. 76 V a 25ºC Zn 2+(aq) + H 2(g) Eo= 0 – (-0. 76)= 0. 76 V DGo=-n. FEo DGo>0 ESPONTÁNEA

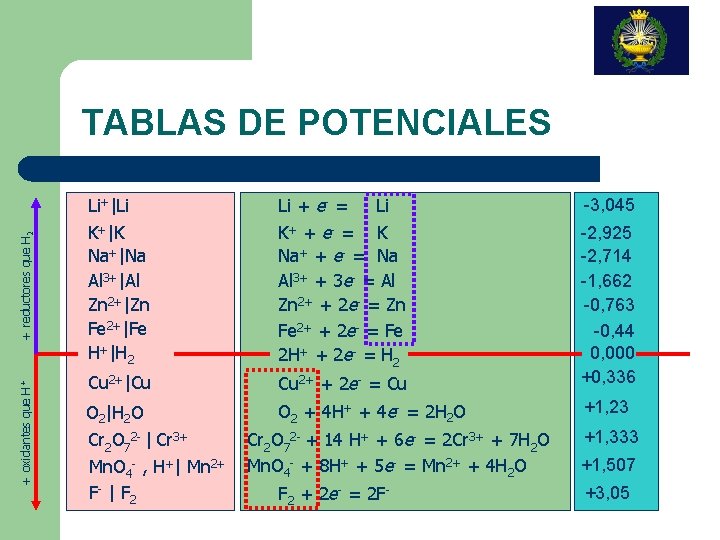
+ oxidantes que H + + reductores que H 2 TABLAS DE POTENCIALES Li+|Li Li + e- = Li -3, 045 K+|K Na+|Na Al 3+|Al Zn 2+|Zn Fe 2+|Fe H+|H 2 K+ + e- = K Na+ + e- = Na Al 3+ + 3 e- = Al Zn 2+ + 2 e- = Zn Fe 2+ + 2 e- = Fe 2 H+ + 2 e- = H 2 Cu 2+|Cu Cu 2+ + 2 e- = Cu -2, 925 -2, 714 -1, 662 -0, 763 -0, 44 0, 000 +0, 336 O 2|H 2 O Cr 2 O 72 - | Cr 3+ Mn. O 4 - , H+| Mn 2+ F- | F 2 O 2 + 4 H+ + 4 e- = 2 H 2 O Cr 2 O 72 - + 14 H+ + 6 e- = 2 Cr 3+ + 7 H 2 O Mn. O 4 - + 8 H+ + 5 e- = Mn 2+ + 4 H 2 O F 2 + 2 e- = 2 F- +1, 23 +1, 333 +1, 507 +3, 05

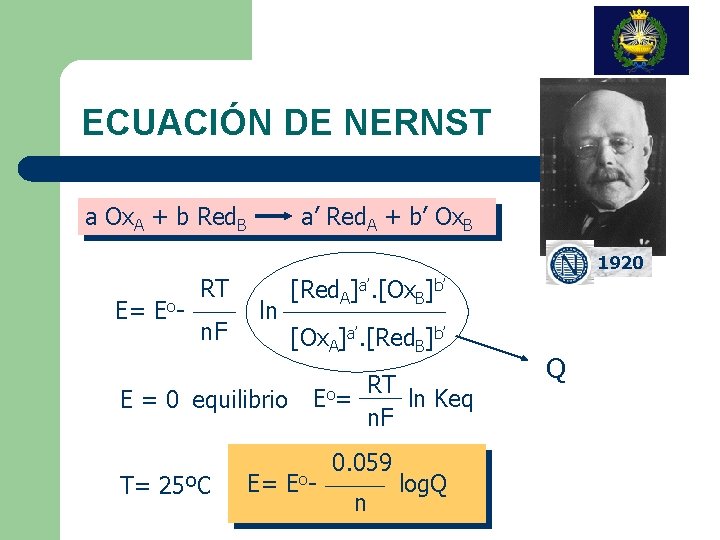
ECUACIÓN DE NERNST a Ox. A + b Red. B a’ Red. A + b’ Ox. B 1920 E= Eo- RT n. F ln E = 0 equilibrio T= 25ºC [Red. A]a’. [Ox. B]b’ [Ox. A]a’. [Red. B]b’ Eo = RT ln Keq n. F 0. 059 E= Eo log. Q n Q

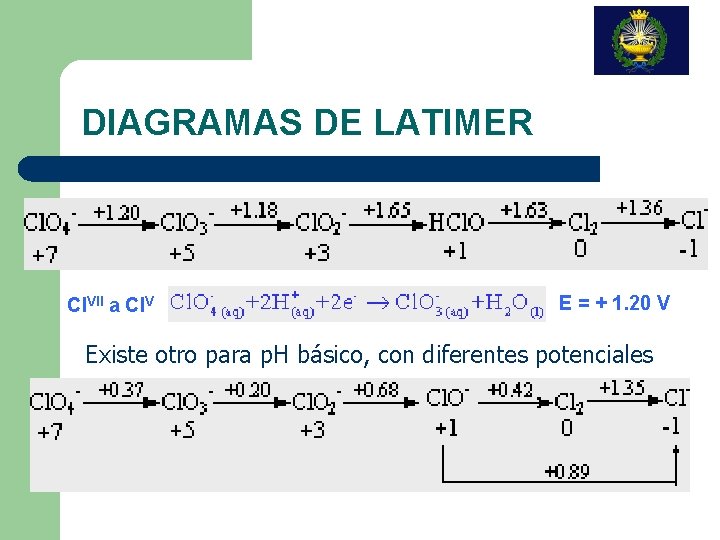
DIAGRAMAS DE LATIMER Cl. VII a Cl. V E = + 1. 20 V Existe otro para p. H básico, con diferentes potenciales

DIAGRAMAS DE LATIMER Calculo de potenciales de reducción para especies no adyacentes del Diagrama de Latimer Consideremos la semirreacción para ir de Cl(+1) a Cl(0): Y la semirreacción para ir de Cl(0) a Cl(-1): El potencial de la semirreacción 1 es: E 1 = +1. 63 V Y el potencial de la semirreacción 2 es: E 2 = +1. 36 V Entonces, la energía libre de la semirreacción 1 ( donde n es el nº de e transferidos = 1) es: DG 1 = -n. FE = -1. 63 F Y para la 2 (n = 1) es: Entonces, la energía libre para la conversión de Cl(+1) a Cl(-1) es: DG 2 = -n. FE = -1. 36 F DG = DG 1 + DG 2 = -2. 99 F Pero la conversión de Cl(+1) a Cl(-1) es una reacción que intercambia 2 electrones. Luego el potencial para la transformación de Cl. O- a Cl- (n = 2) es: DG = -2 FE E = DG/-n. F = -2. 99 F/-2 F = +1. 50 V • DE FORMA GENERAL LA ECUACIÓN QUEDA ASÍ

DESPROPORCIÓN DIAGRAMA DE LATIMER DEL OXÍGENO E 1 = +1. 76 V - E 2 = +0. 70 V E = E 1 - E 2 = +1. 06 V E >0 ENTONCES DG<0 REACCIÓN ESPONTÁNEA

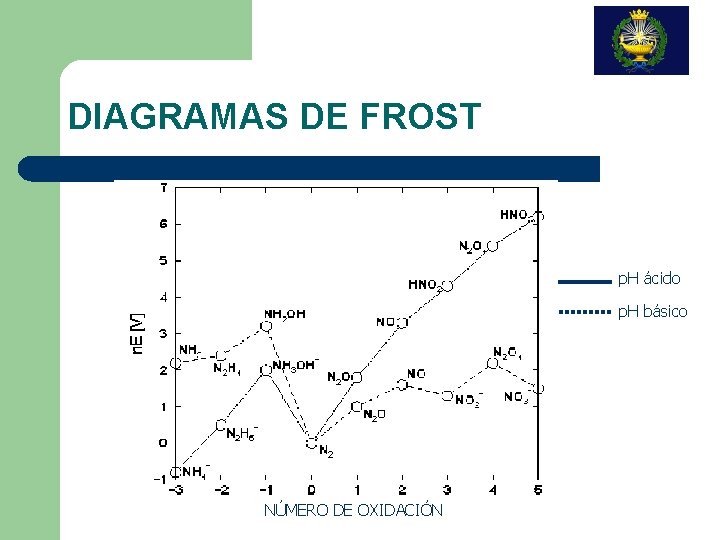
DIAGRAMAS DE FROST p. H ácido p. H básico NÚMERO DE OXIDACIÓN

DIAGRAMAS DE FROST ES OTRA FORMA DE PRESENTAR LOS POTENCIALES DE REDUCCIÓN, PARA VARIOS ESTADOS DE OXIDACIÓN DE UN ELEMENTO. REPRESENTAN n. E FRENTE AL ESTADO OXIDACIÓN N, DONDE E ES EL POTENCIAL REDUCCIÓN DEL PAR X(N)/X(0), Y n ES NÚMERO DE ELECTRONES INTERCAMBIADOS LA CONVERSIÓN DE X(N) A X(0) DE DE EL EN

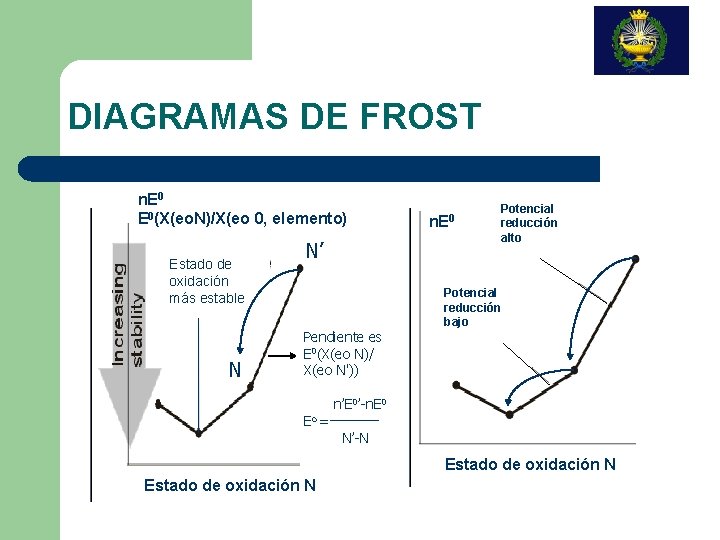
DIAGRAMAS DE FROST n. E 0(X(eo. N)/X(eo 0, elemento) Estado de oxidación más estable N N’ Pendiente es E 0(X(eo N)/ X(eo N')) n. E 0 Potencial reducción alto Potencial reducción bajo n’E 0’-n. E 0 Eo = N’-N Estado de oxidación N

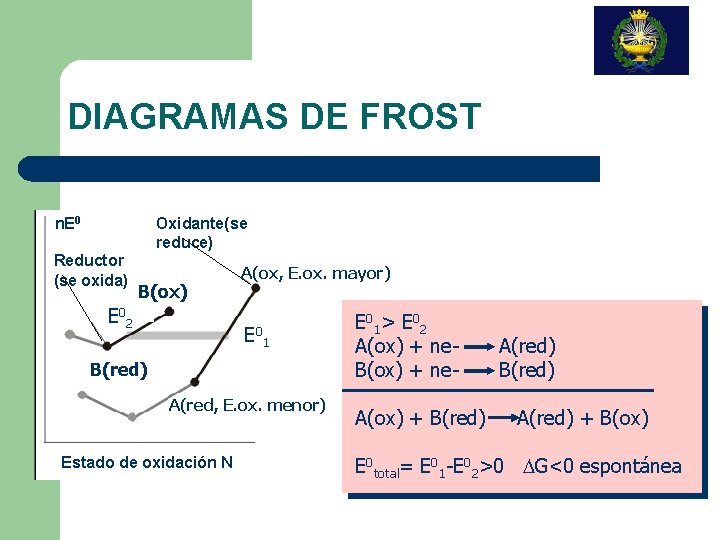
DIAGRAMAS DE FROST Oxidante(se reduce) n. E 0 Reductor (se oxida) B(ox) E 0 2 A(ox, E. ox. mayor) E 0 1 B(red) A(red, E. ox. menor) Estado de oxidación N E 01> E 02 A(ox) + ne. B(ox) + ne- A(red) B(red) A(ox) + B(red) A(red) + B(ox) E 0 total= E 01 -E 02>0 DG<0 espontánea

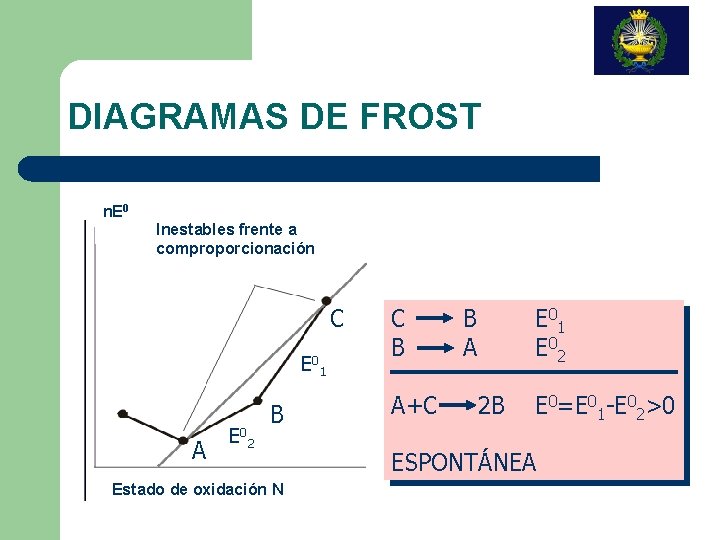
DIAGRAMAS DE FROST n. E 0 Inestables frente a comproporcionación C E 0 1 A E 0 2 B Estado de oxidación N C B B A E 0 1 E 0 2 A+C 2 B E 0=E 01 -E 02>0 ESPONTÁNEA

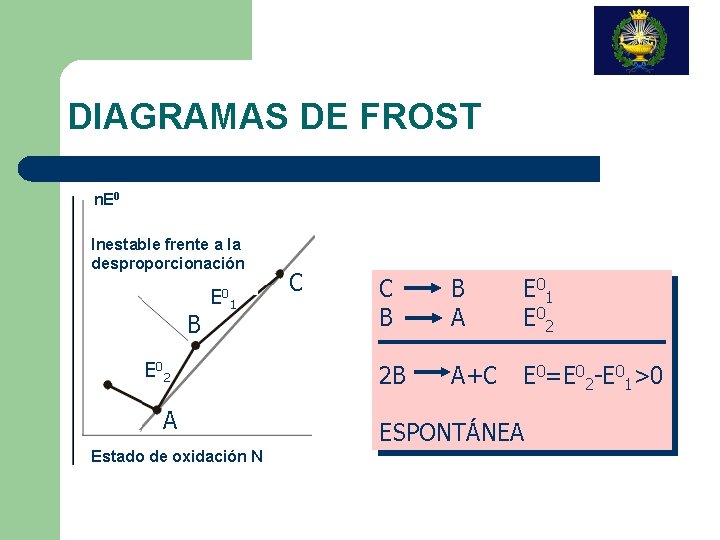
DIAGRAMAS DE FROST n. E 0 Inestable frente a la desproporcionación E 0 B 1 E 0 2 A Estado de oxidación N C C B B A E 0 1 E 0 2 2 B A+C E 0=E 02 -E 01>0 ESPONTÁNEA

DIAGRAMAS DE FROST UN DIAGRAMA DE FROST A MENUDO DA UNA MEJOR IDEA DE LA TERMODINÁMICA DE UNA OXIDACIÓN Y REDUCCIÓN DE UN ELEMENTO, MIENTRAS QUE UN DIAGRAMA DE LATIMER ES MÁS ÚTIL PARA LLEVAR A CABO CÁLCULOS SOBRE EL SISTEMA EN CUESTIÓN.