Reacciones oxidacinreduccin Objetivo Definir conceptos de oxidacin y

Reacciones oxidación-reducción Objetivo: Definir conceptos de oxidación y reducción , relacionarlos con los estados o numero de oxidación.
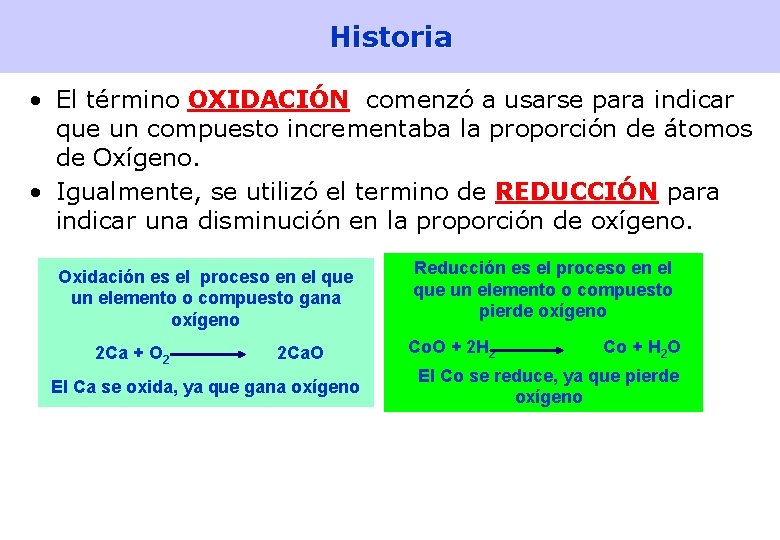
2 Historia • El término OXIDACIÓN comenzó a usarse para indicar que un compuesto incrementaba la proporción de átomos de Oxígeno. • Igualmente, se utilizó el termino de REDUCCIÓN para indicar una disminución en la proporción de oxígeno. Oxidación es el proceso en el que un elemento o compuesto gana oxígeno 2 Ca + O 2 2 Ca. O El Ca se oxida, ya que gana oxígeno Reducción es el proceso en el que un elemento o compuesto pierde oxígeno Co. O + 2 H 2 Co + H 2 O El Co se reduce, ya que pierde oxígeno

3 Definición actual • OXIDACIÓN: Pérdida de electrones (o aumento en el número de oxidación). • Ejemplo: Cu 2+ + 2 e– • REDUCCIÓN: Ganancia de electrones (o disminución en el número de oxidación). • Ejemplo: Ag+ + 1 e– Ag • Siempre que se produce una oxidación debe producirse simultáneamente una reducción. • Cada una de estas reacciones se denomina semirreacción.

Estado de oxidación • Estado de oxidación (o número de oxidación) de un átomo en una molécula – Es un número que se le asigna y que indica de modo aproximado la estructura electrónica de ese átomo en esa molécula – Regla general de asignación de estados de oxidación (e. o. ): • se imagina la situación límite (no real) de que los electrones de un enlace se hayan transferido completamente al átomo más electronegativo del enlace • el estado de oxidación de cada átomo es la carga que tiene tras esta operación mental – e. o. positivo: el átomo pierde total o parcialmente electrones en la molécula respecto al átomo aislado neutro – e. o. negativo: el átomo gana total o parcialmente electrones en la molécula respecto al átomo aislado neutro 4

Estado de oxidación • Reglas básicas de asignación de estados de oxidación: – Los e. o. de los átomos en sus compuestos de determinan aplicando las reglas siguientes, en orden, hasta donde sea necesario: 1. El e. o. de un átomo individual sin combinar químicamente con otros elementos es 0 2. La suma de los e. o. de todos los átomos de una molécula neutra es 0; la de todos los átomos de un ión es la carga del ión 3. En sus compuestos, los metales alcalinos (Grupo 1) tienen e. o. +1 y los alcalinotérreos (Grupo 2) tienen e. o. +2 4. En sus compuestos, el e. o. del F es -1 5. En sus compuestos, el e. o. del H es +1 6. En sus compuestos, el e. o. del O es -2 7. En sus compuestos binarios con metales, los elemetos del Grupo 17 (F, Cl, . . . ) tienen e. o. -1, los del Grupo 16 (O, S, . . . ) tienen e. o. -2, y los del Grupo 15 (N, P, . . . ) tienen e. o. -3

6 Cálculo de estado de oxidación (E. O. ). • La suma de los E. O. de una molécula neutra es siempre 0. • Ejemplo: • Calcular el E. O. del S en Zn. SO 4 E. O. (Zn) = +2; E. O. (O) = – 2; +2 + E. O. (S) + 4 · (– 2) = 0 E. O. (S) = +6 • Si se trata de un ion monoatómico es igual a su carga.

Ejemplos de cálculo de estados de oxidación (E. O. ). 7 • CO 2 : el átomo de C forma dos enlaces covalentes con dos átomos de O más electronegativo que él. Comparte los 4 e– , pero para saber cuales son los E. O. hay que suponer que el C los pierde, y que el O los gana, con lo cual la carga que tendría el C sería “+4” y la del O “– 2” E. O. (C) = +4; E. O. (O) = – 2.

Estado de oxidación Ejercicios: calcular los estados de oxidación de los siguientes compuestos. 8

9 Ejemplo: Cu +Ag. NO 3 • Introducimos un electrodo de cobre en una disolución de Ag. NO 3, • De manera espontánea el cobre se oxidará pasando a la disolución como Cu 2+. • Mientras que la Ag+ de la misma se reducirá pasando a ser plata metálica: • a) Cu 2+ + 2 e– (oxidación) • b) Ag+ + 1 e– Ag (reducción). Imagen cedida por © Grupo ANAYA S. A. Química 2º de bachillerrato

Oxidación, reducción y reacción de oxidación-reducción o redox • Oxidación: – aumento del e. o. o pérdida de electrones • Reducción: – disminución del e. o. o ganancia de electrones • Reacción redox o de oxidación-reducción: – reacción de transferencia de electrones, en la que algunos elementos se oxidan y otros se reducen • Oxidante: – reactivo que gana electrones y se reduce • Reductor: – reactivo que cede electrones y se oxida 10

Oxidación, reducción y reacción de oxidación-reducción o redox gana electrones y se reduce de +3 a 0 pierde electrones y se oxida de +2 a +4 es el oxidante es el reductor se reduce a se oxida a gana electrones y se reduce de +1 a 0 pierde electrones y se oxida de 0 a +2 es el oxidante es el reductor se reduce a se oxida a 11

Oxidación, reducción y reacción de oxidación-reducción o redox : (coenzima de función metabólica) dinucleótido de nicotinamida-adenina : forma oxidada del : forma reducida del gana electrones y se reduce de +1 a -1 pierde electrones y se oxida de -2 a 0 es el oxidante es el reductor se reduce a se oxida a 12

Semirreacciones • Semirreacciones de reducción y de oxidación: – cada una de las dos partes en que se separa una reacción redox y en las que se aíslan la reducción (ganancia de e-) y la oxidación (pérdida de e-) Reacción redox global semirreacción de reducción semirreacción de oxidación 13

Ajustes de reacciones redox • Método del ión-electrón 1. Descomponer los compuestos en sus iones –los que se formarían en disolución acuosa-. 2. Identificar elementos que cambian su número de oxidación y escribir semirreacciones iónicas de oxidación y de reducción. 3. Ajustar las semirreacciones como si éstas tuviesen lugar en medio ácido, con la ayuda de H+ y de H 2 O. 1. 2. 3. 4. Ajustar los átomos que no sean H ni O los O, utilizando H 2 O los H, utilizando H+ la carga utilizando e- 4. Sumar las semirreacciones ponderadas de modo que se equilibre el número de electrones. 1. Los H+ y H 2 O auxiliares se eliminarán automáticamente en este paso. 5. Completar la reacción con los compuestos o iones que no participan en las oxidaciones y reducciones. 6. Obtener los compuestos que se habían disociado en iones en el paso 1. a partir de esos mismos iones 14

15 Etapas en el ajuste redox Ejemplo: Zn + Ag. NO 3 Zn(NO 3)2 + Ag • Primera: Identificar los átomos que cambian su E. O. Zn(0) Zn(+2); Ag (+1) Ag (0) • Segunda: Escribir semirreacciones con moléculas o iones que existan realmente en disolución ajustando el nº de átomos: (Zn, Ag+, NO 3–, Zn 2+, Ag) Oxidación: Zn 2+ + 2 e– Reducción: Ag+ + 1 e– Ag

16 Etapas en el ajuste redox (cont). • Tercera: Ajustar el nº de electrones de forma que al sumar las dos semirreacciones, éstos desaparezcan. En el ejemplo se consigue multiplicando la segunda semirreacción por 2. Oxidación: Zn 2+ + 2 e– Reducción: 2 Ag+ + 2 e– 2 Ag R. global: Zn + 2 Ag+ + 2 e– Zn 2+ + 2 Ag + 2 e–

17 Etapas en el ajuste redox (cont). • Cuarta: Escribir la reacción química completa utilizando los coeficientes hallados y añadiendo las moléculas o iones que no intervienen directamente en la reacción redox (en el el ejemplo, el ion NO 3–) y comprobando que toda la reacción queda ajustada: Zn + 2 Ag. NO 3 Zn(NO 3)2 + 2 Ag

18 Ajuste de reacciones en disolución acuosa ácida o básica. • Si en una disolución aparecen iones poliatómicos con O (ej SO 42–), el ajuste se complica pues aparecen también iones H+, OH– y moléculas de H 2 O. • En medio ácido: – Los átomos de O que se pierdan en la reducción van a parar al agua (los que se ganen en la oxidación provienen del agua). – Los átomos de H provienen del ácido. • En medio básico: – Los átomos de O que se ganan en la oxidación (o pierdan en la reducción) provienen de los OH–, necesitándose tantas moléculas de H 2 O como átomos de oxígeno se ganen o pierdan.

Ajustes de reacciones redox globales Ejemplo: 1. 2+3. 3. 2 3. 3 3. 4 4. 19

Ajustes de reacciones redox globales 5. 6. 20
- Slides: 20