Unidad 5 Reacciones de oxidacinreduccin 1 Reacciones de
















- Slides: 25

Unidad 5 Reacciones de oxidaciónreducción

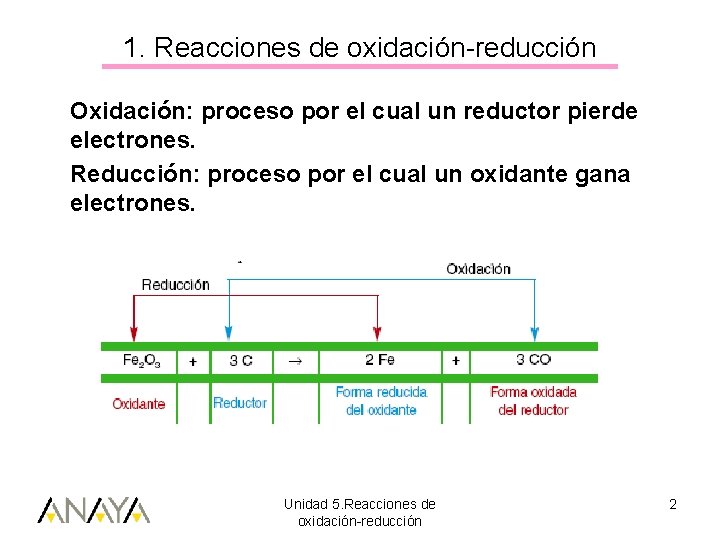
1. Reacciones de oxidación-reducción Oxidación: proceso por el cual un reductor pierde electrones. Reducción: proceso por el cual un oxidante gana electrones. Unidad 5. Reacciones de oxidación-reducción 2

2. Número de oxidación: número de cargas eléctricas que tendría un átomo de un compuesto si se asignasen los electrones del enlace al átomo más electronegativo. Unidad 5. Reacciones de oxidación- 3

3. Ajuste de ecuaciones redox. Método del ion-electrón Unidad 5. Reacciones de oxidación-reducción 4

3. Ajuste de ecuaciones redox. Método del ion-electrón Unidad 5. Reacciones de oxidación-reducción 5

3. Ajuste de ecuaciones redox. Método del ion-electrón Unidad 5. Reacciones de oxidación-reducción 6

3. Ajuste de ecuaciones redox. Método del ion-electrón Unidad 5. Reacciones de oxidación-reducción 7

3. Ajuste de ecuaciones redox. Método del ion-electrón Unidad 5. Reacciones de oxidación-reducción 8

3. Ajuste de ecuaciones redox. Método del ion-electrón Unidad 5. Reacciones de oxidación-reducción 9

3. Ajuste de ecuaciones redox. Método del ion-electrón Unidad 5. Reacciones de oxidación-reducción 10

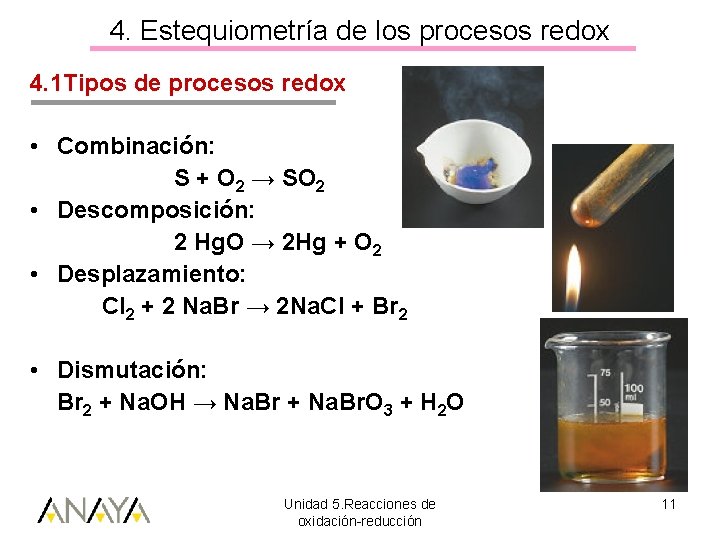
4. Estequiometría de los procesos redox 4. 1 Tipos de procesos redox • Combinación: S + O 2 → SO 2 • Descomposición: 2 Hg. O → 2 Hg + O 2 • Desplazamiento: Cl 2 + 2 Na. Br → 2 Na. Cl + Br 2 • Dismutación: Br 2 + Na. OH → Na. Br + Na. Br. O 3 + H 2 O Unidad 5. Reacciones de oxidación-reducción 11

4. Estequiometría de los procesos redox 4. 2 Valoraciones • Masa equivalente: masa de una sustancia que reacciona o produce un mol de eeq(gramos)= Mm/ nº e • En valoraciones tendremos en cuenta que nº eq oxidante= nº eq reductor 2 Hg. O → 2 Hg + O 2 • Indicadores redox: sustancias que detectan el cambio del potencial de disolución • En general ajustaremos la reacción y realizaremos los cálculos estequiométricos pertinentes Unidad 5. Reacciones de oxidación-reducción 12

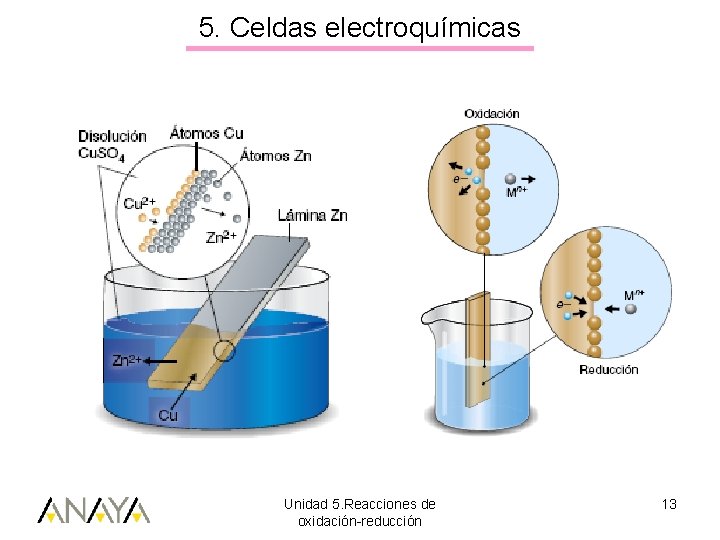
5. Celdas electroquímicas Unidad 5. Reacciones de oxidación-reducción 13

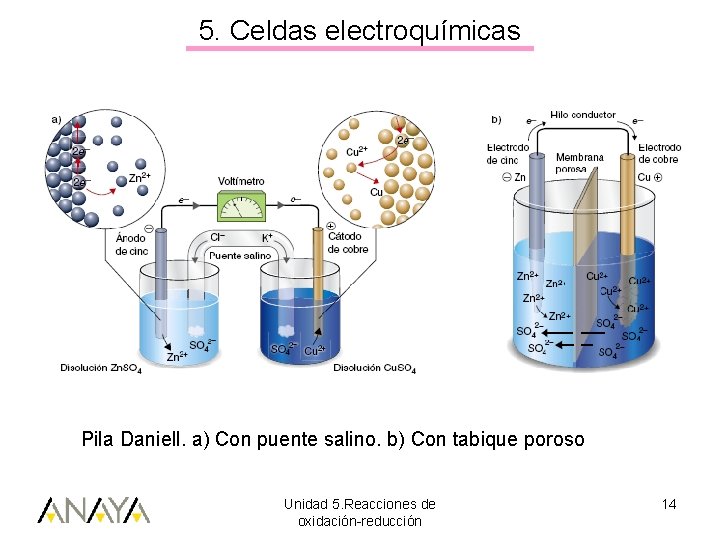
5. Celdas electroquímicas Pila Daniell. a) Con puente salino. b) Con tabique poroso Unidad 5. Reacciones de oxidación-reducción 14

5. Celdas electroquímicas 5. 1 Definición: Permite obtener corriente eléctrica a partir de redox espontánea 5. 2 Partes de una celda • Electrodos ánodo oxidación – cátodo reducción + • Hilo conductor • Sistema que separa las celdas: Tabique poroso o puente salino Permite obtener corriente eléctrica a partir de redox espontánea Unidad 5. Reacciones de oxidación-reducción 15

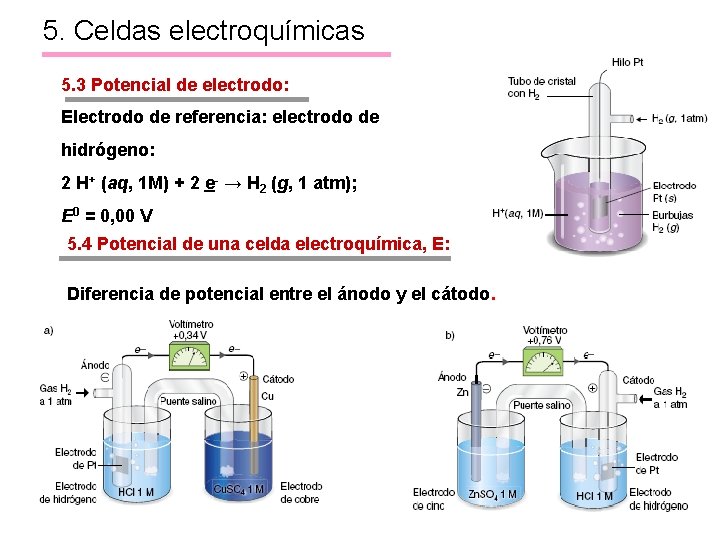
5. Celdas electroquímicas 5. 3 Potencial de electrodo: Electrodo de referencia: electrodo de hidrógeno: 2 H+ (aq, 1 M) + 2 e- → H 2 (g, 1 atm); E 0 = 0, 00 V 5. 4 Potencial de una celda electroquímica, E: Diferencia de potencial entre el ánodo y el cátodo. 16

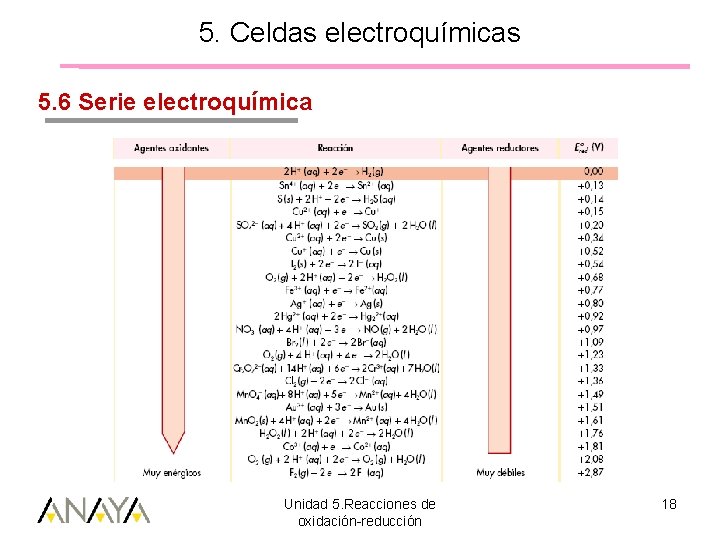
5. Celdas electroquímicas 5. 6 Serie electroquímica Unidad 5. Reacciones de oxidación-reducción 17

5. Celdas electroquímicas 5. 6 Serie electroquímica Unidad 5. Reacciones de oxidación-reducción 18

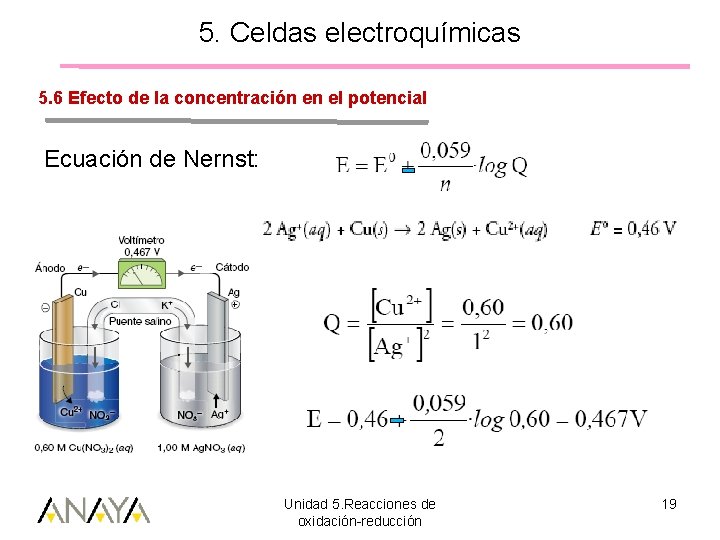
5. Celdas electroquímicas 5. 6 Efecto de la concentración en el potencial Ecuación de Nernst: Unidad 5. Reacciones de oxidación-reducción 19

5. Celdas electroquímicas 5. 7 Espontaneidad de una reacción redox Una reacción es espontánea si su potencial es positivo �� G = - n · F · Ecelda Unidad 5. Reacciones de oxidación-reducción 20

6. Electrólisis 6. 1 Concepto: Se produce una reacción química a partir de energía eléctrica 6. 2 Diferencias con la pila Daniell: Unidad 5. Reacciones de oxidación-reducción 21

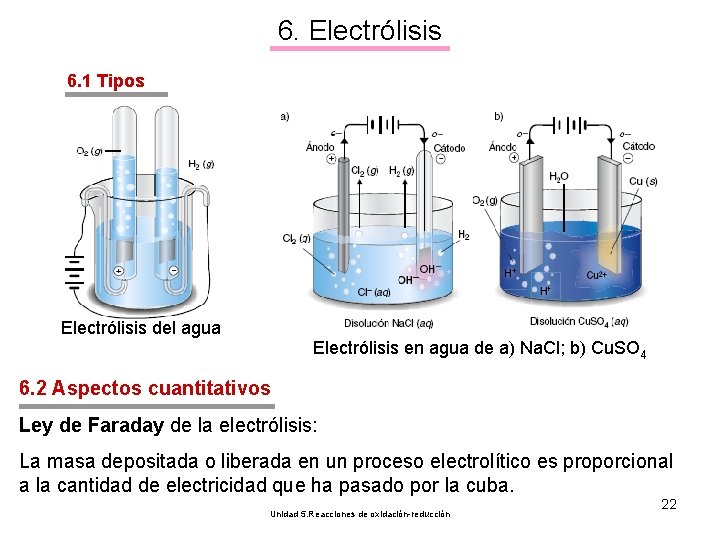
6. Electrólisis 6. 1 Tipos Electrólisis del agua Electrólisis en agua de a) Na. Cl; b) Cu. SO 4 6. 2 Aspectos cuantitativos Ley de Faraday de la electrólisis: La masa depositada o liberada en un proceso electrolítico es proporcional a la cantidad de electricidad que ha pasado por la cuba. Unidad 5. Reacciones de oxidación-reducción 22

6. Electrólisis 6. 2 Aspectos cuantitativos Ley de Faraday de la electrólisis: La masa depositada o liberada en un proceso electrolítico es proporcional a la cantidad de electricidad que ha pasado por la cuba. 1, 6022· 10 -19 C/e- x 6, 0022· 1023 e-/mol = 96485 C· /mol (carga de un mol de electrones= Faraday) Para una misma cantidad de electricidad que pase por varias cubas conectadas en serie, las masas depositadas o liberadas en los electrodos son proporcionales a sus respectivos equivalentes químicos, es decir que 1 F deposita o libera un equivalente de sustancia q=I·t q= cantidad de electricidad t= tiempo I= intensidad de corriente Unidad 5. Reacciones de oxidación-reducción 23

6. Electrólisis 6. 2 Aspectos cuantitativos Ley de Faraday de la electrólisis: El esquema del cálculo se puede resumir del siguiente modo I t q 1/F ne 1/z n metal Mm m metal En la reacción de reducción del ion Cu 2+: Cu 2+ (aq) +2 e- Cu(s) Se necesitan 2 mol de electrones para que se deposite 1 mol de átomos de Cu nmetal = ne/z La cantidad de electrones, ne que circula se puede determinar a partir de la carga eléctrica, Q y de la cte de Faraday, F, que es la carga por mol de electrones n e = q/F Y la carga eléctrica, q, se calcula a través de la intensidad de corriente (I) y el 24 tiempo(t) durante el cual circula. q = I·t

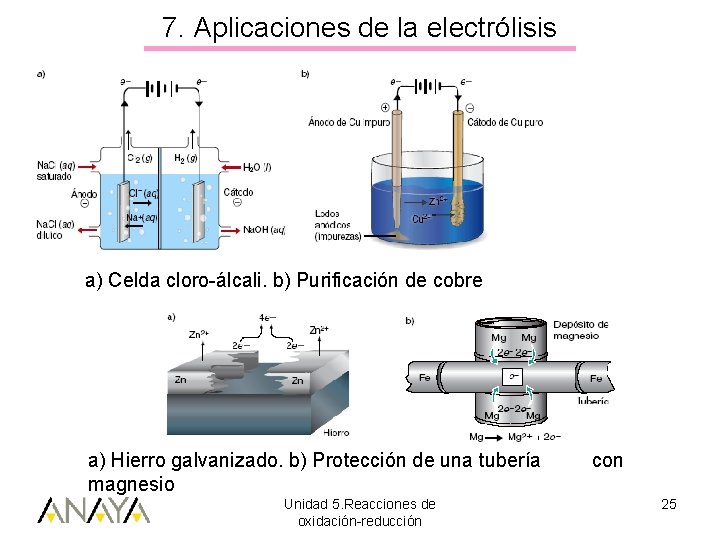
7. Aplicaciones de la electrólisis a) Celda cloro-álcali. b) Purificación de cobre a) Hierro galvanizado. b) Protección de una tubería magnesio Unidad 5. Reacciones de oxidación-reducción con 25