QUELS VACCINS pour QUELS VOYAGEURS Dr Eric GARNOTEL
















































































- Slides: 107

QUELS VACCINS pour QUELS VOYAGEURS ? Dr Eric GARNOTEL HIA Laveran CEU Médecine des voyages Avril 2009

VACCIN « IDEAL » OMS • Contient tous les Ag spécifiques des principales maladies infectieuses • administré en 1 fois par voie orale chez le nourrisson • parfaitement immunogène • réalité…. .

PRISE EN CHARGE DU VOYAGEUR • Insuffisance de la couverture vaccinale – – – Obrecht , 1987 64 à 98% pour la fièvre jaune Fisch , 1994 46 -56% pour la poliomyélite Steiger, 1989 71 -87% pour le tétanos 37% pour la diphtérie 54% pour l ’hépatite A (Picot, 1995) 11% pour l ’hépatite B

TYPES DE VACCINS • ATTENUES (vivants) viraux : Polio oral ROR Fièvre jaune bactériens : B. C. G • INACTIVES – hépatite A – coqueluche entier – polio injectable – rage

TYPES DE VACCINS • FRACTIONS ANTIGENIQUES – Polysaccharides : – Typhoïde – Méningo A+C……. . – Pneumocoque, Hib – Protéiques: – anatoxine tétanique – anatoxine diphtérique • RECOMBINANTS Hépatite B (Ag HBs)

ASSOCIATION VACCINALE • La vaccination combinée : – les vaccins sont mélangés dans la même seringue. • Les vaccinations simultanées : – les vaccins sont injectés au même moment dans des sites différents ou par des voies différentes.

ASSOCIATION VACCINALE • Un vaccin inactivé peut être associé à d'autres vaccins inactivés ou vivants atténués, de façon simultanée ou à n'importe quel intervalle. • Un vaccin vivant atténué peut être associé à d'autres vaccins vivants atténués, de façon simultanée le même jour, sinon un intervalle minimum de 4 semaines doit être respecté entre les deux vaccins.

VOIE D ’INJECTION • 2 éléments guident le choix : tolérance et immunogénicité : – Tolérance : • Vaccins adsorbés sur hydroxyde d ’aluminium : Tetracoq, hépatites A, B + fréquemment réactions locales avec possibilité granulomes, nodules d ’où préférer IM ou sous cutanée profonde

VOIE D ’INJECTION – Tolérance : • Vaccins non-adsorbés : virus vivants atténués (ROR, varicelle, fièvre jaune) , virus inactivés (polio inj, grippal), polysaccharides capsulaires (Hib, pneumocoque, méningocoque, typhoïde) bien tolérés s/s cut ou IM. - Immunogénicité : préférer la voie IM deltoïdienne (hépatite B, grippe, rage - Précautions : Thrombocytopéniques, hémophiles, anticoagulants : préférer la voie s/s cut

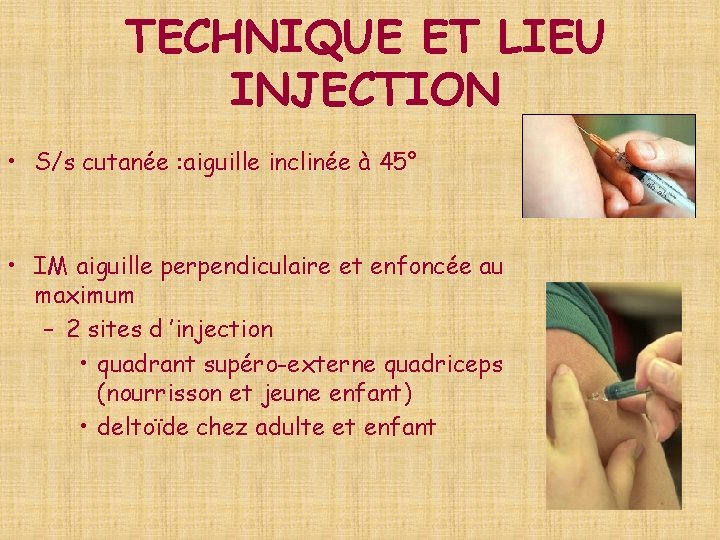
TECHNIQUE ET LIEU INJECTION • S/s cutanée : aiguille inclinée à 45° • IM aiguille perpendiculaire et enfoncée au maximum – 2 sites d ’injection • quadrant supéro-externe quadriceps (nourrisson et jeune enfant) • deltoïde chez adulte et enfant

Comment entretenir l’immunité induite par les vaccins ? • Pour certains agents infectieux : se fait de manière naturelle, mais du nb d’inf. lié à de la couverture ou des conditions d’hygiène : risque en pré éradication (coqueluche) • Pour d’autres : doit être entretenue (tétanos, voyageurs et diphtérie)

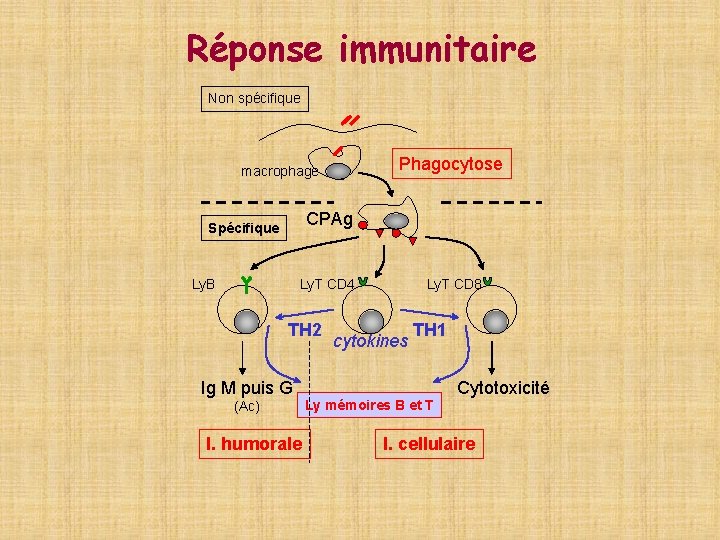
Réponse immunitaire Non spécifique Phagocytose macrophage CPAg Spécifique Ly. B Ly. T CD 4 TH 2 Ig M puis G (Ac) I. humorale Ly. T CD 8 cytokines TH 1 Ly mémoires B et T Cytotoxicité I. cellulaire

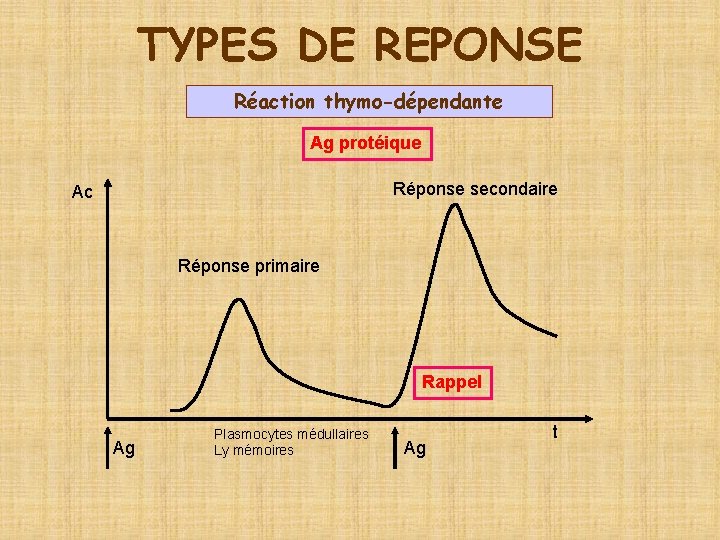
TYPES DE REPONSE Réaction thymo-dépendante Ag protéique Réponse secondaire Ac Réponse primaire Rappel Ag Plasmocytes médullaires Ly mémoires Ag t

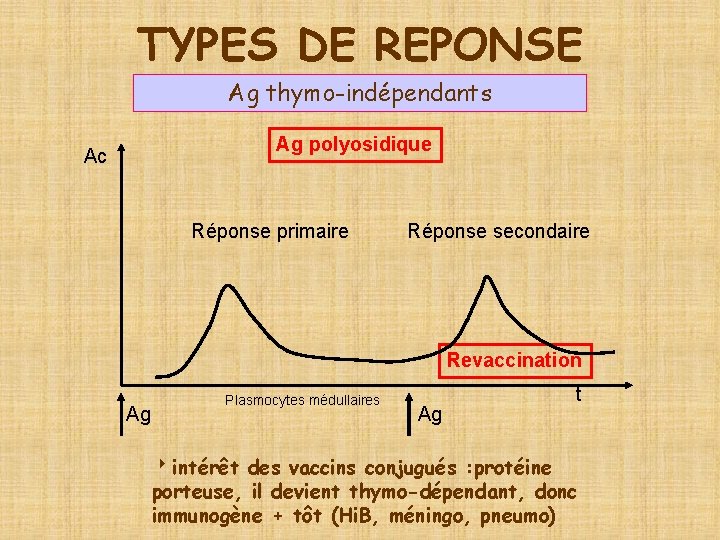
TYPES DE REPONSE Ag thymo-indépendants Ag polyosidique Ac Réponse primaire Réponse secondaire Revaccination Ag Plasmocytes médullaires Ag t 8 intérêt des vaccins conjugués : protéine porteuse, il devient thymo-dépendant, donc immunogène + tôt (Hi. B, méningo, pneumo)

Choix ? Statut vaccinal Pays visité Durée du séjour Type de voyage Contexte pathologique Temps disponible Budget

VACCINS INDISPENSABLES (inscrits au calendrier vaccinal) Tétanos Poliomyélite Diphtérie

TETANOS • Couverture primo-vaccinale antitétanique de l ’enfant élevée en Europe • Rappels rarement effectués chez l ’adulte : 17 -28 cas de tétanos/an, âge moyen de 78 ans (femmes) • Couverture vaccinale des plus de 60 ans <50% • Consultation du voyageur : c ’est l ’occasion!! • Permet d ’éviter un recours aux Ig • Vaccins monovalents ou combinés

TETANOS • Vaccin = anatoxine = toxine modifiée le formol • Plusieurs vaccins et combinaisons disponibles • Revaxis ®: vaccin combiné de l'adulte, en rappel d'une vaccination antérieure, pour la prévention conjointe de la diphtérie, du tétanos et de la poliomyélite. • 10 ans

TETANOS • Repevax®, Boostrixtetra®: vaccin combiné de l'adulte susceptible de devenir parents , en rappel d'une vaccination antérieure, pour la prévention conjointe de la diphtérie, du tétanos, de la poliomyélite et de la coqueluche.

Polyomyélite • Couverture vaccinale pays européens 92% • France/Pays-Bas/Finlande /Suède utilisation du vaccin injectable • France : absence de cas depuis 1990 • Nigeria-Inde : réservoir

POLIOMYELITE • 2 vaccins disponibles : – injectable (Salk) – Oral (Sabin) : OMS • Vaccin trivalent (sérotype 1, 2, 3) • Primovaccination : 3 doses à un mois d'intervalle • Rappel : 1 an après la 3ème inj. puis à tous les 5 ans puis tous les 10 ans • Primovaccination des adultes : 2 inj puis rappel à 612 mois puis tous les 10 ans

Diphtérie • Corynebacterium diphtheriae toxinogène • Transmission interhumaine stricte par voie respiratoire • Angine à fausses membranes, complications neurologiques cardiaques. • Pas de cas en France : 1945 – 45 541 cas, depuis 1979 – moins de 10 cas/an, 1990 -2007 10 cas

DIPHTERIE • Ex URSS, 1995 : 50 425 cas et 1700 décès • Pays de l ’Est : 100 000 cas en 5 ans • Actuellement diminution : 145 cas en 2007 en UE • risque potentiel pour une population française dont l ’immunité est déclinante • Un cas mortel chez un enfant voyageant au Népal en 1997 • Étude: protection insuffisante de l’adulte à partir de 35 ans.

DIPHTERIE • Revaccination : vaccin 1/10 de la valence • vaccins disponibles 1/10 valence : Revaxis® (+ tétanos + polyomyélite ) tous les 10 ans, Repevax®, Boostrixtetra® (+ coqueluche acellulaire) • Rappel tous les 10 ans recommandé (CSHPF, 2005) • Protègent contre la toxine • Ne protègent pas contre la circulation bactérienne

VACCINS OBLIGATOIRES Fièvre jaune Infections invasives à méningocoques (Arabie Saoudite)

Fièvre jaune • Arbovirose due au virus amaril transmis à l ’homme par un moustique hématophage du genre Aedes • Maladie dont la vaccination donne lieu à l ’établissement d ’un carnet international de vaccination par un centre agréé • centre agréé : vaccin thermostable? + carnet


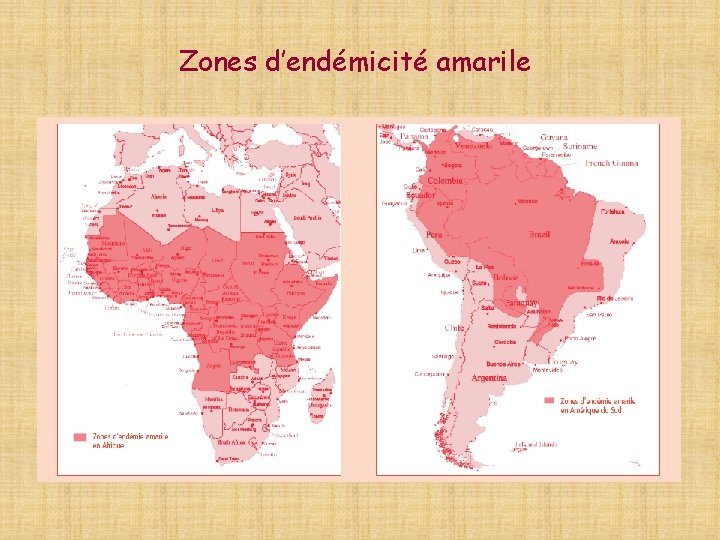
Zones d’endémicité amarile

La maladie est due au virus de la fièvre jaune, ou virus amaril, qui appartient au groupe des flavivirus Après une incubation silencieuse de 3 à 6 jours, la maladie évolue en deux phases : - phase aiguë (ou phase rouge) (3 à 4 jours): fièvre, myalgies, céphalées, congestion de la face. - phase jaune pour 15% des malades avec ictère, vomissements, hémorragies, insuffisance rénale. Létalité de 20 à 50%

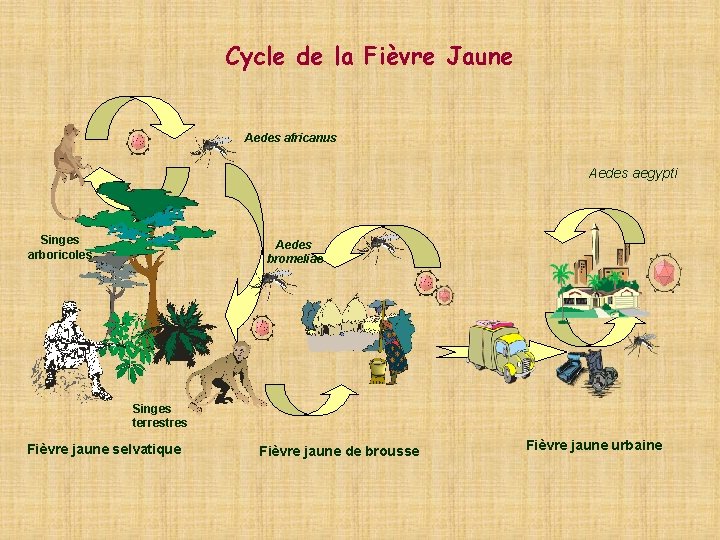
La transmission L'infection touche principalement l'homme et le singe La virus va alors être transmis d’un vertébré à l’autre par la piqûre d’un moustique genre Aedes : Afrique. genre Haemagogus : Amérique du Sud.

Cycle de la Fièvre Jaune Aedes africanus Aedes aegypti Singes arboricoles Aedes bromeliae Singes terrestres Fièvre jaune selvatique Fièvre jaune de brousse Fièvre jaune urbaine

LE VACCIN 1940: Vaccin Dakar (FNV) arrêté en 1960 J. LAIGRET Vaccin Rockefeller 17 D M. THEILER « vivant » atténué par passage sur œufs embryonnés + stabilisant: relative stabilité du lyophilisat STAMARIL® Sanofi Pasteur MSD

Flacon de poudre + seringue préremplie de 0, 5 ml de solvant munie d'un bouchon. Flacon monodose ou multidose

Conservation: +4°C Ne pas congeler Après reconstitution : 3 H sur glace 1 H à T° ambiante Peut être transporté par une équipe de vaccination en glacière ou en porte-vaccins avec des accumulateurs de froid.

Immunité : - >95% - en 10 jours - > 10 ans Le schéma de vaccination est le même chez l'enfant > 6 mois et chez l'adulte. Rappel tous les 10 ans, la protection est alors immédiate.

ASSOCIATION VACCINALE Possible le même jour, dans un site différent: DT, VPI, VPO, BCG, VHB, VHA, Rougeole L’association avec un autre vaccin vivant doit se faire le même jour, sinon un délai de 1 mois est nécessaire

CONTRE-INDICATIONS • C. I chez enfant < 6 mois (+ sensible aux cpc encéphalitiques) • Vaccin à virus vivant donc : – C. I quand déficit de l’immunité cellulaire quelle qu’en soit la cause

VIH • CI: Taux de CD 4 < 200/mm 3 Charge virale plasmatique élevée Traitement par immunosuppresseurs • Corticothérapie CI sauf si : –< 2 semaines –Dose <20 mg/j –Hormonothérapie substitutive –Corticothérapie locale ou inhalée –Injection articulaire • Attendre au moins 3 mois après l’arrêt de la corticothérapie pour vacciner • C. I chimiothérapie/ radiothérapie

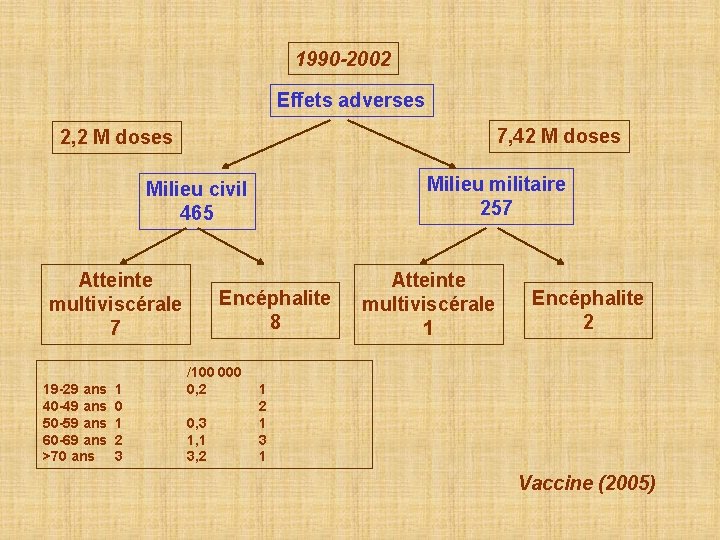
EFFETS INDÉSIRABLES données classiques ØRéactions locales au point d’injection ØDans 2 à 5% des cas du 4ème au 7ème jour: fièvre, fatigue, céphalées, myalgies ØLes réactions allergiques (éruptions cutanées, urticaire, asthme) sont très rares (gélatine) estimation 1/100 000) ØEncéphalites post-vaccinales : <1/8 millions

1990 -2002 Effets adverses 7, 42 M doses 2, 2 M doses Milieu militaire 257 Milieu civil 465 Atteinte multiviscérale 7 19 -29 ans 40 -49 ans 50 -59 ans 60 -69 ans >70 ans 1 0 1 2 3 Encéphalite 8 /100 0, 2 0, 3 1, 1 3, 2 Atteinte multiviscérale 1 Encéphalite 2 1 3 1 Vaccine (2005)

EFFETS INDÉSIRABLES données récentes ØSyndrome multiviscéral (YEL-AVD) üFDR : pathologie thymique ü 3 cas/million de doses ØMoins bonne tolérance chez les sujets >65 ans: précautions particulières (AMM Stamaril 2002) évaluation individuelle, dosage Ac anti. FJ.

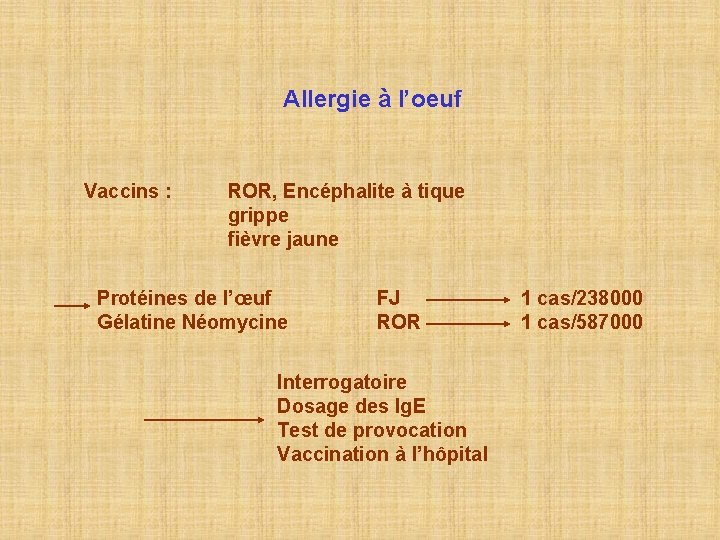
Allergie à l’oeuf Vaccins : ROR, Encéphalite à tique grippe fièvre jaune Protéines de l’œuf Gélatine Néomycine FJ ROR Interrogatoire Dosage des Ig. E Test de provocation Vaccination à l’hôpital 1 cas/238000 1 cas/587000

TERRAINS PARTICULIERS GROSSESSE : Le vaccin est déconseillé pendant la grossesse mais à faire en cas de voyage « obligé » en zone d’endémie ALLAITEMENT : La vaccination contre la fièvre jaune est à éviter (risque théorique du passage du virus par le lait) mais peut être réalisée si l’exposition au risque l’exige. ENFANT : CI si < 6 mois mais déconseillée entre 6 et 9 mois

En cas de contre indication à la vaccination : pensez à fournir au patient un certificat médical de contre-indication

A REPORTER EN CAS DE Ø fièvre Ø maladies aiguës Ø maladies chroniques évolutives ou en poussée

VACCIN NON INDIQUE • Cholera

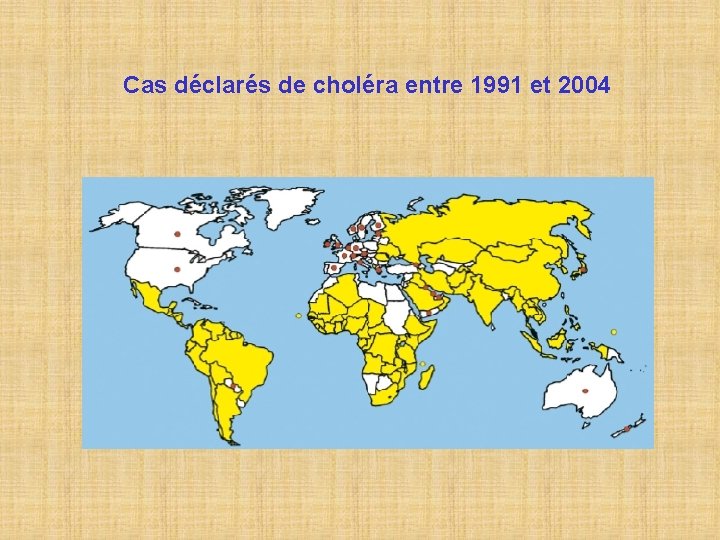
Choléra Importance du choléra dans le monde 2006 : 237 000 cas, 52 pays létalité de 2, 66% (1 -9%) Afrique : 99% des cas importés : 100 cas Sous déclaration : manque de moyens définition des cas (clinique, isolement) craintes de sanctions: tourisme commerce

Cas déclarés de choléra entre 1991 et 2004

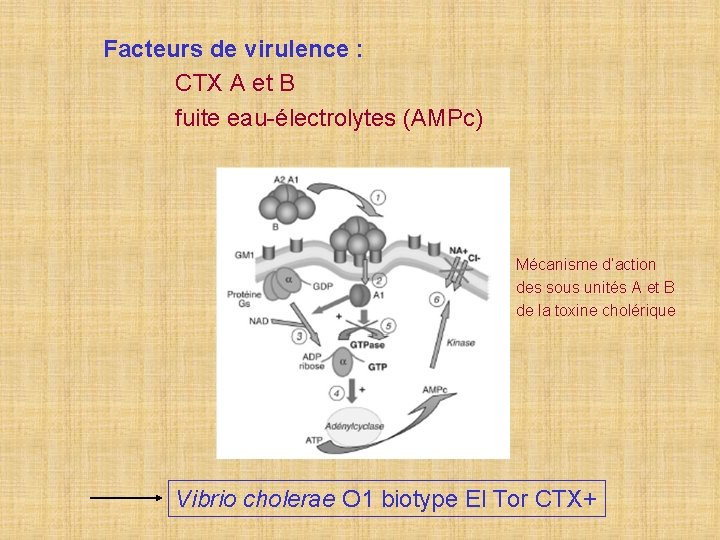
Facteurs de virulence : CTX A et B fuite eau-électrolytes (AMPc) Mécanisme d’action des sous unités A et B de la toxine cholérique Vibrio cholerae O 1 biotype El Tor CTX+

Vaccin oral WC/r. BS DUKORAL WC/r. BS : Whole Cell/ recombinant B Subunit SBL vaccine (Suède) Composition : Classique Inaba El Tor Ogawa + 1 mg Ctx B recombinante Solution de bicarbonate 2, 5%

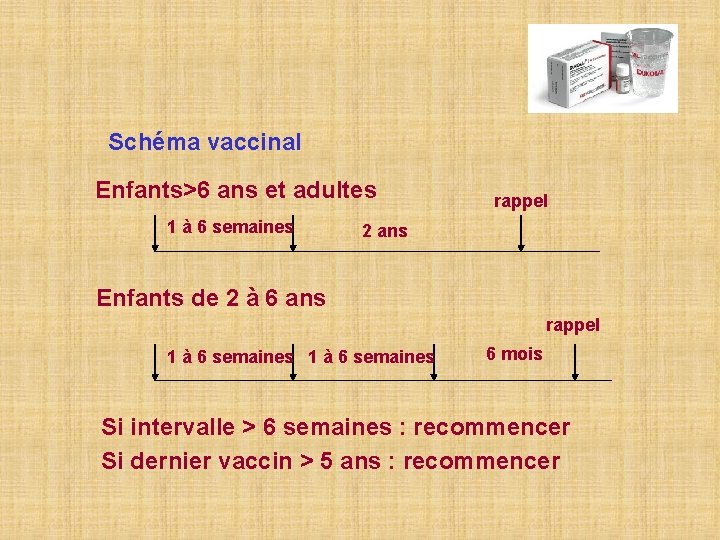
Schéma vaccinal Enfants>6 ans et adultes 1 à 6 semaines rappel 2 ans Enfants de 2 à 6 ans rappel 1 à 6 semaines 6 mois Si intervalle > 6 semaines : recommencer Si dernier vaccin > 5 ans : recommencer

Modalités • Ne pas manger ou boire 1 h avant et après • Bicarbonate : 75 ml si <6 ans 150 ml si >6 ans • Ingestion dans les 2 h après reconstitution (<27°C) • Conservation : 2 à 8°C (bicarbonate < 27°C)

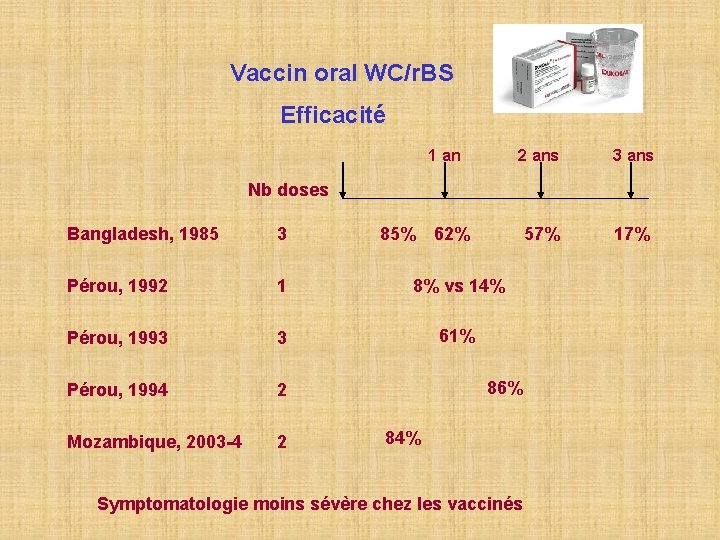
Vaccin oral WC/r. BS Efficacité 1 an 2 ans 3 ans 57% 17% Nb doses 85% 62% Bangladesh, 1985 3 Pérou, 1992 1 8% vs 14% Pérou, 1993 3 61% Pérou, 1994 2 Mozambique, 2003 -4 2 86% 84% Symptomatologie moins sévère chez les vaccinés

Et le voyageur? Choléra 2004 : 763 M de voyageurs Nombre de cas de choléra importés dans le monde en 2004 Sous estimation (2 -3 cas /1 M) Séjour dans famille d’origine Peu de risque : hygiène, acidité gastrique Indications à discuter : longs voyages, épidémies, personnel de soin, Antiacides, pathologie sous jacente (insuffisants rénaux)

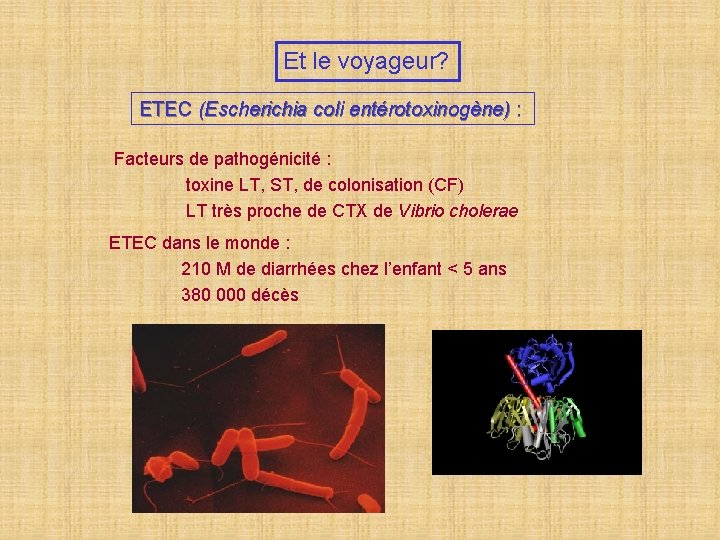
Et le voyageur? ETEC (Escherichia coli entérotoxinogène) : Facteurs de pathogénicité : toxine LT, ST, de colonisation (CF) LT très proche de CTX de Vibrio cholerae ETEC dans le monde : 210 M de diarrhées chez l’enfant < 5 ans 380 000 décès

Diarrhée du voyageur ( « tourista » ) 20 à 60% des voyageurs Place des ETEC 8 -35% chez les voyageurs 10 -44% chez les militaires Place des ETEC LT+ ou. LT/ST+ 5 -20% chez les voyageurs 1 -27% chez les militaires Efficacité du vaccin r. CTB/WC : variable selon les études 50 à 67% Taux d’incidence diarrhée X % d’ETEC ou % ETEC LT+ X efficacité vaccinale Prévention de la diarrhée du voyageur chez 1 à 7% des cas vaccinés Oral cholera vaccine : use in clinical practice, Lancet Infect. Dis. 2006; 6: 361 -73

VACCINS A DISCUTER Hépatite A Hépatite B Typhoïde

Hépatite A VHA Epidémies du passé Grèce et Rome antique Chine 2 ième guerre mondiale : 10 M de cas Campagne El Alamein Novembre 1942 : • blessés : 3602 cas • hépatites aiguës : 1861 cas

VHA Aujourd’hui Shanghai, 1988 292 301 victimes Monde : 1, 5 M de cas cliniques Etats-Unis : 271 000 infections/an 100 décès hospitalisation dans 11 -22% des cas incapacité 15 à 33 jours 300 -500 M $ (1997)

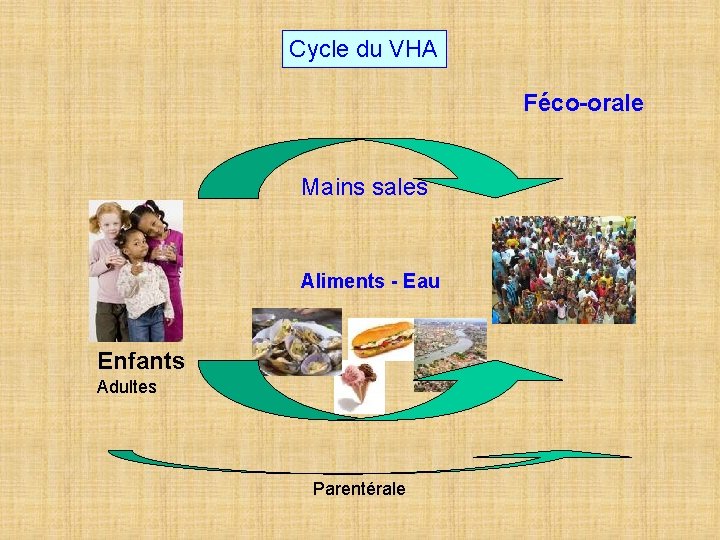
Cycle du VHA Féco-orale Mains sales Aliments - Eau Enfants Adultes Parentérale

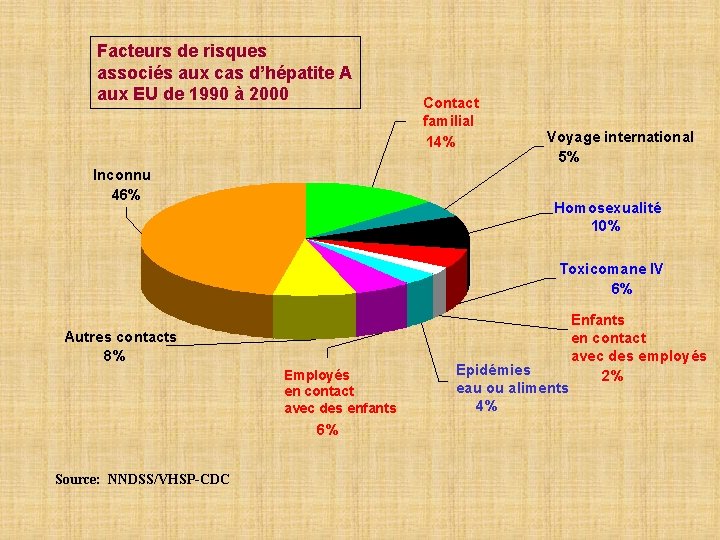
Facteurs de risques associés aux cas d’hépatite A aux EU de 1990 à 2000 Inconnu 46% Contact familial 14% Voyage international 5% Homosexualité 10% Toxicomane IV 6% Autres contacts 8% Employés en contact avec des enfants 6% Source: NNDSS/VHSP-CDC Enfants en contact avec des employés Epidémies 2% eau ou aliments 4%

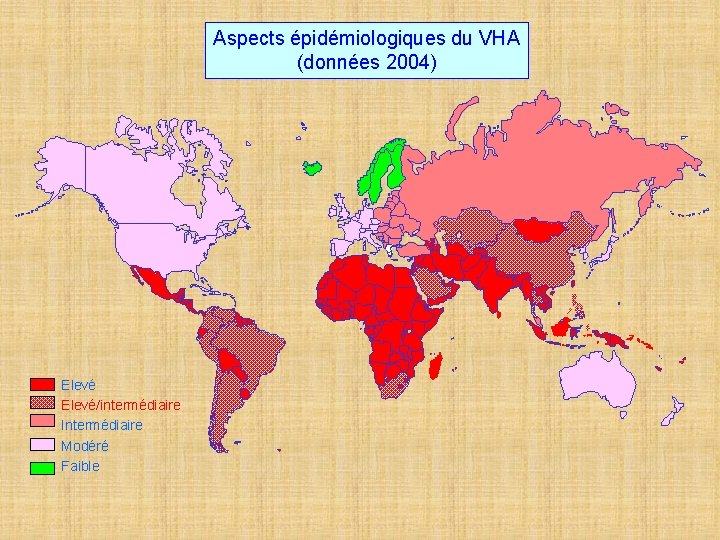
Aspects épidémiologiques du VHA (données 2004) Elevé/intermédiaire Intermédiaire Modéré Faible

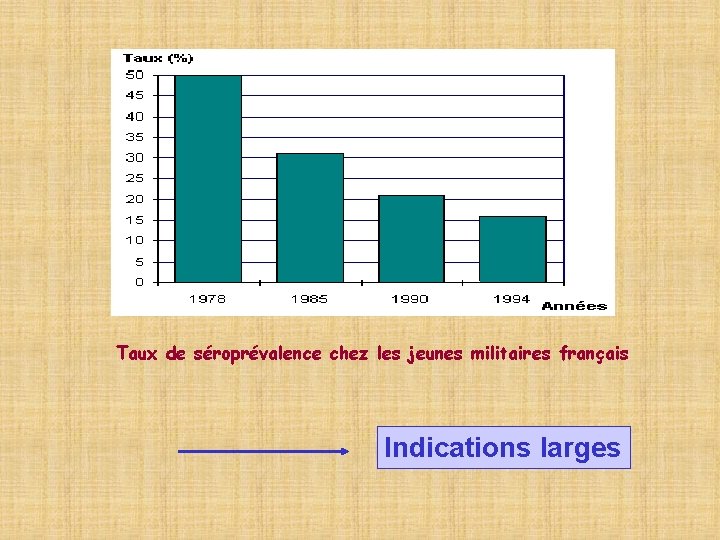
Taux de séroprévalence chez les jeunes militaires français Indications larges

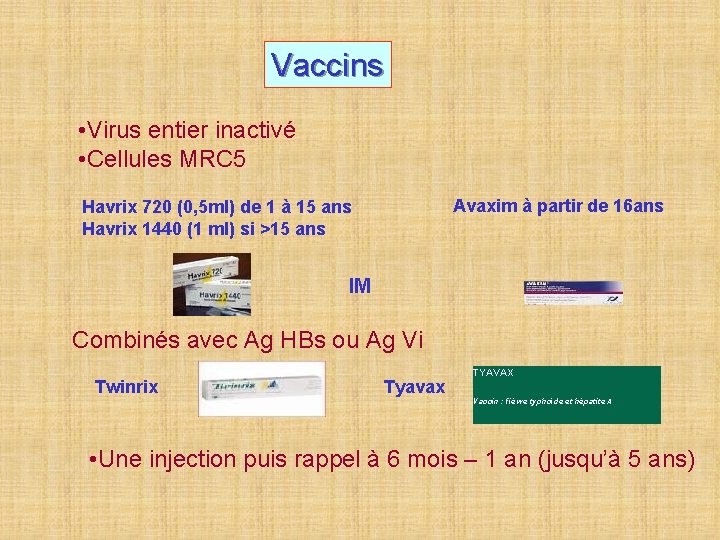
Vaccins • Virus entier inactivé • Cellules MRC 5 Avaxim à partir de 16 ans Havrix 720 (0, 5 ml) de 1 à 15 ans Havrix 1440 (1 ml) si >15 ans IM Combinés avec Ag HBs ou Ag Vi Twinrix Tyavax TYAVAX Vaccin : fièvre typhoïde et hépatite A • Une injection puis rappel à 6 mois – 1 an (jusqu’à 5 ans)

Immunogénicité 90% à J 14 98% à 1 mois 100% à la 2 ième inj efficace chez VIH, maladie chronique du foie Tolérance +++ Efficacité vaccinale Ø Ø Ø Thaïlande : 40 000 enfants de 1 à 16 ans 94% Nicaragua : 274 enfants de 1, 5 à 6 ans 84, 6% Chine (Jiaojiang) : couverture vaccinale de 89% pour les 1 -15 ans TI : 12 -87 cas /an à 0 -1 cas/an

Sérologie pré vaccinale : Ønés avant 1960 Øséjour>1 an en zone de forte endémie Øépisode clinique d’hépatite Pas de nécessité de rappel après un schéma à 2 injections : ØVaccin depuis 1992 ØPersistance des Ac après 12 ans ØModèles mathématiques : persistance au delà de 25 ans ØPersistance d’une mémoire immunitaire ØNécessité d’études dans certaines populations Van Damme, Conscensus statement, The Lancet, 2003, Vol 362

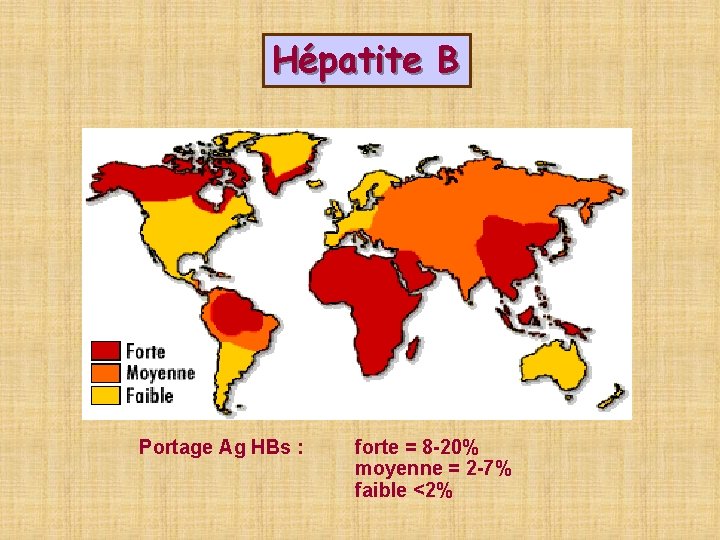
Hépatite B Portage Ag HBs : forte = 8 -20% moyenne = 2 -7% faible <2%

Hépatite B • Risque : hépatite aiguë chronique cirrhose post-hépatitique cancer primitif du foie • Recommandé si séjours fréquents ou prolongés dans pays à forte prévalence. • Risque essentiellement vénérien chez le voyageur (+ tatouage, piercing…), transfusion, aiguilles souillées…

Etat indien du Gujarat : • 120 cas d’hépatites B aiguës • 59 décès par hépatite fulminante • 70 000 contaminations estimées • Entreprise de réutilisation de matériel médical à usage unique • 300 tonnes saisies • 30% des matériels sont réutilisés en Inde

Vaccins contre l’hépatite B • Engerix B (GSK) 20µg ou 10µg • Genhevac B (Pasteur) • HBVax Pro (Sanofi Pasteur MSD) 5µg : enfant de moins de 15 ans 10µg : adulte 40µg pour dialysés • Twinrix : Hépatites A et B adulte enfant • Infanrix Hexa : DTP Coq Hib HB

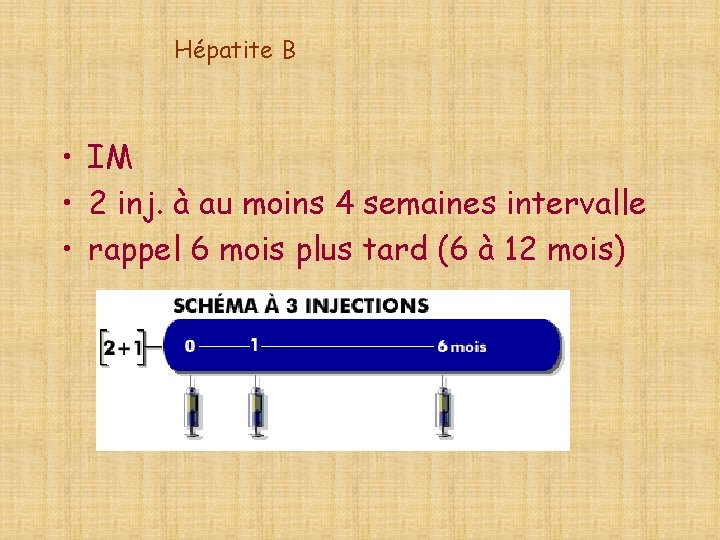
Hépatite B • IM • 2 inj. à au moins 4 semaines intervalle • rappel 6 mois plus tard (6 à 12 mois)

Personnes considérées comme immunisées • Vaccination à 3 injections avant l’âge de 13 ans ou 25 ans (selon le risque) • Vaccination à 3 injections et Ac anti Hbs>100 m. UI/ml • Vaccination à 3 injections et Ac anti Hbs entre 10 et 100 m. UI/ml et Ag Hbs- • Dosage des Ac anti Hbs en post vaccinal à apprécier • Pas d’intérêt lors d’un suivi à long terme

Couverture vaccinale actuelle 1 dose 3 doses Population générale 35% 22% Nourrissons 36% 23% 0 -13 ans 36% 23% 19 -24 ans 71% 47%

comparaison bénéfices/risques de la vaccination contre l ’hépatite B (analyse RNSP, septembre 1998) Vaccination d ’une cohorte de 800 000 préadolescents suivis pendant 20 ans Cas évités 10 à 31 hépatites fulminantes 8 à 195 cirrhoses et hépatocarcinomes Attribuables ? 1 à 2 premières atteintes démyélinisantes centrales

Recombinant hepatitis B vaccine and the risk of multiple sclerosis. A prospective study. Neurology 2004; 63: 838 -842(M. Herman et coll. ) Etude rétrospective : janvier 1993 - décembre 2000 Ø Médecin généralistes anglais dossiers de SEP, ATCD Vaccin VHB 3 ans auparavant Ø 163 patients SEP + : 11 (6. 7%) vaccinés 3 années précédentes Ø 1604 patients indemnes : 2 % vaccinés Association statistiquement significative : risque relatif de 3. 1 Présence de biais, bénéfice > risque Etude HMO aux EU (Health Maintenance Organization) Suivi sur 5 ans Aucune association Etude KIDSEP 356 enfants Aucune association

Typhoïde • Pourquoi vacciner ? – Toxi-infection avec septicémie : gravité = cpc digestive, cardio-vasculaire et neurologique – dans tous les pays hygiène précaire – Transmission féco-orale – 70% des cas en France sont importés

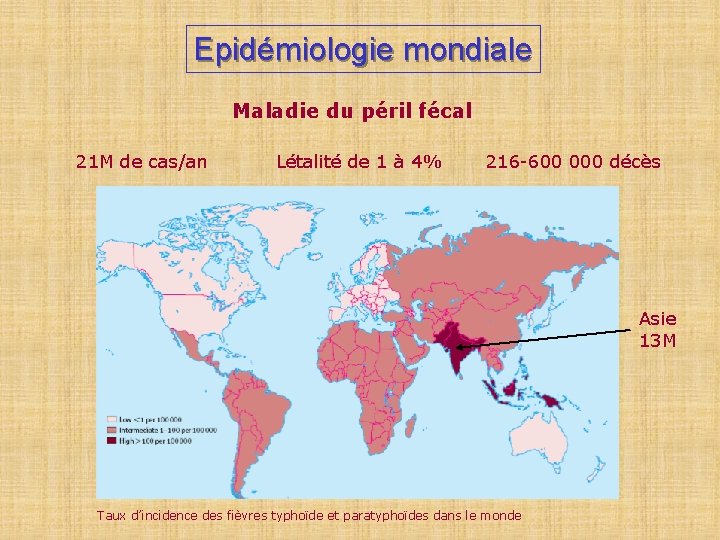
Epidémiologie mondiale Maladie du péril fécal 21 M de cas/an Létalité de 1 à 4% 216 -600 000 décès Asie 13 M Taux d’incidence des fièvres typhoïde et paratyphoïdes dans le monde

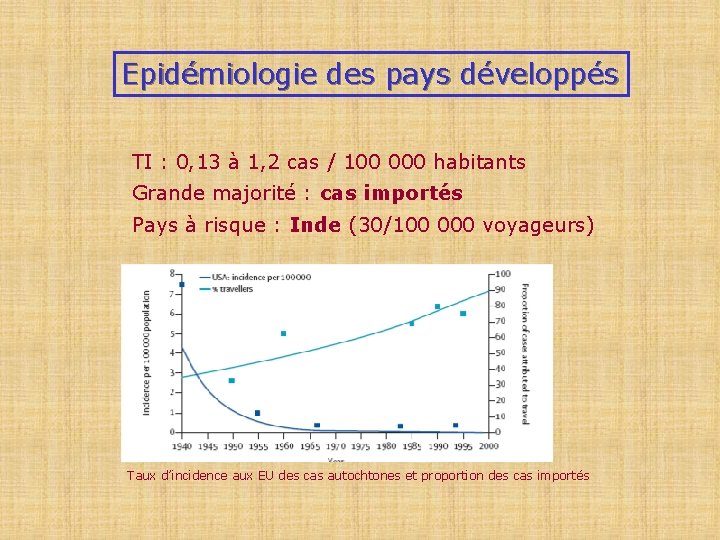
Epidémiologie des pays développés TI : 0, 13 à 1, 2 cas / 100 000 habitants Grande majorité : cas importés Pays à risque : Inde (30/100 000 voyageurs) Taux d’incidence aux EU des cas autochtones et proportion des cas importés

Salmonella Typhi Entérobactérie Salmonella enterica sous espèce enterica sérovar Typhi Ag O somatique Ag Vi (R lyse par le Cpt) Ag H flagellaire Augmentation de la R aux AB : • complication, échec, coût, létalité • ampicilline, cotrimoxazole, chloramphénicol, fluoroquinolone • Asie puis Afrique • facteur principal d’indication de la vaccination

Salmonella Typhi Réservoir : strictement humain malades, porteurs asymptomatiques (1 -4%) Transmission : alimentation, eau, directe Sujet réceptif : septicémie à point de départ lymphatique complications Réaction immunitaire : maladie protection à vie IMH : Ac sériques, rôle des Ig. A IMC

Vaccin polyosidique Vi Introduit en 1994 Typhim Vi Typherix Composition : 25µg du polysaccharide capsulaire Vi de la souche Ty 21 Grande Stabilité : conservation +2 à +8°C (stable 6 mois à 37°C, 2 ans à 22°C) Schéma vaccinal : 1 dose SC ou IM puis revaccination tous les 3 ans association possible (TYAVAX: Vi et hépatite A)

Vaccin polyosidique Vi Efficacité : • inefficace chez l’enfant<2 ans • Immunité débute à J 7, maximale à J 28 • Ac anti Vi > seuil de protecteur (1µg/ml) dans 85 -95% des cas • Essais 1 an 2 ans 3 ans Population Afrique du Sud 11 000 (E) Népal 6 900 (E-A) Chine 131 000 (E-A) Effets indésirables : locaux (3%) 64% 55% 72% 70% 50%

Voyageur • Risque en général faible • Zones à forte endémicité ou épidémie • Séjour de longue durée (>1 mois) • Mauvaise conditions de séjour • Antibiorésistance • Difficulté de recours aux soins

VACCINS CIRCONSTANCIELS Infections invasives à méningocoques Rage Encéphalite japonaise Encéphalite à tiques d ’Europe Centrale

Méningocoques • Neisseria meningitidis • Méningite cérébro-spinale et purpura fulminans • Endémique en Afrique (ceinture de Lapeyssonie), épidémique Asie du Sud. Est et Amérique latine • Transmission maximale saison sèche et froide

MENINGOCOQUE • Plusieurs sérotypes : A, B, C, Y, W 135… – France : Ø B = 70% Ø C= 20% – Grande-Bretagne : Ø B = 60% Ø C = 40% – Afrique - Sahel = A – La Mecque, Burkina Faso = épidémie W 135, a tendance à se substituer au sérogroupe A dans la ceinture méningitique – W 135 en régression

MENINGOCOQUE • 3 vaccins sont disponibles • Vaccin anti-méningococcique – vaccin polyosidique bivalent A et C (50 g de chaque polyoside capsulaire) – une seule inj IM ou SC : protection 3 à 5 ans (85%) – faible immunogénicité chez l’enfant< 24 mois – immunité 5 -10 j après primovaccination

MENINGOCOQUE • Vaccin méningo C conjugué (protéine porteuse) Meningitec®, Meninvact® – – – efficace dès le plus jeune âge plus immunogène (96%), réduction du portage IM plus longue durée de protection schéma vaccinal variable : • < 1 an : 2 doses 0. 5 ml à 2 mois intervalle, rappel à 2 ans • > 1 an, adolescent, adulte : 1 inj unique de 0. 5 ml

MENINGOCOQUE • Vaccin tétravalent : A, C, Y, W 135 – Posysacchariques non conjugués : Mencevax® – Réservé usage hospitalier et CVI – Pèlerinage La Mecque (vaccin obligatoire), Burkina Faso

MENINGOCOQUE Indications • Contacts rapprochés et prolongés avec la population • Séjours en zones et périodes de transmission • Pèlerinage de La Mecque

Rage • Anthropozoonose de répartition mondiale • Virus qui appartient au genre Lyssavirus qui comprend 7 génotypes différents • Contamination par morsure, griffure, …. aérosols. . . • Séjour prolongé ou aventureux et en situation d’isolement dans un pays à haut risque (Asie Inde+++)

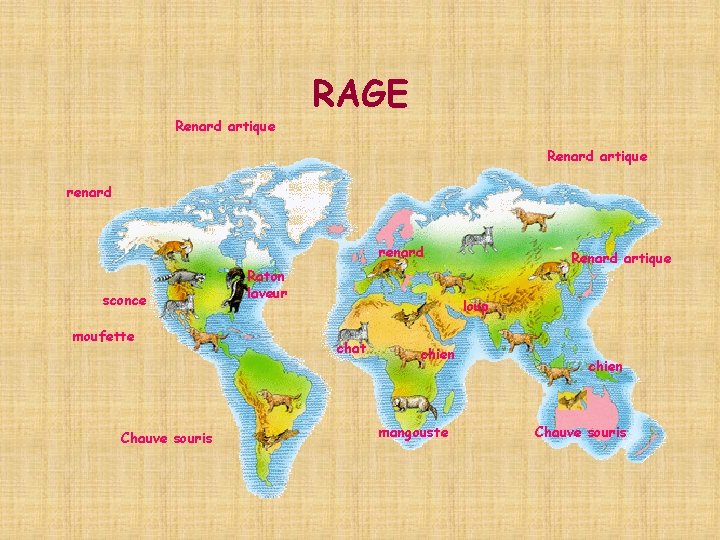
Renard artique RAGE Renard artique renard sconce moufette Chauve souris Raton laveur Renard artique loup chat chien mangouste chien Chauve souris

RAGE Vaccins inactivés avantages: évitent réactions adverses liées au tissu nerveux - produit sur cultures cellulaires Vero (vaccin rabique Pasteur®) - produit sur cellules d’embryons de poulet (Rabipur®) Vaccins lyophilisés, seringue de 1 ml, à reconstituer avant emploi, conservé à 4°C

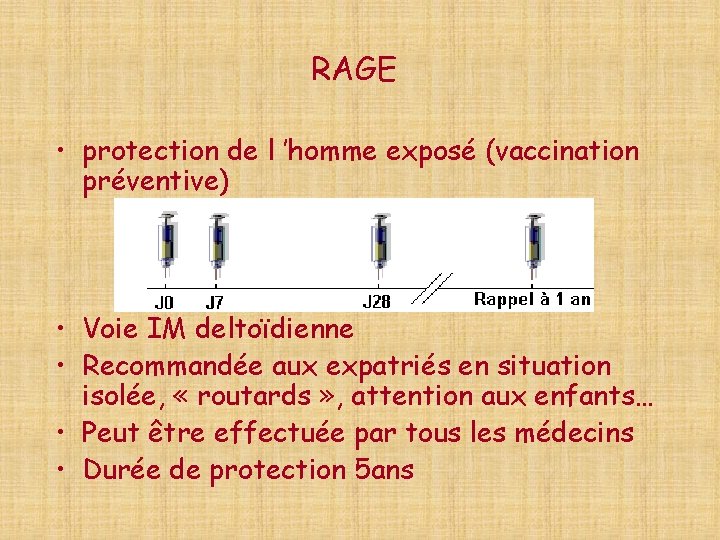
RAGE • protection de l ’homme exposé (vaccination préventive) • Voie IM deltoïdienne • Recommandée aux expatriés en situation isolée, « routards » , attention aux enfants… • Peut être effectuée par tous les médecins • Durée de protection 5 ans

CAT si exposition Nature du contact Traitement Léchage sur peau saine Contact simple Rien Peau mordillée Griffure, excoriation bénigne Vaccin arrêté à J 10 si diagnostic animal possible et animal sain Léchage sur peau érodée Morsure ou griffure ayant traversé la peau Salive sur muqueuse Ig et vaccin arrêté à J 10 si diagnostic animal possible et animal sain Non vacciné : J 0, 3, 7, 14, 28 ou J 0+J 0, 7, 21 Vacciné : J et J 3 (pas d’Ig)

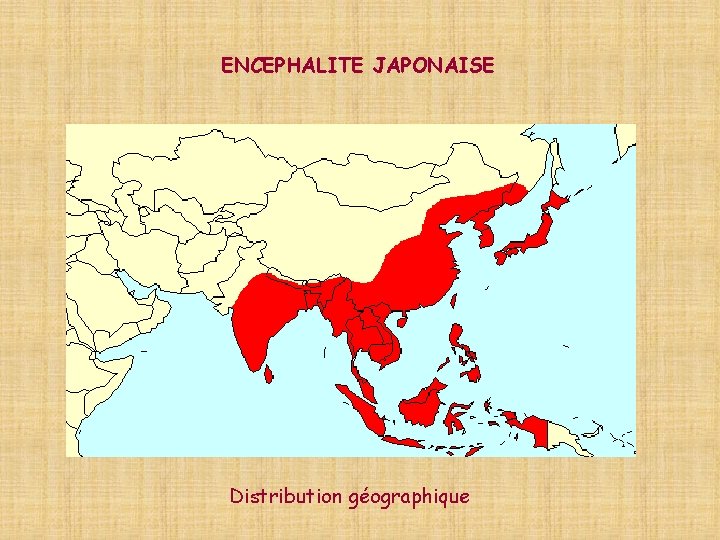
Encéphalite japonaise • Arbovirus famille des Flavivirus • cycle : – moustique genre Culex = vecteur – porc = hôte intermédiaire amplificateur • 50 000 cas / an • Clinique – – – Incubation 4 à 15 j. Méningo-encéphalite à début brutal Mortalité: 25 à 30% des formes patentes Séquelles: 30 à 50% Forme asymptomatiques : 98%

ENCEPHALITE JAPONAISE Distribution géographique

Aspects épidémiologiques Zone endémique: zone de l’Asie tropicale Cas peu nombreux rythmés par la riziculture (mise en eau) Zone endémo-épidémique: zone montagneuse: contreforts de l ’Himalaya Pic d ’avril à octobre, lié à la mousson Fond de transmission faible, épidémies sévères Zone épidémique: zone de l’Asie tempérée: Corée, Japon, centre et nord de la Chine Rythme lié aux températures et non aux pluies: fi n de l ’été et automne

Risque pour le voyageur Probabilité pour un voyageur (CDC): • 1 cas/5 -20 000/semaine en zone et période à risque • moins de 1 pour 1 million 1978 -1992 : 24 cas dont 2 voyageurs

Indications • < 30 j en zone urbaine : inutile • OMS et CDC : Séjour en région d ’endémie En zone rurale Pendant la saison de transmission Plusieurs semaines

Vaccin • Vaccin virus inactivé (souche Nakayama) : JEVAX • A. T. U nominative par centre agréé de vaccination amarile • vaccination : 3 inj de 1 ml SC à J 0 J 7 J 30 • Enfant 1 à 3 ans : 0. 5 ml • Risque allergie tardive : différer le départ de 10 j • Rappel : 1 à 3 ans Pb : Arrêt commercialisation de JEVAX

Encéphalite à tiques d’Europe Centrale • • Flavivirus famille des Flaviviridae Transmission par tiques Réservoir : petits rongeurs Transmission max mai-juin et septembre-octobre • biotopes : zones humides et boisées (campeurs, randonneurs, bûcherons. . . )

ENCÉPHALITE À TIQUES D ’EUROPE CENTRALE • • Vaccin à virus inactivé (souche Neudoerfl) à conserver entre +2°C et +8°C administré voie IM 3 inj de 0. 5 ml (demi-dose enfant 315 ans) • J 0 - J 30 et 3ème inj 9 à 12 mois après • 1 ier Rappel à 3 ans

ENCÉPHALITE À TIQUES D ’EUROPE CENTRALE • Vaccin disponible en France : TICOVAC • C. I : allergie protéines de l ’œuf, gentamycine, néomycine • 3 inj. : M 0; M 1 -3; M 5 -12 et 1 ier Rappel à 3 ans puis tous les 3 à 5 ans

VACCINS COMPLEMENTAIRES Grippe: Voyageurs âgés, groupe, croisière Hémisphère sud: hiver austral (vaccin ATU) BCG : Dès la naissance si séjour prolongé dans pays à forte endémie tuberculeuse Rougeole : Fonction épidémiologie, voir au cas par cas.

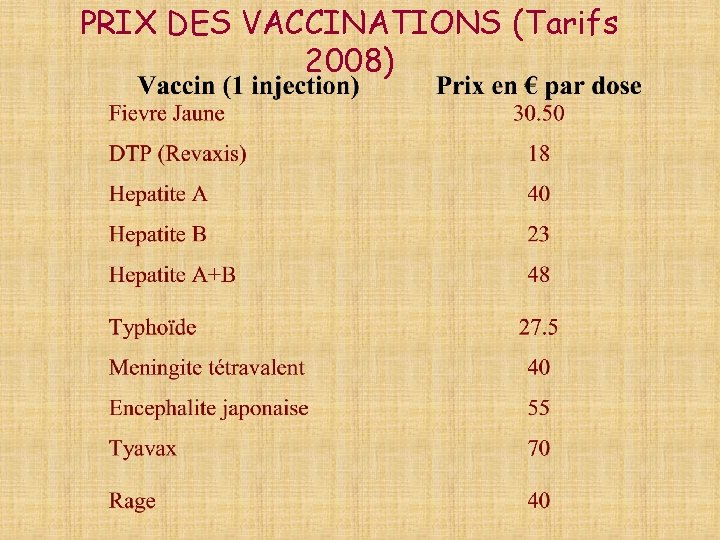
PRIX DES VACCINATIONS (Tarifs 2008)

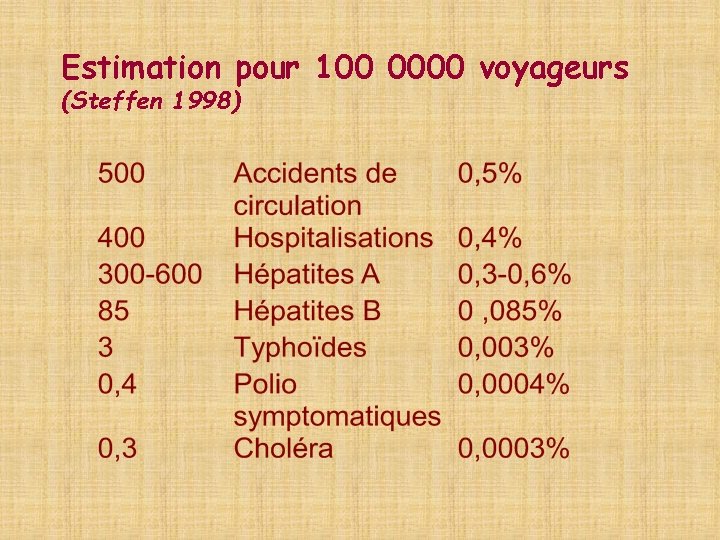
Estimation pour 100 0000 voyageurs (Steffen 1998)