MEDIZINISCHE EMBRYOLOGIE II 20192020 FRHLINGSSEMESTER Placenta III Die

MEDIZINISCHE EMBRYOLOGIE II 2019/2020 FRÜHLINGSSEMESTER Placenta III. Die plazentare Zirkulation Dr. Attila Magyar 26. 03. 2020

Entwicklung der Lakunen und intervillösen Räume

Stadien der plazentaren Entwicklung • • • Prälakunäres Stadium (ET 7 -8) Lakunäres Stadium (ET 9 -12) Primärzotten: ab der zweiten Woche Sekundärzotten: ab dem Ender zweiten Woche Tertiärzotten: ab dritten Woche: - unreife Intermediärzotten -Terminalzotten
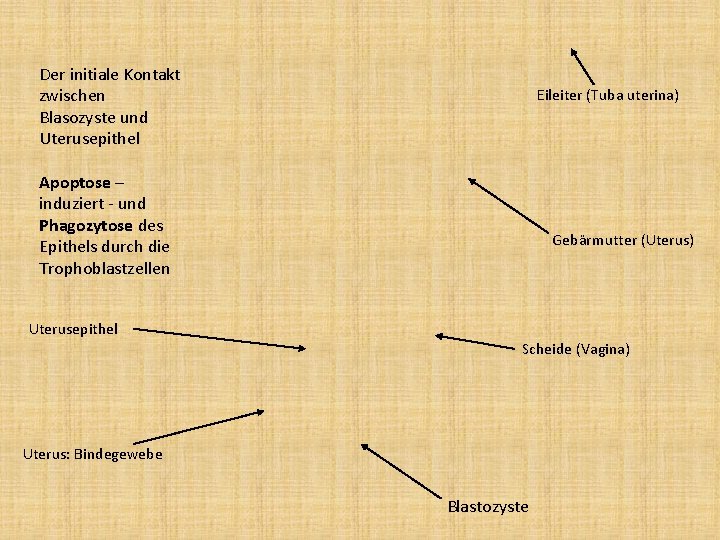
Der initiale Kontakt zwischen Blasozyste und Uterusepithel Eileiter (Tuba uterina) Apoptose – induziert - und Phagozytose des Epithels durch die Trophoblastzellen Gebärmutter (Uterus) Uterusepithel Scheide (Vagina) Uterus: Bindegewebe Blastozyste

Uteruslumen Dezidua Blastozyste besteht aus Embryo-bildenden Zellen (Embryoblasten) und die embryonale Hülle bildende Zellen (Trophoblasten)
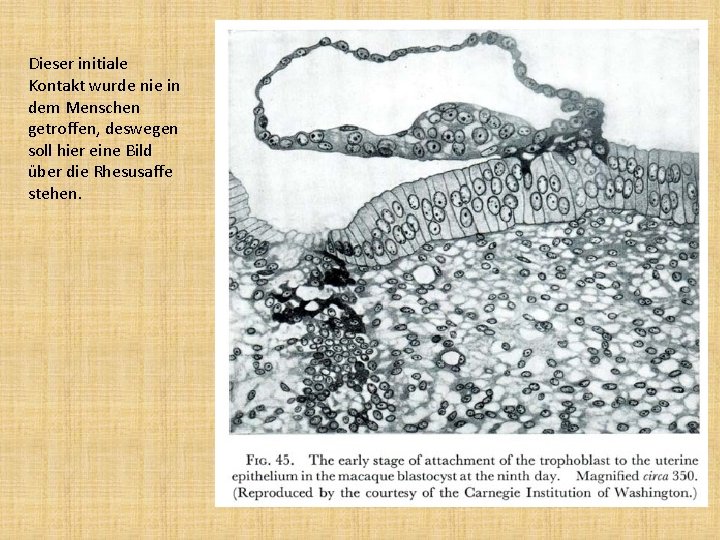
Dieser initiale Kontakt wurde nie in dem Menschen getroffen, deswegen soll hier eine Bild über die Rhesusaffe stehen.
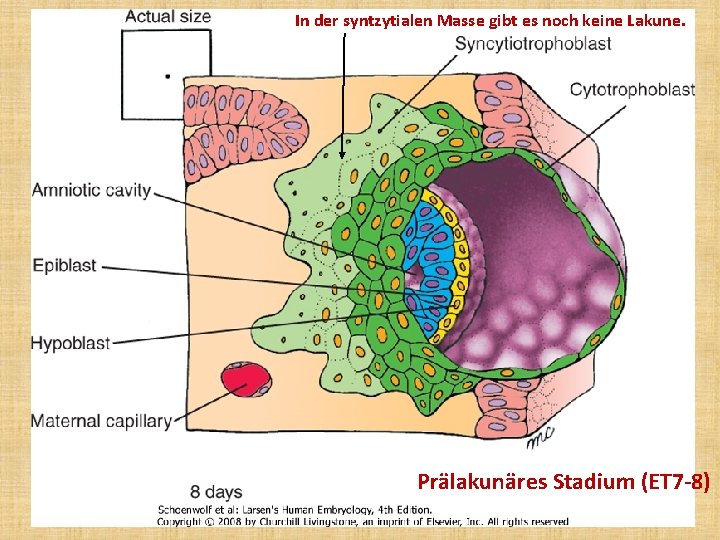
In der syntzytialen Masse gibt es noch keine Lakune. Prälakunäres Stadium (ET 7 -8)
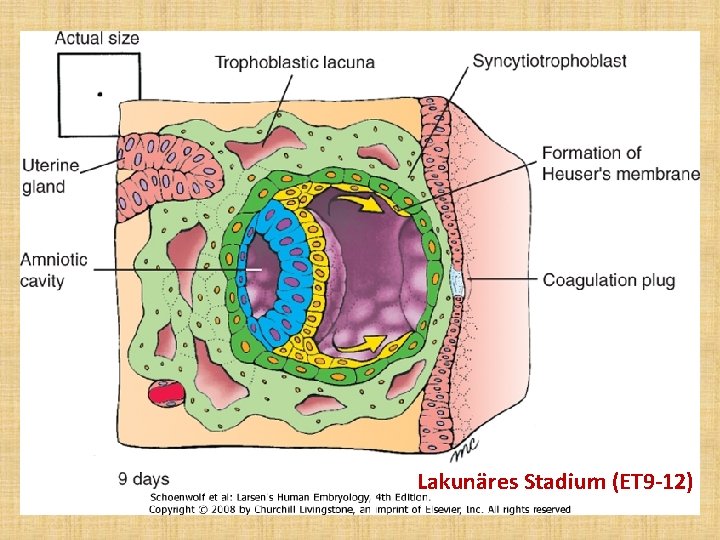
Lakunäres Stadium (ET 9 -12)
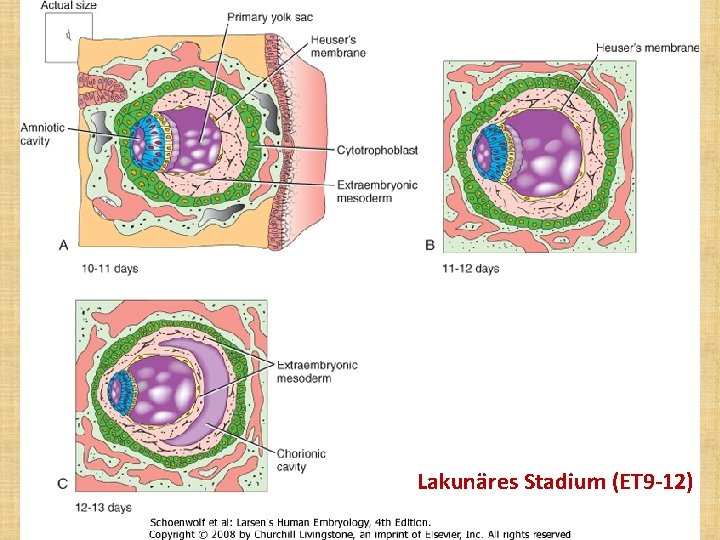
Lakunäres Stadium (ET 9 -12)
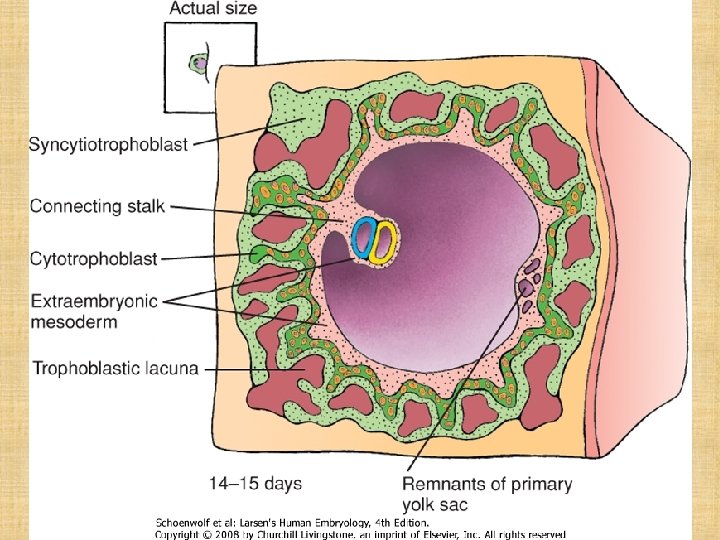
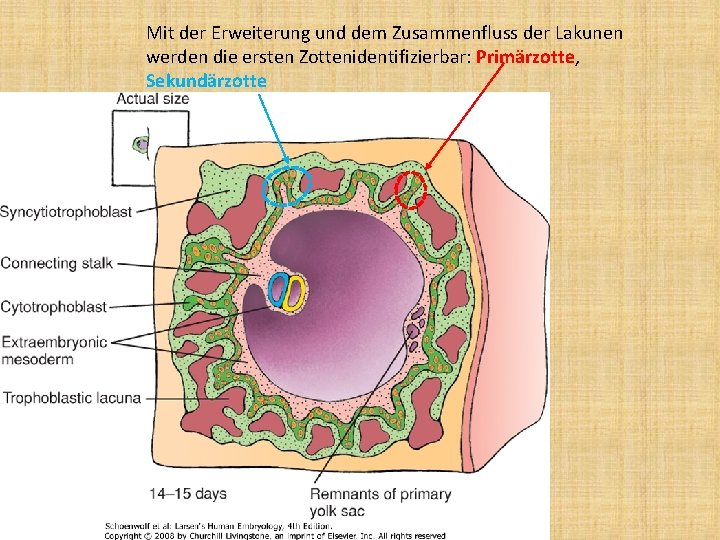
Mit der Erweiterung und dem Zusammenfluss der Lakunen werden die ersten Zottenidentifizierbar: Primärzotte, Sekundärzotte

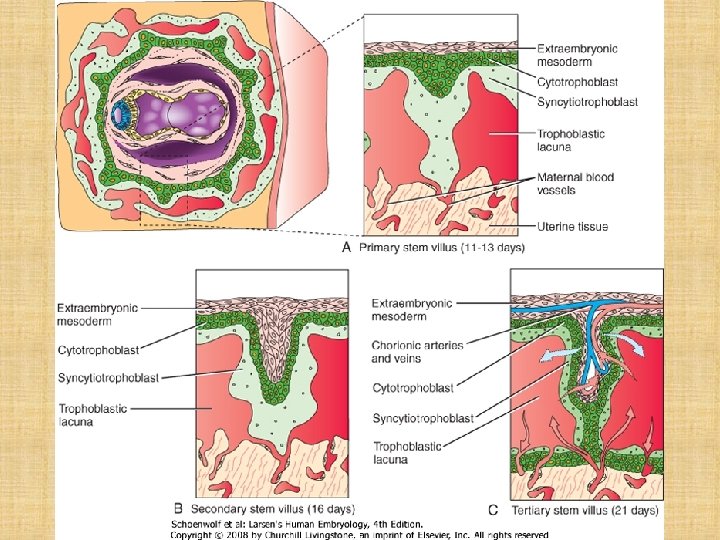
Typen der Chorionzotten • Primärzotte: nur aus Trophoblastzellen • Sekundärzotte: aus Trophoblastzellen und Mesenchm (kern) • Tertiärzotte: enthält außer Trophoblast und Mesenchym auch Blutgefäße
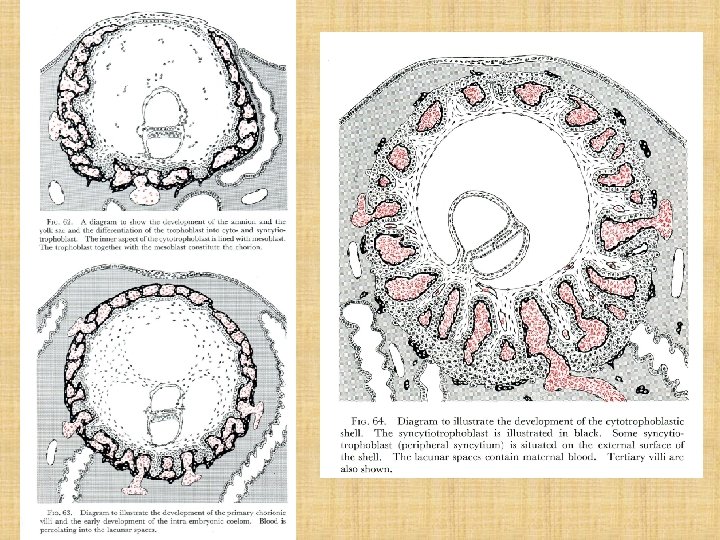
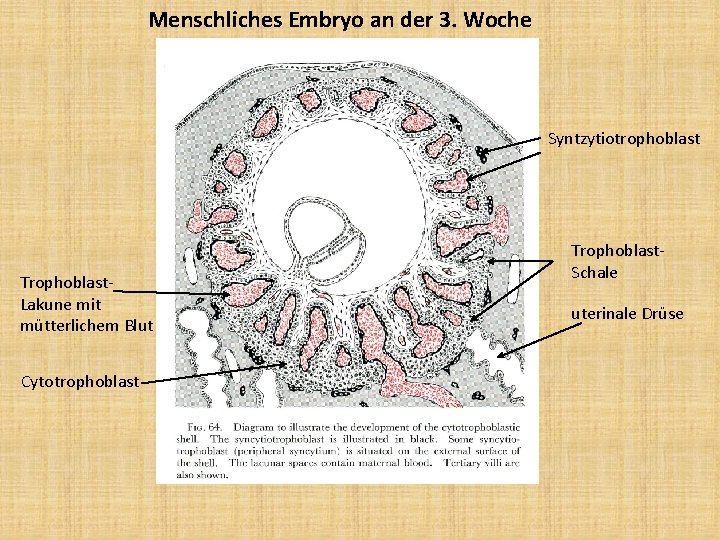
Menschliches Embryo an der 3. Woche Syntzytiotrophoblast Trophoblast. Lakune mit mütterlichem Blut Cytotrophoblast Trophoblast. Schale uterinale Drüse

Inhalt der Trophoblast-Lakunen • In den Embryo-Textbüchern steht, wie z. B. im Sadler (Thieme, 2014): „Zotten am Ende der 3, Entwicklungswoche: die mütterlichen Gefäße durchdringen die Zytotrophoblasthülle und ergießen sich in die intervillösen Räume zwischen den Zotten. ” • Das soll eine sehr frühe Blutzirkulation zwoischen den Zotten bedeuten.

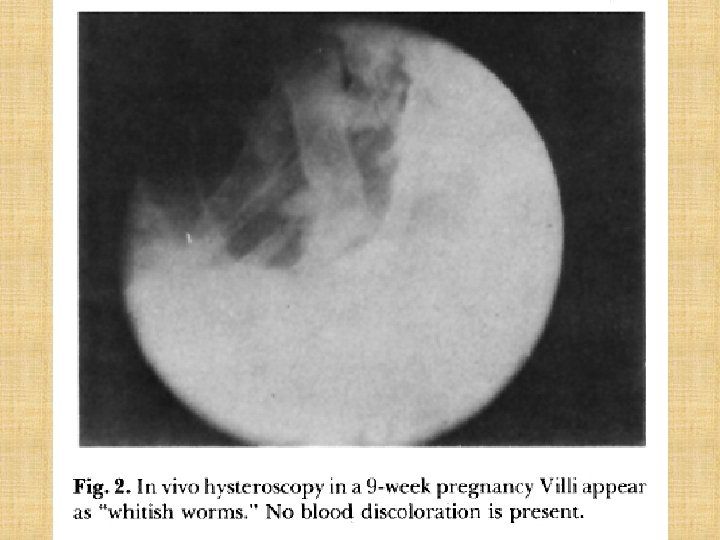
Ab den 80 -90’er Jahren gibt es Angaben, • dass mütterliches Blut in dem ersten Trimester: also bis zur 12 EW, kaum in die intervillösen Räume gelingt: • Befunde mit Hysteroskope: Zotten sind nicht mit Blut kontaminiert, es war keine Blutung bei der Zottenbiospie; Hysterektomie von schwangerem Uterus (EW 9 -10): RTG-Kontrastmittel in die A. uterina und perfusion: keine Schatten in der Plazenta • Hustin, Am J Obstet Gynecol, 1987
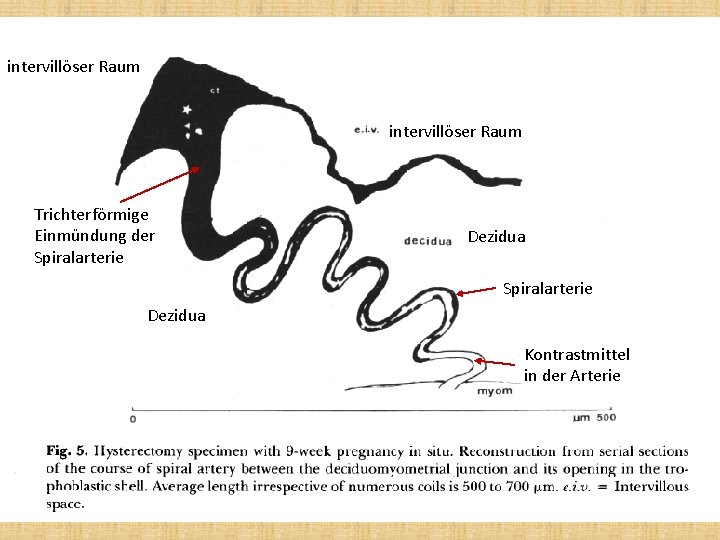
intervillöser Raum Trichterförmige Einmündung der Spiralarterie Dezidua Kontrastmittel in der Arterie
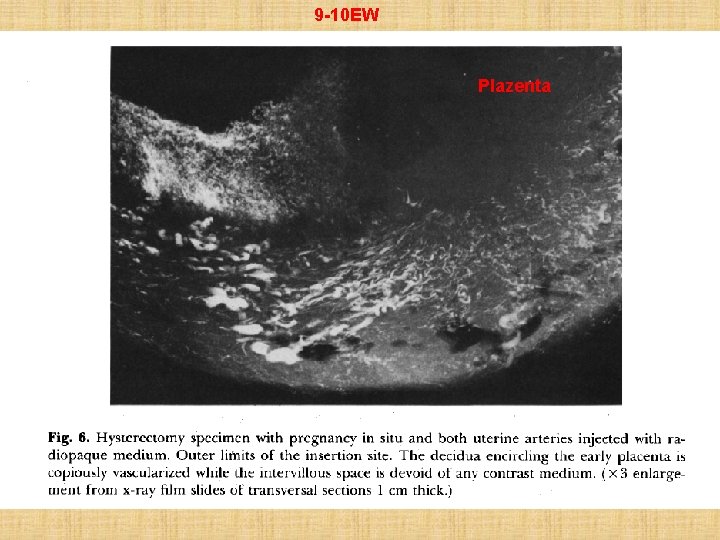
9 -10 EW Plazenta
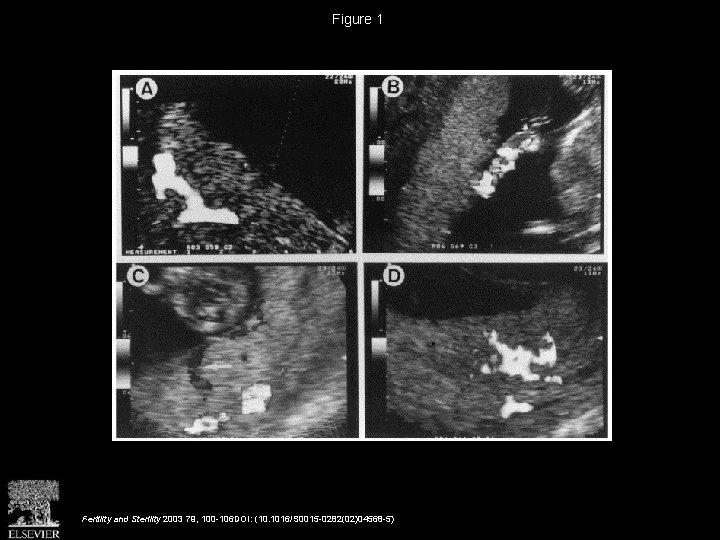
Figure 1 Fertility and Sterility 2003 79, 100 -106 DOI: (10. 1016/S 0015 -0282(02)04568 -5)
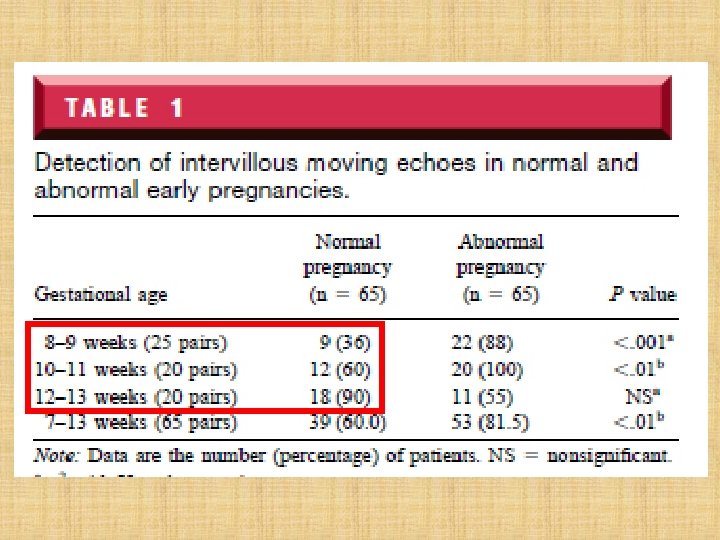

• Nach der 12 EW gelingt das mütterliche Blut in die intervillösen Räume, wie in älteren Schwangeschaften (nahc Hysterektomie) mit Kontrastmittel nachgewiesen wurde:
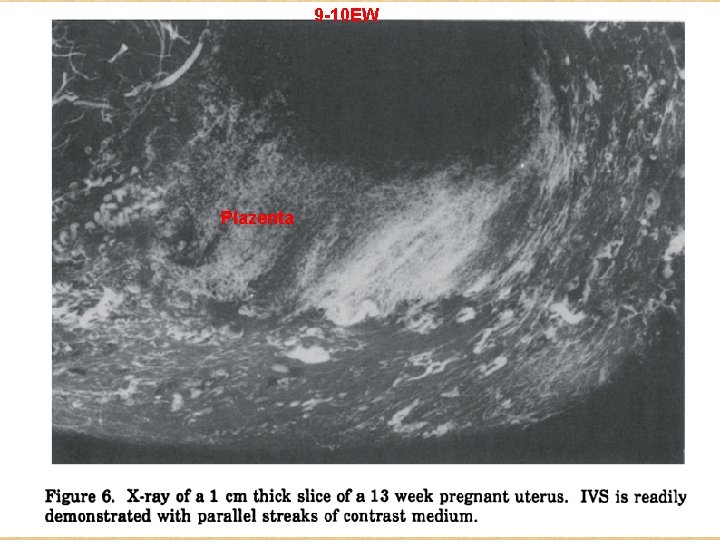
9 -10 EW Plazenta

Was ist dann in den intervillösen Räume im ersten Trimester? • eine Flüssigkeit, mit wenigen mütterlichen Erythrozyten: also keinesfalls eine internsive Strömung des mütterlichen Blutes • Transsudatum des mütterlichen Blutes plus Sekret der Uterindrüsen (? ) • Das Embryo entwicklet sich im ersten Trimester in relativer Sauerstoffmangel (Anaerob)

Warum gibt es fast keine intervillöse Zirkulation? • Siehe Plazenta I Vorlesung: die verschiedenen extravillösen Trophoblasttypen • endovaskulärer trophoblast (aus der Trophoblast-Schale) dringt in die Spiralarterien ein: • Abbau des Endothels, Abbau oder Verdringen der Muskulatur • Trophoblast-Propfen, die das Lumen verstopfen
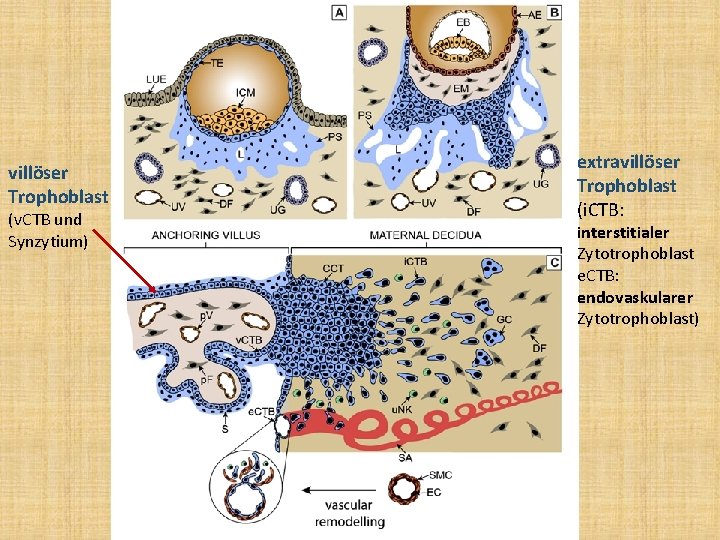
villöser Trophoblast (v. CTB und Synzytium) extravillöser Trophoblast (i. CTB: interstitialer Zytotrophoblast e. CTB: endovaskularer Zytotrophoblast)
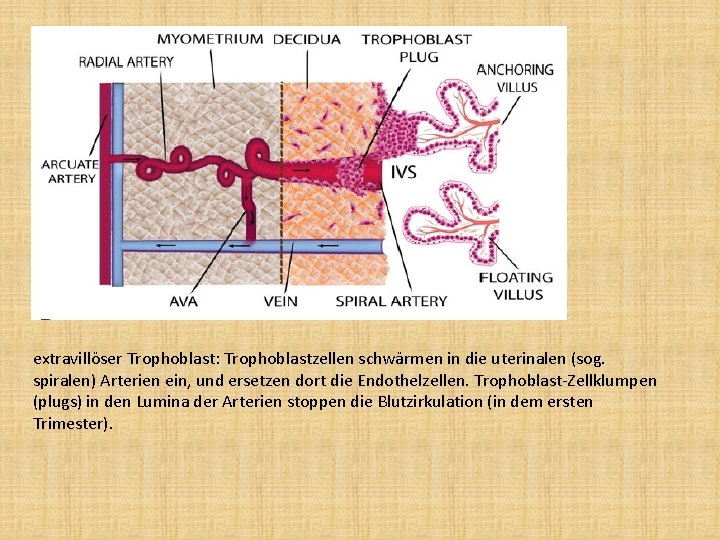
extravillöser Trophoblast: Trophoblastzellen schwärmen in die uterinalen (sog. spiralen) Arterien ein, und ersetzen dort die Endothelzellen. Trophoblast-Zellklumpen (plugs) in den Lumina der Arterien stoppen die Blutzirkulation (in dem ersten Trimester).
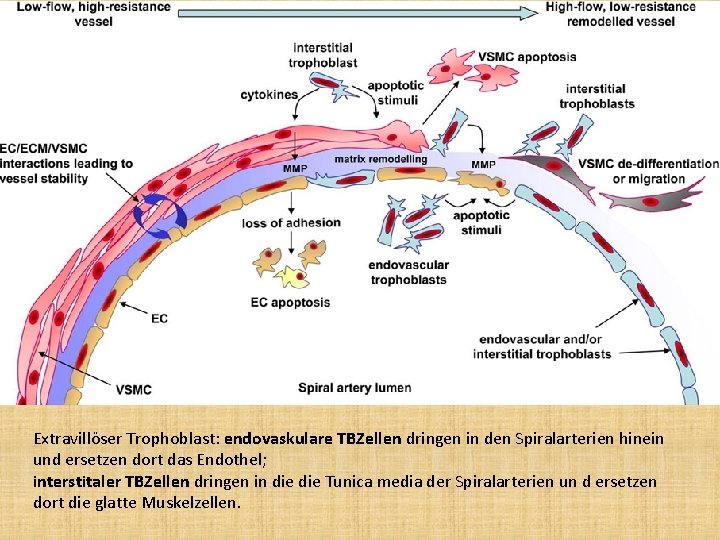
Extravillöser Trophoblast: endovaskulare TBZellen dringen in den Spiralarterien hinein und ersetzen dort das Endothel; interstitaler TBZellen dringen in die Tunica media der Spiralarterien un d ersetzen dort die glatte Muskelzellen.
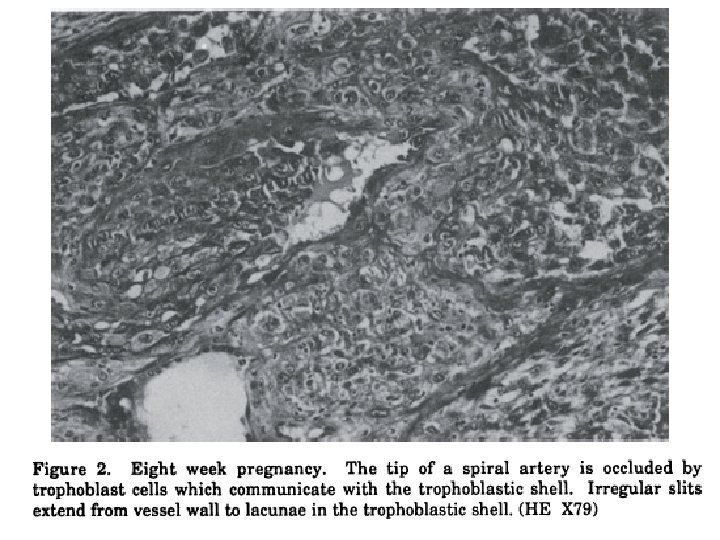
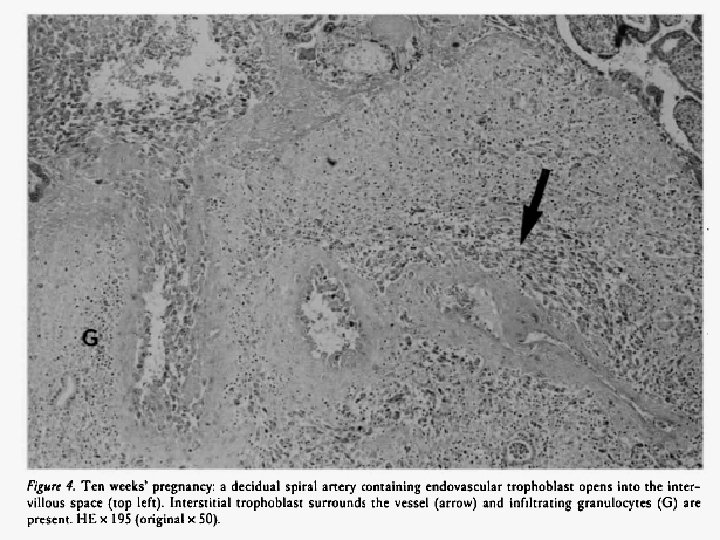

Base of the placenta, showing a large maternal vessel entering the intervillous space (HE × 4).
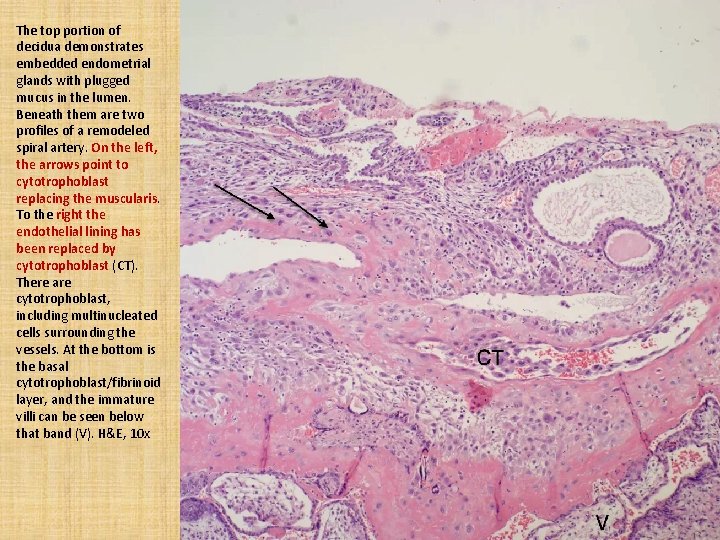
The top portion of decidua demonstrates embedded endometrial glands with plugged mucus in the lumen. Beneath them are two profiles of a remodeled spiral artery. On the left, the arrows point to cytotrophoblast replacing the muscularis. To the right the endothelial lining has been replaced by cytotrophoblast (CT). There are cytotrophoblast, including multinucleated cells surrounding the vessels. At the bottom is the basal cytotrophoblast/fibrinoid layer, and the immature villi can be seen below that band (V). H&E, 10 x
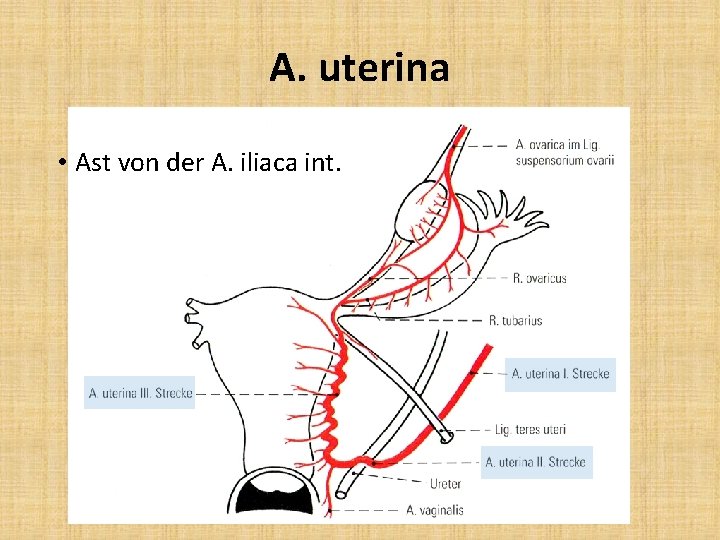
A. uterina • Ast von der A. iliaca int.
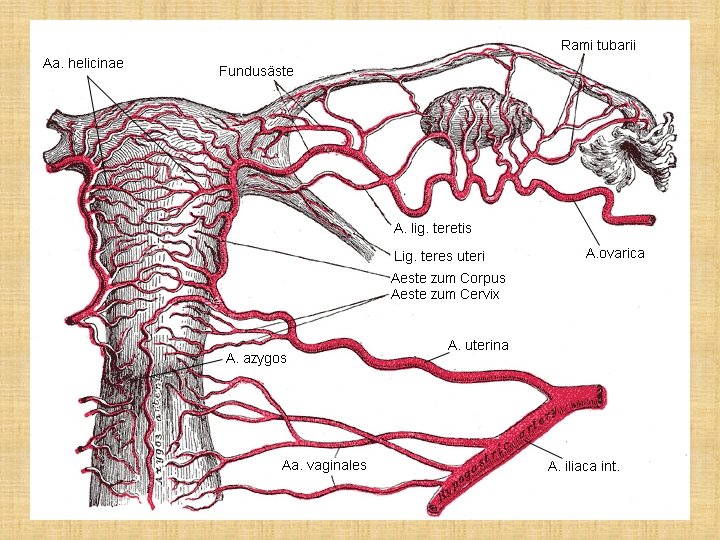

A. uterina • hat ungefähr eine Duzente rechtwinklig austretender Äste: die Aa. helicinae oder Aa. arcuatae • sie teilen sich in eine vordere und eine hintere Ast auf, die geschlingelt weiterlaufen • diese Äste werden (können) ventral oder dorsal miteinander anastomosieren
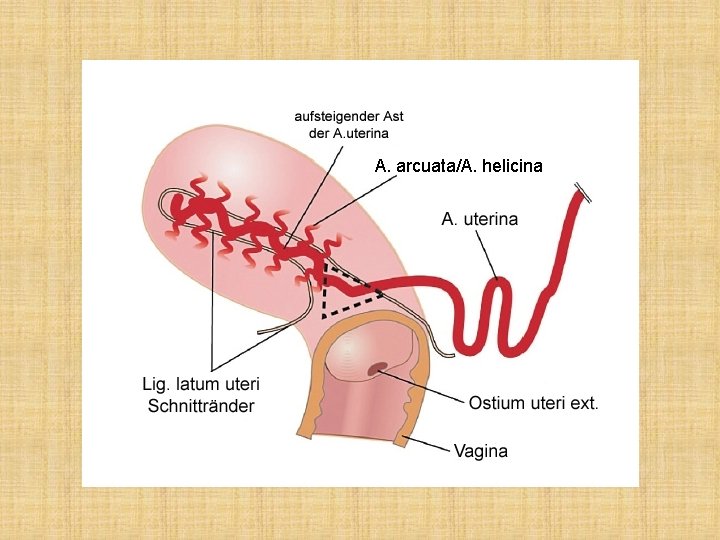
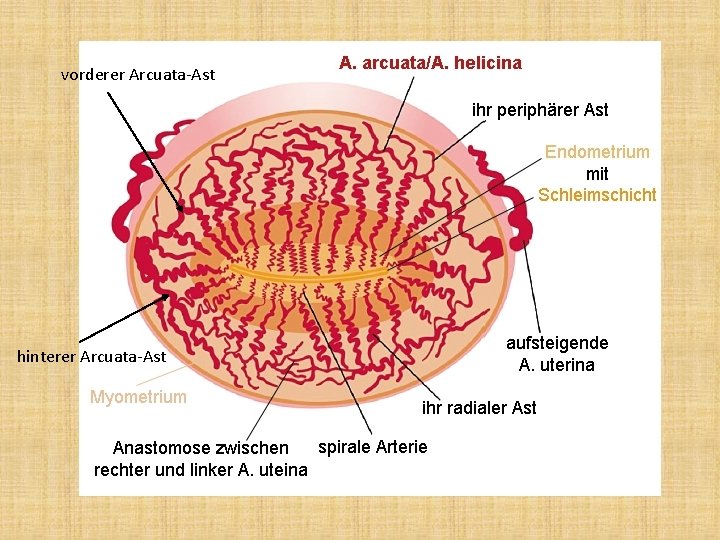
vorderer Arcuata-Ast hinterer Arcuata-Ast

Fortsetzung der A. arcuata • radiale Arterie, die auch geschlingelt in die Richtung Endometrium läuft • an der Grenze von Myometrium zum Endometrium: spaltet die radiale Arterie: in eine basale Arterie und die Spirale Arterie auf
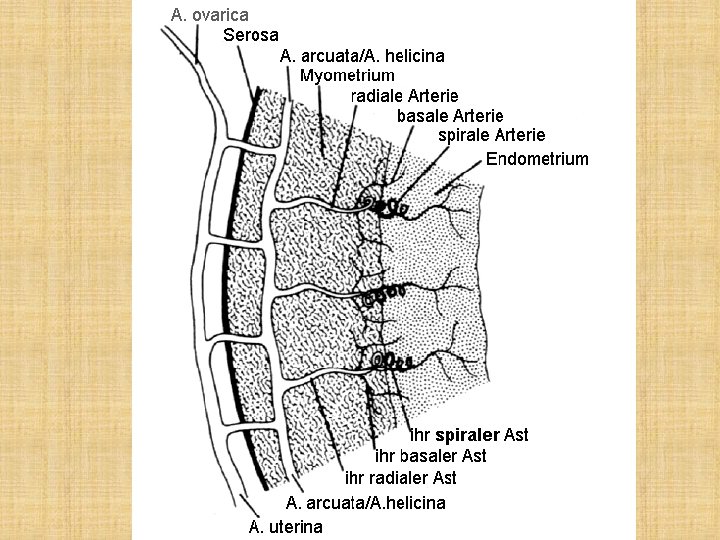

Uterinale Durchblutung • verschiedene Messtechniken (ab den 1950 er Jahren): N 2 O, 133 Xe oder transvaginaler Doppler • uteroplacental blood flow (UPBF) • Basal: 20 -50 ml/Min • Einzelschwangerschaft: 450 -800 ml/Min; bei Zwillingen bis zum 1 L/Min • Voraussetzungen für diese Veränderungen: starke Reduzierung des uterinalen Gefäßwiederstandes (uterine vascular resistance)

Uterinale Durchblutung • diese starke Vergrößerung der UPBF ist durch komplementäre Mechanismen möglich: • cardiac output (Herzzeitvolumen) ist vergrößert • Gefäßvolumen auch vergrößert • UPBF Zunahme bei der Frau: linear, stufenweise • Blutdruck in den Spiralarterien: 9 -15 Hgmm • (zu hoher Druck würde die Chorionzotten komprimieren)

Herzzeitvolumen ist vergrößert • In den ersten 27 Wochen nimmt die Ruhe. Herzfrequenz um ca. 15 Schläge/Minute, das Ruhe. Schlagvolumen um ca. 10 ml, das Herzzeitvolumen um 30 -50% zu, ohne weitere Änderung bis zur Geburt.

Uterinale Durchblutung • Durchmesser der A. uterina der Frau während der Schwangerschaft wird verdoppelt: von 1, 4 mm (nichtschwanger) bis 2, 8 mm (an EW 21), dann bleibt unverändert bis zum EW 30, dann vergrößert bis zum 3, 4 mm (EW 36) • wodurch? Teilung und Verlängerung der glatten Muskelzellen

Umbau der Spiralarterien • Trichterförmige Erweiterung der letzten Abschnitt • Einwanderung von extravillösen, endovaskulären Trophoblastzellen: Abbau des Endothels, Vertreibung der glatten Muskulatur
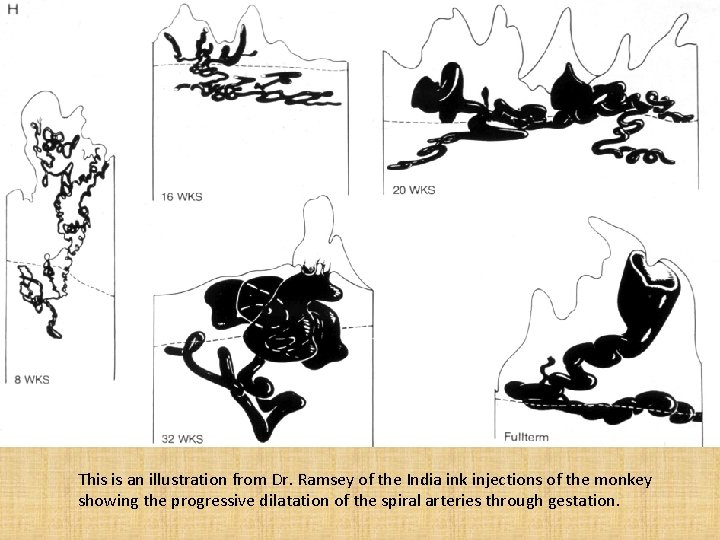
This is an illustration from Dr. Ramsey of the India ink injections of the monkey showing the progressive dilatation of the spiral arteries through gestation.

Umbau der uterinalen Gefäßen • in den Spiralarterien: verschwindet die MEI und T. media (diese Veränderungen der Arterienwände sind bis zum inneren Drittel des Myometriums zu folgen) • Einmündungsstelle der Spiralarterien (in die intervillösen Räume): breitet sich trichterförmig 5 -10 mal aus • dadurch verlangsamt die arteriele Blutstromvon 2 -3 m/s in den Arterien mit einem Durchmesser von 0, 4 -0, 5 mmbis zm 10 cm/s in den Trichtern (Durchmesser 2, 5 mm) • ohne diese Verlangsamung würde das arterielle Blut in den IVR mit 1 -2 m/s Geschwindigkeit strömen (wie bei der Präeklampsie)
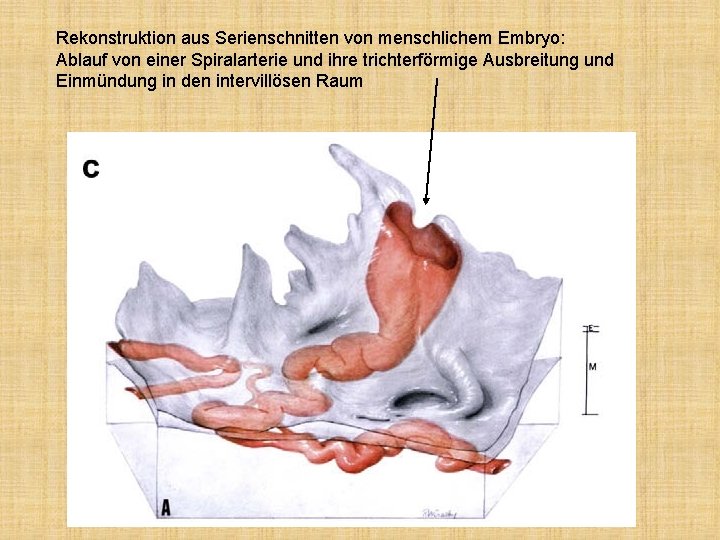
Rekonstruktion aus Serienschnitten von menschlichem Embryo: Ablauf von einer Spiralarterie und ihre trichterförmige Ausbreitung und Einmündung in den intervillösen Raum
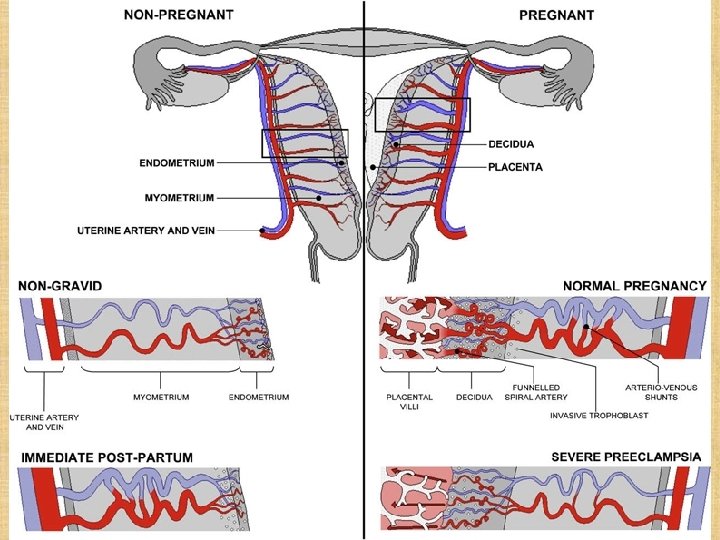

Voriges Bild: Diagrammatic representation of uterine and placental vasculature (red shading = arterial; blue shading = venous) in the non-pregnant, pregnant and immediate postpartum state. Normal pregnancy is characterized by the formation of large arterio-venous shunts that persist in the immediate post-partum period. By contrast pregnancies complicated by severe preeclampsia are characterized by minimal arterio-venous shunts, and thus narrower uterine arteries. Extravillous cytotrophoblast invasion in normal pregnancy (diamonds) extends beyond the decidua into the inner myometrium resulting in the formation of funnels at the discharging tips of the spiral arteries. Contrast with severe preeclampsia.
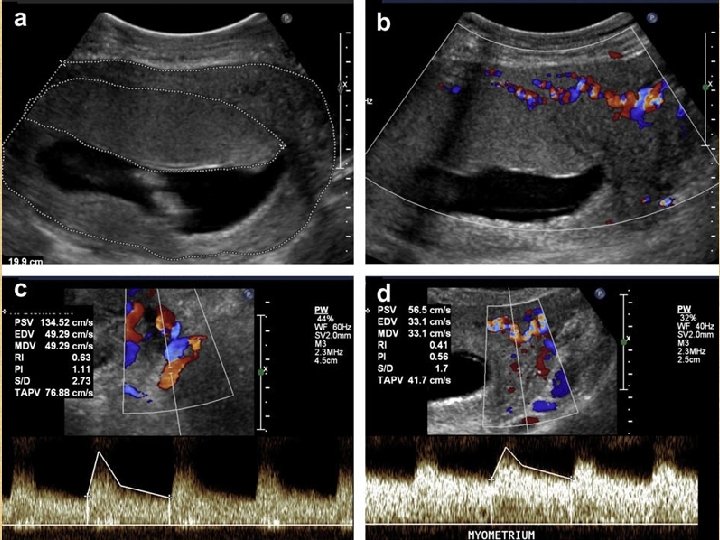

Representative real-time and colour/pulsed Doppler images of placental development at 12 weeks gestation. a) Transverse view of body of uterus outlining the uterine wall (outer line) with an anteriorly located placenta (inner line). b) The same view with colour Doppler (at conventional arterial setting of 38 cm/s). Note flow signals in this range are confined to the myometrium. c) Colour/pulsed Doppler identification of the proximal left uterine artery. Note low-impedance waveform with high (135 cm/s) peak systolic velocity. d) Colour-pulsed Doppler identification of arterial signals in the lateral myometrium, above the left proximal uterine artery. Note low-impedance waveform similar to Fig. 3 c but at lower (56 cm/s) velocity. No such signals are observed entering the basal plate of the placenta. Whilst these images suggest intra-myometrial shunting at the end of the first trimester, the extent to which this phenomenon occurs in the second and third trimesters requires further research.

Letztes Bild gibt eine sehr gute Zusammenfassung über die plazentare Blutkreislauf in normalen Schwangerschaft und in Präeklampsie:
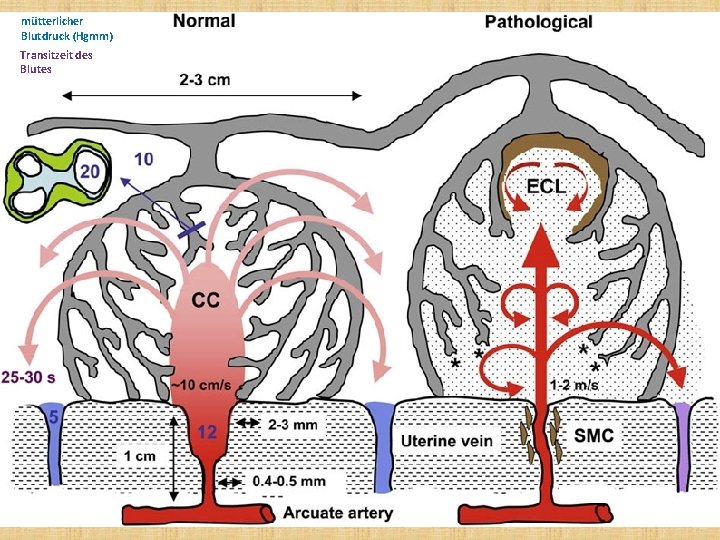
mütterlicher Blutdruck (Hgmm) Transitzeit des Blutes

Diagrammatic representation (not to scale) of the effects of spiral artery conversion on the inflow of maternal blood into the intervillous space and on lobule architecture predicted by modelling. Dilation of the distal segment in normal pregnancies will reduce the velocity of incoming blood, and the residual momentum will carry the blood into the central cavity (CC) of the lobule, from where it will disperse evenly through the villous tree. Transit time to the uterine vein is estimated to be in the order of 25– 30 s, allowing adequate time for oxygen exchange. The pressure of the maternal blood, indicated in mm. Hg by the figures in blue, will drop across the nondilated segment of the spiral artery, the dimensions of which are given alongside. In pathological pregnancies, where no or very limited conversion occurs, the maternal blood will enter the intervillous space at speeds of 1– 2 m/s. The high Reynolds number predicts turbulent flow, indicated by the circular arrows. We suggest that the high momentum ruptures anchoring villi (asterisked) and displaces others to form echogenic cystic lesions (ECL) lined by thrombus (brown). The transit time will be reduced, so that oxygen exchange is impaired and blood leaves in the uterine vein with a higher oxygen concentration than normal. Trophoblastic microparticulate debris (dotted) may be dislodged from the villous surface, leading to maternal endothelial cell activation. Finally, the retention of smooth muscle cells (SMC) around the spiral artery will increase the risk of spontaneous vasoconstriction and ischaemia–reperfusion injury.
- Slides: 55