MEDIZINISCHE EMBRYOLOGIE I 20192020 WINTERSEMESTER Die axonale Wegfindung

MEDIZINISCHE EMBRYOLOGIE I 2019/2020 WINTERSEMESTER Die axonale Wegfindung und der Wachstumskegel Axonal pathfinding and growth cone DR. ATTILA MAGYAR 22. 10. 2019
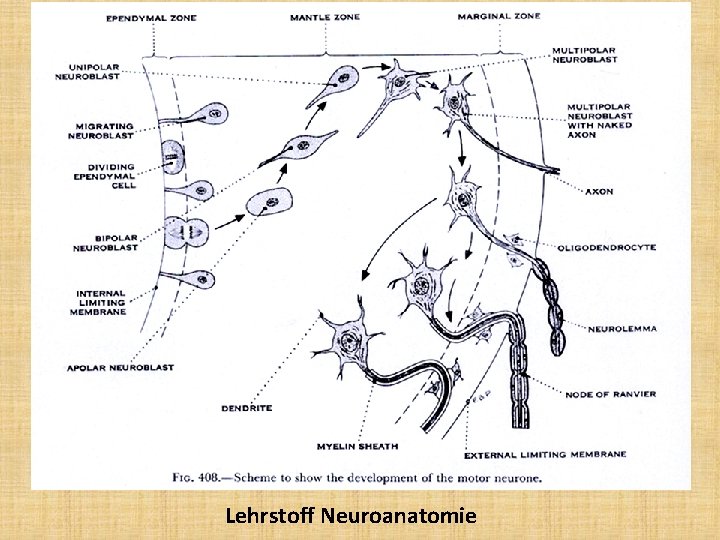
Lehrstoff Neuroanatomie
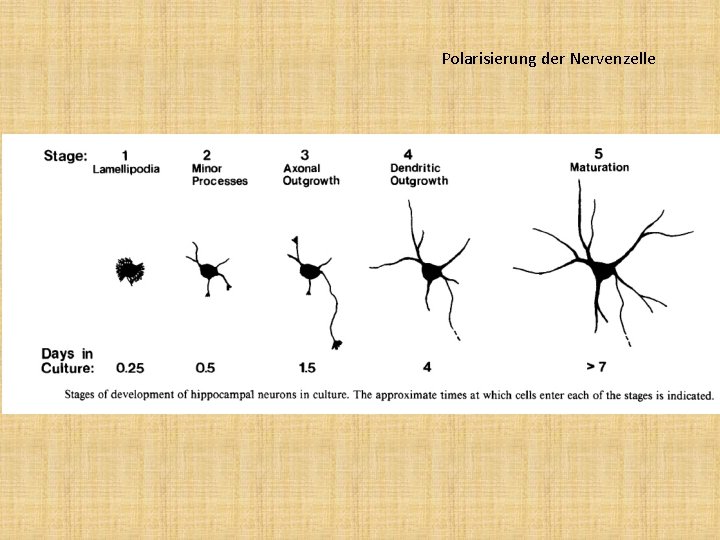
Polarisierung der Nervenzelle
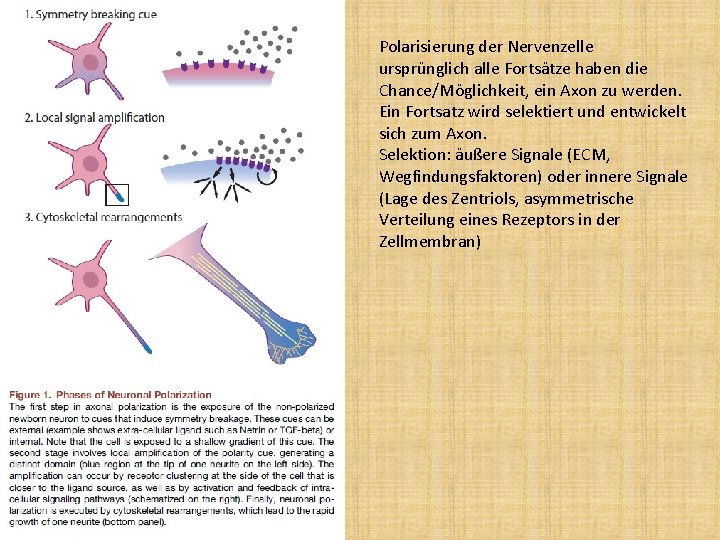
Polarisierung der Nervenzelle ursprünglich alle Fortsätze haben die Chance/Möglichkeit, ein Axon zu werden. Ein Fortsatz wird selektiert und entwickelt sich zum Axon. Selektion: äußere Signale (ECM, Wegfindungsfaktoren) oder innere Signale (Lage des Zentriols, asymmetrische Verteilung eines Rezeptors in der Zellmembran)
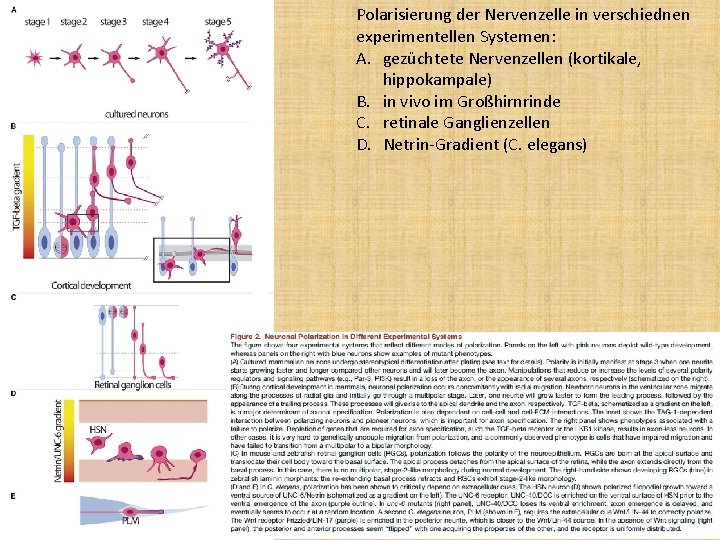
Polarisierung der Nervenzelle in verschiednen experimentellen Systemen: A. gezüchtete Nervenzellen (kortikale, hippokampale) B. in vivo im Großhirnrinde C. retinale Ganglienzellen D. Netrin-Gradient (C. elegans)

Although in culture the neurite that becomes the axon is largely a matter of chance, in vivo the initial symmetry breaking event is thought to be induced by shallow gradients of diffusible signals, such as TGF-b and neurotrophins; contact with earlier formed cells may also play a role. These small environmental signals are then amplified by positive feedback loops and interpreted by several intracellular signaling cascades that ultimately impinge on the cytoskeleton, leading to spatial differences in actin-based motility, microtubule stability, and microtubule based transport that underlie the distinct patterns of growth of axons and dendrites. Polarisierung der ursprünglich gleichwertige Fortsätze: Induktion von Axonen: kortikale Neuronen: BDNF; Neurotrophine; TGF-b retinale Ganglienzellen: Laminin Cytochalasin (Depolymerisierung von Mikrofilamenten) Induktion von Dendriten: autonome Ganglien (SCG): BMP 2, BMP 6 Drosi: hamlet (für monopolare Dendriten) und cut (für multidendritische Zellen) Gene Aktivität: weaver Mausstamm (keine Körnerzellen in der Kleinhirnrinde): Purkinje Dendritbaum

Axonogenesis From the cell biological perspective, how is it that proteins synthesized in a common compartment are differentially delivered to axonal and somatodendritic domains? In the case of membrane proteins, current evidence suggests that axonal and dendritic proteins are sorted into different vesicles as they leave the Golgi complex, then undergo selective microtubule-based transport to reach their final destinations in the cell.
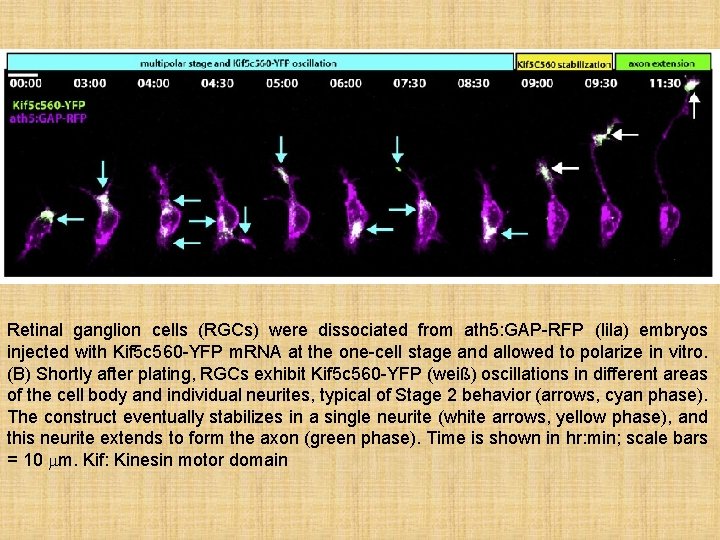
Retinal ganglion cells (RGCs) were dissociated from ath 5: GAP-RFP (lila) embryos injected with Kif 5 c 560 -YFP m. RNA at the one-cell stage and allowed to polarize in vitro. (B) Shortly after plating, RGCs exhibit Kif 5 c 560 -YFP (weiß) oscillations in different areas of the cell body and individual neurites, typical of Stage 2 behavior (arrows, cyan phase). The construct eventually stabilizes in a single neurite (white arrows, yellow phase), and this neurite extends to form the axon (green phase). Time is shown in hr: min; scale bars = 10 mm. Kif: Kinesin motor domain
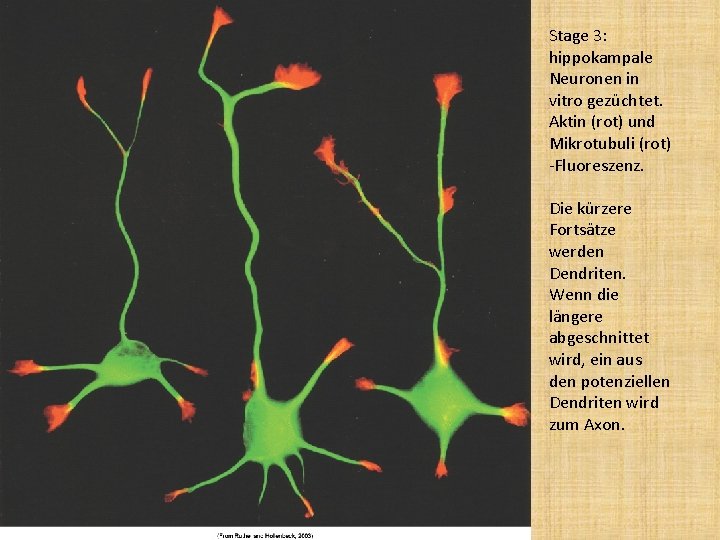
Stage 3: hippokampale Neuronen in vitro gezüchtet. Aktin (rot) und Mikrotubuli (rot) -Fluoreszenz. Die kürzere Fortsätze werden Dendriten. Wenn die längere abgeschnittet wird, ein aus den potenziellen Dendriten wird zum Axon.

• Pioneer (Bahnbrecher) und follower (Verfolger) axons • Pioneer Axonen: sollen durch Adhäsion, Leitstoffe (molecular cues, guidance) ihren Weg zu finden • Wachstumskegel (growth cone, GC) sucht nach diesem Stoffen; hier: breit, mit vielen Filopodien, Lamellipodien • Follower Axonen: binden an den Pioneer Axonen mit Zelladhäsionsmolekülen; kleiner als beim Pioneeren; schießkugelförmig, wenigere Filopodien





Wachstumskegel • Breite, distale Spitze des Axons während seines Wachstums • Viele Membranproteine (Rezeptoren) • MT und MF • zentrale und periphäre Zonen • erstmals gesehen: Ramón y Cajal
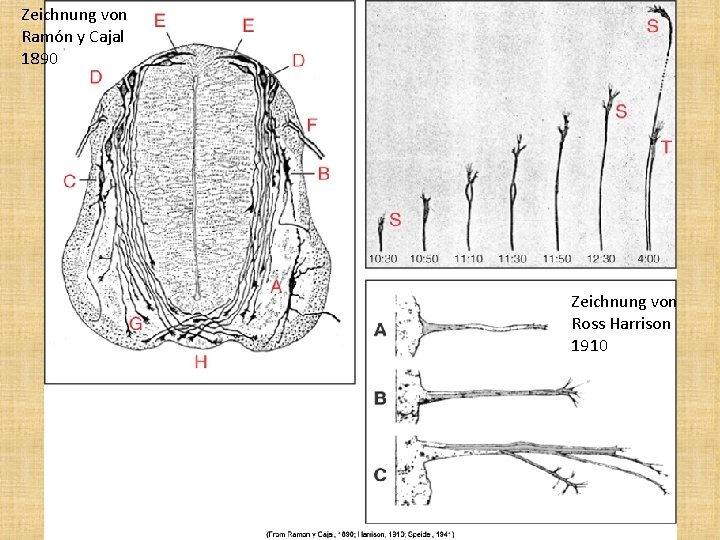
Zeichnung von Ramón y Cajal 1890 Zeichnung von Ross Harrison 1910
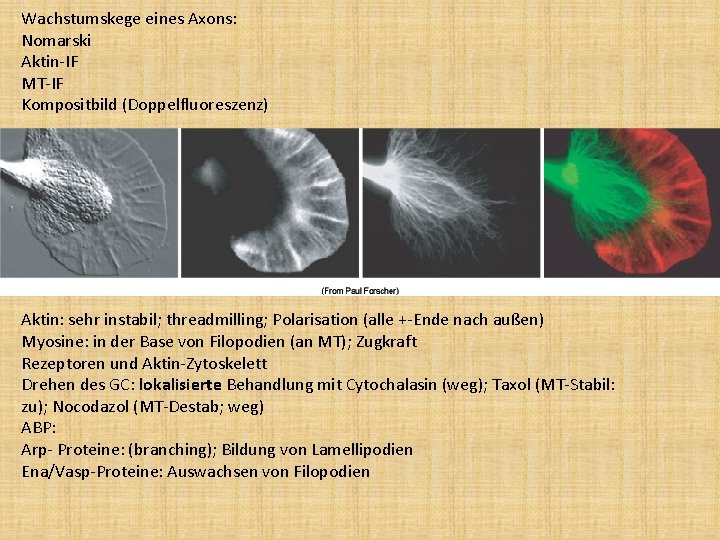
Wachstumskege eines Axons: Nomarski Aktin-IF MT-IF Kompositbild (Doppelfluoreszenz) Aktin: sehr instabil; threadmilling; Polarisation (alle +-Ende nach außen) Myosine: in der Base von Filopodien (an MT); Zugkraft Rezeptoren und Aktin-Zytoskelett Drehen des GC: lokalisierte Behandlung mit Cytochalasin (weg); Taxol (MT-Stabil: zu); Nocodazol (MT-Destab; weg) ABP: Arp- Proteine: (branching); Bildung von Lamellipodien Ena/Vasp-Proteine: Auswachsen von Filopodien

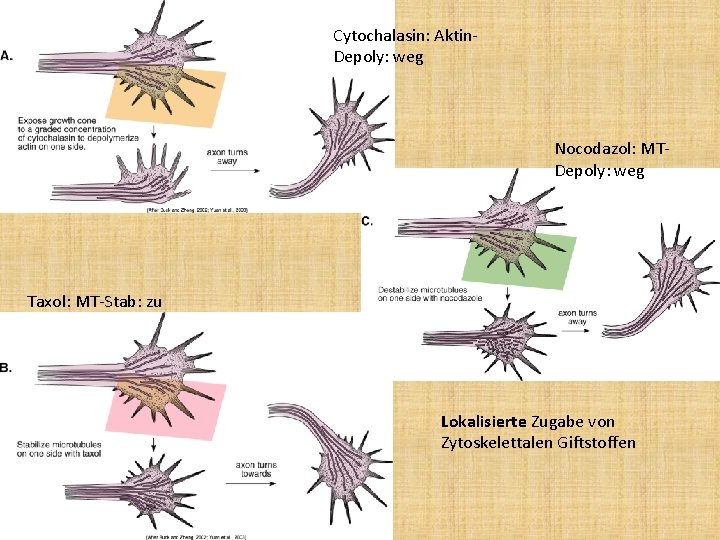
Cytochalasin: Aktin. Depoly: weg Nocodazol: MTDepoly: weg Taxol: MT-Stab: zu Lokalisierte Zugabe von Zytoskelettalen Giftstoffen

Aktin: dynamische Instabilität im GC; Ena/Vasp Lokalisation (grün) an den Aktinfilamenten (rot); Ena/Vasp: Antikapping-Protein (+-Ende)
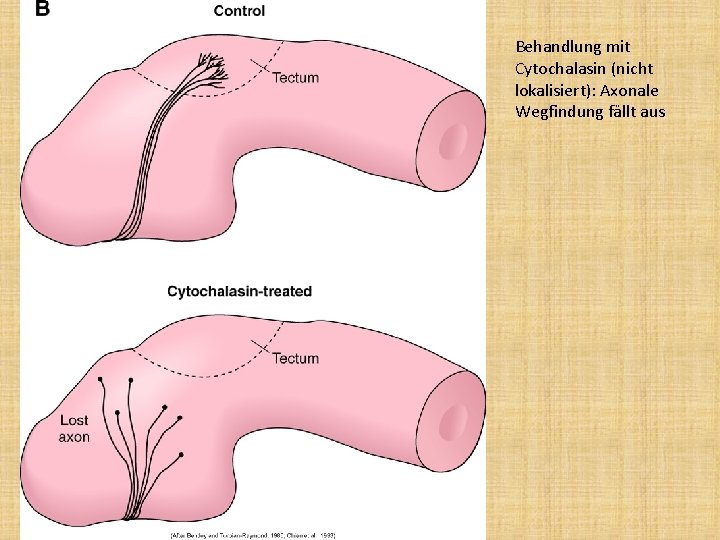
Behandlung mit Cytochalasin (nicht lokalisiert): Axonale Wegfindung fällt aus
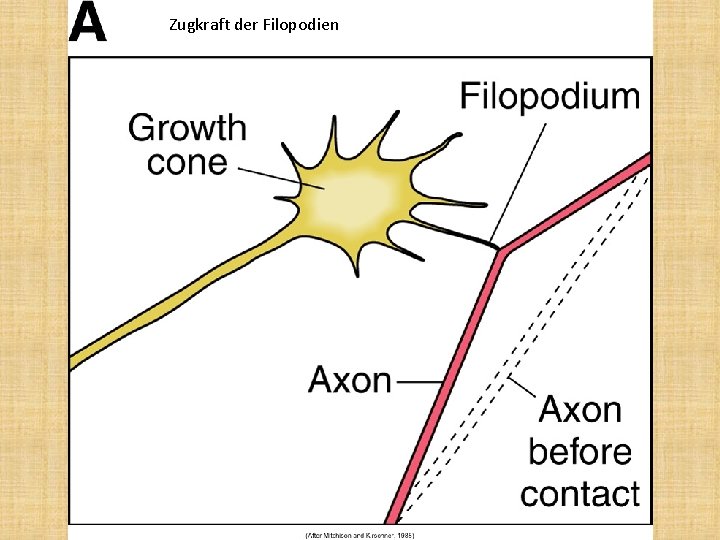
Zugkraft der Filopodien
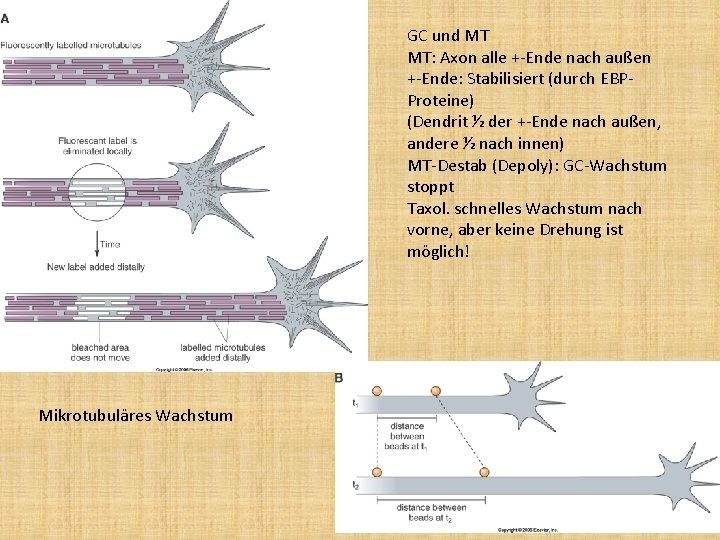
GC und MT MT: Axon alle +-Ende nach außen +-Ende: Stabilisiert (durch EBPProteine) (Dendrit ½ der +-Ende nach außen, andere ½ nach innen) MT-Destab (Depoly): GC-Wachstum stoppt Taxol. schnelles Wachstum nach vorne, aber keine Drehung ist möglich! Mikrotubuläres Wachstum
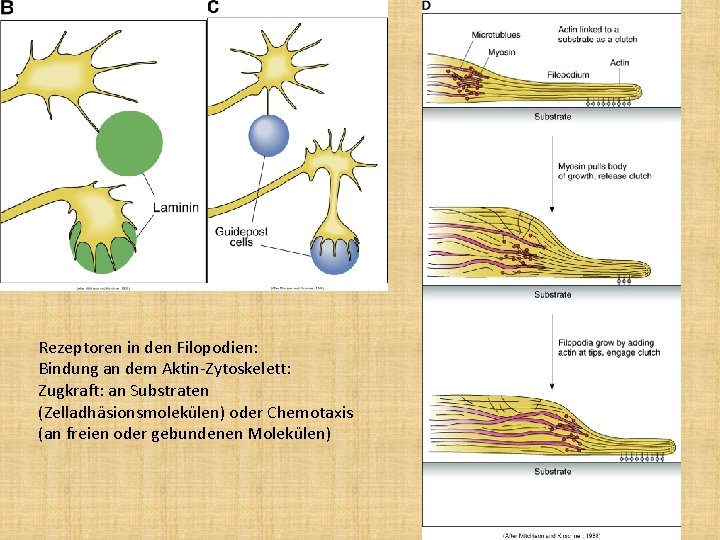
Rezeptoren in den Filopodien: Bindung an dem Aktin-Zytoskelett: Zugkraft: an Substraten (Zelladhäsionsmolekülen) oder Chemotaxis (an freien oder gebundenen Molekülen)
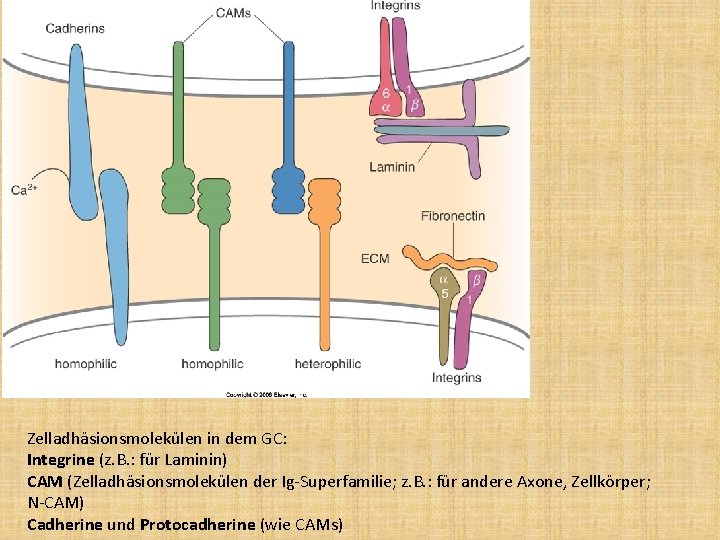
Zelladhäsionsmolekülen in dem GC: Integrine (z. B. : für Laminin) CAM (Zelladhäsionsmolekülen der Ig-Superfamilie; z. B. : für andere Axone, Zellkörper; N-CAM) Cadherine und Protocadherine (wie CAMs)
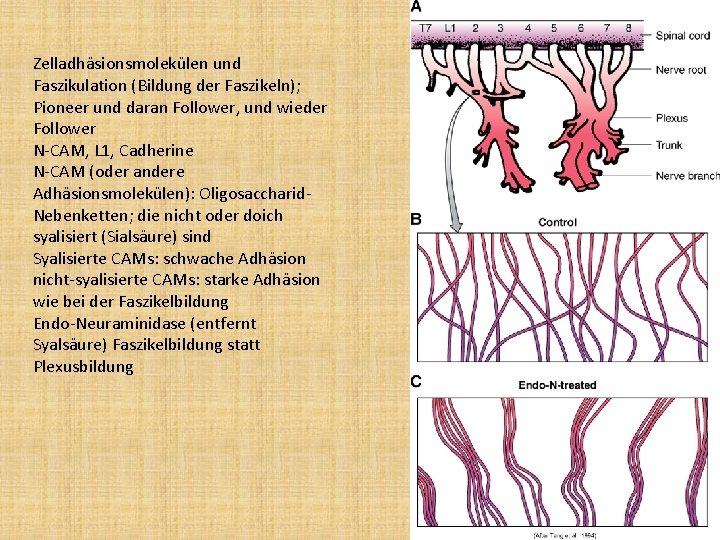
Zelladhäsionsmolekülen und Faszikulation (Bildung der Faszikeln); Pioneer und daran Follower, und wieder Follower N-CAM, L 1, Cadherine N-CAM (oder andere Adhäsionsmolekülen): Oligosaccharid. Nebenketten; die nicht oder doich syalisiert (Sialsäure) sind Syalisierte CAMs: schwache Adhäsion nicht-syalisierte CAMs: starke Adhäsion wie bei der Faszikelbildung Endo-Neuraminidase (entfernt Syalsäure) Faszikelbildung statt Plexusbildung

Signale für den Wachstumskegel • mechanische Signale (Steifheit des Substrats) • molekulare Signale: Adhäsionsmolekülen; Chemoattraktante und Repellente
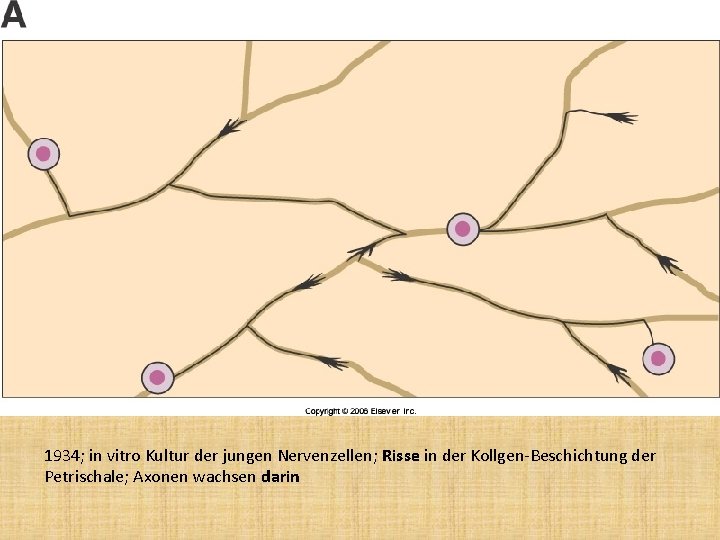
1934; in vitro Kultur der jungen Nervenzellen; Risse in der Kollgen-Beschichtung der Petrischale; Axonen wachsen darin






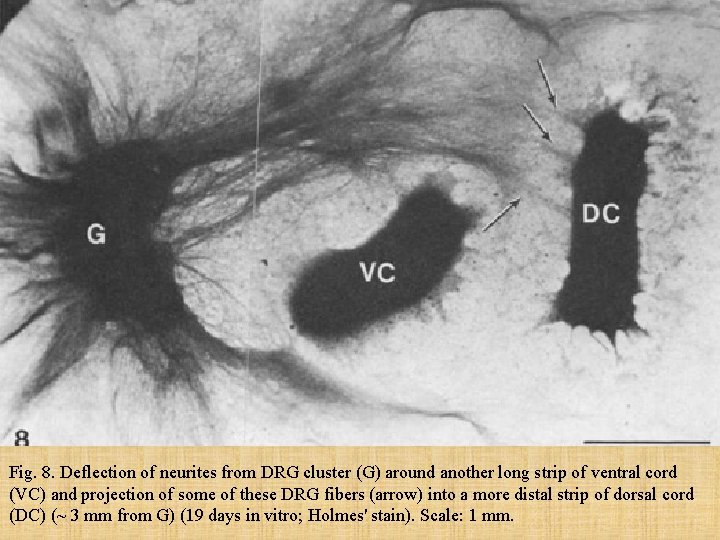
Fig. 8. Deflection of neurites from DRG cluster (G) around another long strip of ventral cord (VC) and projection of some of these DRG fibers (arrow) into a more distal strip of dorsal cord (DC) (~ 3 mm from G) (19 days in vitro; Holmes' stain). Scale: 1 mm.

(D) “Sandwich” experiment, with a stage 28 DRG placed between stage 17 dermamyotome and notochord (from the same embryo). Axons project in a bipolar manner parallel to the two sources of repellent. Scale bar: 200 mm

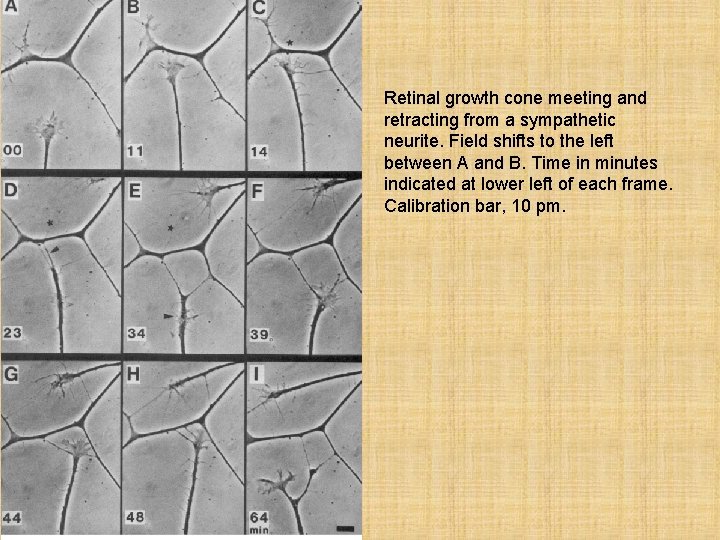
Retinal growth cone meeting and retracting from a sympathetic neurite. Field shifts to the left between A and B. Time in minutes indicated at lower left of each frame. Calibration bar, 10 pm.

Guidance molecules • Molekülen der axonalen Wegfindung (aber auch: bei den NL-Migration!) • Repellente und Chemoattraktante

Repellente • Molekülen, die eine Abwenden des Wachstumskegels verursachen (Wachstumskegel wendet sich vom der Quelle der Repellente ab) • Semaphorine und ihre Rezeptoren • Slit und sein Rezeptoren • Ephrins und ihre Rezeptoren, die Eph. Rezeptoren

Semaphorine • Semaphorine (sezernierte oder membrangebundene Proteine) werden in acht Klassen unterteilt: 1 bis 7 und V. • Klassen 1 und 2 kommen nur in Insekten und Würmern vor, Sema 3 bis 7 in Wirbeltieren, und V in Viren. • Ihre Rezeptoren: Plexine • Für Sema 3 Molekülen das Rezeptor ist heteromer (Neuropiline plus Plexin). • Wachstumskegel: exprimiert den Rezeptor.

Neuropilin KO Maus Whole-mount immunostaining with anti-neurofilament monoclonal antibody 2 H 3 of the wild-type (+/+) and homozygous mutant (-/-) embryos at 12. 5 dpc (E and F). op, ophthalmic nerve; mx, maxillary nerve. Eye pigmentation differred from embryo to embryo because the chimeric mice that were produced using TT-2 ES cells were crossed with ICR mice. Neuropilin: Ko-Rezeptor für Sema 3.

Slit • Slit Proteine: human Slit 1 -3 • repellente • ihre Rezeptor: Robo-Proteine (Robo 1 -4); Robo kommt aus „roundabout”: ohne diese Rezeptor die Nervenzellfortsätze (Drosi) gehen rund umherum, ohne ihre Zielzelle zu finden. • Das Wachstumskegel exprimiert in meisten Fällen das Robo-Protein, a lso den Rezeptor.
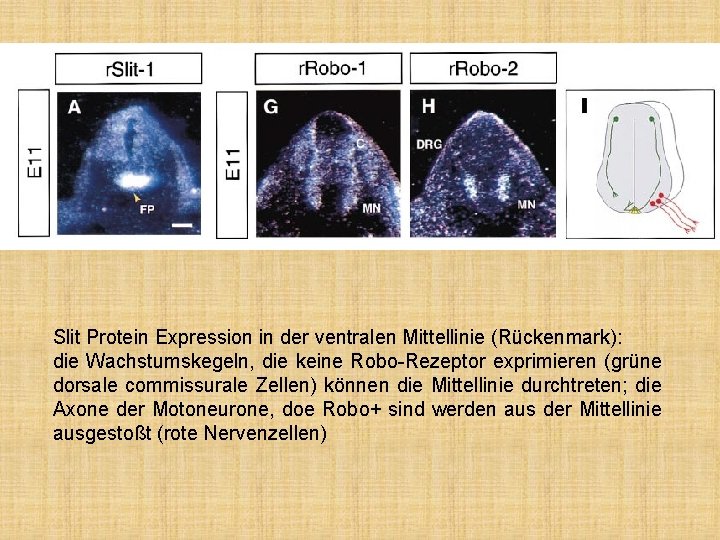
Slit Protein Expression in der ventralen Mittellinie (Rückenmark): die Wachstumskegeln, die keine Robo-Rezeptor exprimieren (grüne dorsale commissurale Zellen) können die Mittellinie durchtreten; die Axone der Motoneurone, doe Robo+ sind werden aus der Mittellinie ausgestoßt (rote Nervenzellen)

Ephrins und Eph-Rezeptoren • Ephrin: Liganden für die Eph-Rezeptoren • Eph-Rezeptoren: hinsichtlich der Bindung von Ephrine unterteilt man diese Rezeptoren in Eph. A und Eph. B Klasse (insgesamt 16 Mitglieder) • Bidirektionelle Wirkung: nicht nur die Eph-Rezeptor tragende Zellen antworten auf eine Ephrin-Signal, sondern das Ligand Ephrin tragende Zellen auch. • Für das Wachstumskegel: sie sind repellente. • In meisten Fällen: das Wachstumskegel exprimiert das Ligand (Ephrin).

Chemoattraktante • Nerve Growth Factor, NGF • Neurotroiphine • BDNF (brain derived neurotrophic factor) • Netrine
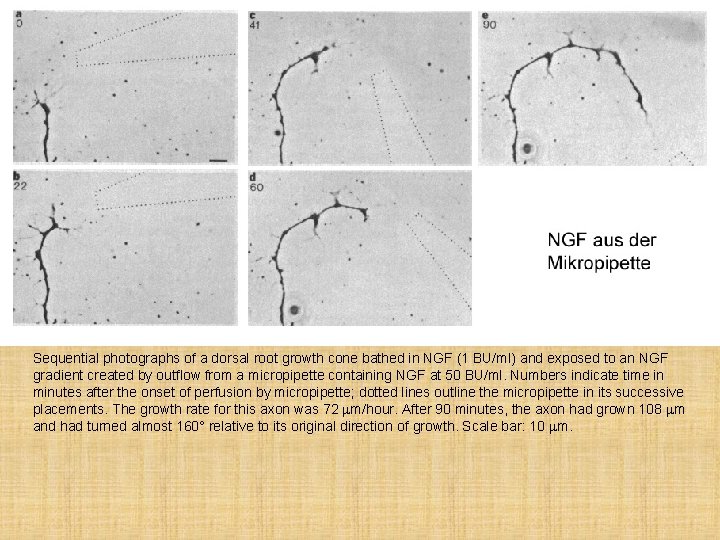
Sequential photographs of a dorsal root growth cone bathed in NGF (1 BU/ml) and exposed to an NGF gradient created by outflow from a micropipette containing NGF at 50 BU/ml. Numbers indicate time in minutes after the onset of perfusion by micropipette; dotted lines outline the micropipette in its successive placements. The growth rate for this axon was 72 mm/hour. After 90 minutes, the axon had grown 108 mm and had turned almost 160° relative to its original direction of growth. Scale bar: 10 mm.

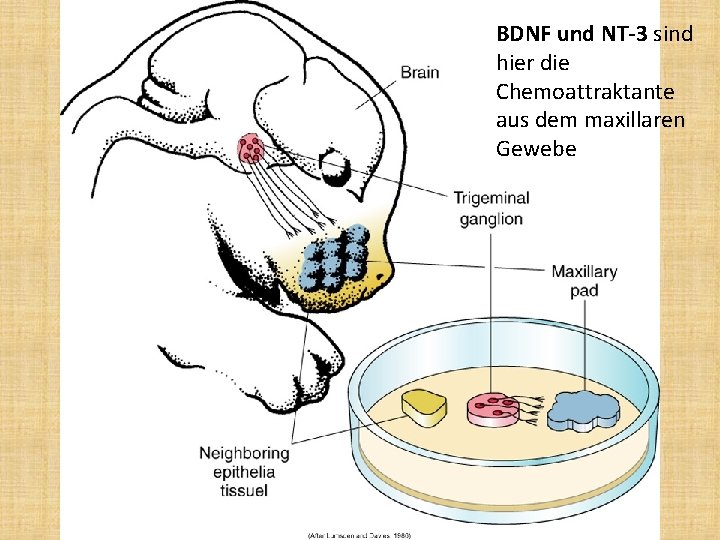
BDNF und NT-3 sind hier die Chemoattraktante aus dem maxillaren Gewebe
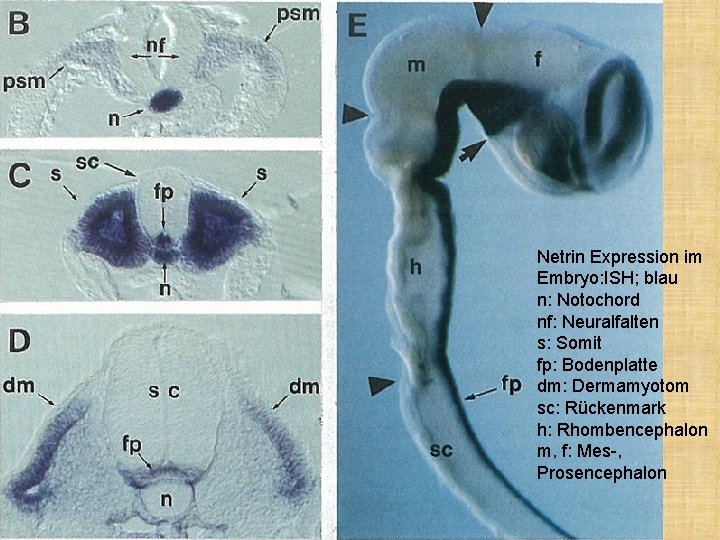
Netrin Expression im Embryo: ISH; blau n: Notochord nf: Neuralfalten s: Somit fp: Bodenplatte dm: Dermamyotom sc: Rückenmark h: Rhombencephalon m, f: Mes-, Prosencephalon
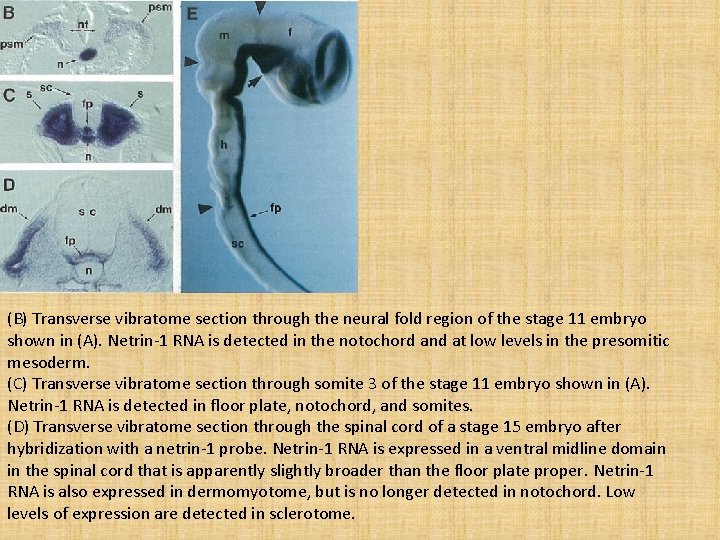
(B) Transverse vibratome section through the neural fold region of the stage 11 embryo shown in (A). Netrin-1 RNA is detected in the notochord and at low levels in the presomitic mesoderm. (C) Transverse vibratome section through somite 3 of the stage 11 embryo shown in (A). Netrin-1 RNA is detected in floor plate, notochord, and somites. (D) Transverse vibratome section through the spinal cord of a stage 15 embryo after hybridization with a netrin-1 probe. Netrin-1 RNA is expressed in a ventral midline domain in the spinal cord that is apparently slightly broader than the floor plate proper. Netrin-1 RNA is also expressed in dermomyotome, but is no longer detected in notochord. Low levels of expression are detected in sclerotome.
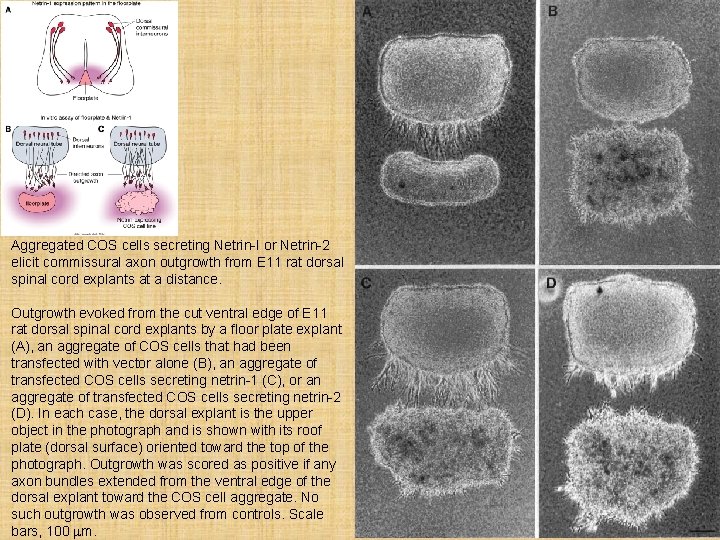
Aggregated COS cells secreting Netrin-I or Netrin-2 elicit commissural axon outgrowth from E 11 rat dorsal spinal cord explants at a distance. Outgrowth evoked from the cut ventral edge of E 11 rat dorsal spinal cord explants by a floor plate explant (A), an aggregate of COS cells that had been transfected with vector alone (B), an aggregate of transfected COS cells secreting netrin-1 (C), or an aggregate of transfected COS cells secreting netrin-2 (D). In each case, the dorsal explant is the upper object in the photograph and is shown with its roof plate (dorsal surface) oriented toward the top of the photograph. Outgrowth was scored as positive if any axon bundles extended from the ventral edge of the dorsal explant toward the COS cell aggregate. No such outgrowth was observed from controls. Scale bars, 100 mm.
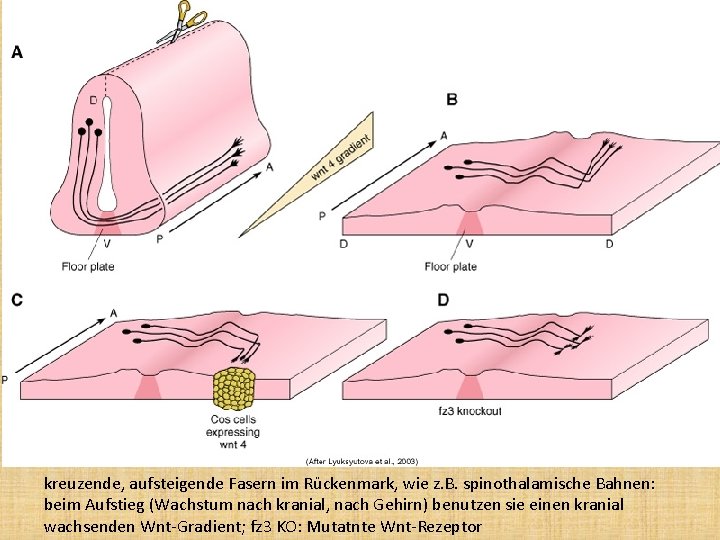
kreuzende, aufsteigende Fasern im Rückenmark, wie z. B. spinothalamische Bahnen: beim Aufstieg (Wachstum nach kranial, nach Gehirn) benutzen sie einen kranial wachsenden Wnt-Gradient; fz 3 KO: Mutatnte Wnt-Rezeptor
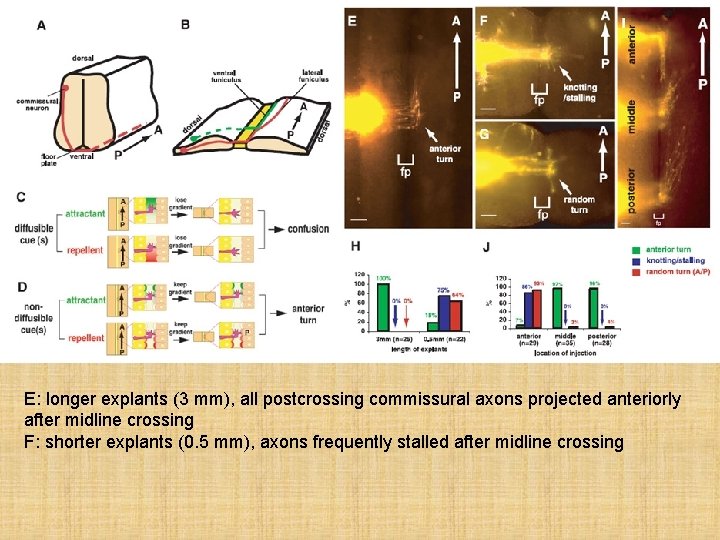
E: longer explants (3 mm), all postcrossing commissural axons projected anteriorly after midline crossing F: shorter explants (0. 5 mm), axons frequently stalled after midline crossing

Fig. 1. Chemoattractant(s) guides commissural axons along the A-P axis. (A) Transverse section of E 13 rat spinal cord showing the D-V trajectory (solid red line) and A-P trajectory (dashed red line) of commissural axons. (B) “Open-book” view of E 13 rat spinal cord showing midline crossing and anterior turning. The green subpopulation of commissural axons projects anteriorly along a medial pathway, close to the floor plate (ventral funiculus). The red subpopulation projects along the floor plate initially but gradually fans out to occupy more lateral positions (lateral funiculus). Both populations project anteriorly immediately after midline crossing. (C) Agradient of diffusible guidance cue(s) might be disrupted when explants are cut shorter, causing misrouting of commissural axons along the A-P axis. (D) Agradient of nondiffusible guidance cue(s) will not be affected when the explants are cut shorter, and the axons should still project anteriorly. (E) In longer explants (3 mm), all postcrossing commissural axons projected anteriorly after midline crossing (fp, floor plate) after 16 to 20 hours of culture. Commissural axons were labeled by lipophilic Di. I injection into the dorsal side of the explants by iontophoresis. (F) In shorter explants (0. 5 mm), axons frequently stalled after midline crossing. (G) In shorter explants (0. 5 mm), axons often projected randomly along the A-P axis. (H) Quantification of data. Anterior turn indicates normal projection. Knotting/stalling and random A-P turns are abnormal behaviors observed in shorter explants. n: number of explants. (I) A long explant (3 mm) was injected with Di. I close to the anterior end, in the middle, and at the posterior end. The axons at anterior ends are almost always misrouted (90%). (J) Quantification of the open-book assays with anterior, middle, and posterior injections. n: number of injection sites. Scale bars, 100 mm.
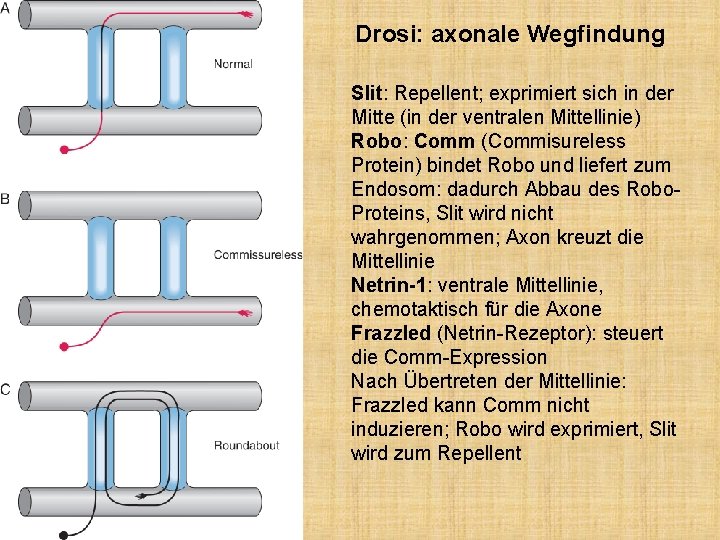
Drosi: axonale Wegfindung Slit: Repellent; exprimiert sich in der Mitte (in der ventralen Mittellinie) Robo: Comm (Commisureless Protein) bindet Robo und liefert zum Endosom: dadurch Abbau des Robo. Proteins, Slit wird nicht wahrgenommen; Axon kreuzt die Mittellinie Netrin-1: ventrale Mittellinie, chemotaktisch für die Axone Frazzled (Netrin-Rezeptor): steuert die Comm-Expression Nach Übertreten der Mittellinie: Frazzled kann Comm nicht induzieren; Robo wird exprimiert, Slit wird zum Repellent
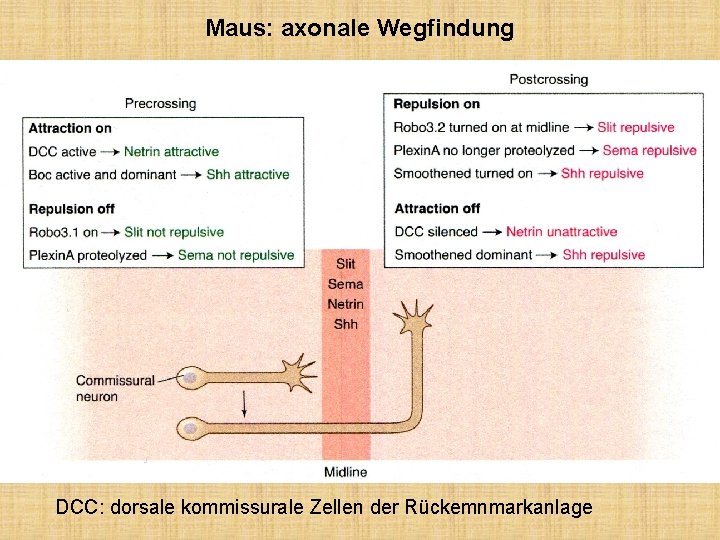
Maus: axonale Wegfindung DCC: dorsale kommissurale Zellen der Rückemnmarkanlage

Axonale Wegfindung der retinalen Ganglienzellen
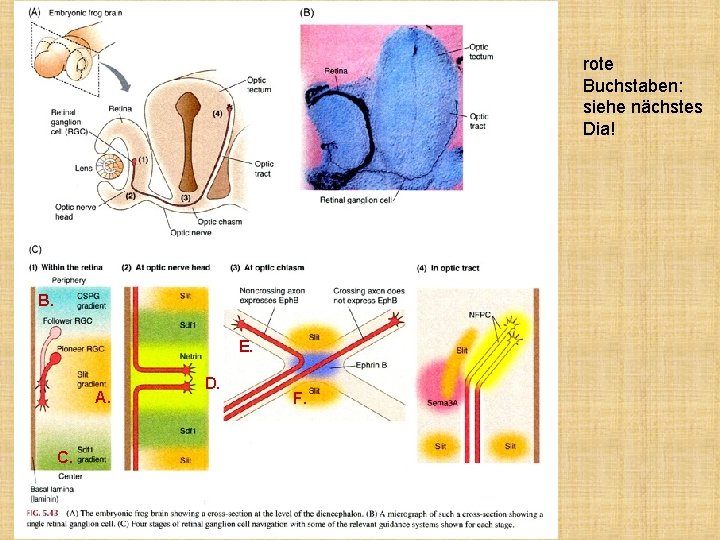
rote Buchstaben: siehe nächstes Dia! B. E. A. C. D. F.

Retinale Wegfindung des Wachstumkegels • A. Slit Gradient: immer kleiner nach vitreal (Axone der retinalen Ganglienzellen (RG) gelingen nie in den oberflächlichen Schichten) • B. periphere Retina: Chondroitinsulfat-Proteoglykan. Gradient (Gradien nimmt ab nach Papilla): die Axone der RG wachsen nach der Papilla • C. Chemoattraktant bei der Papilla: Sdf-1 Produktion • D. sehr hohe Konzentration von Netrin in der Papilla (Chemoattraktant) • E. N. opticus: Adhäsion an den schon vonrhandenen Nerven (sihe früher: Integrine, CAm, usw. )

Retinale Wegfindung des Wachstumkegels • F. Slit-Expression kranial und kaudal der Chiasma, aber nicht in der Chiasma: diese Expression fokusiert die Wachstumskegeln in die Chiasma-Mitte • F’. In der Chiasma-Mitte exprimiert sich das Ephrin Ligand. Die Wachstumskegel exprimieren Eph. B Rezeptor, wenn sie aus dem kleinen ventromedialen Retinateil kommen. Diese Axone werden aus der Chiasma abstoßen: IPSILATERALE Projektion • Die Axone aus dem übrigen Retina (dorsonasal; Maus!!) exprimieren kein Eph. B Rezeptor, so sie sind blind für das repellenede Chiasma-Signal. Diese Axone wachsen durch die Chiasma: KONTRALATERALE Projektion.


Albino Tiere und Menschen • Albino Tiere: die meiste ipsilaterale Axone weden in diesen Tieren kontralateral. • Human: wenige Daten, aber die Chiasma ist extrem schmal in diesen Patienten.


- Slides: 65