Le niveau chimique 2 Les atomes et les





















































- Slides: 63

Le niveau chimique § 2

Les atomes et les molécules • Chimie: science qui étudie la structure de la matière • Matière: substance qui occupe un volume et possède une masse • Masse: = quantité de matière, détermine le poids d’un objet sur la terre

Structure de l’atome (p. 29) • Atome = plus petite unité de matière stable • Composé de particules subatomiques: • Protons charge positive • Neutrons • Électrons charge négative • Les atomes s’attirent en fonction de leurs charges

• Atome = système solaire miniature • L’atome est formé d’un noyau et d’un nuage électronique Protons et neutrons au centre de l’atome, dans le noyau ( dense, charge positive ) Électrons tournent autour du noyau ( charge négative) = nuage électronique La plus grande partie du volume d’un atome est vide, presque toute sa masse est concentrée dans le noyau qui se trouve au centre

Les molécules (p. 29) • Molécule: - interaction entre deux atomes - création d’une structure plus grosse et plus complexe

Principaux éléments du corps humain • p. 31 • 13 éléments les plus courants • Oligoéléments • Connaitre le symbole chimique (13 él. ) • Pouvoir citer quelques oligoéléments

Électrons / niveaux d’énergie • Les atomes sont électriquement neutres • Augmentation du numéro atomique • Nuage électronique / séquence structurée du niveau d’énergie • Trajet complexe autour du noyau • Première couche / niveau d’énergie le plus bas

Éléments réactifs • Niveau d’énergie le plus externe = surface de l’atome • Niveaux d’énergie incomplets = recherche de stabilité en complétant le niveau d’énergie externe • Niveau d’énergie externe complet = atome stable et réagissant peu avec les autres atomes

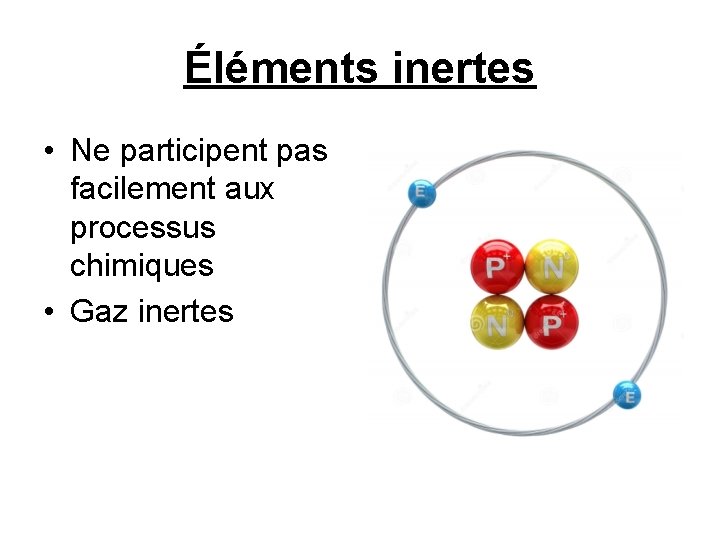
Éléments inertes • Ne participent pas facilement aux processus chimiques • Gaz inertes

Éléments réactifs / stabilité • Les éléments réactifs / niveau d’énergie incomplet / interaction ou combinaison facile avec d’autres atomes • Stabilité = gagner, perdre ou mettre en commun électron de la couche externe • Perte électron au niveau d’énergie ext. = atome n’est plus électriquement neutre (possède plus de protons que d’électrons) • Atome charge nette positive = ion positif = cation • p. 33

Éléments réactifs / stabilité • Compléter le niveau d’énergie ext. • Obtenir des électrons auprès d’autres atomes • N’est plus électriquement neutre (possède plus d’électrons que de protons) • Atome charge nette négative = ion négatif = anion

Liaisons chimiques • Interactions qui stabilisent le niveau d’énergie ext. • Retiennent ensemble les atomes lorsque la réaction est terminée • Ioniques et covalentes • Liaison chimique = nouvelles entités chimiques crées = molécules et composés • Composé: substance chimique composée de deux ou plusieurs atomes différents

Liaisons ioniques • Attraction électrique anions / cations • Transfert d’un ou plusieurs électrons - atome perdant - atome gagnant

Liaisons covalentes • Mise en commun des électrons avec d’autres atomes • Molécule = structure chimique d’atomes réunis par une liaison covalente • Molécule non polaire = ne possède pas de charge • Hydrogène, oxygène, dioxyde de carbone • p. 35

Liaisons covalentes avec partage inégal d’électrons • Ex. molécule d’eau (H 2 O) • Molécule polaire (H lég + /O lég -) • Il y a deux atomes H (charges lég +) qui vont être attirées par des charges lég – • Changement de la forme des molécules ou rapprochement des molécules voisines • Liaisons hydrogènes

Les réactions chimiques (p. 37) • Création de nouvelles liaisons entre des atomes • Les réactifs sont réorganisés pour former de nouvelles substances : les produits • Métabolisme = ensembles des réactions chimiques dans les cellules et les tissus du corps • Cellule = usine de produits chimiques

Travail / énergies • Travail: mouvement d’un objet ou changement de la structure physique • Énergie: capacité à effectuer un travail • Énergie cinétique: mouvement • Énergie potentielle: sous forme stockée

Énergie d’activation / enzymes / catalyseurs (p. 39) • Énergie d’activation: quantité d’énergie nécessaire pour activer une réaction • Enzymes: protéines particulières qui interviennent dans la plupart des réactions complexes de l’organisme, facilitent les réactions chimiques, font parties des catalyseurs • Catalyseurs: accélèrent les réactions chimiques, sans être modifiés • Les réactions enzymatiques sont en général réversibles

La voie métabolique • • Réactions complexes néc. à la vie Suite d’étapes reliées Régies par une enzyme précise Énergie d’activation / déclenchement d’une réaction chimique • Réactions exothermiques / endothermiques

Types de réactions chimiques • Dégradation, hydrolyse, catabolisme • Synthèse, synthèse par déshydratation, anabolisme, métabolisme • Échange • p. 40 -41

Eau • Le plus important et le plus abondant dans le corps • Env. 2/3 masse corporelle • Variation de la quantité d’eau dans le corps = peut avoir des conséquences fatales


Propriétés de l’eau • • Lubrification Réactivité Grande capacité thermique Solubilité

Lubrification • Peu de friction entre les molécules d’eau • Mince couche d’eau entre deux surfaces = diminution importante de la friction • L’eau réduit la friction dans les articulations et les cavités corporelles

réactivité • Des réaction chimiques se produisent dans l’eau • Les molécules d’eau participent à certaines réactions (hydrolyse, synthèse) • • exemples digérer des aliments permet le transport des nutriments, des déchets support des sécrétions (salive, mucus, suc gastrique, bile ), des hormones

Grande capacité thermique • Capacité d’absorber de la chaleur et de la conserver (liaisons hydrogène) • Vapeur d’eau • Transpiration • Inertie thermique

Grande capacité thermique • Exemples: • absorbe ou dégage une grande quantité de chaleur avant que la T° corporelle ne change de façon marquée • empêche les changements soudains de température (facteurs externes, rayons du soleil, exposition au vent, ou processus internes, activité musculaire intense qui libère une importante quantité de chaleur) • permet au corps de transpirer, en s’évaporant l’eau prélève de la chaleur, refroidit la peau et permet ainsi au corps de maintenir une température constante

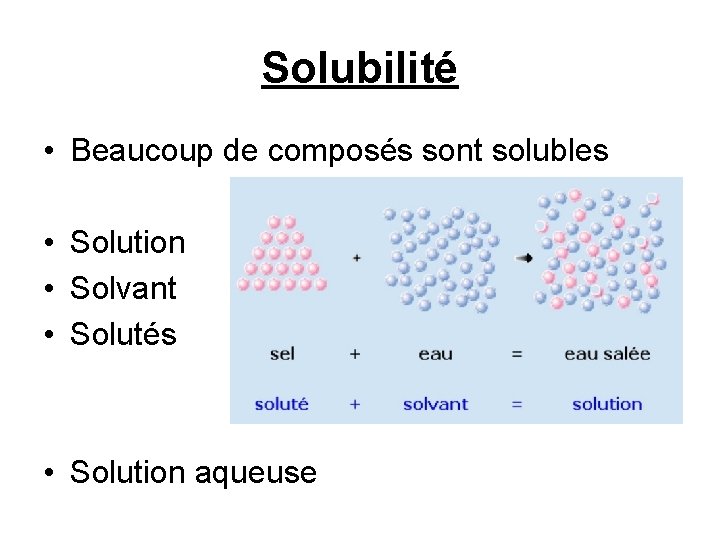
Solubilité • Beaucoup de composés sont solubles • Solution • Solvant • Solutés • Solution aqueuse

L’eau • l’eau n’est pas nécessaire à la vie, l’eau c’est la vie (A. de Saint-Exupéry) • l’eau facilite le déroulement de tous les processus biologiques et sans elle la vie n’est pas possible • l’eau du corps, donc 99% de nos cellules se renouvelle tous les 10 jours • l’eau que l’on ingère quotidiennement deviendra l’eau qui nous constitue • l’eau de notre corps est notre mer intérieure

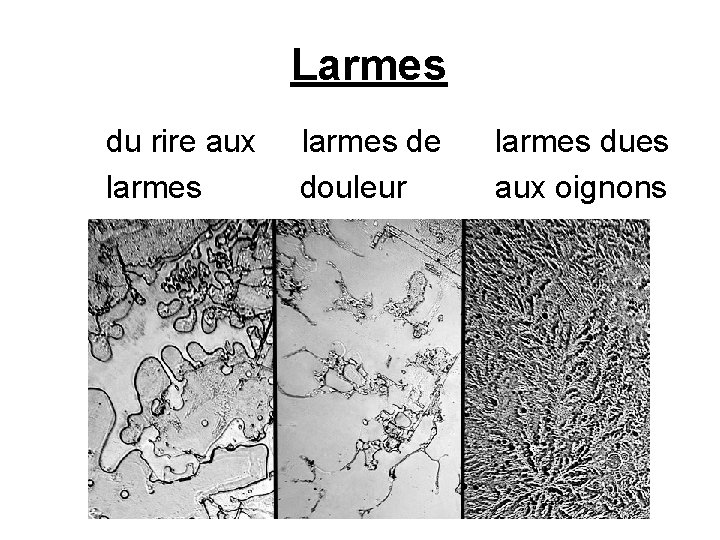
Rose Lynn Fischer analyse les larmes • Larmes lors d’une catastrophe nationale • Larmes de changement

Larmes • Pleurs • Larmes de rire jusqu’aux pleurs

Larmes du rire aux larmes de douleur larmes dues aux oignons

Masaru Emoto

Électrolytes (p. 44) • = composés solubles(dont les ions) • peuvent conduire un courant électrique dans une solution • les forces électriques qui traversent les membranes cellulaires ont une incidence sur le fonctionnement de toutes les cellules • interviennent par exemple dans - la propagation de l’influx nerveux - la contraction musculaire, la coagulation sanguine - le transport d’O 2, la perméabilité des cellules - le métabolisme et bien d’autres réactions

Hydrophiles / hydrophobes • Molécules hydrophiles: interagissent facilement avec les molécules d’eau, se lient fortement à l’eau (ex: glucose) • Molécules hydrophobes: ne se dissolvent pas lorsqu’elles sont exposées à l’eau, elles n’interagissent pas facilement avec les molécules d’eau (ex: huiles et graisses)

Concentration • = quantité de soluté par unité de volume de solution (gr/litre) • Une variation d’une de concentration en dehors des valeurs normales peut être une indication d’une maladie • Ex: analyse sanguine

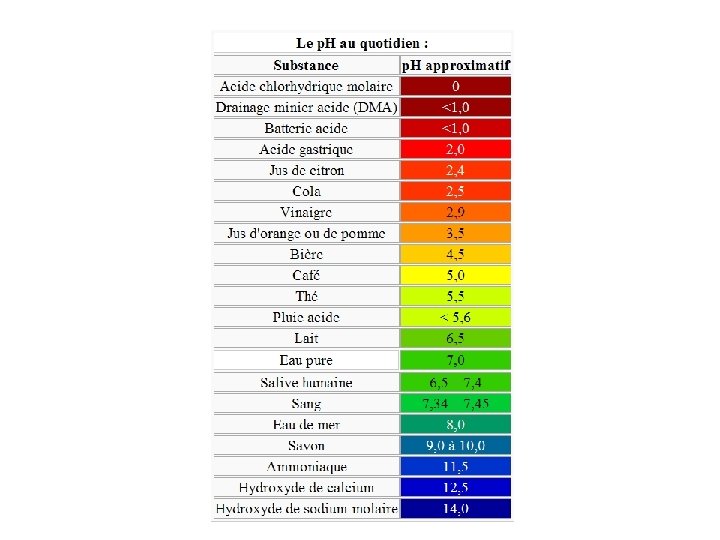
Régulation du p. H (p. 46) • La régulation du p. H des liquides corporels est essentielle au maintien de l’homéostasie • Ion hydrogène H+, extrêmement réactif • Concentration des ions hydrogène dans les liquides corporels influe sur les processus physiologiques • Échelle de p. H: de 0 à 14

p. H du sang • Varie normalement entre 7, 35 et 7, 45 • Fluctuations du p. H • Acidose: baisse du p. H sanguin en dessous de 7, 35 • Alcalose: p. H anormalement élevé, audelà de 7, 45 • p. H supérieur à 7, 8: contractions des muscles squelettiques incontrôlables et constantes


Acide • • • Soluté qui se dissocie dans une solution Libère des ions hydrogène Abaisse le p. H Donneur de protons Ex: acide chlorhydrique HCl = H+ et Cl-

Base • Soluté qui enlève des ions hydrogène dans une solution • Agit comme un accepteur de protons • Libère des ions hydroxyde (OH) forte affinité avec les ions hydrogène pour former des molécules d’eau

Les tampons • Composés qui stabilisent le p. H d’une solution • Enlèvent ou remplacent des ions hydrogène • Sont constitués d’acides et de bases faibles, ne se dissocient pas complètement • Les tampons et systèmes tampons des liquides corporels permettent de maintenir le p. H dans les limites normales

Sels • • Composé ionique formé soit d’un cation(+), sauf ion hydrogène d’un anion (-), sauf ion hydroxyde Sont maintenu par des liaison ioniques = se dissolvent complètement dans l’eau • Ex: Na. Cl

Métabolites / nutriments • Métabolites: molécules métabolisées à l’intérieur du corps humain • Nutriments: métabolites essentiels qui proviennent du régime alimentaire Deux grandes catégories: - Composés organiques - Composés inorganiques

Composés organiques • Contiennent toujours du carbone et de l’hydrogène, généralement aussi oxygène • Glucides, lipides, protéines et acides nucléiques (produits par les organismes vivants)

Composés inorganiques • La plupart n’ont pas le carbone et l’hydrogène comme principaux constituants structuraux • Oxygène, eau, acides forts, bases fortes, sels

Glucides • Sucres, amidon • Composent environ la moitié du régime alimentaire • Sources d’énergie (catabolisées plutôt que stockées) • Participent à la structure de certaines composantes cellulaires (membrane cellulaire) • Principaux glucides utiles à l’organisme (p. 50)

Lipides • Graisses, huiles, cires • La plupart sont insolubles dans l’eau, mécanismes spéciaux pour leur transport dans le sang • Dépôts de lipides = réserves d’énergie (homme: 12 -18% poids total, femme 18 -24%) • Principaux lipides utiles à l’organisme (p. 53)

Acide gras saturé / insaturé • Acide gras: longue chaine de carbone et atomes d’hydrogène(= queue), tête • Acide gras saturé: chaque atome de carbone de la queue possède quatre liaisons covalentes simple • Acide gras insaturé: une ou plusieurs liaisons covalentes simples sont remplacées par des liaisons covalentes doubles

Acide gras insaturé • Chaque atome de carbone avec une liaison covalente double se lie a une seul atome d’hydrogène (plutôt qu’à deux) • =changement de forme de la queue • =changement de manière dont l’organisme va métaboliser l’acide gras • Mono-insaturé: une liaison double • Polyinsaturé: plusieurs liaison double

Graisses • Les acides gras doivent se fixer au glycérol (composé) pour former des chaines • Monoglycéride: glycérol et un acide gras • Diglycéride: glycérol et deux acides gras • Triglycéride: glycérol et trois acides gras (graisses les plus courantes de l’organisme) • p. 63 lire et résumer le texte: «bonne nouvelle, tous les gras ne sont pas mauvais»

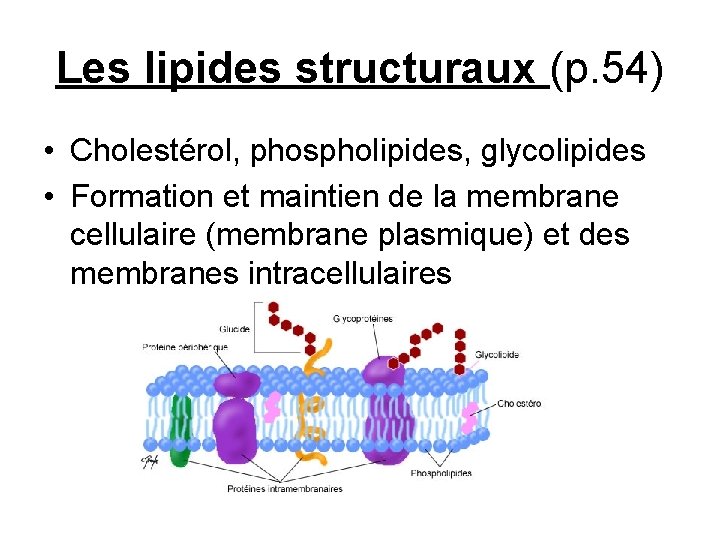
Les lipides structuraux (p. 54) • Cholestérol, phospholipides, glycolipides • Formation et maintien de la membrane cellulaire (membrane plasmique) et des membranes intracellulaires

Les stéroïdes • Grosses molécules de lipides • Structure particulière en forme d’anneaux de carbone • Cholestérol: entretien membrane plasmique, croissance et division de la cellule • Cortisol: hormone produite par les surrénales, rôle important lors de stress à long terme • Œstrogènes, testostérone: hormones sexuelles, régulation de la fonction sexuelle

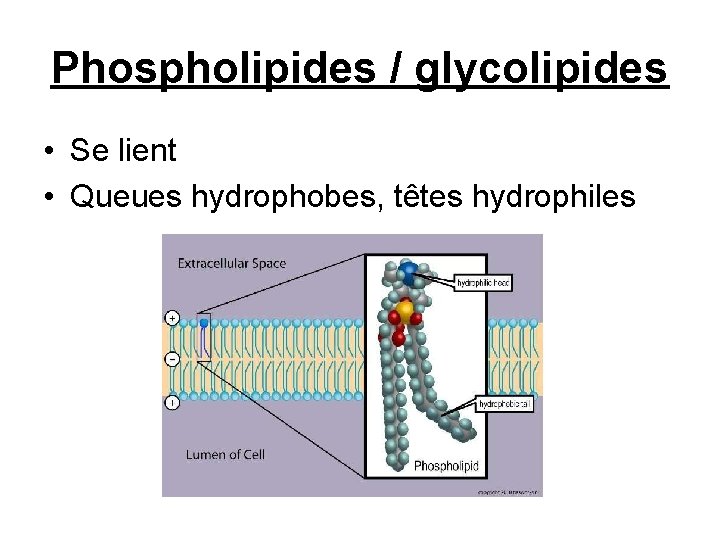
Phospholipides / glycolipides • Se lient • Queues hydrophobes, têtes hydrophiles

Les protéines • Constituant organique le plus abondant dans le corps humain (20% du poids) • Nombreuses protéines différentes • Contiennent toutes du carbone, de l’oxygène et de l’azote, et év. un peu de soufre et phosphore • Composées de molécules organiques: acides aminés

Les acides aminés • 20 sont présents en grandes quantités dans l’organisme • Une protéine typique = 1000 a. a • Les plus grosses 100’ 000 ou plus • Liaison entre les a. a: liaison peptidique • Peptide: molécules formées de a. a • Dipeptide: molécule qui contient deux a. a • Tripeptide: trois a. a • Polypeptide: chaînes de peptides • Protéines: contient plus de 100 a. a

Dénaturation des proteines • T° corporelle dépasse les valeurs normales = changement de forme des protéines et détérioration de la fonction enzymatique • T° sup à 43° = issue fatale (mort) • Les variations importantes de p. H peuvent aussi dénaturer les protéines

Les enzymes (p. 58) • Sont des protéines qui assurent d’importantes fonctions de régulation • Enzymes spécifiques • Substrats: réactifs des réactions enzymatiques • Site actif • Complexe enzyme-substrat • Énergie d’activation / produit fini

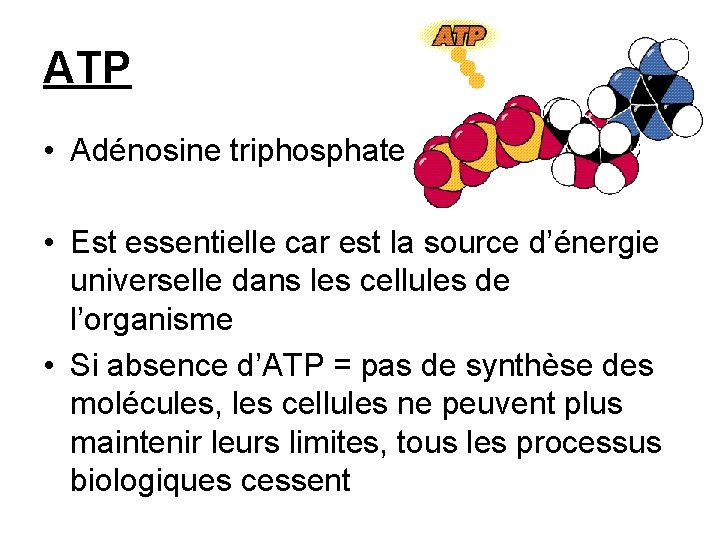
ATP: adénosine triphosphate • = énergie (c’est un composé de grande énergie qui contient des liaisons de grande énergie) • Rupture des liaisons covalentes = libération d’énergie • L’ATP fournit l’énergie nécessaire à de nombreuses fonctions vitales (contraction musculaire, synthèse des protéines, glucides, lipides)

ATP • Adénosine triphosphate • Est essentielle car est la source d’énergie universelle dans les cellules de l’organisme • Si absence d’ATP = pas de synthèse des molécules, les cellules ne peuvent plus maintenir leurs limites, tous les processus biologiques cessent

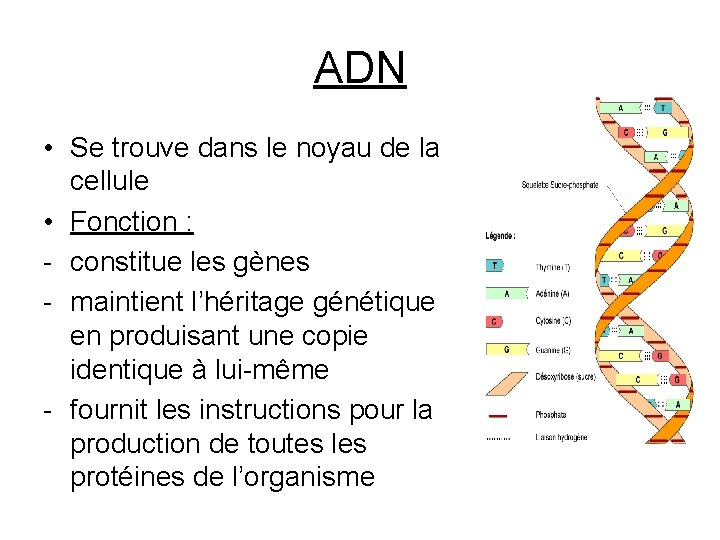
Acides nucléiques: ADN/ARN • ADN acide désoxyribonucléique • ARN acide ribonucléique • Rôle fondamental : stocker et transférer l’information (synthèse des protéines) • Sous-unité acides nucléiques: nucléotides • constituent les gênes qui déterminent quel type d’organisme nous sommes, notre croissance, notre développement • Lire attentivement p. 63 l’identification génétique

ADN • Se trouve dans le noyau de la cellule • Fonction : - constitue les gènes - maintient l’héritage génétique en produisant une copie identique à lui-même - fournit les instructions pour la production de toutes les protéines de l’organisme

ARN • Se trouve dans le cytoplasme de la cellule • Fonction : - assure la synthèse des protéines en suivant l’instruction de l’ADN