PHOTOPOLYMERISATION PRINCIPES APPLICATIONS Laurence LECAMP Matre de confrences













































- Slides: 67

PHOTOPOLYMERISATION : PRINCIPES & APPLICATIONS Laurence LECAMP Maître de conférences à l’IUFM de Haute-Normandie Laboratoire de Matériaux Macromoléculaires INSA de Rouen – CNRS FRE 3101 PBS 76131 MONT SAINT AIGNAN CEDEX Congrès national des Professeurs de Physique et de Chimie - 27 au 30 Octobre 2008 - Rouen

Introduction

Plan de l’exposé I – Rappels sur la polymérisation II – Généralités sur la photopolymérisation III – Avantages et applications du procédé de photopolymérisation IV – Quelques problématiques liées au procédé de photopolymérisation 3

I – Rappels sur la polymérisation

I. 1. Définitions n Polymère : substance constituée de macromolécules n Macromolécule : molécule de masse molaire élevée dont la structure résulte essentiellement de la répétition d’unités dérivées, de fait ou conceptuellement, de molécules de faible masse molaire (IUPAC) n Monomère : molécule pouvant être polymérisée et contribuant à la formation d’unités constitutives et à la structure principale de la 5

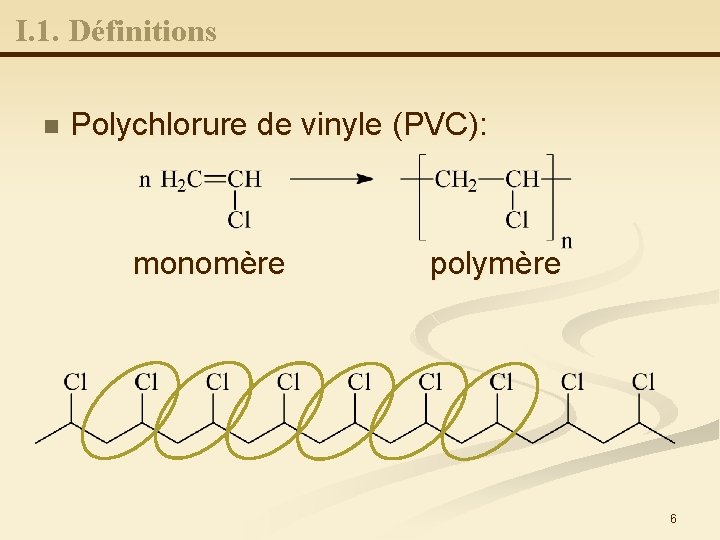
I. 1. Définitions n Polychlorure de vinyle (PVC): monomère polymère 6

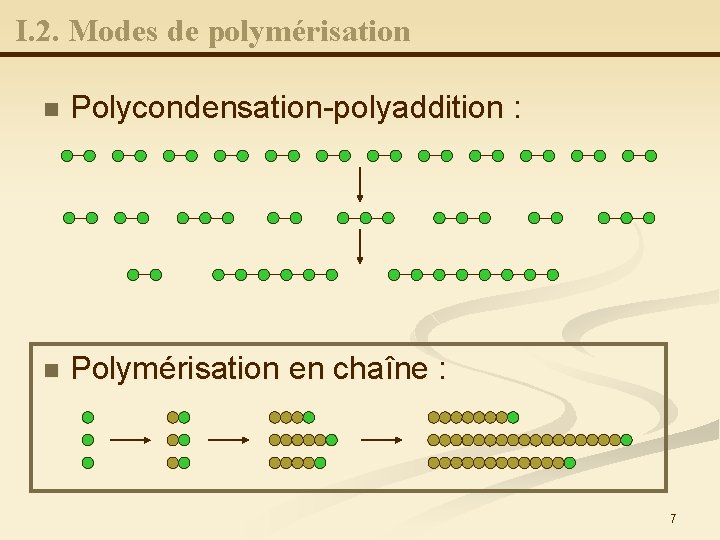
I. 2. Modes de polymérisation n Polycondensation-polyaddition : n Polymérisation en chaîne : 7

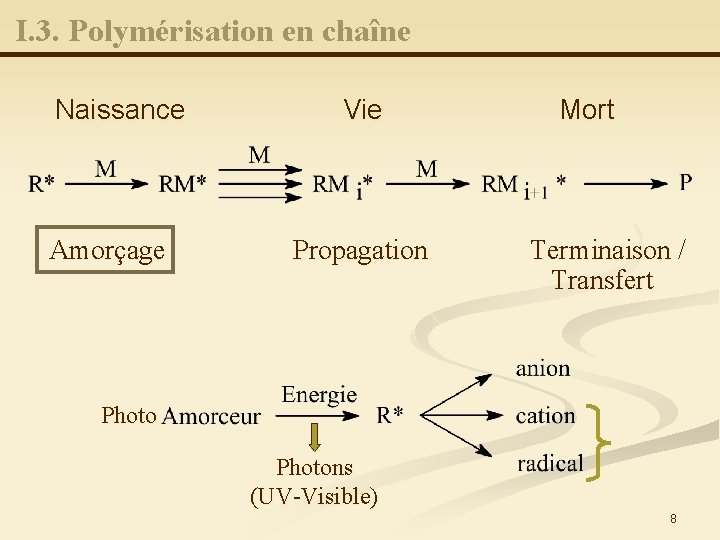
I. 3. Polymérisation en chaîne Naissance Amorçage Vie Propagation Mort Terminaison / Transfert Photons (UV-Visible) 8

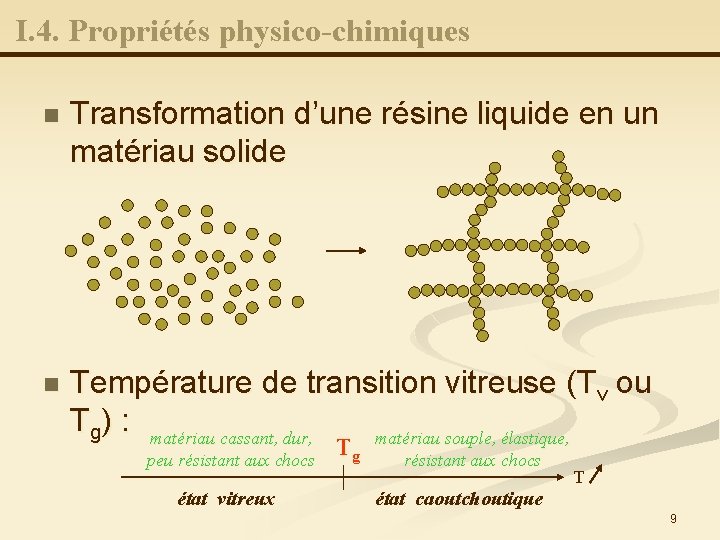
I. 4. Propriétés physico-chimiques n Transformation d’une résine liquide en un matériau solide n Température de transition vitreuse (Tv ou Tg) : matériau cassant, dur, matériau souple, élastique, peu résistant aux chocs état vitreux Tg résistant aux chocs T état caoutchoutique 9

II – Généralités sur la photopolymérisation

II. 1. Formulation photopolymérisable n Réaction rapide (excellente absorption et très grande réactivité du système photosensible) n Facilité de mise en œuvre (solubilité / compatibilité des différents constituants, viscosité de la formulation …) n Sécurité des produits employés (pas d’odeur, pas de toxicité …) n Propriétés finales correspondant à celles recherchées (pas de jaunissement, pas de composés extractibles, bonne stabilité dans le temps, propriétés diverses et variées en fonction de la nature des applications …) 11

II. 1. Formulation photopolymérisable Oligomère (résine) : courte chaîne polymère terminée, à chaque extrémité, par une fonction réactive polymérisable réseau polymère tridimensionnel propriétés caractéristiques n Système photosensible libération d’espèces réactives envers le groupement fonctionnel de l’oligomère n n Monomère ajustement de la viscosité Additifs de formulation : stabilisants, agents mouillants, charges, pigments … n 12

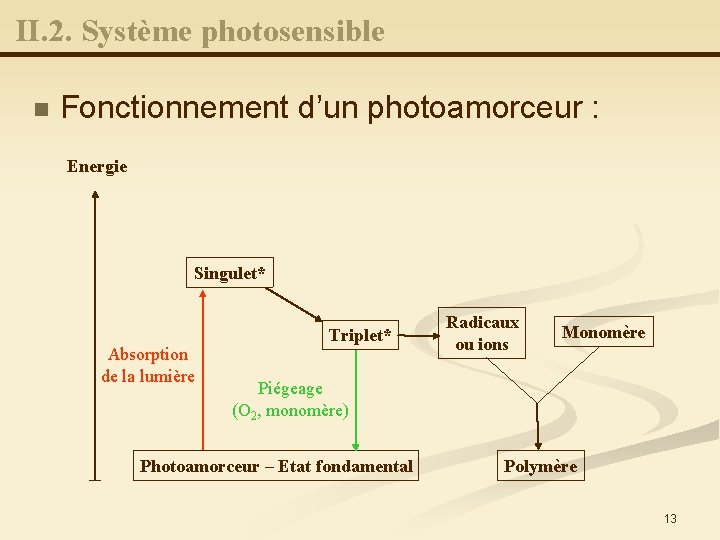
II. 2. Système photosensible n Fonctionnement d’un photoamorceur : Energie Singulet* Absorption de la lumière Triplet* Radicaux ou ions Monomère Piégeage (O 2, monomère) Photoamorceur – Etat fondamental Polymère 13

II. 2. Système photosensible n Critères d’efficacité d’un photoamorceur : n forte réactivité des centres actifs vis-à-vis des groupements fonctionnels 14

II. 2. Système photosensible n Photoamorceurs radicalaires : Norrish II n Photoamorceurs cationiques : 15

II. 2. Système photosensible n Critères d’efficacité d’un photoamorceur : n forte réactivité des centres actifs vis-à-vis des groupements fonctionnels n rendement quantique élevé n courte durée de vie des états excités singulet et triplet (quelques nanosecondes) pour éviter leur désactivation par l’oxygène moléculaire ou le monomère n forte absorption dans le domaine d’émission 16

II. 2. Système photosensible Photoamorceur de type acétophénone : 17

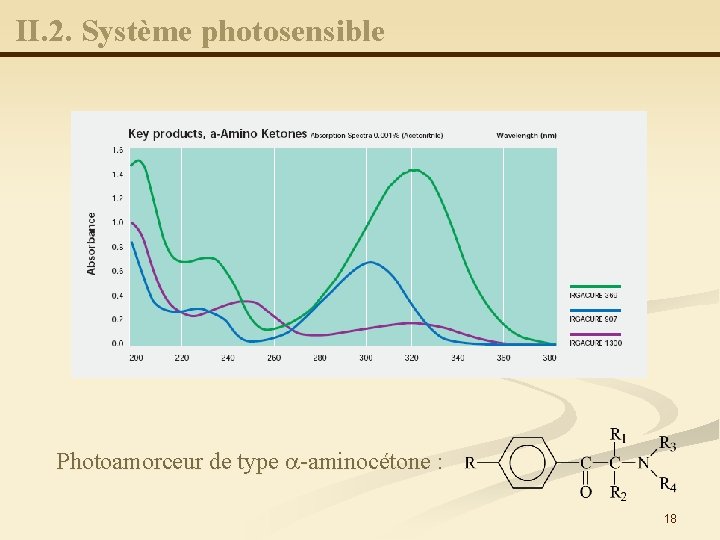
II. 2. Système photosensible Photoamorceur de type a-aminocétone : 18

II. 2. Système photosensible Photoamorceur de type acylphosphine : 19

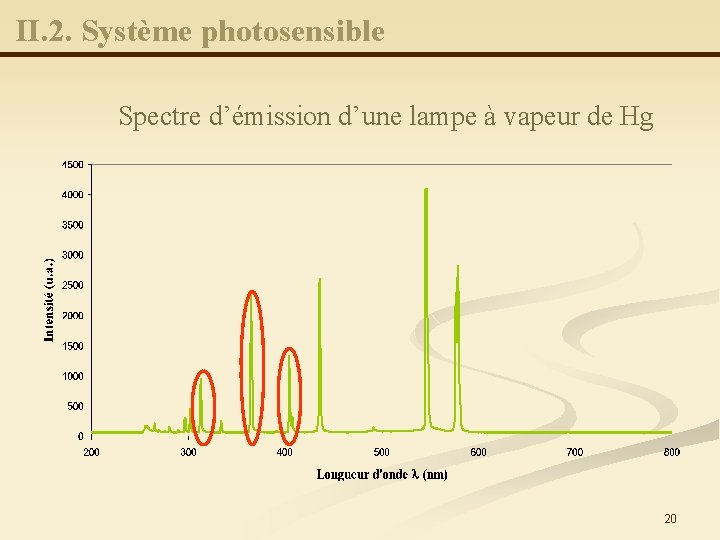
II. 2. Système photosensible Spectre d’émission d’une lampe à vapeur de Hg 20

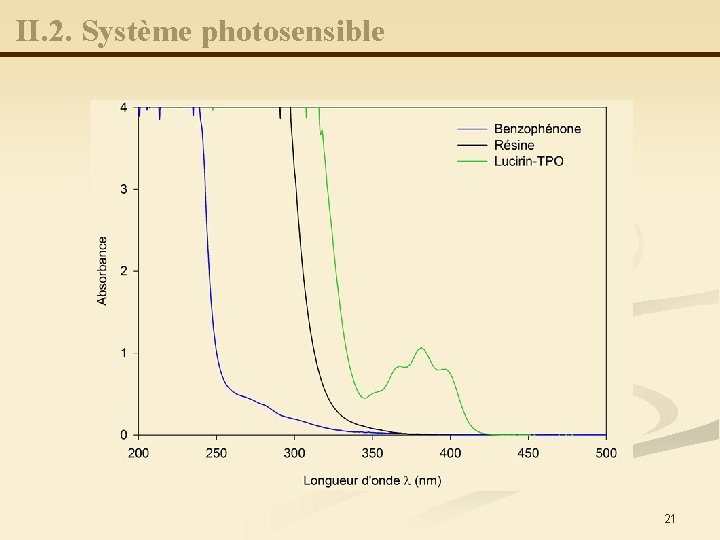
II. 2. Système photosensible 21

II. 2. Système photosensible 22

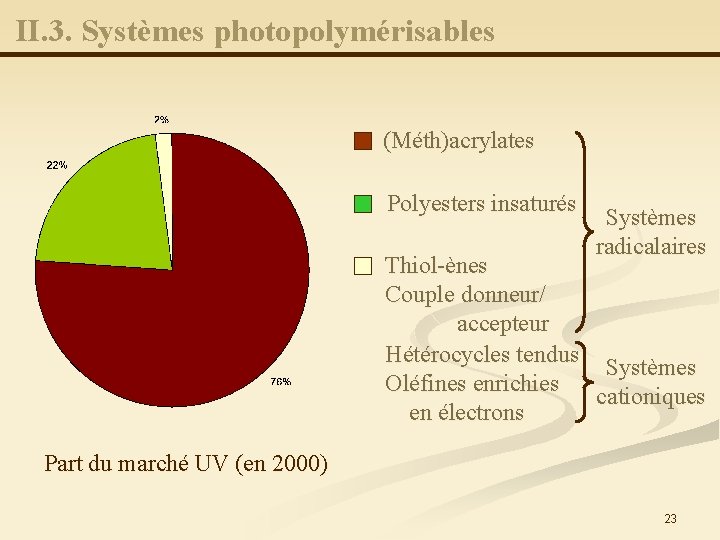
II. 3. Systèmes photopolymérisables (Méth)acrylates Polyesters insaturés Systèmes radicalaires Thiol-ènes Couple donneur/ accepteur Hétérocycles tendus Systèmes Oléfines enrichies cationiques en électrons Part du marché UV (en 2000) 23

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Résines (méth)acryliques : n Oligomère : n Principe : polymérisation en chaîne des doubles liaisons acryliques obtention de réseaux fortement réticulés (très denses) 24

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Résines (méth)acryliques : n Caractéristiques : n polymérisation extrêmement rapide n très grand nbre de polymères et de monomères disponibles très large gamme de produits n très sensible à l’inhibition par le dioxygène de l’air n important retrait après polymérisation n Application : arts graphiques, revêtements industriels (bois, plastiques, métal), électronique, adhésifs … 25

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Résines polyesters insaturés : Oligomère : polymaléate/fumarate de divers diols n Monomère : styrène n n Principe : copolymérisation directe du monomère vinylique avec les doubles liaisons de la chaîne de polyester 26

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Résines polyesters insaturés : n Caractéristiques : n polymérisation relativement lente n nombre limité d’oligomères disponibles n volatilité du styrène n sensible à l’inhibition par le dioxygène de l’air n bon marché n Application : revêtement du bois 27

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Résines thiol-ènes : n Oligomère/monomère : acrylates ou allyliques/thiol n Principe : addition radicalaire d’une liaison S-H sur une oléfine puis propagation par transfert 28

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Résines thiol-ènes : n Caractéristiques : n problème d’odeur n insensible à l’inhibition par le dioxygène de l’air n problème de stabilité au stockage du mélange oléfine/thiol n coût élevé n Application : revêtements souples et adhérents. 29

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Couple donneur (D) / accepteur (A) : n Oligomère/monomère : polyester insaturé (accepteur) / vinyl éther multifonctionnel (donneur) n Principe : l’espèce réactive est constituée du couple formé par la double liaison riche en électrons (D) et la double liaison pauvre en électrons (A) 30

II. 3. Systèmes photopolymérisables II. 3. 1. Systèmes radicalaires n Couple donneur (D) / accepteur (A) : n Caractéristiques : n étroite palette de monomères disponibles n peu sensible à l’inhibition par le dioxygène de l’air n Application : revêtement du bois 31

II. 3. Systèmes photopolymérisables II. 3. 2. Systèmes cationiques n Insensibilité à l’inhibition par le dioxygène de l’air n Sensibilité à l’inhibition par l’humidité et les espèces basiques n Très faible disponibilité des oligomères n Vitesse de polymérisation plus faible que celle des systèmes radicalaires 32

II. 3. Systèmes photopolymérisables II. 3. 2. Systèmes cationiques n Hétérocycles tendus : n Oligomère : époxy, oxétanes, époxy cycloaliphatiques (plus rapides) n Principe : polymérisation par ouverture de cycle avec formation d’ions oxonium qui propagent la réaction en chaîne obtention d’un polyéther 33

II. 3. Systèmes photopolymérisables II. 3. 2. Systèmes cationiques n Hétérocycles tendus : n Caractéristiques : n retrait plus faible que dans le cas des systèmes radicalaires n résines plus chères que les résines radicalaires n excellente adhésion sur métaux n excellentes propriétés mécaniques (dureté, flexibilité) et très bonne tenue aux solvants et à la chaleur n Application : décoration du métal, revêtements antiadhérents (release coatings) 34

II. 3. Systèmes photopolymérisables II. 3. 2. Systèmes cationiques n Oléfines enrichies en électrons : n Oligomère : n Caractéristiques : n plus grande réactivité que les résines à fonctions hétéro- cycliques n retrait identique à celui des systèmes radicalaires 35

II. 3. Systèmes photopolymérisables II. 3. 3. Systèmes hybrides n Oligomères : couples éther vinylique/acrylate, éther vinylique/polyester insaturé, époxy/acrylate … n Principe : polymérisation simultanée mais indépendante des deux systèmes radicalaire et cationique obtention de 2 réseaux polymères enchevêtrés ou interpénétrés (IPN) 36

II. 3. Systèmes photopolymérisables II. 3. 3. Systèmes hybrides n Caractéristiques : n combinaison en un seul matériau des principales caractéristiques deux réseaux ex : caractère élastomère du poly(éther vinylique) et rigidité du polyacrylate ou du polyépoxyde matériau dur et flexible à la fois bonne résistance aux chocs et à la rayure n variation des propriétés physico-chimiques de l’IPN en jouant sur les proportions de chaque oligomère 37

II. 4. Paramètres influents n Résine / fonction réactive : n Mécanisme réactionnel (radicalaire ou cationique) n Vitesse de polymérisation : n radicalaire : méthacrylate < polyester insaturé/styrène < thiol/polyène < acrylate n cationique : époxyde < éther vinylique n Taux de conversion final maximum : arrêt de la réaction quand Tg ~Tréaction 38

II. 4. Paramètres influents n Photoamorceur : Domaine et efficacité d’absorption n Vitesse de polymérisation n Taux de conversion final n n Intensité lumineuse : Vitesse de polymérisation n Taux de conversion final n 39

III – Avantages et applications du procédé de photopolymérisation

III. 1. Intérêt de l’amorçage photochimique n Rapidité de la réaction (qqs sec. sous irradiation intense) n Contrôle spatial de la réaction : elle n’intervient que dans les zones exposées au rayonnement lumineux n Contrôle temporel de la réaction : elle peut être déclenchée à un instant précis et être arrêtée à tout moment n Contrôle de la vitesse de la réaction : l’intensité du rayonnement lumineux est modulable dans une très large gamme 41

III. 1. Intérêt de l’amorçage photochimique n Contrôle de l’épaisseur polymérisée (de qqs µm à qqs mm) : en jouant sur la longueur d’onde et/ou l’intensité du rayonnement lumineux, et/ou sur la concentration en photoamorceur, on peut régler la profondeur de pénétration du rayonnement Loi de Beer-Lambert : n Réduction des émissions de composés organiques volatils (COV) grâce à l’emploi de systèmes sans solvant ou à base aqueuse et à la possibilité de travailler à température ambiante 42

III. 2. Avantages industriels n Réduction considérable de la pollution par les solvants organiques et les émissions de COV e t n Gain de place dans les ateliers deer production (fours v UV beaucoup moins volumineux que tunnels de e i g séchage thermiques) o l o n h c n Abaissement des ecoûts de production (four UV T cher qu’un four à séchage jusqu’à moitié moins thermique et cadences de séchage beaucoup plus rapides (qqs dizaines à qqs centaines de m/min)) 43

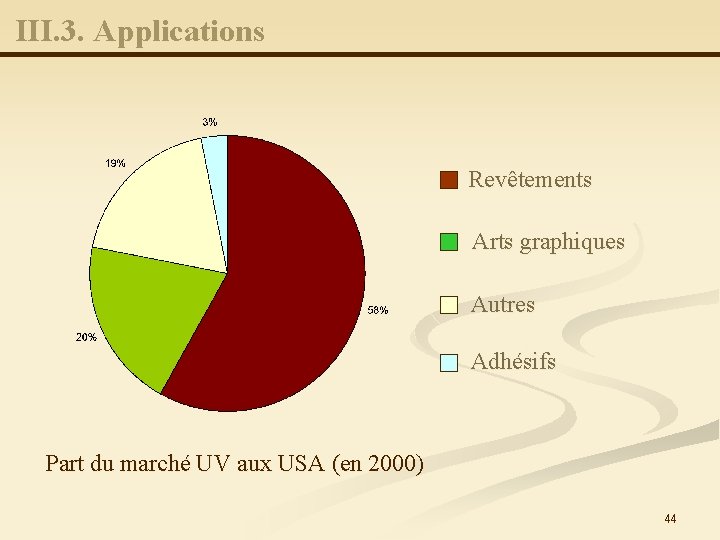
III. 3. Applications Revêtements Arts graphiques Autres Adhésifs Part du marché UV aux USA (en 2000) 44

III. 3. Applications Revêtements sur une large gamme de substrats (bois, plastique, métal, papier, verre, cuir, textile …) n 45

III. 3. Applications Revêtements sur une large gamme de substrats (bois, plastique, métal, papier, verre, cuir, textile …) n 46

III. 3. Applications n Arts graphiques Séchage des encres d’impression appliquées sur une large gamme de substrats (plastique, métal, papier, carton) n n Fabrication de circuits imprimés par photolithographie 47

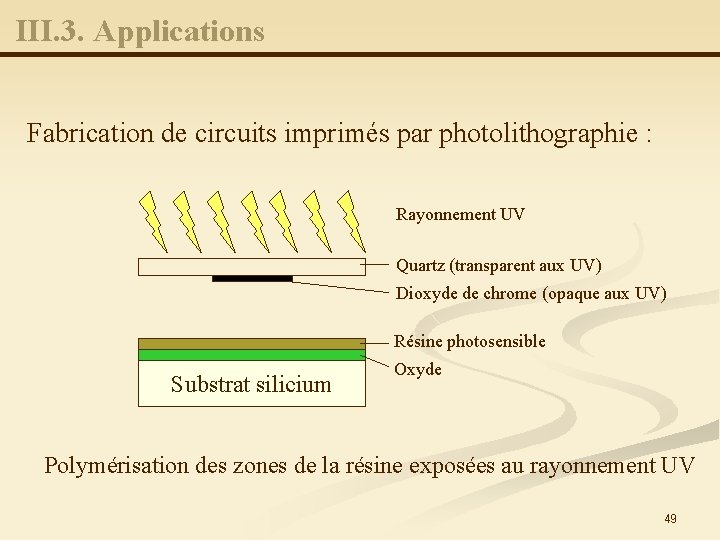
III. 3. Applications Fabrication de circuits imprimés par photolithographie : Procédé qui permet la gravure, suivant un motif bien défini, d'une (ou plusieurs) couche(s) solide(s) telle que nitrure, oxyde, métal, etc. . . , à la surface d’un substrat semi-conducteur. n Principe : transfert par insolation du motif défini sur un masque vers la plaquette du semi-conducteur. n 48

III. 3. Applications Fabrication de circuits imprimés par photolithographie : Rayonnement UV Quartz (transparent aux UV) Dioxyde de chrome (opaque aux UV) Résine photosensible Substrat silicium Oxyde Polymérisation des zones de la résine exposées au rayonnement UV 49

III. 3. Applications Fabrication de circuits imprimés par photolithographie : Résine photosensible Substrat silicium Photoresist positif (zones exposées insolubles dans le solvant de développement) Oxyde Substrat silicium Photoresist négatif (zones exposées solubles dans le solvant de développement) Retrait Révélation Gravure de la résine dedelade lapartie résine la surface non parprotégée un de solvant l’oxyde de de l’oxyde pardéveloppement un solvant par HFpuissant 50

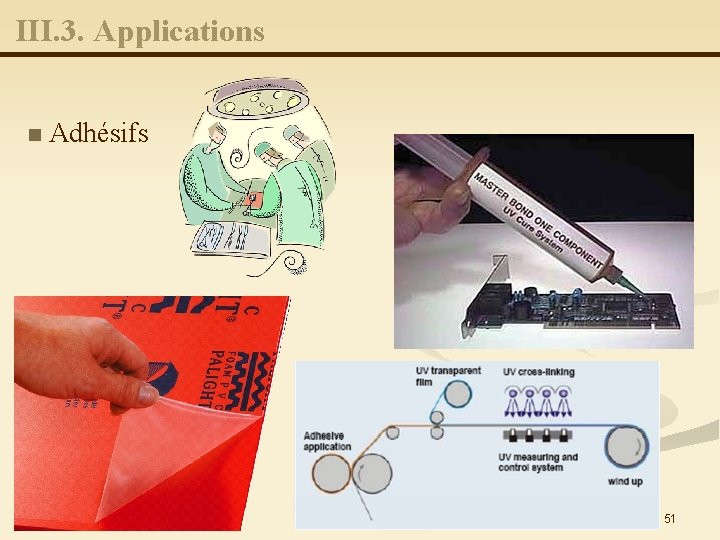
III. 3. Applications n Adhésifs 51

III. 3. Applications Réparation d’un éclat de pare-brise : Etape : préparation pour la par réparation Etape 234: : 1: remplissage durcissement élimination de dede l’éclat l’excès la résine dela sous résine UV 52

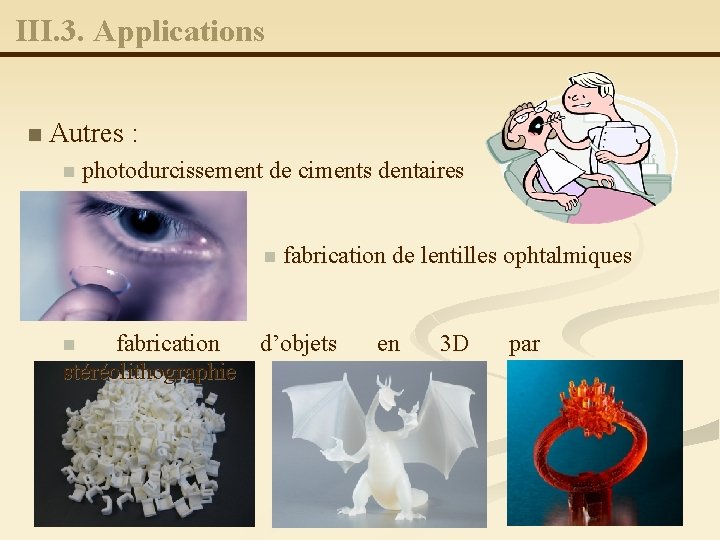
III. 3. Applications n Autres : n photodurcissement de ciments dentaires n fabrication de lentilles ophtalmiques fabrication d’objets stéréolithographie n en 3 D par 53

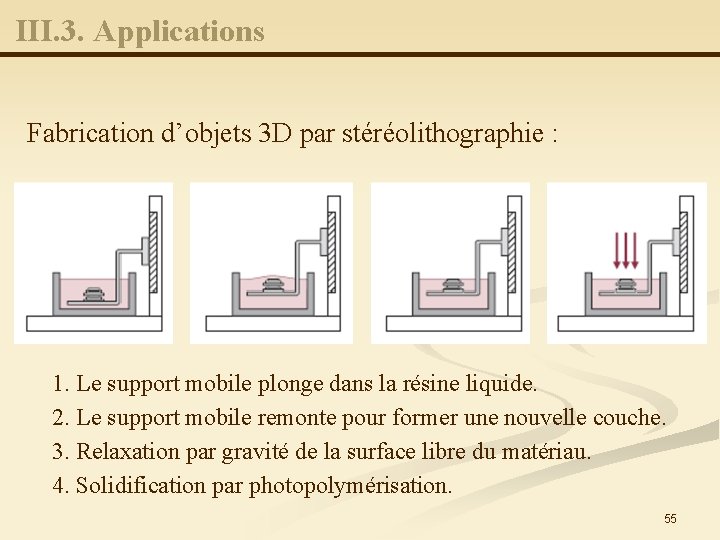
III. 3. Applications Fabrication d’objets 3 D par stéréolithographie : Procédé qui permet d’obtenir sans usinage une pièce tridimensionnelle à partir d’un modèle numérique établi par CAO. n Principe : le point de focalisation d’un faisceau laser polymérise la zone de la surface libre de la résine photopolymérisable en suivant la géométrie des différentes couches 2 D définies numériquement. n 54

III. 3. Applications Fabrication d’objets 3 D par stéréolithographie : 1. Le support mobile plonge dans la résine liquide. 2. Le support mobile remonte pour former une nouvelle couche. 3. Relaxation par gravité de la surface libre du matériau. 4. Solidification par photopolymérisation. 55

IV – Quelques problématiques liées au procédé de photopolymérisation

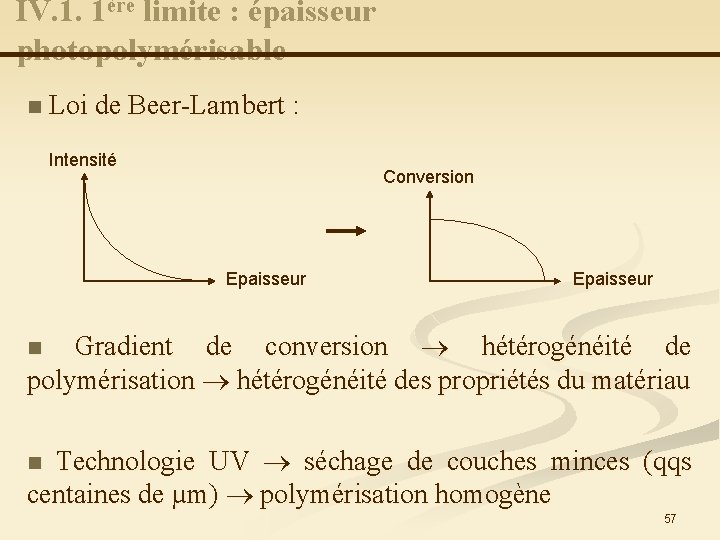
IV. 1. 1ère limite : épaisseur photopolymérisable n Loi de Beer-Lambert : Intensité Conversion Epaisseur Gradient de conversion hétérogénéité de polymérisation hétérogénéité des propriétés du matériau n Technologie UV séchage de couches minces (qqs centaines de µm) polymérisation homogène n 57

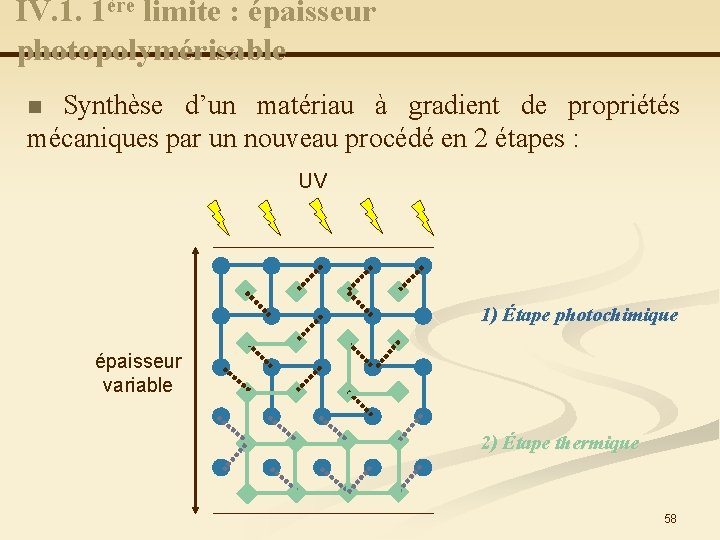
IV. 1. 1ère limite : épaisseur photopolymérisable Synthèse d’un matériau à gradient de propriétés mécaniques par un nouveau procédé en 2 étapes : n UV 1) Étape photochimique épaisseur variable 2) Étape thermique 58

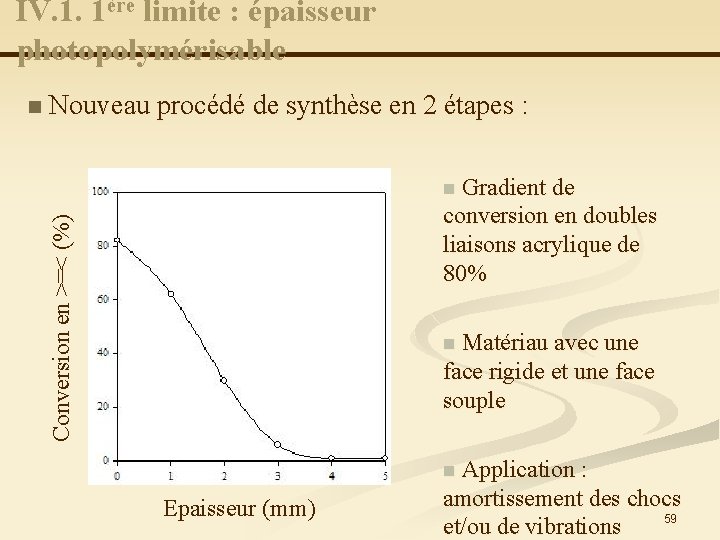
IV. 1. 1ère limite : épaisseur photopolymérisable Nouveau procédé de synthèse en 2 étapes : Gradient de conversion en doubles liaisons acrylique de 80% n Conversion en >=< (%) n Matériau avec une face rigide et une face souple n Application : amortissement des chocs 59 et/ou de vibrations n Epaisseur (mm)

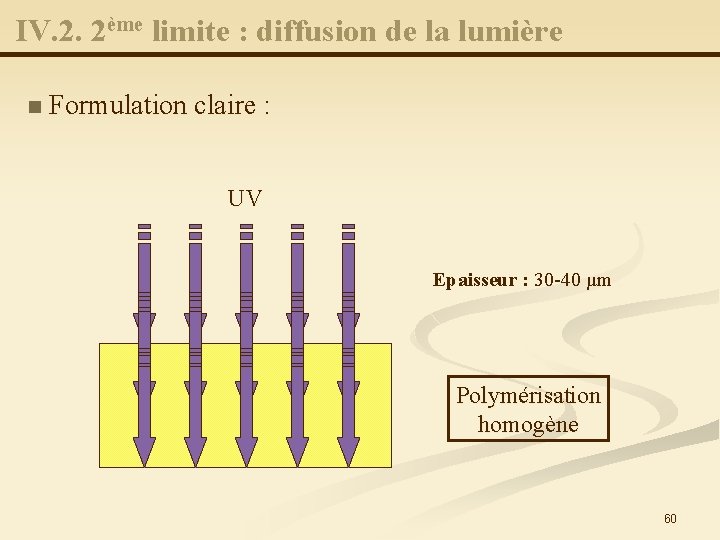
IV. 2. 2ème limite : diffusion de la lumière n Formulation claire : UV Epaisseur : 30 -40 µm Polymérisation homogène 60

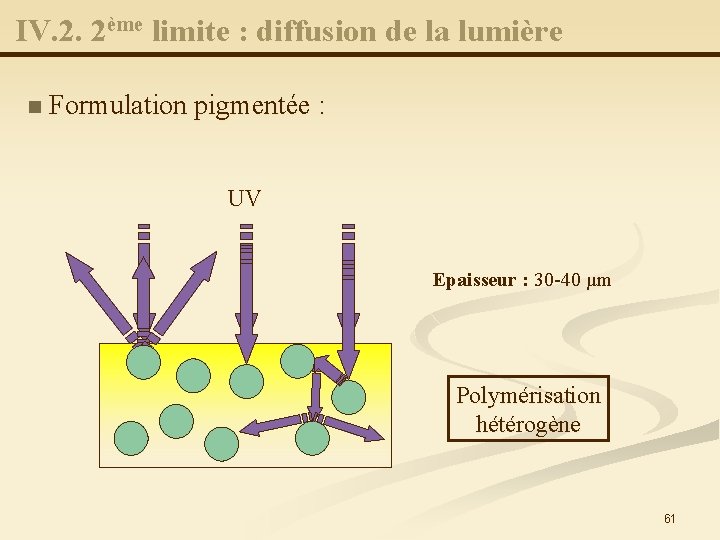
IV. 2. 2ème limite : diffusion de la lumière n Formulation pigmentée : UV Epaisseur : 30 -40 µm Polymérisation hétérogène 61

IV. 2. 2ème limite : diffusion de la lumière Revêtement mal photopolymérisé Revêtement bien photopolymérisé 62

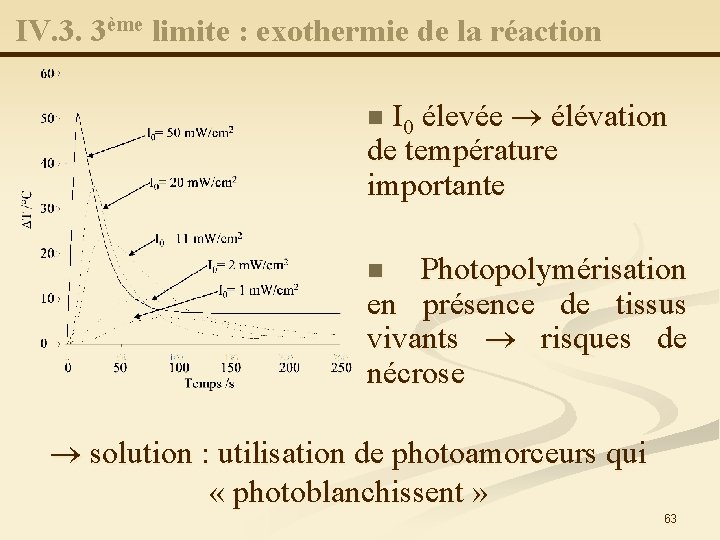
IV. 3. 3ème limite : exothermie de la réaction élevée élévation de température importante n I 0 Photopolymérisation en présence de tissus vivants risques de nécrose n solution : utilisation de photoamorceurs qui « photoblanchissent » 63

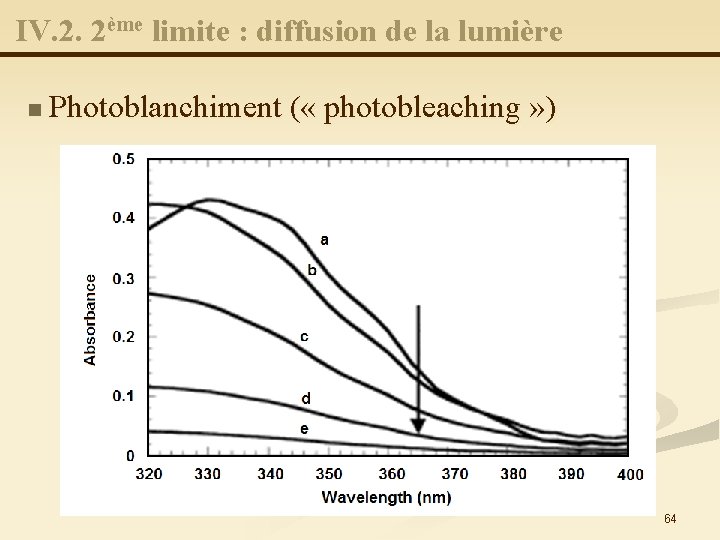
IV. 2. 2ème limite : diffusion de la lumière n Photoblanchiment ( « photobleaching » ) 64

Conclusion

Conclusion n Technologie performante, écologique et économique n Applications nombreuses et variées Þ Technologie verte avec un fort potentiel de développement n Recherche constante de nouveaux photoamorceurs, résines, sources d’émission … 66

MERCI DE VOTRE ATTENTION ! 67