Cours de thermodynamique Aline BrunetBruneau Matre de confrences

Cours de thermodynamique Aline Brunet-Bruneau Maître de conférences de l’Université Paris 6 1 Température et chaleur 2 Travail 3 Quatre transformations de base, 1 er principe de la thermo. 4 Chaleur, travail et énergie interne des gaz parfaits 5 Transformations réversibles, 2 nd principe de la thermo. 6 Changement de phase des corps purs 7 Machines thermiques dithermes

Cours 1 : Température et chaleur 1. 1 Notion de chaleur 1. 2 Chaleur = grandeur physique 1. 3 Chaleur = énergie 1. 4 Signe de la chaleur et énergie interne 1. 5 Chaleur latente et chaleur de combustion
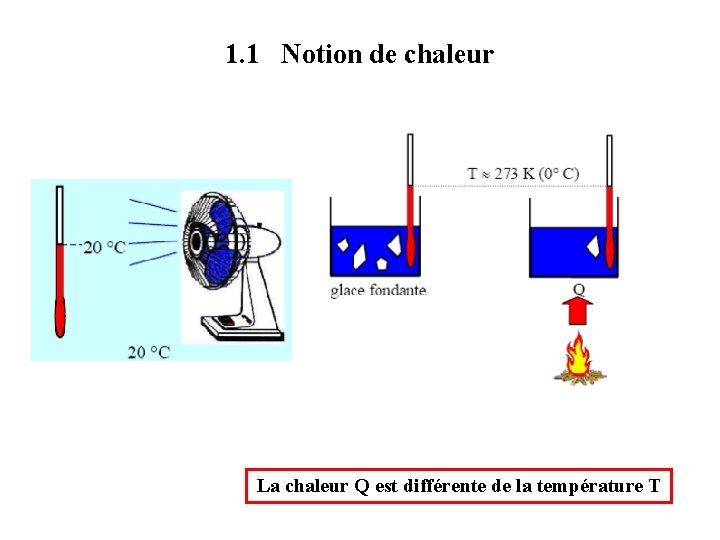
1. 1 Notion de chaleur La chaleur Q est différente de la température T
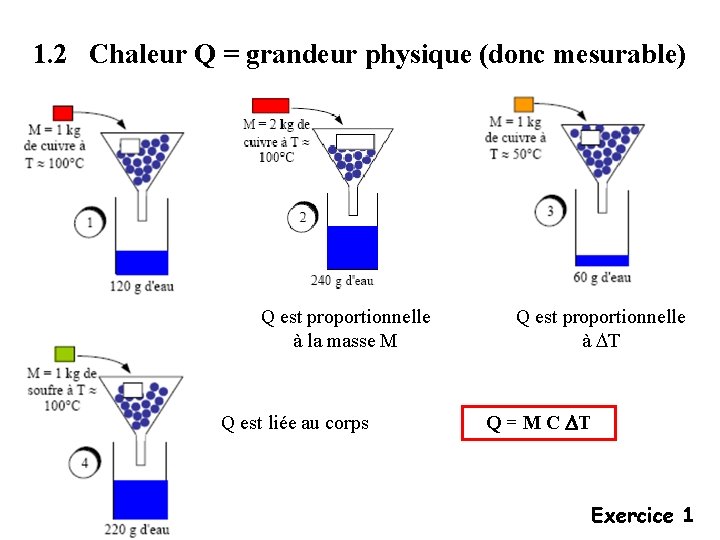
1. 2 Chaleur Q = grandeur physique (donc mesurable) Q est proportionnelle à la masse M Q est liée au corps Q est proportionnelle à T Q = M C T Exercice 1

Exercice 1 Calculer la quantité de chaleur Q nécessaire pour commencer à faire bouillir 1 L d’eau initialement à 10°C. On donne la capacité calorifique massique de l’eau : C~1 kcal kg-1 K-1 et la masse volumique de l’eau ~1 Kg/dm 3.
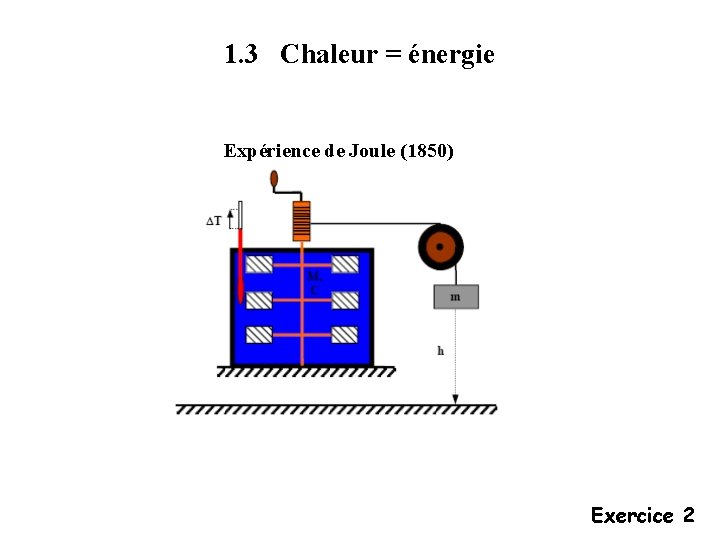
1. 3 Chaleur = énergie Expérience de Joule (1850) Exercice 2
Exercice 2 Une bouilloire électrique a pour puissance P = 1 k. W lorsqu’elle est alimentée par la prise secteur (tension efficace de 230 V). On y place 1 L d’eau à 10° C. En combien de temps l’eau va bouillir ?
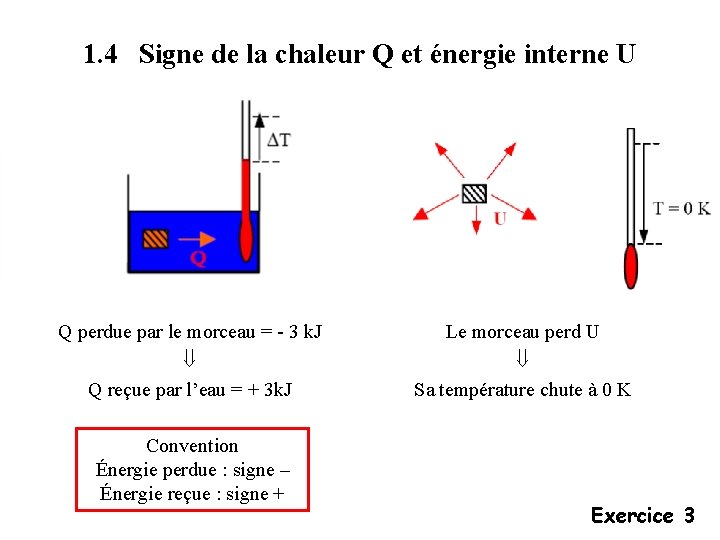
1. 4 Signe de la chaleur Q et énergie interne U Q perdue par le morceau = - 3 k. J Q reçue par l’eau = + 3 k. J Convention Énergie perdue : signe – Énergie reçue : signe + Le morceau perd U Sa température chute à 0 K Exercice 3

Exercice 3 Un ressort spiral est compressé ( « remonté » ). De cette manière il emmagasine une énergie de 8000 J. Ce ressort sert à entraîner les pales d’une hélice qui remue 1 L d’eau liquide. Quel va être l’échauffement (augmentation de température) de l’eau après détente totale du ressort ?
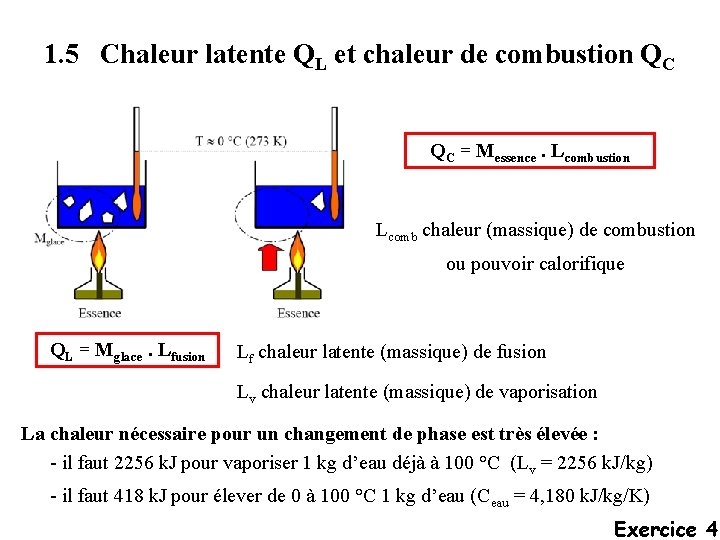
1. 5 Chaleur latente QL et chaleur de combustion QC QC = Messence. Lcombustion Lcomb chaleur (massique) de combustion ou pouvoir calorifique QL = Mglace. Lfusion Lf chaleur latente (massique) de fusion Lv chaleur latente (massique) de vaporisation La chaleur nécessaire pour un changement de phase est très élevée : - il faut 2256 k. J pour vaporiser 1 kg d’eau déjà à 100 °C (Lv = 2256 k. J/kg) - il faut 418 k. J pour élever de 0 à 100 °C 1 kg d’eau (Ceau = 4, 180 k. J/kg/K) Exercice 4

Exercice 4 On possède Mess~260 g d’essence que l’on brûle pour échauffer M = 4 kg de glace initialement à -20°C sous la pression atmosphérique : Quelle est la température finale de la vapeur obtenue ? Données : Chaleur latente de fusion de la glace : LF = 352 k. J/kg Chaleur latente de vaporisation de l’eau : Lv = 2256 k. J/kg Capacité calorifique massique de la glace : Cglace = 2000 J/kg/K Capacité calorifique massique de l’eau : Ceau = 4186 J/kg/K Capacité calorifique massique de la vapeur d’eau : Cvapeur = 2020 J/Kg/K Pouvoir calorifique de l’essence : Less = 48. 103 k. J/kg

Correction de l’Exercice 4 Chaleur de combustion Qc dégagée par l’essence : 0, 26 . 48. 103 = 12, 5. 103 k. J Chaleur Q nécessaire pour échauffer M=4 kg d’eau de -20°C à Tvap : Q = Q (de -20 à 0°C) + QF(sol-liq 0°C) + Q(de 0 à 100°C) + QV(liq-vap 100°C) + Q(de 100 à Tvapeur) Q = MCgl T 20 + MLF + MCeau T 100 + MLv + MCvap T (Tvap -100) Température finale Tvap : Q = Qc

Correction de l’Exercice 4 Température finale Tvap : A. N. T = 126°C

Exercice 5 Une enceinte de 22, 4 dm 3 de gaz à 25°C possède une énergie interne U = 3/2 RT avec R = 8, 32 U. S. I et T sa température (en kelvin). Est-il possible, à l’aide de ce gaz, de fournir 5000 J à un corps solide plongé dans l’enceinte? Si oui, de quelle manière ?
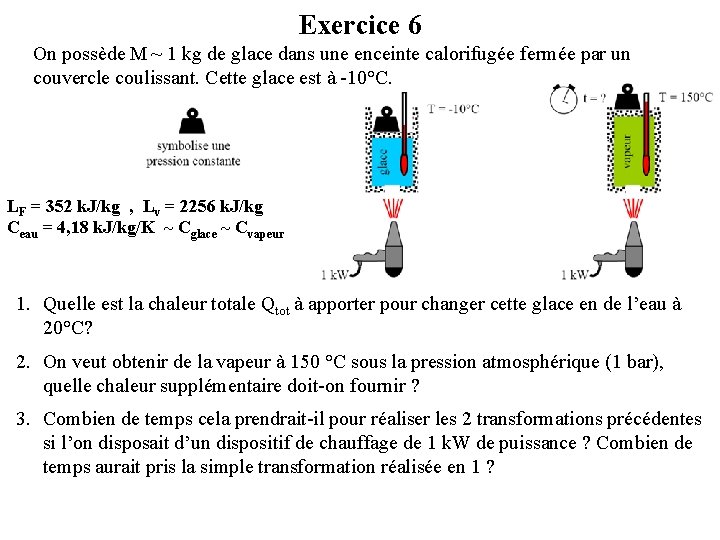
Exercice 6 On possède M ~ 1 kg de glace dans une enceinte calorifugée fermée par un couvercle coulissant. Cette glace est à -10°C. LF = 352 k. J/kg , Lv = 2256 k. J/kg Ceau = 4, 18 k. J/kg/K ~ Cglace ~ Cvapeur 1. Quelle est la chaleur totale Qtot à apporter pour changer cette glace en de l’eau à 20°C? 2. On veut obtenir de la vapeur à 150 °C sous la pression atmosphérique (1 bar), quelle chaleur supplémentaire doit-on fournir ? 3. Combien de temps cela prendrait-il pour réaliser les 2 transformations précédentes si l’on disposait d’un dispositif de chauffage de 1 k. W de puissance ? Combien de temps aurait pris la simple transformation réalisée en 1 ?
- Slides: 15