Neurobiologa y etiologa Enfermedad de Parkinson 1 Neurobiologa

Neurobiología y etiología Enfermedad de Parkinson 1

Neurobiología 2
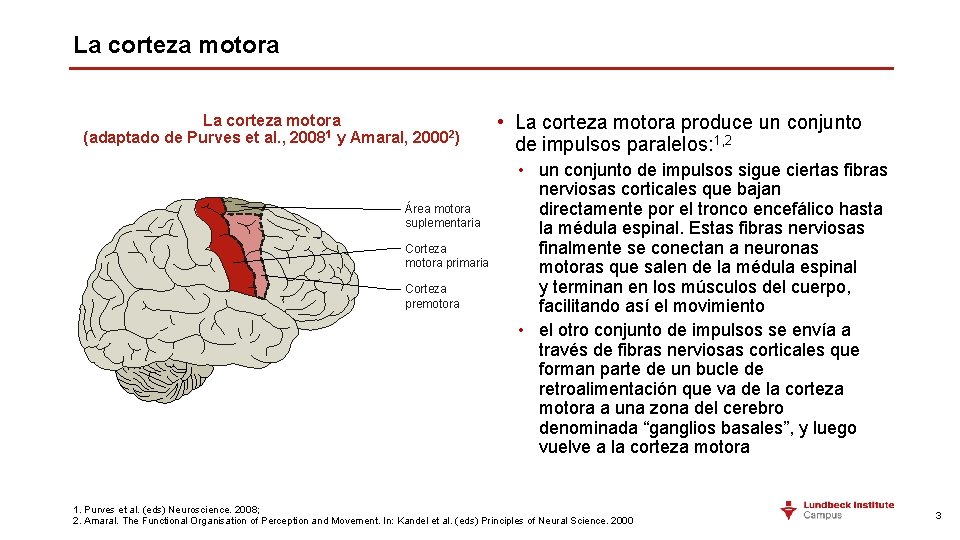
La corteza motora (adaptado de Purves et al. , 20081 y Amaral, 20002) Área motora suplementaria Corteza motora primaria Corteza premotora • La corteza motora produce un conjunto de impulsos paralelos: 1, 2 • un conjunto de impulsos sigue ciertas fibras nerviosas corticales que bajan directamente por el tronco encefálico hasta la médula espinal. Estas fibras nerviosas finalmente se conectan a neuronas motoras que salen de la médula espinal y terminan en los músculos del cuerpo, facilitando así el movimiento • el otro conjunto de impulsos se envía a través de fibras nerviosas corticales que forman parte de un bucle de retroalimentación que va de la corteza motora a una zona del cerebro denominada “ganglios basales”, y luego vuelve a la corteza motora 1. Purves et al. (eds) Neuroscience. 2008; 2. Amaral. The Functional Organisation of Perception and Movement. In: Kandel et al. (eds) Principles of Neural Science. 2000 3
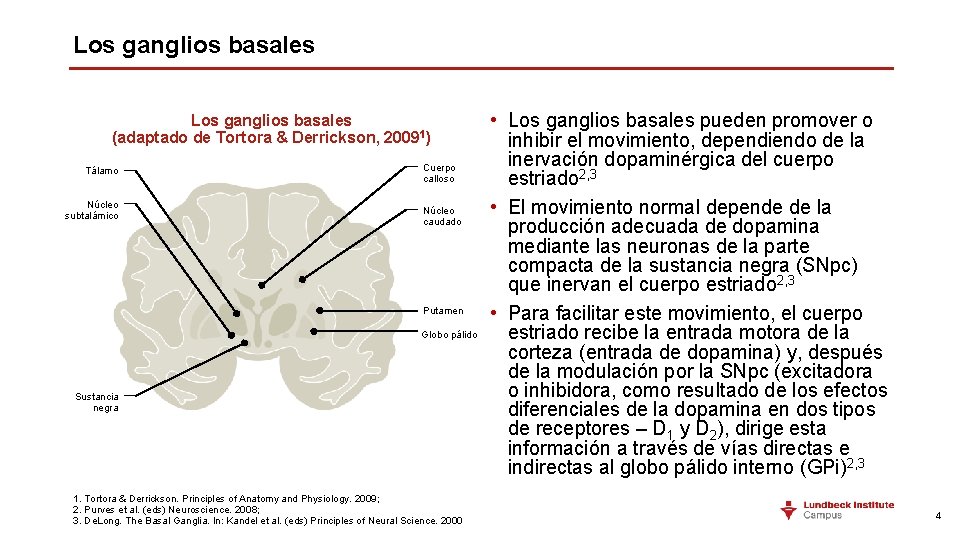
Los ganglios basales (adaptado de Tortora & Derrickson, 20091) Tálamo Núcleo subtalámico Cuerpo calloso Núcleo caudado Putamen Globo pálido Sustancia negra 1. Tortora & Derrickson. Principles of Anatomy and Physiology. 2009; 2. Purves et al. (eds) Neuroscience. 2008; 3. De. Long. The Basal Ganglia. In: Kandel et al. (eds) Principles of Neural Science. 2000 • Los ganglios basales pueden promover o inhibir el movimiento, dependiendo de la inervación dopaminérgica del cuerpo estriado 2, 3 • El movimiento normal depende de la producción adecuada de dopamina mediante las neuronas de la parte compacta de la sustancia negra (SNpc) que inervan el cuerpo estriado 2, 3 • Para facilitar este movimiento, el cuerpo estriado recibe la entrada motora de la corteza (entrada de dopamina) y, después de la modulación por la SNpc (excitadora o inhibidora, como resultado de los efectos diferenciales de la dopamina en dos tipos de receptores – D 1 y D 2), dirige esta información a través de vías directas e indirectas al globo pálido interno (GPi)2, 3 4
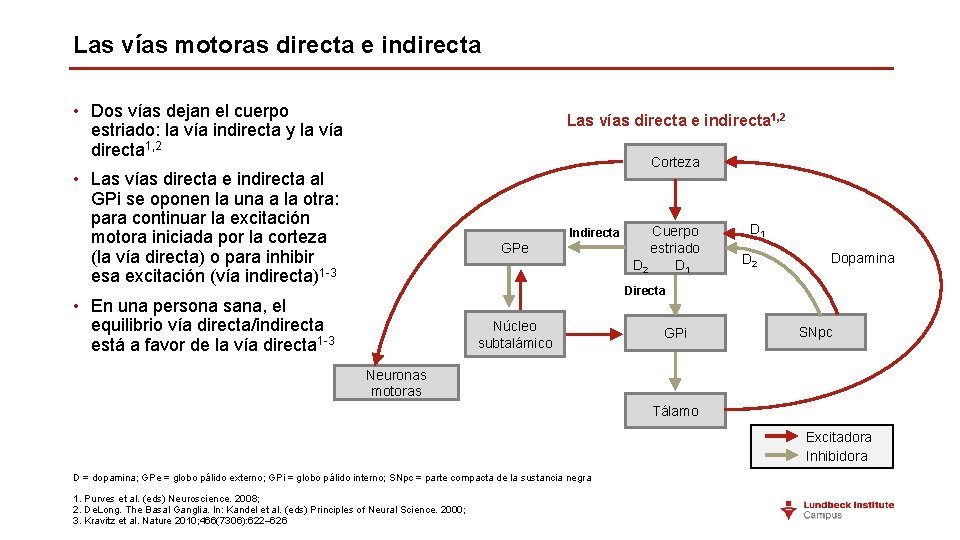
Las vías motoras directa e indirecta • Dos vías dejan el cuerpo estriado: la vía indirecta y la vía directa 1, 2 Las vías directa e indirecta 1, 2 Corteza • Las vías directa e indirecta al GPi se oponen la una a la otra: para continuar la excitación motora iniciada por la corteza (la vía directa) o para inhibir esa excitación (vía indirecta)1 -3 Indirecta GPe Cuerpo estriado D 2 D 1 D 2 Dopamina Directa • En una persona sana, el equilibrio vía directa/indirecta está a favor de la vía directa 1 -3 Núcleo subtalámico GPi SNpc Neuronas motoras Tálamo Excitadora Inhibidora D = dopamina; GPe = globo pálido externo; GPi = globo pálido interno; SNpc = parte compacta de la sustancia negra 1. Purves et al. (eds) Neuroscience. 2008; 2. De. Long. The Basal Ganglia. In: Kandel et al. (eds) Principles of Neural Science. 2000; 3. Kravitz et al. Nature 2010; 466(7306): 622– 626
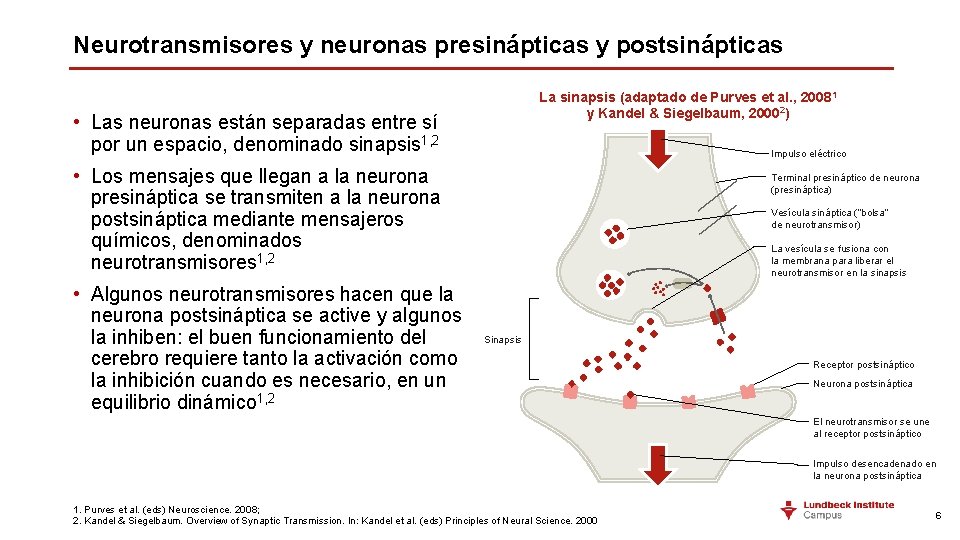
Neurotransmisores y neuronas presinápticas y postsinápticas La sinapsis (adaptado de Purves et al. , 20081 y Kandel & Siegelbaum, 20002) • Las neuronas están separadas entre sí por un espacio, denominado sinapsis 1, 2 Impulso eléctrico • Los mensajes que llegan a la neurona presináptica se transmiten a la neurona postsináptica mediante mensajeros químicos, denominados neurotransmisores 1, 2 • Algunos neurotransmisores hacen que la neurona postsináptica se active y algunos la inhiben: el buen funcionamiento del cerebro requiere tanto la activación como la inhibición cuando es necesario, en un equilibrio dinámico 1, 2 Terminal presináptico de neurona (presináptica) Vesícula sináptica (“bolsa” de neurotransmisor) La vesícula se fusiona con la membrana para liberar el neurotransmisor en la sinapsis Sinapsis Receptor postsináptico Neurona postsináptica El neurotransmisor se une al receptor postsináptico Impulso desencadenado en la neurona postsináptica 1. Purves et al. (eds) Neuroscience. 2008; 2. Kandel & Siegelbaum. Overview of Synaptic Transmission. In: Kandel et al. (eds) Principles of Neural Science. 2000 6
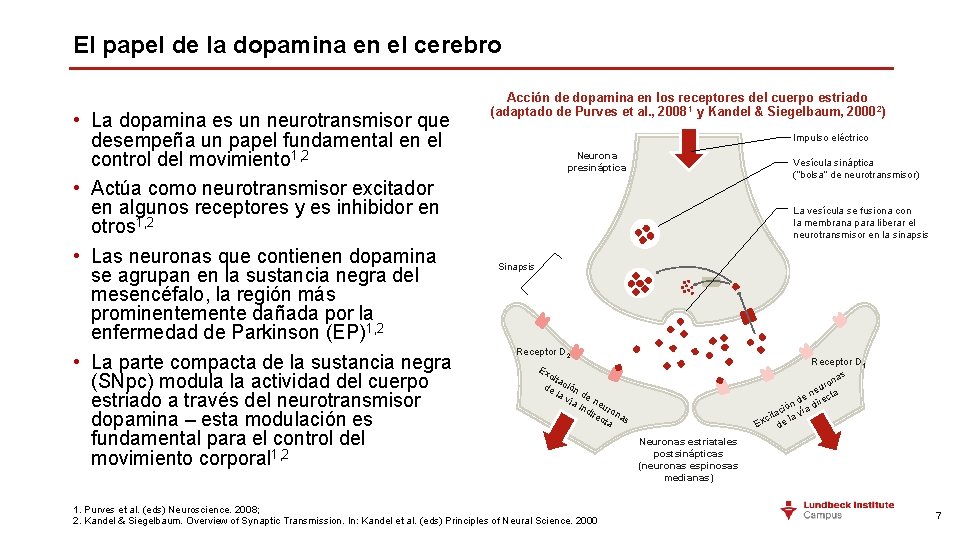
El papel de la dopamina en el cerebro • La dopamina es un neurotransmisor que desempeña un papel fundamental en el control del movimiento 1, 2 • Actúa como neurotransmisor excitador en algunos receptores y es inhibidor en otros 1, 2 • Las neuronas que contienen dopamina se agrupan en la sustancia negra del mesencéfalo, la región más prominentemente dañada por la enfermedad de Parkinson (EP)1, 2 • La parte compacta de la sustancia negra (SNpc) modula la actividad del cuerpo estriado a través del neurotransmisor dopamina – esta modulación es fundamental para el control del movimiento corporal 1, 2 Acción de dopamina en los receptores del cuerpo estriado (adaptado de Purves et al. , 2008 1 y Kandel & Siegelbaum, 2000 2) Impulso eléctrico Neurona presináptica Vesícula sináptica (“bolsa” de neurotransmisor) La vesícula se fusiona con la membrana para liberar el neurotransmisor en la sinapsis Sinapsis Receptor D 2 Receptor D 1 as ron u ne ta de irec n d ció a ita la ví c Ex de Ex cita de ción la vía de ne ind uro ire na cta s 1. Purves et al. (eds) Neuroscience. 2008; 2. Kandel & Siegelbaum. Overview of Synaptic Transmission. In: Kandel et al. (eds) Principles of Neural Science. 2000 Neuronas estriatales postsinápticas (neuronas espinosas medianas) 7

La patogenia de la enfermedad de Parkinson 8
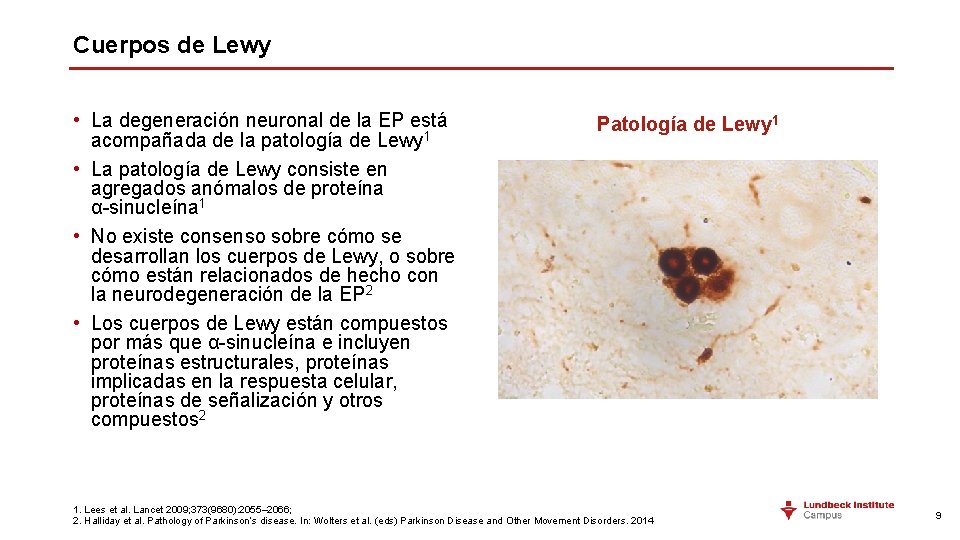
Cuerpos de Lewy • La degeneración neuronal de la EP está acompañada de la patología de Lewy 1 • La patología de Lewy consiste en agregados anómalos de proteína α-sinucleína 1 • No existe consenso sobre cómo se desarrollan los cuerpos de Lewy, o sobre cómo están relacionados de hecho con la neurodegeneración de la EP 2 • Los cuerpos de Lewy están compuestos por más que α-sinucleína e incluyen proteínas estructurales, proteínas implicadas en la respuesta celular, proteínas de señalización y otros compuestos 2 Patología de Lewy 1 1. Lees et al. Lancet 2009; 373(9680): 2055– 2066; 2. Halliday et al. Pathology of Parkinson’s disease. In: Wolters et al. (eds) Parkinson Disease and Other Movement Disorders. 2014 9
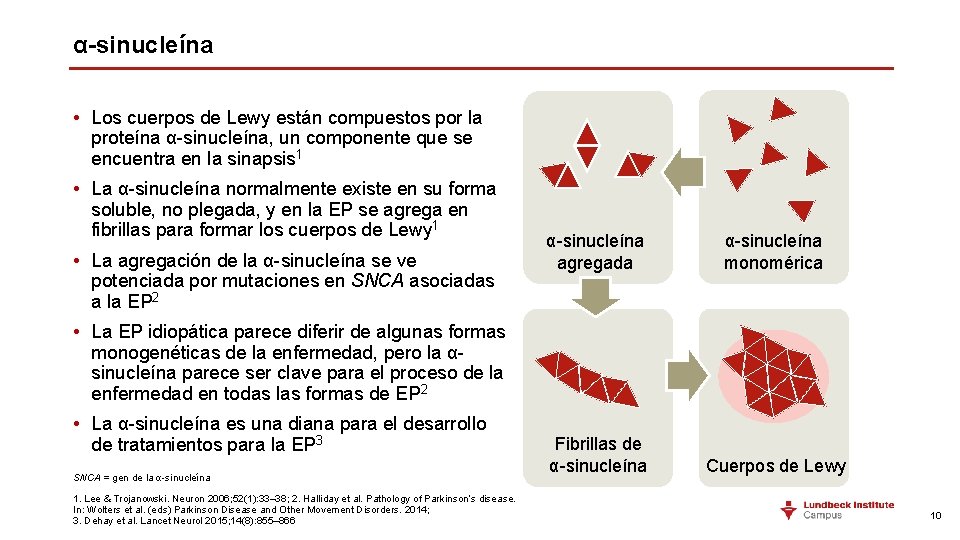
α-sinucleína • Los cuerpos de Lewy están compuestos por la proteína α-sinucleína, un componente que se encuentra en la sinapsis 1 • La α-sinucleína normalmente existe en su forma soluble, no plegada, y en la EP se agrega en fibrillas para formar los cuerpos de Lewy 1 • La agregación de la α-sinucleína se ve potenciada por mutaciones en SNCA asociadas a la EP 2 α-sinucleína agregada α-sinucleína monomérica Fibrillas de α-sinucleína Cuerpos de Lewy • La EP idiopática parece diferir de algunas formas monogenéticas de la enfermedad, pero la αsinucleína parece ser clave para el proceso de la enfermedad en todas las formas de EP 2 • La α-sinucleína es una diana para el desarrollo de tratamientos para la EP 3 SNCA = gen de la α-sinucleína 1. Lee & Trojanowski. Neuron 2006; 52(1): 33– 38; 2. Halliday et al. Pathology of Parkinson’s disease. In: Wolters et al. (eds) Parkinson Disease and Other Movement Disorders. 2014; 3. Dehay et al. Lancet Neurol 2015; 14(8): 855– 866 10
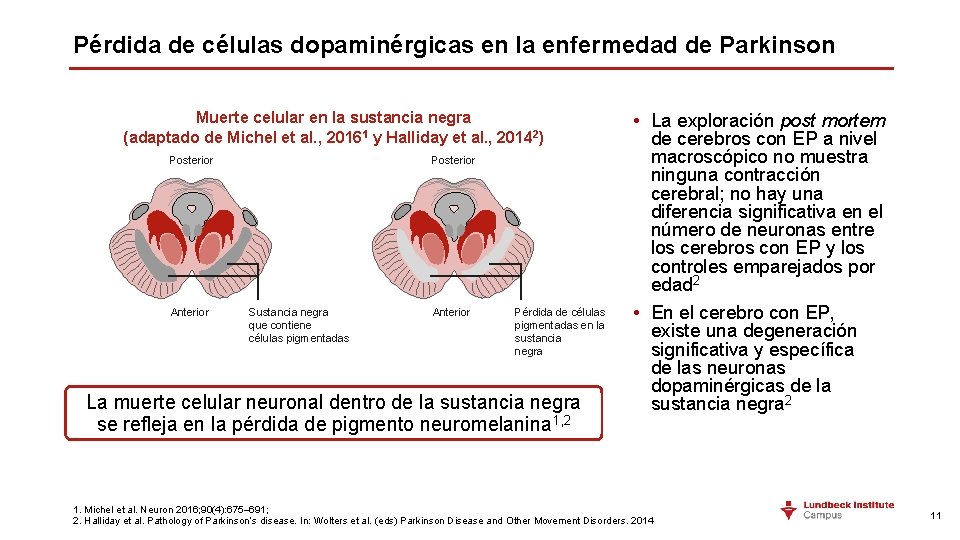
Pérdida de células dopaminérgicas en la enfermedad de Parkinson Muerte celular en la sustancia negra (adaptado de Michel et al. , 20161 y Halliday et al. , 20142) Posterior Anterior Posterior Sustancia negra que contiene células pigmentadas Anterior Pérdida de células pigmentadas en la sustancia negra La muerte celular neuronal dentro de la sustancia negra se refleja en la pérdida de pigmento neuromelanina 1, 2 • La exploración post mortem de cerebros con EP a nivel macroscópico no muestra ninguna contracción cerebral; no hay una diferencia significativa en el número de neuronas entre los cerebros con EP y los controles emparejados por edad 2 • En el cerebro con EP, existe una degeneración significativa y específica de las neuronas dopaminérgicas de la sustancia negra 2 1. Michel et al. Neuron 2016; 90(4): 675– 691; 2. Halliday et al. Pathology of Parkinson’s disease. In: Wolters et al. (eds) Parkinson Disease and Other Movement Disorders. 2014 11
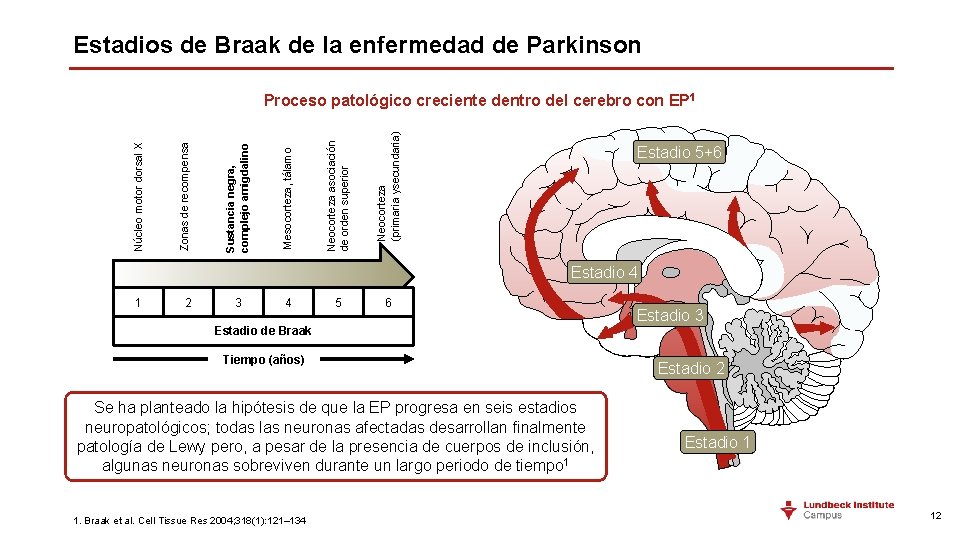
Estadios de Braak de la enfermedad de Parkinson Neocorteza (primaria ysecundaria) Neocorteza asociación de orden superior Mesocorteza, tálamo Sustancia negra, complejo amigdalino Zonas de recompensa Núcleo motor dorsal X Proceso patológico creciente dentro del cerebro con EP 1 Estadio 5+6 Estadio 4 1 2 3 4 5 6 Estadio 3 Estadio de Braak Tiempo (años) Se ha planteado la hipótesis de que la EP progresa en seis estadios neuropatológicos; todas las neuronas afectadas desarrollan finalmente patología de Lewy pero, a pesar de la presencia de cuerpos de inclusión, algunas neuronas sobreviven durante un largo periodo de tiempo 1 1. Braak et al. Cell Tissue Res 2004; 318(1): 121– 134 Estadio 2 Estadio 1 12
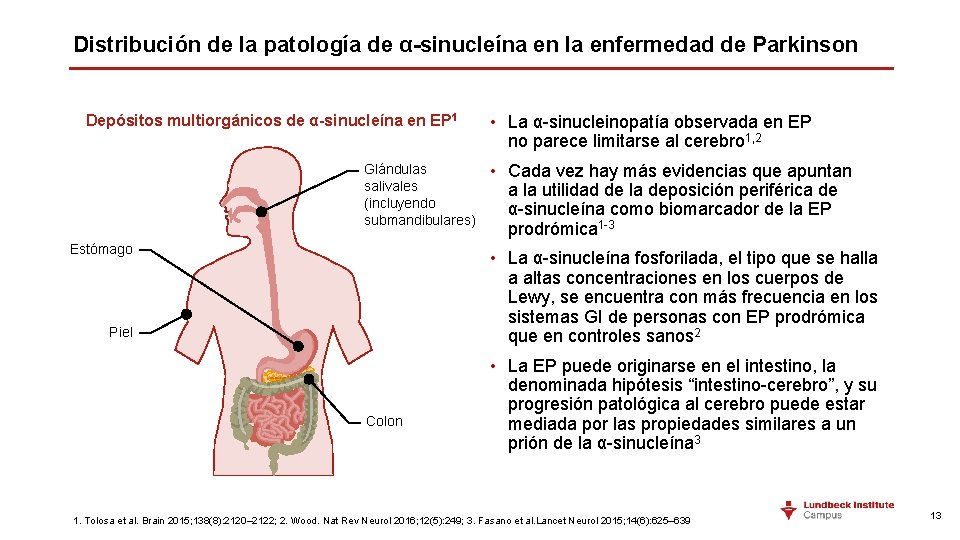
Distribución de la patología de α-sinucleína en la enfermedad de Parkinson Depósitos multiorgánicos de α-sinucleína en EP 1 Glándulas salivales (incluyendo submandibulares) Estómago • La α-sinucleinopatía observada en EP no parece limitarse al cerebro 1, 2 • Cada vez hay más evidencias que apuntan a la utilidad de la deposición periférica de α-sinucleína como biomarcador de la EP prodrómica 1 -3 • La α-sinucleína fosforilada, el tipo que se halla a altas concentraciones en los cuerpos de Lewy, se encuentra con más frecuencia en los sistemas GI de personas con EP prodrómica que en controles sanos 2 Piel Colon • La EP puede originarse en el intestino, la denominada hipótesis “intestino-cerebro”, y su progresión patológica al cerebro puede estar mediada por las propiedades similares a un prión de la α-sinucleína 3 1. Tolosa et al. Brain 2015; 138(8): 2120– 2122; 2. Wood. Nat Rev Neurol 2016; 12(5): 249; 3. Fasano et al. Lancet Neurol 2015; 14(6): 625– 639 13

El sistema gastrointestinal y la enfermedad de Parkinson • Las funciones del sistema GI están controladas por el “sistema nervioso entérico” (SNE)1 Posible propagación de la sinucleinopatía del SNE al cerebro 2 • Cada vez más evidencias sugieren que las enfermedades que afectan al SNC podrían tener una patogenia similar en el SNE 1 • Las agresiones al tubo GI pueden provocar una patología de α-sinucleína en el SNE, que luego asciende a lo largo del eje intestino-cerebro hasta el cerebro 1 • Por lo tanto, la detección de esta patología en el SNE puede ser potencialmente útil para el diagnóstico o la monitorización de la EP 1 Propagación a lo largo de las neuronas motoras dorsales de nervio vago Propagación a través de la médula espinal Tejido intestinal inflamado SNC = sistema nervioso central; SNE = sistema nervioso entérico; GI = gastrointestinal 1. Rao & Gershon. Nat Rev Gastroenterol Hepatol 2016; 13(9): 517– 528; 2. Lema Tomé et al. Mol Neurobiol 2013; 47(2): 561– 574 14

α-sinucleína y la “hipótesis de priones” de la EP 15

Agregación de proteínas mal plegadas • En el corazón del proceso de la enfermedad de Parkinson se encuentra el mal plegado y la propagación de la proteína α-sinucleína. 1 • La patología típica de la EP se observa por primera vez, dentro del cerebro, en el núcleo motor dorsal y desde ahí se propaga hacia arriba. 2 • Un hito en su conocimiento llegó en 2008, cuando se observaron inclusiones similares a los cuerpos de Lewy en las neuronas que habían sido injertadas (de tejido fetal) en el cerebro de pacientes con EP, 11 -16 años después de que se llevaran a cabo los injertos. 1 Esta observación fue revolucionaria, porque sugirió la transmisión de huésped a injerto de la patología de la EP. 1 1. Hauser. Lancet Neurol 2015; 14(8): 785– 786; 2. Braak et al. Cell Tissue Res 2004; 318(1): 121– 134 16
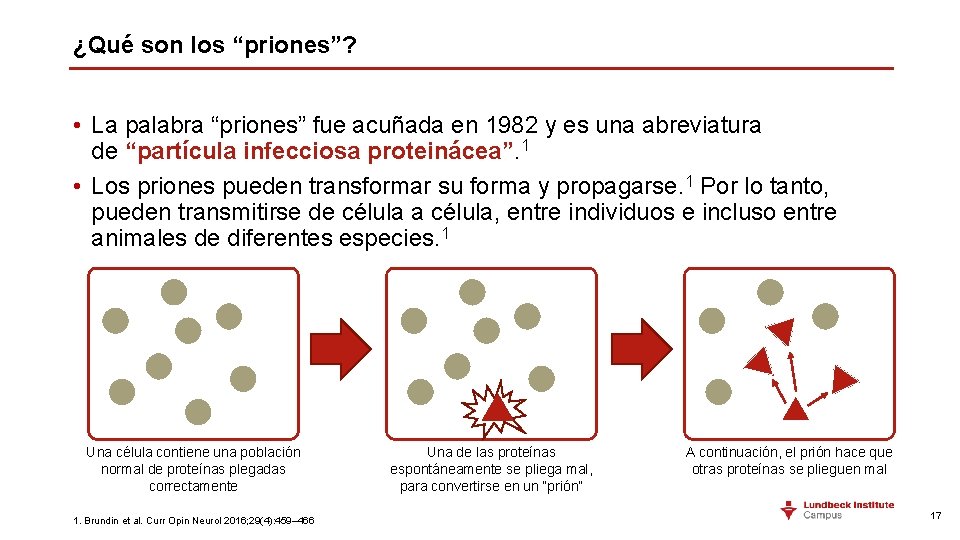
¿Qué son los “priones”? • La palabra “priones” fue acuñada en 1982 y es una abreviatura de “partícula infecciosa proteinácea”. 1 • Los priones pueden transformar su forma y propagarse. 1 Por lo tanto, pueden transmitirse de célula a célula, entre individuos e incluso entre animales de diferentes especies. 1 Una célula contiene una población normal de proteínas plegadas correctamente 1. Brundin et al. Curr Opin Neurol 2016; 29(4): 459– 466 Una de las proteínas espontáneamente se pliega mal, para convertirse en un “prión” A continuación, el prión hace que otras proteínas se plieguen mal 17

¿Hasta qué punto son sólidas las evidencias de que la enfermedad de Parkinson es una enfermedad priónica? Evidencia de la hipótesis del prión 1 • Las neuronas pueden segregar α-sinucleína y tomarla del espacio extracelular. • La α-sinucleína añadida a un medio de neuronas cultivadas es tomada por las células. • Una vez tomada, la α-sinucleína se oligomeriza (se une químicamente) con la α-sinucleína endógena para formar agregados. • Los estudios en animales han respaldado las observaciones en cultivos celulares descritas anteriormente. • Surge una pregunta evidente: ¿es la EP una enfermedad transmisible? • Aunque es difícil estar seguro, los estudios que buscan evidencias epidemiológicas no han encontrado ninguna evidencia de que la EP pueda transmitirse de persona a persona. 1 • Existen trastornos conocidos causados por priones que no son transmisibles, como la enfermedad de Creutzfeldt-Jakob esporádica. 1 Estudios experimentales que demuestran la transferencia de célula a célula de la patología de la α-sinucleína establecen con firmeza que, además de su plegado normal, la α-sinucleína puede plegarse de una forma alterada y que se autopropaga 1 1. Brundin et al. Curr Opin Neurol 2016; 29(4): 459– 466 18

Priones y demencia en la enfermedad de Parkinson • La propagación de la patología de α-sinucleína desde el tronco encefálico hasta ciertas estructuras corticales del cerebro parece ser la correlación más fuerte de la demencia en pacientes con EP. 1 • Además, hasta el 50 % de los pacientes con demencia por EP siguen desarrollando un número suficiente de placas de β-amiloide y ovillos neurofibrilares para un diagnóstico secundario de enfermedad de Alzheimer. 1 • Las placas y los ovillos neurofibrilares pueden actuar sinérgicamente con la patología de α-sinucleína para conferir un peor pronóstico en los pacientes con patologías subyacentes. 1 1. Irwin et al. Nat Rev Neurosci 2013; 14(9): 626– 636 19

Factores de riesgo de la enfermedad de Parkinson 20
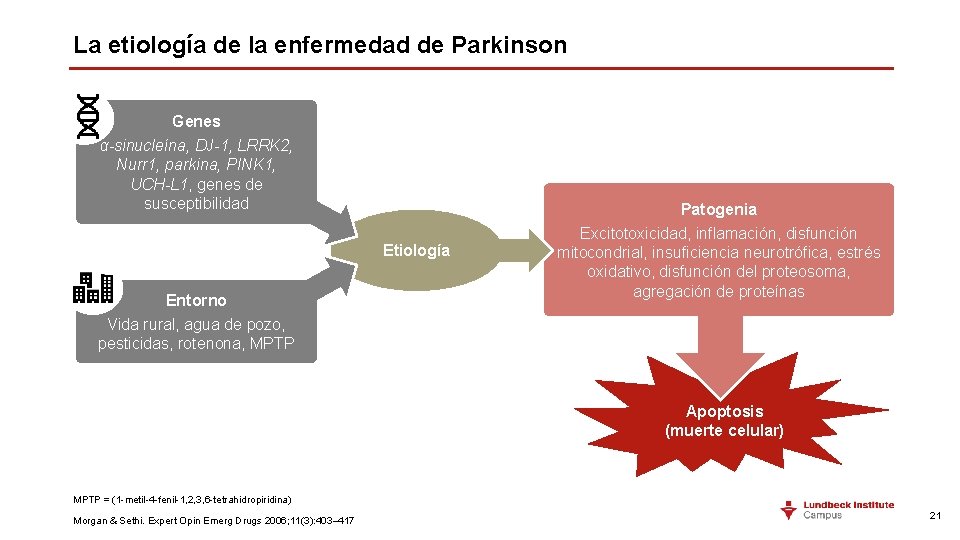
La etiología de la enfermedad de Parkinson Genes α-sinucleína, DJ-1, LRRK 2, Nurr 1, parkina, PINK 1, UCH-L 1, genes de susceptibilidad Etiología Entorno Vida rural, agua de pozo, pesticidas, rotenona, MPTP Patogenia Excitotoxicidad, inflamación, disfunción mitocondrial, insuficiencia neurotrófica, estrés oxidativo, disfunción del proteosoma, agregación de proteínas Apoptosis (muerte celular) MPTP = (1 -metil-4 -fenil-1, 2, 3, 6 -tetrahidropiridina) Morgan & Sethi. Expert Opin Emerg Drugs 2006; 11(3): 403– 417 21

Factores de riesgo medioambiental para la enfermedad de Parkinson Factores de riesgo para el desarrollo de EP 1 Nivel de evidencia Factor de riesgo medioambiental Mayor riesgo (evidencia sólida) • Pesticidas Mayor riesgo (evidencia débil) • Consumo elevado de leche (hombres) Menor riesgo (evidencia sólida) Riesgo reducido (evidencia débil) • Ingesta elevada de hierro • Anemia crónica • Hiperuricemia • Tabaquismo • Consumo de café • Ingesta elevada de vitamina E • Consumo moderado de alcohol • Consumo de té • Ejercicio físico vigoroso • AINE • Uno de los factores de riesgo mejor elucidados para la EP es la exposición a pesticidas. 1 • Se sabe que ciertos pesticidas destruyen las neuronas dopaminérgicas, por lo que se utilizan en modelos animales de EP. 1 • Se sabe que otros factores reducen el riesgo de desarrollar EP, entre ellos, la ingesta de cafeína. 1 • Se sabe que la cafeína activa a los receptores de adenosina, lo que se cree que es neuroprotector. 1 AINE = antiinflamatorio no esteroideo 1. Campdelacreu. Neurología 2014; 29(9): 541– 549 22
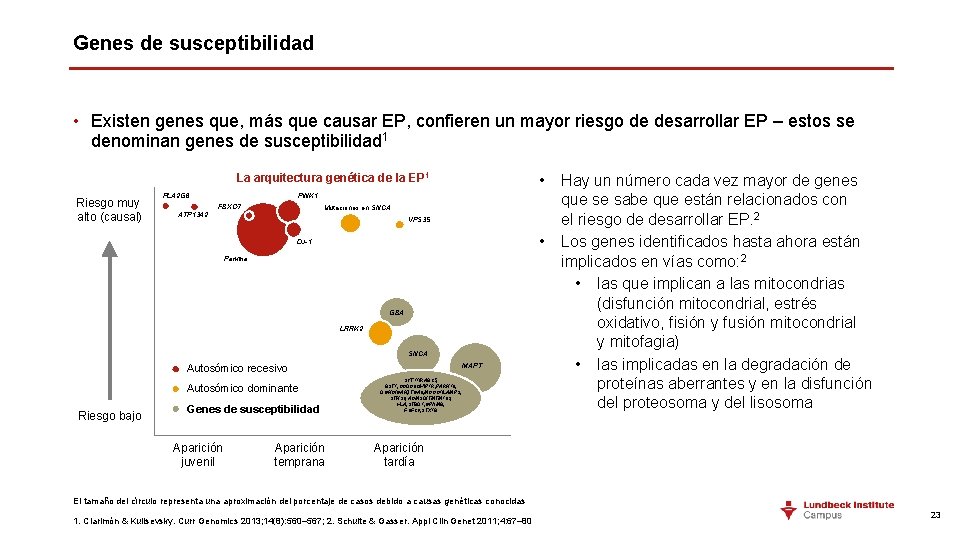
Genes de susceptibilidad • Existen genes que, más que causar EP, confieren un mayor riesgo de desarrollar EP – estos se denominan genes de susceptibilidad 1 La arquitectura genética de la EP 1 Riesgo muy alto (causal) PLA 2 G 6 • PINK 1 FBXO 7 Mutaciones en SNCA ATP 13 A 2 VPS 35 • DJ-1 Parkina GBA LRRK 2 SNCA MAPT Autosómico recesivo Autosómico dominante Riesgo bajo Genes de susceptibilidad Aparición juvenil Aparición temprana SYT 11/RAB 25, BST 1, CCDC 62/HIP 1 R, PARK 16, DGKQ/GAK, ITGA 8, MCCC 1/LAMP 3, STK 39, ACMSD/TMTM 163, HLA, STBD 1, GPNMB, FGF 20, STX 1 B Hay un número cada vez mayor de genes que se sabe que están relacionados con el riesgo de desarrollar EP. 2 Los genes identificados hasta ahora están implicados en vías como: 2 • las que implican a las mitocondrias (disfunción mitocondrial, estrés oxidativo, fisión y fusión mitocondrial y mitofagia) • las implicadas en la degradación de proteínas aberrantes y en la disfunción del proteosoma y del lisosoma Aparición tardía El tamaño del círculo representa una aproximación del porcentaje de casos debido a causas genéticas conocidas 1. Clarimón & Kulisevsky. Curr Genomics 2013; 14(8): 560– 567; 2. Schulte & Gasser. Appl Clin Genet 2011; 4: 67– 80 23
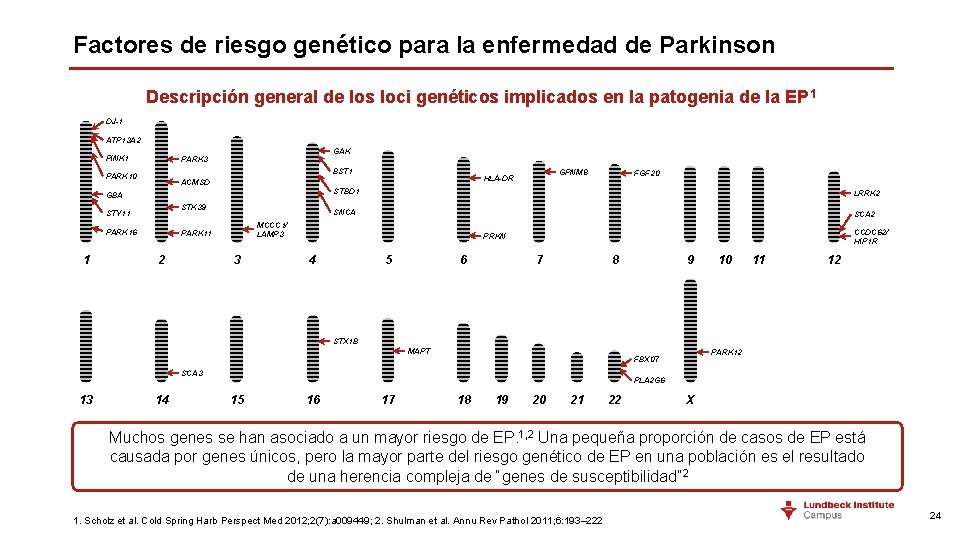
Factores de riesgo genético para la enfermedad de Parkinson Descripción general de los loci genéticos implicados en la patogenia de la EP 1 DJ-1 ATP 13 A 2 PINK 1 GAK PARK 3 BST 1 PARK 10 GBA STK 39 STY 11 PARK 16 1 2 3 FGF 20 STBD 1 LRRK 2 SNCA SCA 2 MCCC 1/ LAMP 3 PARK 11 GPNM 8 HLA-DR ACMSD CCDC 62/ HIP 1 R PRKN 4 5 6 7 8 9 10 11 12 STX 1 B MAPT SCA 3 13 14 PARK 12 FBX 07 PLA 2 G 6 15 16 17 18 19 20 21 22 X Muchos genes se han asociado a un mayor riesgo de EP. 1, 2 Una pequeña proporción de casos de EP está causada por genes únicos, pero la mayor parte del riesgo genético de EP en una población es el resultado de una herencia compleja de “genes de susceptibilidad” 2 1. Scholz et al. Cold Spring Harb Perspect Med 2012; 2(7): a 009449; 2. Shulman et al. Annu Rev Pathol 2011; 6: 193– 222 24
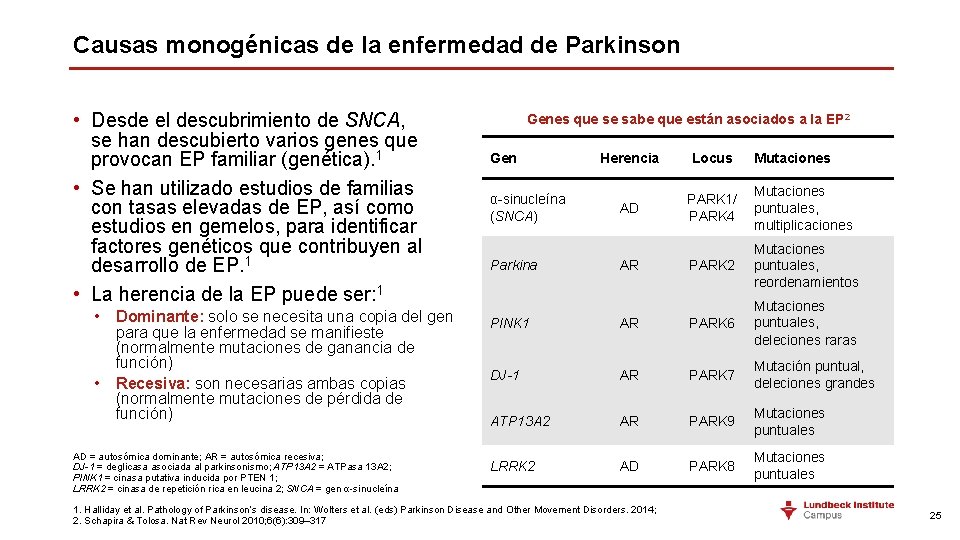
Causas monogénicas de la enfermedad de Parkinson • Desde el descubrimiento de SNCA, se han descubierto varios genes que provocan EP familiar (genética). 1 • Se han utilizado estudios de familias con tasas elevadas de EP, así como estudios en gemelos, para identificar factores genéticos que contribuyen al desarrollo de EP. 1 • La herencia de la EP puede ser: 1 • Dominante: solo se necesita una copia del gen para que la enfermedad se manifieste (normalmente mutaciones de ganancia de función) • Recesiva: son necesarias ambas copias (normalmente mutaciones de pérdida de función) AD = autosómica dominante; AR = autosómica recesiva; DJ-1 = deglicasa asociada al parkinsonismo; ATP 13 A 2 = ATPasa 13 A 2; PINK 1 = cinasa putativa inducida por PTEN 1; LRRK 2 = cinasa de repetición rica en leucina 2; SNCA = gen α-sinucleína Genes que se sabe que están asociados a la EP 2 Gen α-sinucleína (SNCA) Parkina Herencia Locus AD PARK 1/ PARK 4 Mutaciones puntuales, multiplicaciones PARK 2 Mutaciones puntuales, reordenamientos AR Mutaciones PINK 1 AR PARK 6 Mutaciones puntuales, deleciones raras DJ-1 AR PARK 7 Mutación puntual, deleciones grandes ATP 13 A 2 AR PARK 9 Mutaciones puntuales LRRK 2 AD PARK 8 Mutaciones puntuales 1. Halliday et al. Pathology of Parkinson’s disease. In: Wolters et al. (eds) Parkinson Disease and Other Movement Disorders. 2014; 2. Schapira & Tolosa. Nat Rev Neurol 2010; 6(6): 309– 317 25

Factores genéticos en la enfermedad de Parkinson que varían según la etnia • Cada vez se reconoce más que los antecedentes étnicos deben tenerse en cuenta al considerar el riesgo genético de desarrollar EP. 1 • Cuando se compararon los resultados de estudios GWAS realizados en diferentes grupos éticos, se observaron diferencias en las frecuencias de alelos y los tamaños de efecto. 1 • Esto significa que se puede caracterizar erróneamente a un paciente como paciente con un mayor riesgo de desarrollar EP, porque da un resultado positivo para una asociación genética que solo es un factor de riesgo en personas de un grupo étnico diferente. 1 1. Foo et al. Nat Rev Neurol 2012; 8: 508– 517 26

Vías comunes bajo la patogenia de la EP 27
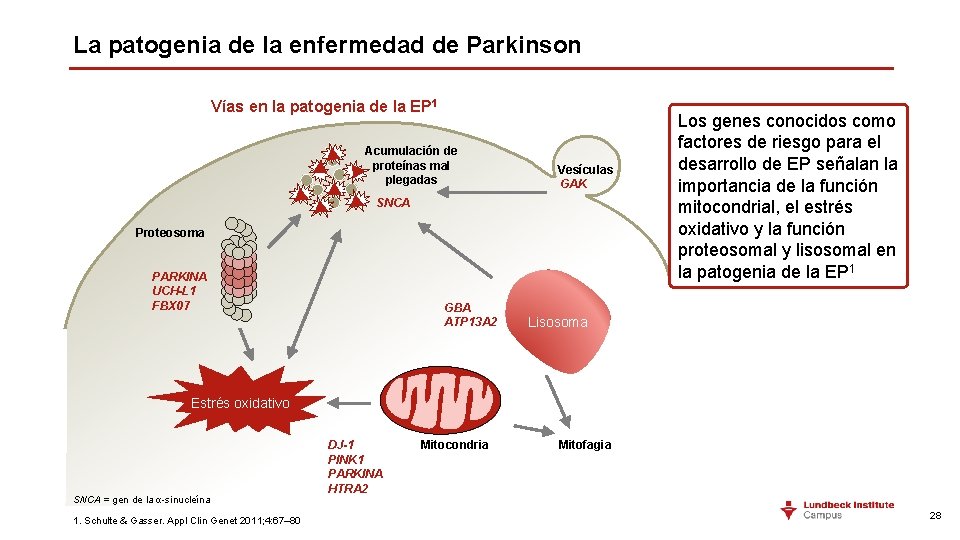
La patogenia de la enfermedad de Parkinson Vías en la patogenia de la EP 1 Acumulación de proteínas mal plegadas Vesículas GAK SNCA Proteosoma PARKINA UCH-L 1 FBX 07 GBA ATP 13 A 2 Los genes conocidos como factores de riesgo para el desarrollo de EP señalan la importancia de la función mitocondrial, el estrés oxidativo y la función proteosomal y lisosomal en la patogenia de la EP 1 Lisosoma Estrés oxidativo SNCA = gen de la α-sinucleína 1. Schulte & Gasser. Appl Clin Genet 2011; 4: 67– 80 DJ-1 PINK 1 PARKINA HTRA 2 Mitocondria Mitofagia 28
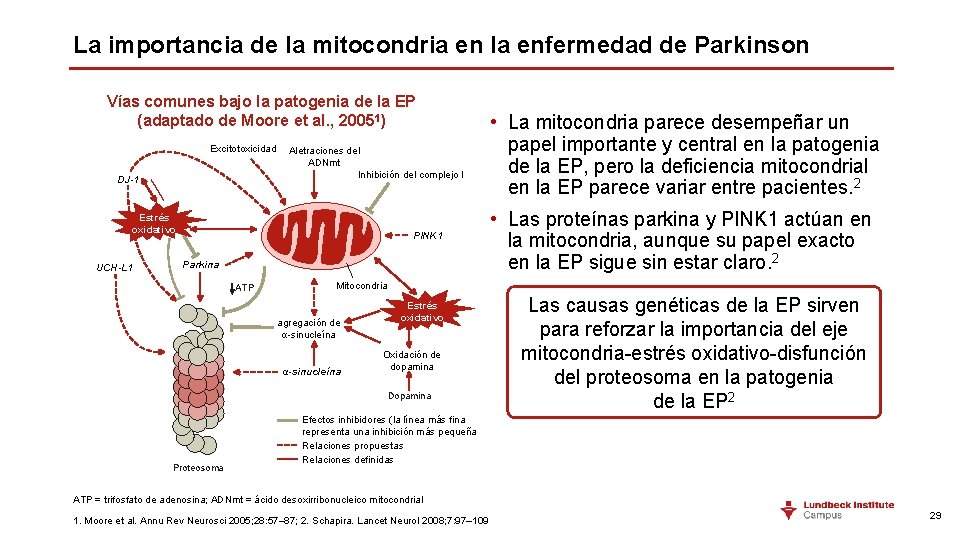
La importancia de la mitocondria en la enfermedad de Parkinson Vías comunes bajo la patogenia de la EP (adaptado de Moore et al. , 20051) Excitotoxicidad DJ-1 Aletraciones del ADNmt Inhibición del complejo I Estrés oxidativo UCH-L 1 PINK 1 Parkina ATP • Las proteínas parkina y PINK 1 actúan en la mitocondria, aunque su papel exacto en la EP sigue sin estar claro. 2 Mitocondria agregación de α-sinucleína Estrés oxidativo Oxidación de dopamina Dopamina Proteosoma • La mitocondria parece desempeñar un papel importante y central en la patogenia de la EP, pero la deficiencia mitocondrial en la EP parece variar entre pacientes. 2 Las causas genéticas de la EP sirven para reforzar la importancia del eje mitocondria-estrés oxidativo-disfunción del proteosoma en la patogenia de la EP 2 Efectos inhibidores (la línea más fina representa una inhibición más pequeña Relaciones propuestas Relaciones definidas ATP = trifosfato de adenosina; ADNmt = ácido desoxirribonucleico mitocondrial 1. Moore et al. Annu Rev Neurosci 2005; 28: 57– 87; 2. Schapira. Lancet Neurol 2008; 7: 97– 109 29

La disfunción mitocondrial desempeña un papel clave en la enfermedad de Parkinson • Se ha observado disfunción mitocondrial en células de la sustancia negra en pacientes con EP. 1 • Estas células muestran un deterioro en la actividad del complejo-I de la mitocondria. 1 • También se observa una disfunción similar en las plaquetas y en las células del músculo esquelético de los pacientes con EP. 1 • Varias mutaciones en el ADN mitocondrial se han asociado a la EP. 1 • Unos cíbridos (células de híbridos citoplasmáticos humanos que carecen de su propio ADN mitocondrial) que contienen ADN mitocondrial de pacientes con EP han mostrado menores niveles de actividad del complejo-I de la mitocondria. 1, 2 La disfunción mitocondrial, que se produce como resultado de mutaciones en el ADN mitocondrial, parece desempeñar un papel clave en la patogenia de la EP 1, 2 ADN = ácido desoxirribonucleico 1. Chaturvedi & Beal. Ann N Y Acad Sci 2008; 1147: 395– 412; 2. Trimmer et al. J Neurochem 2004; 88(4): 800– 812 30
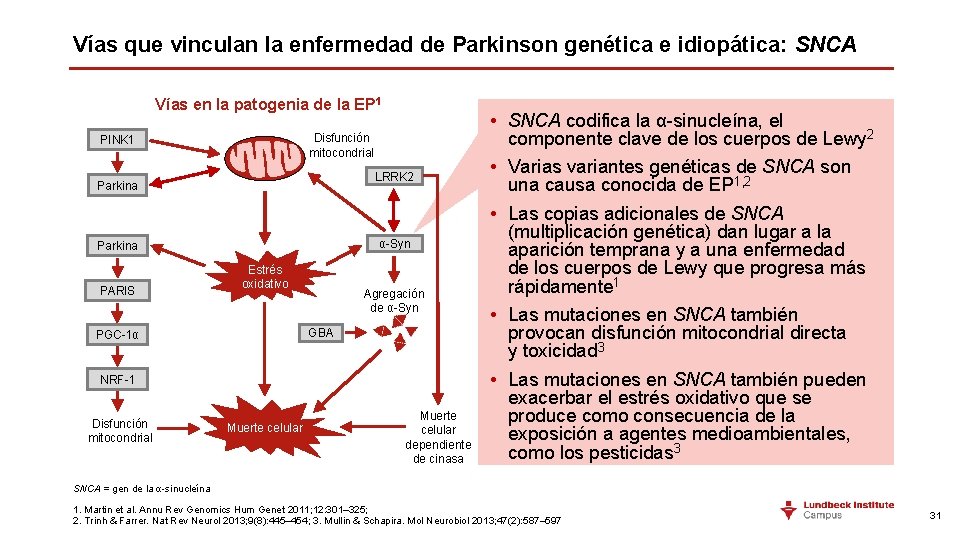
Vías que vinculan la enfermedad de Parkinson genética e idiopática: SNCA Vías en la patogenia de la EP 1 Disfunción mitocondrial PINK 1 LRRK 2 Parkina α-Syn Parkina PARIS Estrés oxidativo Agregación de α-Syn GBA PGC-1α NRF-1 Disfunción mitocondrial Muerte celular dependiente de cinasa • SNCA codifica la α-sinucleína, el componente clave de los cuerpos de Lewy 2 • Varias variantes genéticas de SNCA son una causa conocida de EP 1, 2 • Las copias adicionales de SNCA (multiplicación genética) dan lugar a la aparición temprana y a una enfermedad de los cuerpos de Lewy que progresa más rápidamente 1 • Las mutaciones en SNCA también provocan disfunción mitocondrial directa y toxicidad 3 • Las mutaciones en SNCA también pueden exacerbar el estrés oxidativo que se produce como consecuencia de la exposición a agentes medioambientales, como los pesticidas 3 SNCA = gen de la α-sinucleína 1. Martin et al. Annu Rev Genomics Hum Genet 2011; 12: 301– 325; 2. Trinh & Farrer. Nat Rev Neurol 2013; 9(8): 445– 454; 3. Mullin & Schapira. Mol Neurobiol 2013; 47(2): 587– 597 31
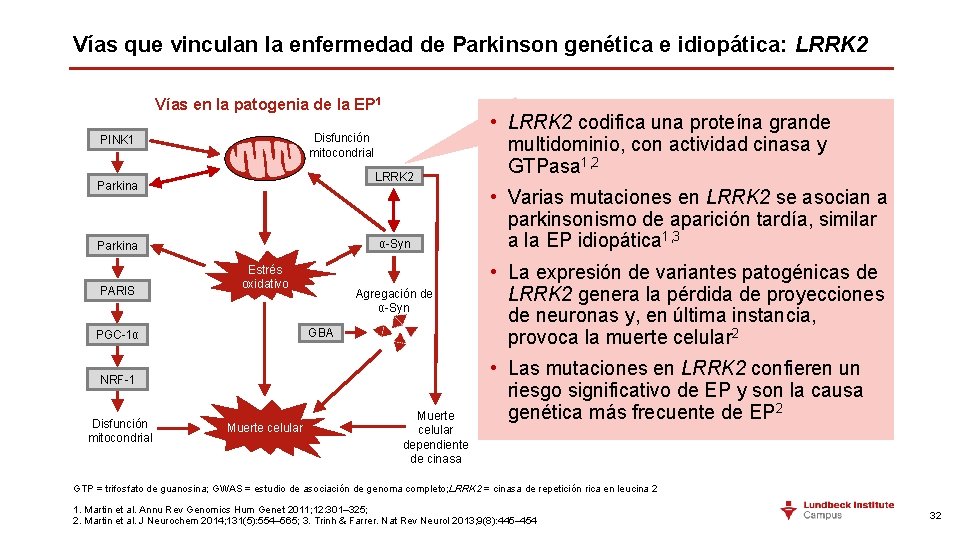
Vías que vinculan la enfermedad de Parkinson genética e idiopática: LRRK 2 Vías en la patogenia de la EP 1 Disfunción mitocondrial PINK 1 LRRK 2 Parkina α-Syn Parkina PARIS Estrés oxidativo Agregación de α-Syn GBA PGC-1α NRF-1 Disfunción mitocondrial Muerte celular dependiente de cinasa • LRRK 2 codifica una proteína grande multidominio, con actividad cinasa y GTPasa 1, 2 • Varias mutaciones en LRRK 2 se asocian a parkinsonismo de aparición tardía, similar a la EP idiopática 1, 3 • La expresión de variantes patogénicas de LRRK 2 genera la pérdida de proyecciones de neuronas y, en última instancia, provoca la muerte celular 2 • Las mutaciones en LRRK 2 confieren un riesgo significativo de EP y son la causa genética más frecuente de EP 2 GTP = trifosfato de guanosina; GWAS = estudio de asociación de genoma completo; LRRK 2 = cinasa de repetición rica en leucina 2 1. Martin et al. Annu Rev Genomics Hum Genet 2011; 12: 301– 325; 2. Martin et al. J Neurochem 2014; 131(5): 554– 565; 3. Trinh & Farrer. Nat Rev Neurol 2013; 9(8): 445– 454 32
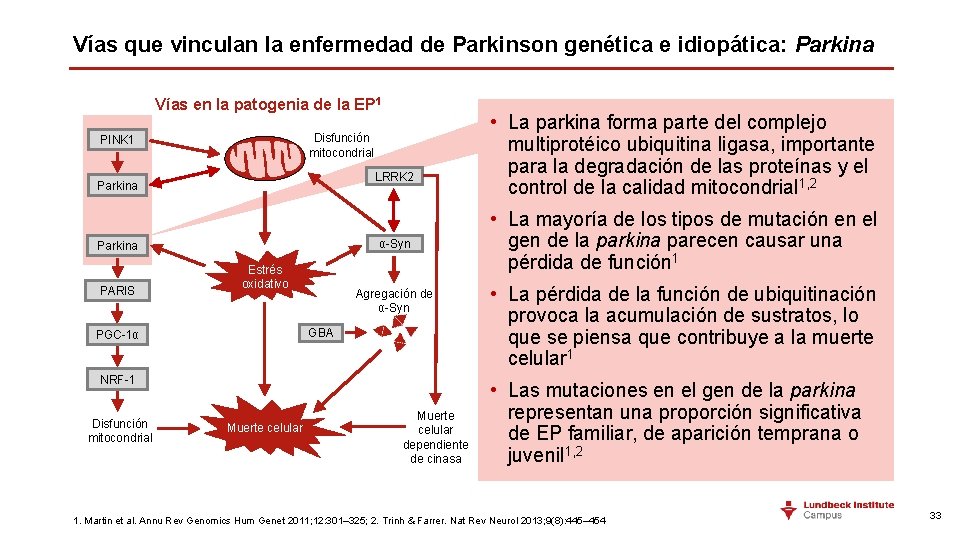
Vías que vinculan la enfermedad de Parkinson genética e idiopática: Parkina Vías en la patogenia de la EP 1 Disfunción mitocondrial PINK 1 LRRK 2 Parkina α-Syn Parkina PARIS Estrés oxidativo Agregación de α-Syn GBA PGC-1α NRF-1 Disfunción mitocondrial Muerte celular dependiente de cinasa • La parkina forma parte del complejo multiprotéico ubiquitina ligasa, importante para la degradación de las proteínas y el control de la calidad mitocondrial 1, 2 • La mayoría de los tipos de mutación en el gen de la parkina parecen causar una pérdida de función 1 • La pérdida de la función de ubiquitinación provoca la acumulación de sustratos, lo que se piensa que contribuye a la muerte celular 1 • Las mutaciones en el gen de la parkina representan una proporción significativa de EP familiar, de aparición temprana o juvenil 1, 2 1. Martin et al. Annu Rev Genomics Hum Genet 2011; 12: 301– 325; 2. Trinh & Farrer. Nat Rev Neurol 2013; 9(8): 445– 454 33

El papel de la neuroinflamación en la enfermedad de Parkinson • La presencia de α-sinucleína agregada desencadena la activación de microglías, lo que hace que: 1 • cambien sus características morfo-funcionales • aumenten las tasas de proliferación • liberen mediadores inflamatorios • Las moléculas inflamatorias reclutan leucocitos periféricos en el SNC, lo que fomenta la eliminación de residuos celulares. 1 • Los mediadores inflamatorios también pueden provocar neurodegeneración. 1 • La neurodegeneración activa aún más los mecanismos inflamatorios, lo que provoca un ciclo vicioso de inflamación y muerte neuronal. 1 SNC = sistema nervioso central 1. Rocha et al. Biomed Res Int 2015; 2015: 628192 34

Enfermedad de Gaucher: glucocerebrosidasa • Las mutaciones en el gen de la glucocerebrosidasa (GBA 1) causan la “enfermedad de Gaucher”, un trastorno de almacenamiento de lisosomas autosómico recesivo. 1 • Las personas homocigóticas con enfermedad de Gaucher y sus familiares heterocigóticos asintomáticos tienen un mayor riesgo de EP que la población general. 1 • El riesgo de vida de desarrollar EP en personas con mutaciones en GBA 1 es de hasta un 20 % a los 70 años y un 30 % a los 80 años. 1 • Se estima que la proporción de pacientes con EP con mutaciones en GBA 1 es del ~5 -10 %. 1 Las mutaciones en GBA 1 representan el factor de riesgo más importante para la EP identificado hasta la fecha 1 1. Schapira. Mol Cell Neurosci 2015; 66(Pt A): 37– 42 • Los pacientes con GBA 1 -EP siguen mostrando los síntomas fundamentales de EP, pero tienden a una aparición más joven y tienen un mayor riesgo de deterioro cognitivo. 1 • Las personas con mutación en GBA 1 sin evidencias clínicas de EP siguen mostrando las características prodrómicas de la enfermedad, como disfunción olfativa. 1 • La respuesta de los pacientes con GBA 1 -EP a la medicación dopaminérgica parece reproducir la de las personas con EP idiopática. 1 • Dada su importancia como factor de riesgo para la EP, GBA 1 se está examinando por su potencial terapéutico. 1 35
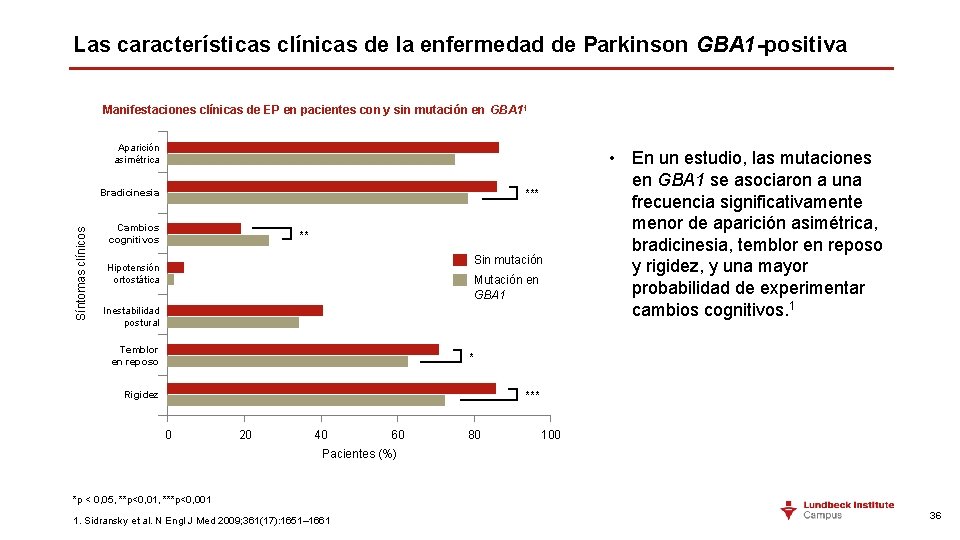
Las características clínicas de la enfermedad de Parkinson GBA 1 -positiva Manifestaciones clínicas de EP en pacientes con y sin mutación en GBA 11 Aparición asimétrica Síntomas clínicos Bradicinesia *** Cambios cognitivos ** Sin mutación Hipotensión ortostática Mutación en GBA 1 Inestabilidad postural Temblor en reposo • En un estudio, las mutaciones en GBA 1 se asociaron a una frecuencia significativamente menor de aparición asimétrica, bradicinesia, temblor en reposo y rigidez, y una mayor probabilidad de experimentar cambios cognitivos. 1 * Rigidez *** 0 20 40 60 80 100 Pacientes (%) *p < 0, 05, **p<0, 01, ***p<0, 001 1. Sidransky et al. N Engl J Med 2009; 361(17): 1651– 1661 36

Diseño de tratamientos basados en el modelo de patogenia; dónde actuar 37
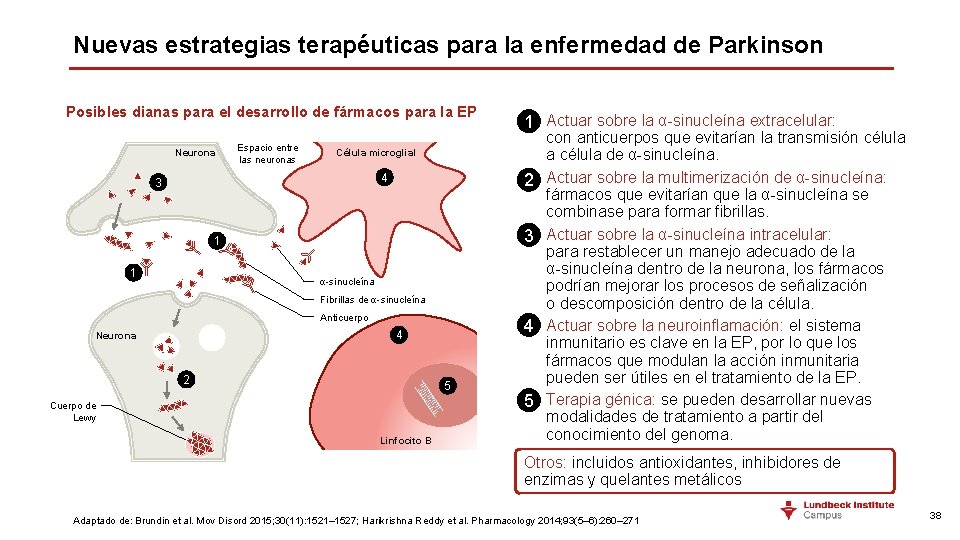
Nuevas estrategias terapéuticas para la enfermedad de Parkinson Posibles dianas para el desarrollo de fármacos para la EP Neurona Espacio entre las neuronas Célula microglial 4 3 1 1 α-sinucleína Fibrillas de α-sinucleína Anticuerpo 4 Neurona 2 5 Cuerpo de Lewy Linfocito B 1. 1 Actuar sobre la α-sinucleína extracelular: con anticuerpos que evitarían la transmisión célula a célula de α-sinucleína. 2. 2 Actuar sobre la multimerización de α-sinucleína: fármacos que evitarían que la α-sinucleína se combinase para formar fibrillas. 3. 3 Actuar sobre la α-sinucleína intracelular: para restablecer un manejo adecuado de la α-sinucleína dentro de la neurona, los fármacos podrían mejorar los procesos de señalización o descomposición dentro de la célula. 4. 4 Actuar sobre la neuroinflamación: el sistema inmunitario es clave en la EP, por lo que los fármacos que modulan la acción inmunitaria pueden ser útiles en el tratamiento de la EP. 5. 5 Terapia génica: se pueden desarrollar nuevas modalidades de tratamiento a partir del conocimiento del genoma. Otros: incluidos antioxidantes, inhibidores de enzimas y quelantes metálicos Adaptado de: Brundin et al. Mov Disord 2015; 30(11): 1521– 1527; Harikrishna Reddy et al. Pharmacology 2014; 93(5– 6): 260– 271 38

El futuro de los tratamientos para la enfermedad de Parkinson • Los investigadores se ven constantemente derrotados por los retos de encontrar estrategias modificadoras de la enfermedad en las enfermedades neurodegenerativas. 1, 2 • Estas estrategias modificadoras de la enfermedad, una vez descubiertas, pueden tener un mejor uso mediante: 1, 2 • combinación de fármacos con diferentes mecanismos de acción (por ejemplo, como se hace de forma rutinaria en el tratamiento de distintos tipos de cáncer) • apreciar que la EP es un conjunto de enfermedades y que es posible que haya que tratar cada fenotipo de forma diferente 1. Brundin et al. Mov Disord 2015; 30(11): 1521– 1527; 2. Kalia et al. Mov Disord 2015; 30(11): 1442– 1450 39
- Slides: 39