Experimentalvortrag OC Die Chemie der Orange Meike Griesel
































- Slides: 45

Experimentalvortrag OC „Die Chemie der Orange“ Meike Griesel WS 2009/2010

Gliederung 1. Einleitung 2. Inhaltsstoffe der Orange 2. 1. Limonen D 1, V 2 2. 2. Fruchtsäuren: Citronensäure D 2, V 3, D 3, V 4 2. 3. Vitamin C V 5, V 6 3. Schulrelevanz 4. Literatur 2

1. Einleitung

1. Einleitung Der Orangenbaum - wissenschaftlicher Name: Citrus sinensis - Baum ist 8 – 15 m hoch immergrün weiße, stark duftende Blüten Früchte haben runde oder breit-ovale Formen www. schulbilder. org - wichtigste Sorten: Blondorange, Navelorange, Blutorange 4

1. Einleitung Verbreitung - Herkunft: Südchina und Indochina - Verbreitung in vorchristlicher Zeit schon bis in den vorderen Orient - 15. – 16. Jahrhundert: Zierpflanze an europäischen Höfen - heute weltweit bedeutende Nutzpflanze in warmen Ländern - heutige Hauptanbaugebiete: Brasilien, USA, Mexiko, Indien 5

1. Einleitung Die Frucht - Schale kann grün, gelb oder orange sein - Schale ist 5 mm dick - weiße Albedo ist dünn - Fruchtfleisch ist in 10 – 14 Segmente unterteilt - pro Spalte bis zu 4 Kerne - www. food. foto 24. de Geschmack: aromatisch süß bis säuerlich süß 6

2. Inhaltsstoffe der Orange 7

2. Inhaltsstoffe der Orange Inhaltsstoffe In 100 g Fruchtfleisch durchschnittlich enthalten: Wasser: 85, 7 g Mineralstoffe: 0, 48 g Eiweiß: 1, 0 g Fruchtsäuren: 1, 13 g Fett: 0, 2 g Vitamin B 1: 0, 079 mg Kohlenhydrat 8, 25 g e: Vitamin B 2: 0. 042 mg Ballaststoffe: Vitamin C: 49, 4 mg 1, 6 g 8

2. 1. Limonen 9

2. 1. Limonen Demonstration 1: Isolation von Limonen aus Orangenschalen 10

2. 1. Limonen Durchführung 11

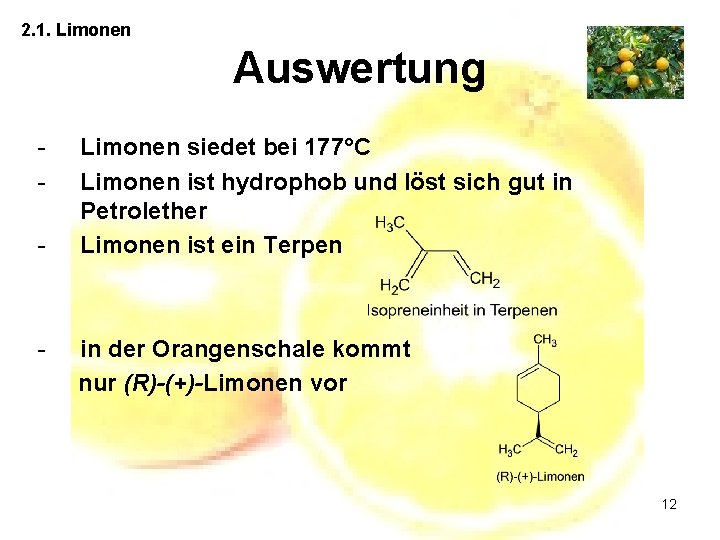
2. 1. Limonen Auswertung - - Limonen siedet bei 177°C Limonen ist hydrophob und löst sich gut in Petrolether Limonen ist ein Terpen in der Orangenschale kommt nur (R)-(+)-Limonen vor 12

2. 1. Limonen Versuch 1: Mischverhalten von Limonen 13

2. 1. Limonen Auswertung - „Ähnliches löst Ähnliches“ - Limonen ist lipophil und unpolar - Limonen ist mischbar mit unpolaren, lipophilen Substanzen wie Speiseöl oder Fette 14

2. 1. Limonen Alltagsbezug - Reinigungswirkung beruht auf lipophilen Eigenschaften des Limonens - außerdem schützen die Terpene in den Orangenschalen die Frucht vor Pilzen und Bakterien www. frosch. de ==> desinfizierende Wirkung von Limonen 15

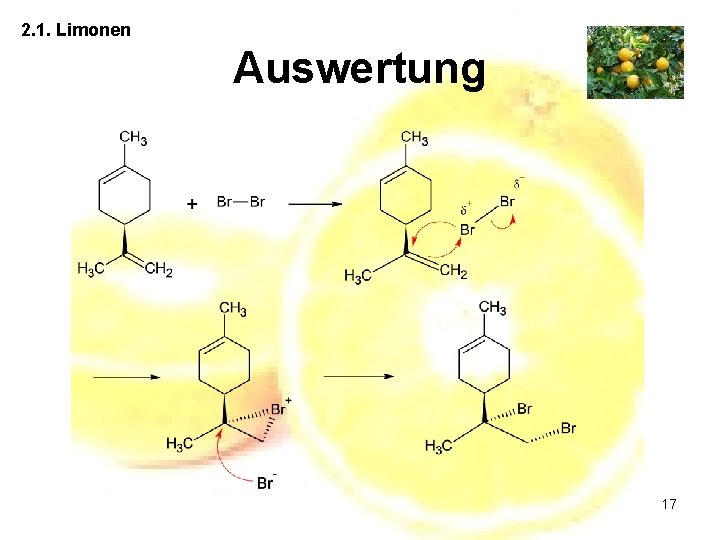
2. 1. Limonen Versuch 2: Bromierung von Limonen 16

2. 1. Limonen Auswertung 17

2. 2. Fruchtsäuren: Citronensäure 18

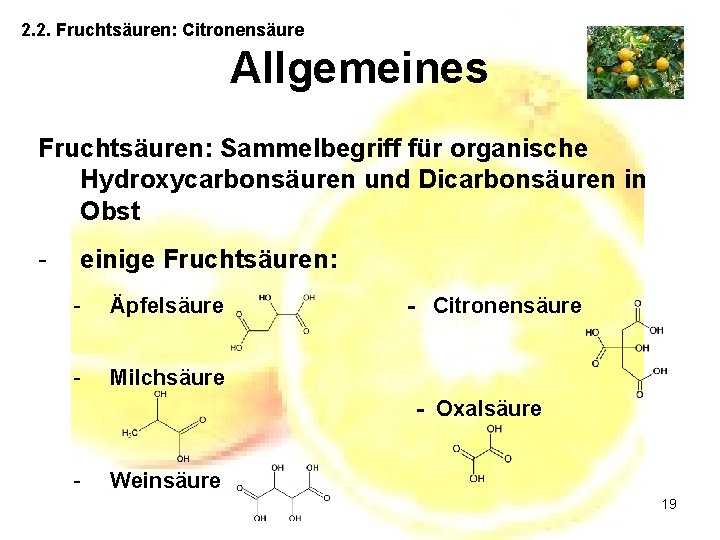
2. 2. Fruchtsäuren: Citronensäure Allgemeines Fruchtsäuren: Sammelbegriff für organische Hydroxycarbonsäuren und Dicarbonsäuren in Obst - einige Fruchtsäuren: - Äpfelsäure - Milchsäure - Citronensäure - Oxalsäure - Weinsäure 19

2. 2. Fruchtsäuren: Citronensäure Allgemeines (2) - in der Orange sind in 100 g Fruchtfleisch 1, 13 g Fruchtsäuren enthalten - davon etwa 1, 06 g Citronensäure - Citronensäure ist eine der am weitesten verbreiteten Fruchtsäuren im Pflanzenreich - Citronensäure ist ein Stoffwechselprodukt aller Organismen im Citratzyklus 20

2. 2. Fruchtsäuren: Citronensäure Demonstation 2: Isolierung von Citronensäure aus Orangen 21

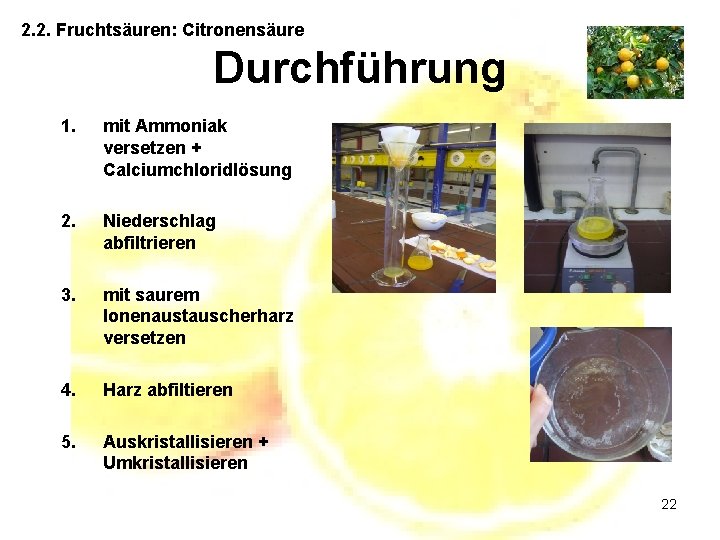
2. 2. Fruchtsäuren: Citronensäure Durchführung 1. mit Ammoniak versetzen + Calciumchloridlösung 2. Niederschlag abfiltrieren 3. mit saurem Ionenaustauscherharz versetzen 4. Harz abfiltieren 5. Auskristallisieren + Umkristallisieren 22

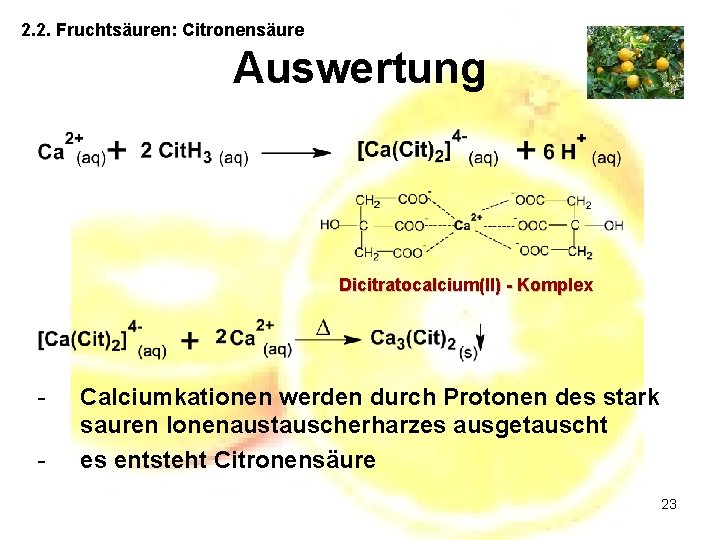
2. 2. Fruchtsäuren: Citronensäure Auswertung Dicitratocalcium(II) - Komplex - Calciumkationen werden durch Protonen des stark sauren Ionenaustauscherharzes ausgetauscht es entsteht Citronensäure 23

2. 2. Fruchtsäuren: Citronensäure Versuch 3: Nachweisreaktionen zur Identifizierung von Citronensäure 24

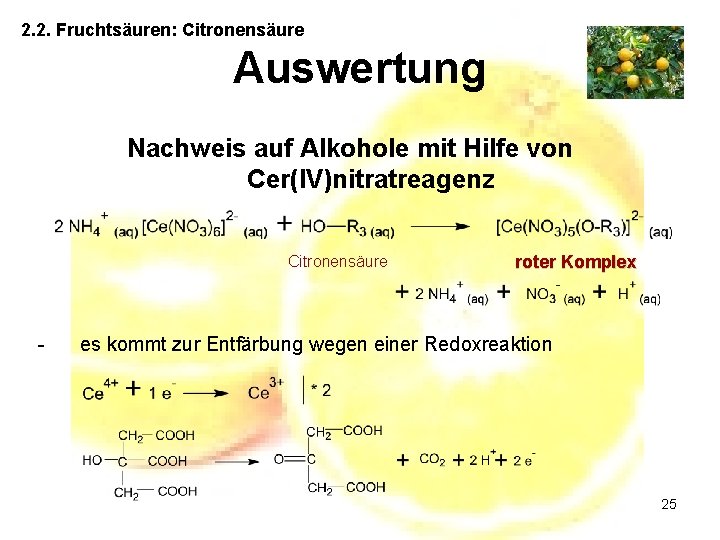
2. 2. Fruchtsäuren: Citronensäure Auswertung Nachweis auf Alkohole mit Hilfe von Cer(IV)nitratreagenz Citronensäure - roter Komplex es kommt zur Entfärbung wegen einer Redoxreaktion 25

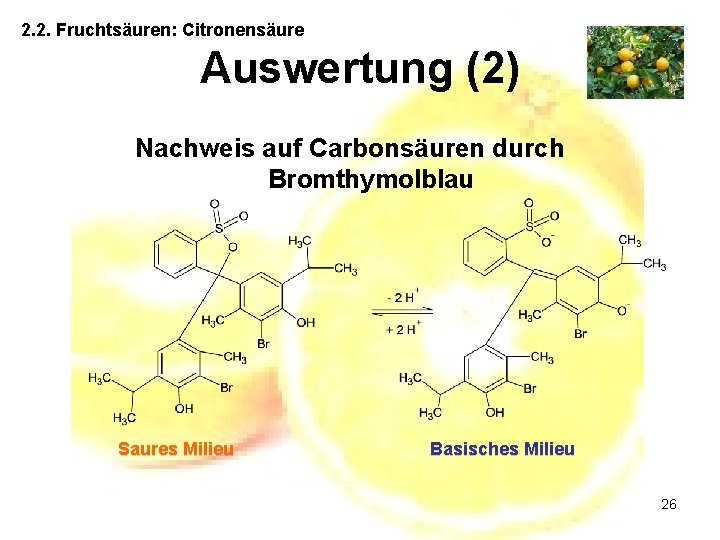
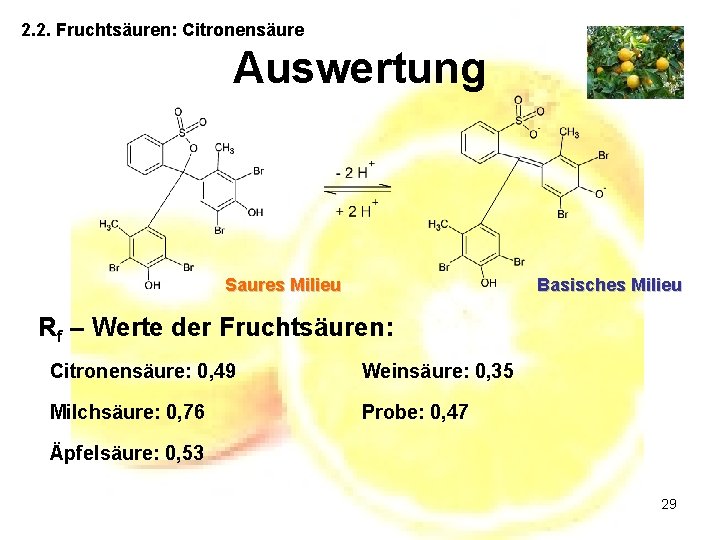
2. 2. Fruchtsäuren: Citronensäure Auswertung (2) Nachweis auf Carbonsäuren durch Bromthymolblau Saures Milieu Basisches Milieu 26

2. 2. Fruchtsäuren: Citronensäure Demonstration 3: DC von Fruchtsäuren zur Identifizierung der Citronensäure 27

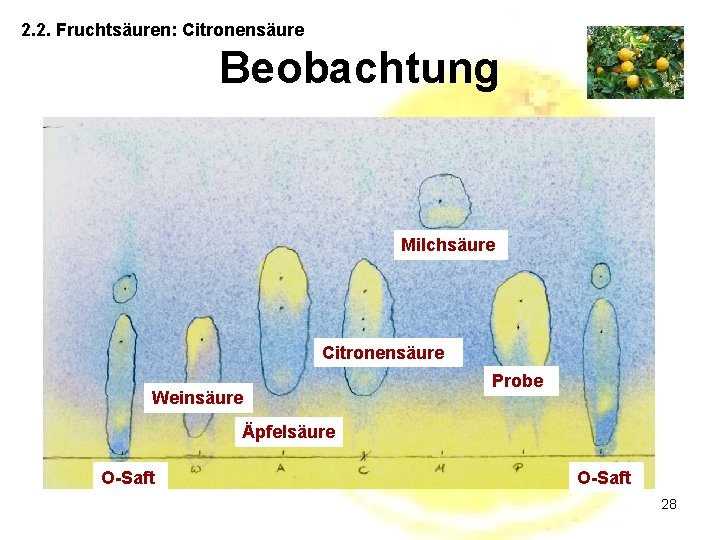
2. 2. Fruchtsäuren: Citronensäure Beobachtung Milchsäure Citronensäure Weinsäure Probe Äpfelsäure O-Saft 28

2. 2. Fruchtsäuren: Citronensäure Auswertung Saures Milieu Basisches Milieu Rf – Werte der Fruchtsäuren: Citronensäure: 0, 49 Weinsäure: 0, 35 Milchsäure: 0, 76 Probe: 0, 47 Äpfelsäure: 0, 53 29

2. 2. Fruchtsäuren: Citronensäure Versuch 4: Herstellung eines Polyesters aus Citronensäure 30

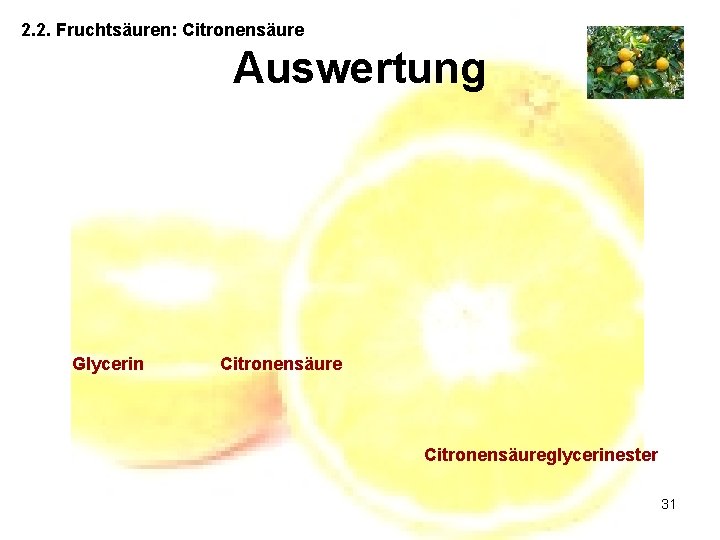
2. 2. Fruchtsäuren: Citronensäure Auswertung Glycerin Citronensäureglycerinester 31

2. 2. Fruchtsäuren: Citronensäure Auswertung (2) Mechanismus 32

2. 3. Vitamin C 33

2. 3. Vitamin C Allgemeines Vitamine: im Pflanzen- und Tierreich verbreitete Stoffe, die in der Nahrung nur in kleinen Mengen vorhanden sind und für das Wachstum und die Erhaltung des tierischen Körpers unentbehrlich sind (Hofmeister) - Vitamin C ist in vivo ein Quencher für Singulett. Sauerstoff Cofaktor bei der Hydoxylierung von Lysin- und Prolin-Resten bei der Biosynthese des Kollagens 34

2. 3. Vitamin C Allgemeines (2) - - - Die Biosynthese erfolgt bei Tieren und Pflanzen auf verschiedenen Wegen, geht aber immer von Glucose aus Tagesbedarf eines Menschen: 75 – 100 mg Vitamin C Mangel: Skorbut - Symptome: Zahnfleischbluten, Anfälligkeit für Infektionskrankheiten, Muskelschwund - Symptome gehen auf das Fehlen des Kollagens zurück in Nahrungsmittelindustrie dient Ascorbinsäure als Antioxidans 35

2. 3. Vitamin C Versuch 5: Gehaltsbestimmung von Vitamin C in Orangen 36

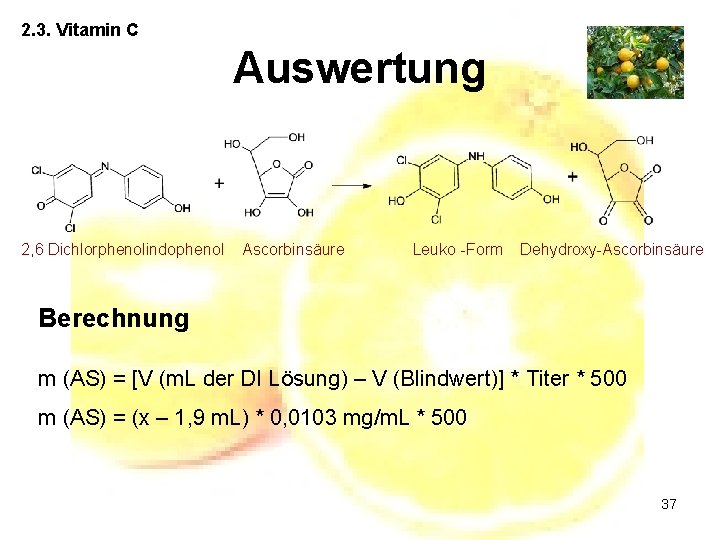
2. 3. Vitamin C Auswertung 2, 6 Dichlorphenolindophenol Ascorbinsäure Leuko -Form Dehydroxy-Ascorbinsäure Berechnung m (AS) = [V (m. L der DI Lösung) – V (Blindwert)] * Titer * 500 m (AS) = (x – 1, 9 m. L) * 0, 0103 mg/m. L * 500 37

2. 3. Vitamin C Versuch 6: Reduktionsmittel Ascorbinsäure 38

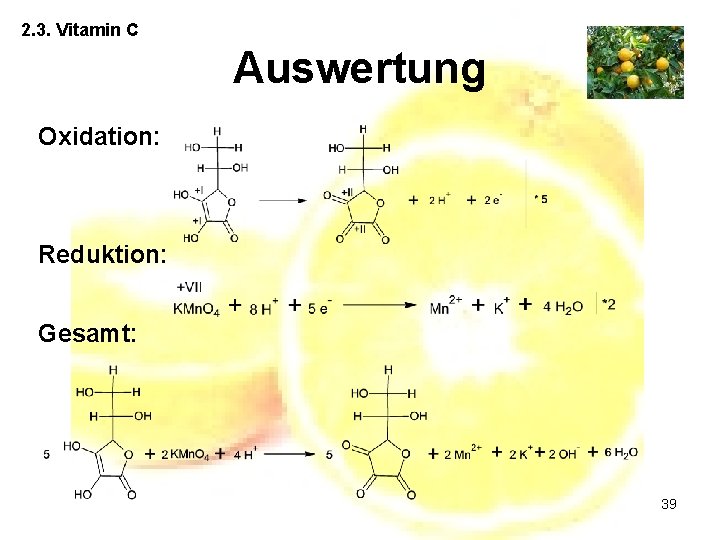
2. 3. Vitamin C Auswertung Oxidation: Reduktion: Gesamt: 39

2. 3. Vitamin C Auswertung (2) - der Lactonring der Ascorbinsäure ist im sauren stabil - die Oxidation von Ascorbinsäure zu Dehydroxy. Ascorbinsäure ist reversibel - Dehydroxy-Ascorbinsäure wird jedoch im neutralen oder basischen leicht hydrolytisch gespalten - Mechanismus ist nicht gesichert 40

3. Schulrelevanz 41

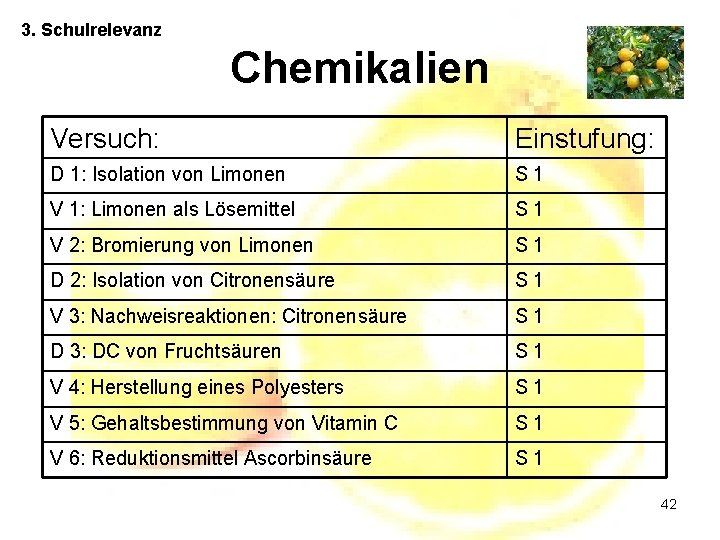
3. Schulrelevanz Chemikalien Versuch: Einstufung: D 1: Isolation von Limonen S 1 V 1: Limonen als Lösemittel S 1 V 2: Bromierung von Limonen S 1 D 2: Isolation von Citronensäure S 1 V 3: Nachweisreaktionen: Citronensäure S 1 D 3: DC von Fruchtsäuren S 1 V 4: Herstellung eines Polyesters S 1 V 5: Gehaltsbestimmung von Vitamin C S 1 V 6: Reduktionsmittel Ascorbinsäure S 1 42

3. Schulrelevanz Themen Klassenstufe: Thema: Versuch: 11. 1 Esterbildung V 4 Redoxgleichungen mit organischen Stoffen V 6 Duftstoffe; Lösungsmittel D 1, V 1 Alkansäuren im Alltag D 2, D 3 Identifizierung von Kohlenstoffverbindungen V 2, V 3 11. 2 Polymere mit besonderen V 4 Eigenschaften 12. 2 Nahrungsmittel D 3, V 5, V 6, 43

4. Literatur 44

4. Literaturverzeichnis - Arndt, C. et al. „Ester der Zitronensäure“. Praxis der Naturwissenschaften – Chemie. 2006 (8). 41 -44. Espel, D. „Orangen – eine Erfrischung für den Chemieunterricht“. Praxis der Naturwissenschaften – Chemie. 1999 (7). 17 -22. Gessner, Sandra. „Fett weg mit Orangenöl? “. Naturwissenschaften im Unterricht – Chemie. 1999 (53). 21 -23. Heinmann, R. „Einem unbekannten Stoff auf der Spur –“ Praxis der Naturwissenschaften – Chemie. 1999 (7). 26 -29. Nuhn, Peter. Naturstoffchemie. 4. Aufl. Stuttgart: S. Hirzel Verlag, 2006. Schwedt, Georg. Experimente mit Supermarktprodukten. Weinheim, Wiley-VCH Gmb. H & Co KGa. A, 2003. Vollhardt, Peter, K. C. und Neil E. Schore. Organische Chemie. 4. Aufl. Weinheim: Wiley-VCH Gmb. H & Co KGa. A, 2005. 45