Chemie der Aquaristik Chemie der Aquaristik 1 Lebenswelt

Chemie der Aquaristik

Chemie der Aquaristik 1. Lebenswelt Aquarium- Einführung 2. Das Aquarienwasser • Kohlenstoffdioxid-Carbonat-Kreislauf • Sauerstoffgehalt • Stickstoffkreislauf • Schwermetalle • Pflanzen und ihre Nährstoffe 3. Bodengrund 4. Schulrelevanz
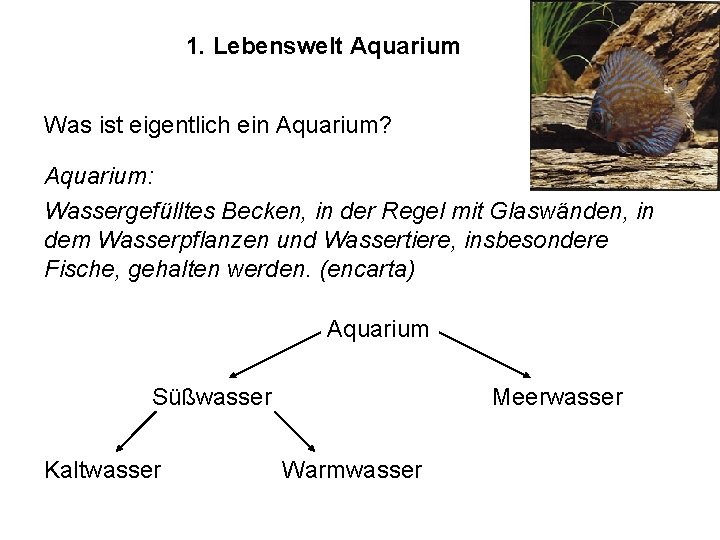
1. Lebenswelt Aquarium Was ist eigentlich ein Aquarium? Aquarium: Wassergefülltes Becken, in der Regel mit Glaswänden, in dem Wasserpflanzen und Wassertiere, insbesondere Fische, gehalten werden. (encarta) Aquarium Süßwasser Kaltwasser Meerwasser Warmwasser
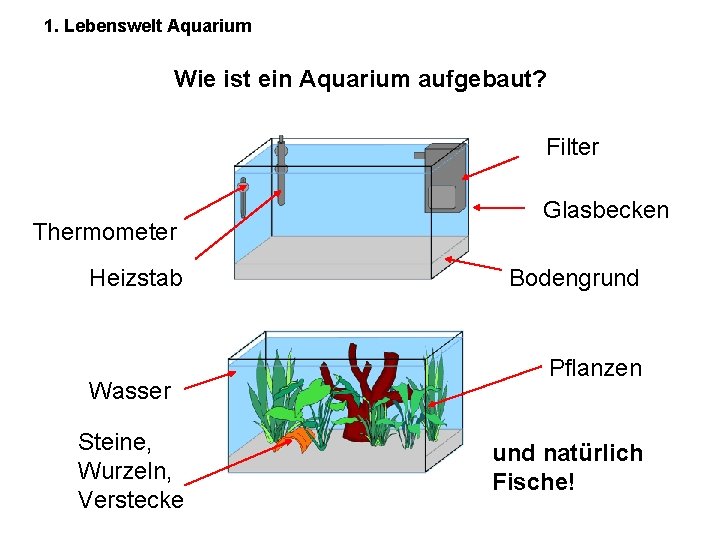
1. Lebenswelt Aquarium Wie ist ein Aquarium aufgebaut? Filter Thermometer Heizstab Wasser Steine, Wurzeln, Verstecke Glasbecken Bodengrund Pflanzen und natürlich Fische!

2. Das Aquarienwasser • Fische: Enger Kontakt zu Wasser • Atmen über Kiemen– Nehmen gelöste Stoffe auf • Aquarium sollte möglichst natürlicher Lebensraum sein

2. Das Aquarienwasser Natur • Wasserqualität prägende Faktoren in Gleichgewicht • Tiere, Pflanzen, Bakterien halten Stoffkreisläufe im Gang • Giftstoffabbau • Wasser lebt Aquarium • Wasser aus Leitung biologisch tot • Abgeschlossenes System • Mensch: Nachahmung der Gleichgewichte

2. 1 Das Aquarienwasser Der p. H-Wert im tropischen Aquarium: • angelehnt an natürlichen Lebensraum der Fische • leicht sauer: p. H 6 -7 p. H-Wert entscheidend für: • Löslichkeit von Stoffen • Lage von Gleichgewichten (z. B. : NH 3/NH 4(aq)+)

2. 1 Das Aquarienwasser- Der p. H-Wert Versuch 1 Zusammenhang p. H-Wert CO 2 -Gehalt
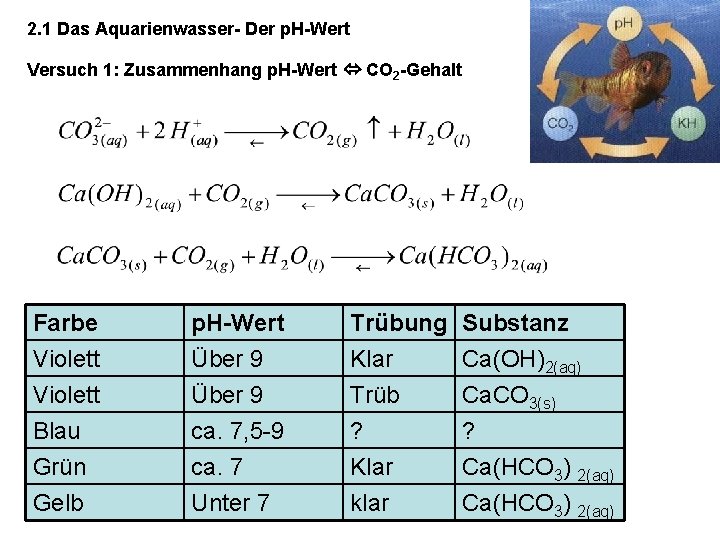
2. 1 Das Aquarienwasser- Der p. H-Wert Versuch 1: Zusammenhang p. H-Wert CO 2 -Gehalt Farbe Violett Blau p. H-Wert Über 9 ca. 7, 5 -9 Trübung Klar Trüb ? Substanz Ca(OH)2(aq) Ca. CO 3(s) ? Grün Gelb ca. 7 Unter 7 Klar klar Ca(HCO 3) 2(aq)

2. 1 Das Aquarienwasser Der p. H-Wert im Aquarium p. H-Wert abhängig von Carbonathärte & CO 2 -Gehalt: Massenwirkungsgesetz: p. H-Wert umso niedriger • je höher CO 2 -Gehalt • je niedriger Konzentration an Hydrogencarbonat-Ionen

2. 1 Das Aquarienwasser- Der p. H-Wert Leitungswasser: • neutral bis schwach basisch • meist Senkung nötig Senkung durch: • Kohlenstoffdioxid-Düngung • Torffilterung (Huminsäure) • Anorganische Säuren (Schwefelsäure, Salzsäure)
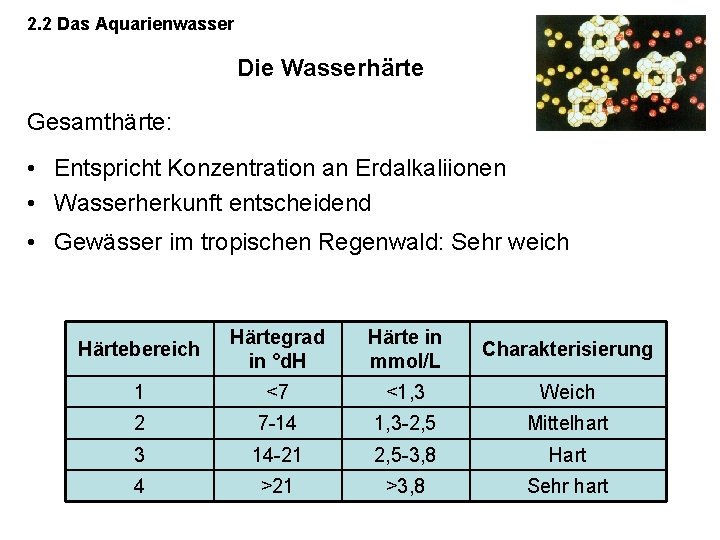
2. 2 Das Aquarienwasser Die Wasserhärte Gesamthärte: • Entspricht Konzentration an Erdalkaliionen • Wasserherkunft entscheidend • Gewässer im tropischen Regenwald: Sehr weich Härtebereich Härtegrad in °d. H Härte in mmol/L Charakterisierung 1 <7 <1, 3 Weich 2 7 -14 1, 3 -2, 5 Mittelhart 3 14 -21 2, 5 -3, 8 Hart 4 >21 >3, 8 Sehr hart

2. 2. Das Aquarienwasser- Wasserhärte Carbonathärte: • Zu Erdalkalimetallionen äquivalente Menge an Carbonatoder Hydrogencarbonationen • Zusammenhang zw. p. H-Wert, Carbonathärte & gelöstem CO 2 • Zugabe von CO 2 => senkt p. H-Wert, erhöht Carbonathärte • Zugabe von Säuren=> senkt p. H-Wert & Carbonathärte

2. 2 Das Aquarienwasser- Wasserhärte Demo 1 Torf als Ionenaustauscher
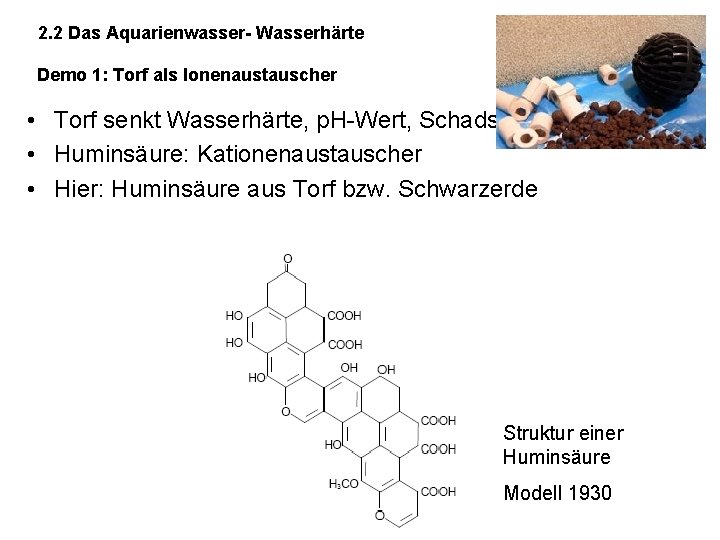
2. 2 Das Aquarienwasser- Wasserhärte Demo 1: Torf als Ionenaustauscher • Torf senkt Wasserhärte, p. H-Wert, Schadstoffkonzentration • Huminsäure: Kationenaustauscher • Hier: Huminsäure aus Torf bzw. Schwarzerde Struktur einer Huminsäure Modell 1930
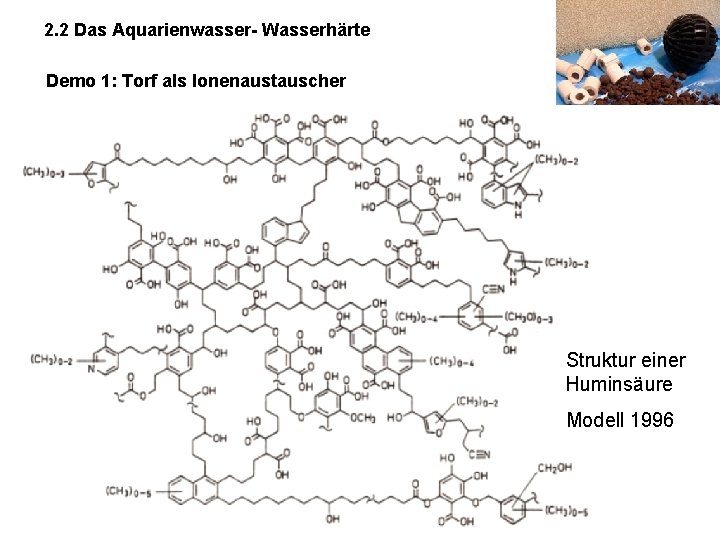
2. 2 Das Aquarienwasser- Wasserhärte Demo 1: Torf als Ionenaustauscher Struktur einer Huminsäure Modell 1996

2. 3. Das Aquarienwasser Gelöster Sauerstoff wichtig für: • Atmung der Fische • aeroben Schadstoffabbau • Vorliegen Eisen(II)- /Eisen(III)-Ionen Wie kann Sauerstoff in Aquarium gelangen? • Oberfläche • Fotosynthese (Wasserpflanzen) • Sauerstoffmembranpumpe

2. 3. Das Aquarienwasser- Gelöster Sauerstoff Menge des gelösten Sauerstoffs abhängig von: • Größe der Oberfläche • Oberflächenbewegung • Anzahl und Größe der Pflanzen • Druck und Temperatur +15°C Temperatur O 2(aq) in mg/L in °C (p=1 bar) 10 11, 2 25 8, 35 -25%

2. 3. Das Aquarienwasser- Gelöster Sauerstoff Versuch 2 Bestimmung des Sauerstoffgehalts nach Winkler

2. 3. Das Aquarienwasser- Gelöster Sauerstoff Versuch 2: Bestimmung des Sauerstoffgehalts nach Winkler 1. Zugabe von Fällungsreagenz 2. Falls Sauerstoff in Probe:

2. 3. Das Aquarienwasser- Gelöster Sauerstoff Versuch 2: Bestimmung des Sauerstoffgehalts nach Winkler 3. Ansäuern => Freisetzen von Iod => Braunfärbung der Lösung 4. Titration von freiem Iod mit Natriumthiosulfat =>Entfärbung Endpunkt: Stärkeindikator (blau => farblos)

2. 3. Das Aquarienwasser- Gelöster Sauerstoff Versuch 2: Bestimmung des Sauerstoffgehalts nach Winkler Berechnung absolute Sauerstoffkonzentration: Faktor 0, 08: 1 m. L 0, 01 M Na 2 S 2 O 3 -Lsg. ~ 8 mg O 2 V(Zusätze) = 2 m. L
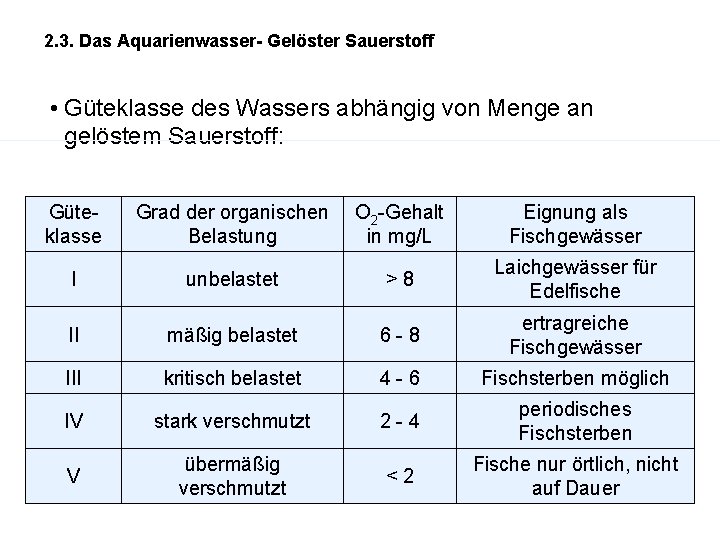
2. 3. Das Aquarienwasser- Gelöster Sauerstoff • Güteklasse des Wassers abhängig von Menge an gelöstem Sauerstoff: Güteklasse Grad der organischen Belastung O 2 -Gehalt in mg/L Eignung als Fischgewässer I unbelastet >8 Laichgewässer für Edelfische II mäßig belastet 6 -8 ertragreiche Fischgewässer III kritisch belastet 4 -6 Fischsterben möglich IV stark verschmutzt 2 -4 periodisches Fischsterben V übermäßig verschmutzt <2 Fische nur örtlich, nicht auf Dauer
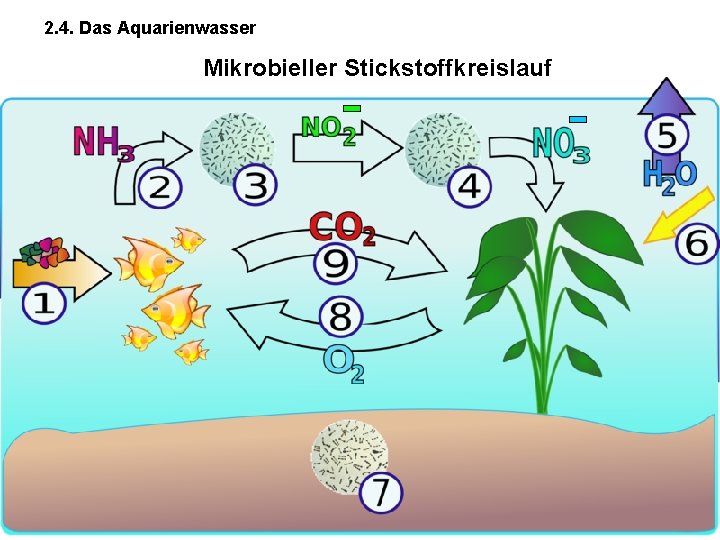
2. 4. Das Aquarienwasser Mikrobieller Stickstoffkreislauf
2. 4. 1. Das Aquarienwasser Ammonifizierung • Organische Stickstoffverbindungen von Bakterien und Pilzen mit Urease (Enzym) hydrolysiert

2. 4. 1. Das Aquarienwasser- Ammonifizierung Versuch 3 Warum ist Ammoniak gefährlich für Fische?
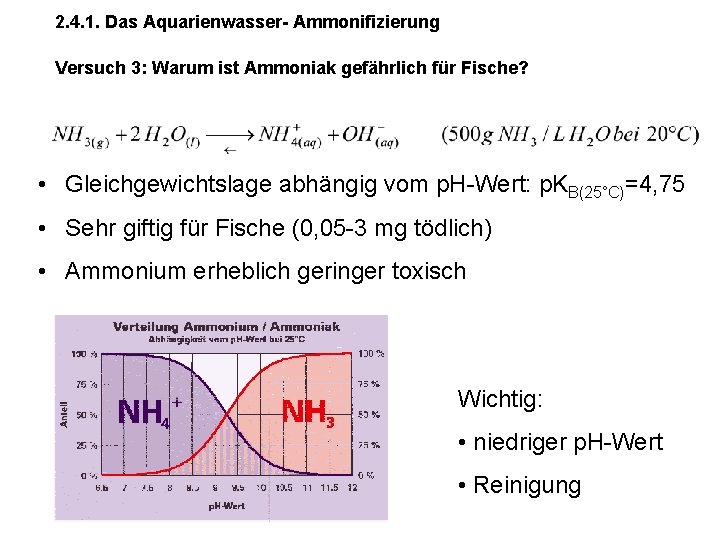
2. 4. 1. Das Aquarienwasser- Ammonifizierung Versuch 3: Warum ist Ammoniak gefährlich für Fische? • Gleichgewichtslage abhängig vom p. H-Wert: p. KB(25°C)=4, 75 • Sehr giftig für Fische (0, 05 -3 mg tödlich) • Ammonium erheblich geringer toxisch Wichtig: • niedriger p. H-Wert • Reinigung

2. 4. 2. Das Aquarienwasser Nitrifikation • Aerobe Umwandlung von Ammonium- über Nitrit- zu Nitrat-Ionen mit nitrifizierenden Bakterien 1. Nitritation: 2. Nitratation:

2. 4. 2. Das Aquarienwasser- Nitrifikation: • Wichtigster Vorgang zum Schadstoffabbau • Im Filter, Boden (Bakterien auf Oberfläche) • Oxidative Umwandlung

2. 4. 2. Das Aquarienwasser- Nitrifikation Versuch 3: Halbquantitativer Nachweis von Nitrat Warum Nitrat messen? • Große Mengen für Fische tödlich • Starke Förderung des Algenwachstums
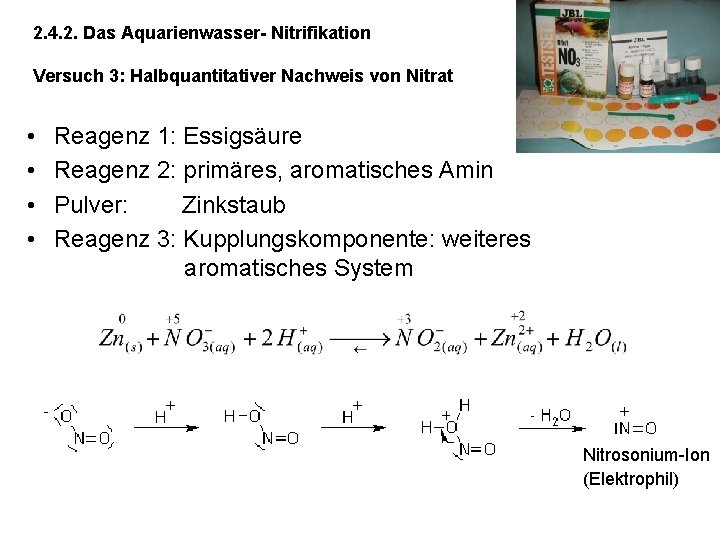
2. 4. 2. Das Aquarienwasser- Nitrifikation Versuch 3: Halbquantitativer Nachweis von Nitrat • • Reagenz 1: Essigsäure Reagenz 2: primäres, aromatisches Amin Pulver: Zinkstaub Reagenz 3: Kupplungskomponente: weiteres aromatisches System Nitrosonium-Ion (Elektrophil)
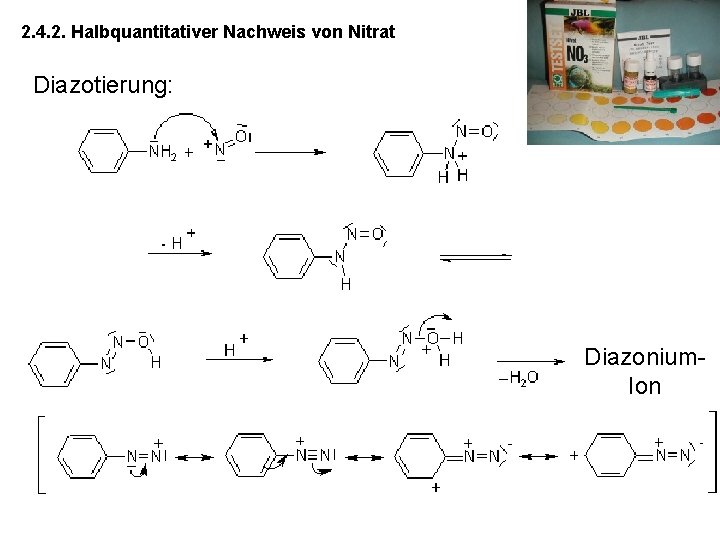
2. 4. 2. Halbquantitativer Nachweis von Nitrat Diazotierung: Diazonium. Ion
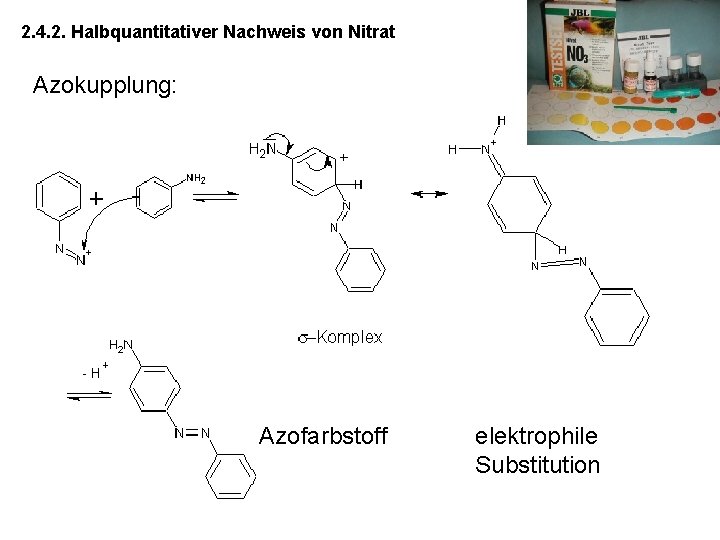
2. 4. 2. Halbquantitativer Nachweis von Nitrat Azokupplung: Azofarbstoff elektrophile Substitution

2. 5. Das Aquarienwasser Kupfer(II)-Ionen • Wie kommen Kupferionen in Aquarienwasser? – Wasserwechsel – Arbeiten an Leitungen – Medikamente • Cu 2+-Ionen toxisch (für Bakterien und Fische) • andere Schwermetalle ebenso möglich • Entfernung von Schwermetallen: – Wasserwechsel – Wasseraufbereiter(EDTA)

2. 7. Das Aquarienwasser- Kupfer(II)-Ionen Versuch 4 Selbstgebastelte Kupfer-Teststäbchen
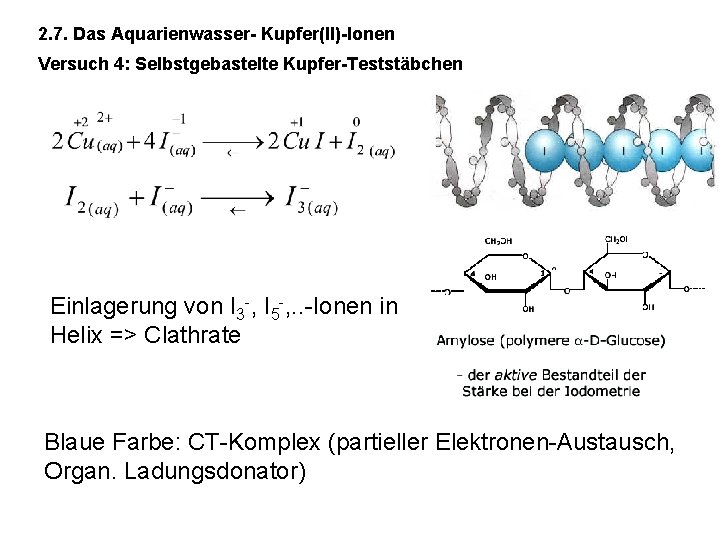
2. 7. Das Aquarienwasser- Kupfer(II)-Ionen Versuch 4: Selbstgebastelte Kupfer-Teststäbchen Einlagerung von I 3 -, I 5 -, . . -Ionen in Helix => Clathrate Blaue Farbe: CT-Komplex (partieller Elektronen-Austausch, Organ. Ladungsdonator)

2. 6. Das Aquarienwasser Wasserpflanzen • Pflanzen: – produzieren Sauerstoff (Fotosynthese) – reduzieren Schadstoffkonzentration – bieten Versteckmöglichkeiten für Fische – sehen schön aus
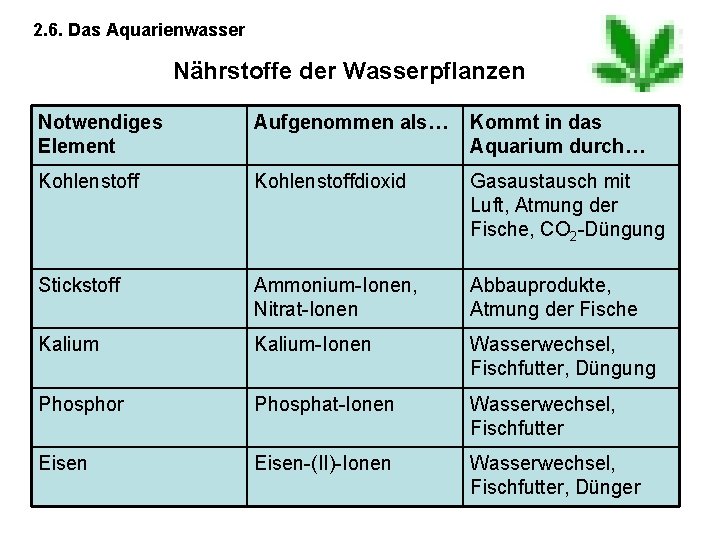
2. 6. Das Aquarienwasser Nährstoffe der Wasserpflanzen Notwendiges Element Aufgenommen als… Kommt in das Aquarium durch… Kohlenstoffdioxid Gasaustausch mit Luft, Atmung der Fische, CO 2 -Düngung Stickstoff Ammonium-Ionen, Nitrat-Ionen Abbauprodukte, Atmung der Fische Kalium-Ionen Wasserwechsel, Fischfutter, Düngung Phosphor Phosphat-Ionen Wasserwechsel, Fischfutter Eisen-(II)-Ionen Wasserwechsel, Fischfutter, Dünger

2. 6. Das Aquarienwasser- Eisen(II)- und Eisen(III)-Ionen Versuch 5 Eisen(II)-Ionen im Aquarienwasser

2. 5. Das Aquarienwasser- Eisen(II)- und Eisen(III)-Ionen Versuch 5: Eisen(II)-Ionen im Aquarienwasser • Reaktion mit Sauerstoff zu schwerlöslichen Eisen(III)Niederschlägen: • Oxidation p. H-Wert abhängig: p. H-Wert-Erhöhung => drastischen Erhöhung Reaktionsgeschwindigkeit

2. 5. Das Aquarienwasser- Eisen(II)- und Eisen(III)-Ionen • Pflanzen können nur Eisen(II)-Ionen aufnehmen • Im Aquarium aerobes Milieu: Eisenionen: Eisen(III)-Niederschlag (Filter, Bodengrund) • Förderlich für Aufnahme von Eisen(II)-Ionen durch Pflanzen: – niedriger p. H-Wert – anaerobes Milieu

2. 5. Das Aquarienwasser- Eisen(II)- und Eisen(III)-Ionen • p. H-Wert überall konstant • Sauerstoffgehalt unterschiedlich: Untere Bodenschichten anaerobes Milieu: Reduktion: Eisen(III)- zu Eisen(II)-Ionen • Wasserpflanzendünger: Eisen(II)-Ionen in Chelatkomplexen
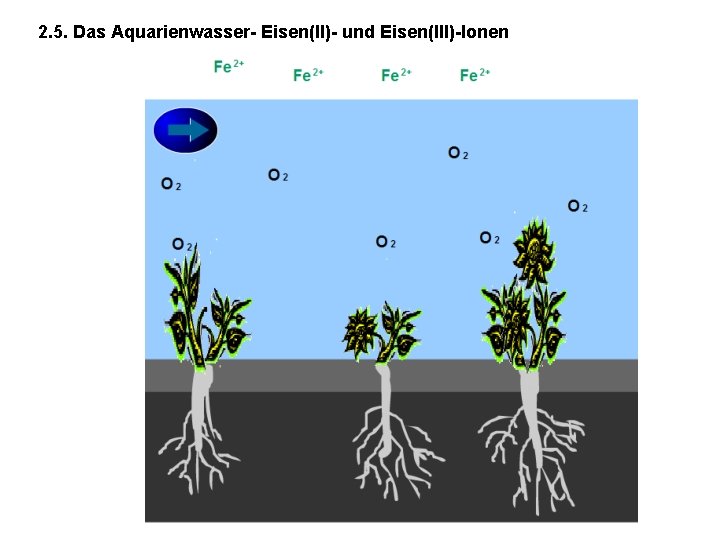
2. 5. Das Aquarienwasser- Eisen(II)- und Eisen(III)-Ionen

3. Bodengrund • Funktion: – Halt und Nährstoffe für Pflanzenwurzel – Futter für Fische – Lebensraum: Schadstoffe abbauende Mikroorganismen Spezielles Pflanzensubstrat Aquarienkies oder Sand (5 cm) (Nährstoffdepot) (aerobe Schicht) (anaerobe Schicht, sauerstoffarm)

3. Bodengrund • Aquarienboden verwittert => gelöste Stoffe in Aquarium • Bspl. Verwitterungsprozess: Kalkstein: • Verwitterung => Wasseraufhärtung: Verwendung von Quarz-Kies

4. Schulrelevanz Lehrplan für G 9: Klasse 8: • Ökologische Bildung und Umwelterziehung: Wasserverschmutzung • Aufbereitung von Abwässern, Trink- und Flusswasser • Wasseruntersuchung mit analytischen Schnelltestverfahren Klasse 10: • Stoffmengenkonzentrationen; Maßanalyse: Titration • Stoffkreisläufe

4. Schulrelevanz Klasse 13: • Umkehrbare Reaktionen und chemisches Gleichgewicht • Massenwirkungsgesetz • Prinzip vom Zwang • Sauerstofflöslichkeit in Wasser • Umweltchemie / Umweltanalytik

Vielen Dank!
- Slides: 48