Philipps Universitt Marburg Fachbereich Chemie 15 Experimentalvortrag Sommersemester

Philipps Universität Marburg Fachbereich Chemie (15) Experimentalvortrag Sommersemester 2007 Sauerstoff Referent: Stefan Dönges
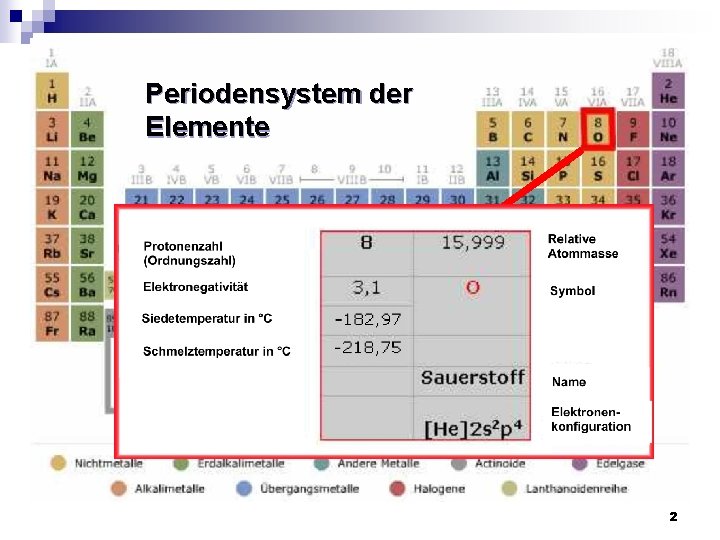
Periodensystem der Elemente 2

Gliederung Allgemeines n Entstehung n Vorkommen n Darstellung n Verwendung n Eigenschaften n Schulische Relevanz n 3

Allgemeines n Farb- und geruchloses Gas n Typisches Nichtmetall n Reagiert mit den meisten Elementen des PSE direkt n Oxidationsmittel Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 4

n Gasf. Sauerstoff: reaktionsträge n Fl. Sauerstoff: wirkt stark oxidierend n Oxidationsprozesse: exotherm (Bsp. : „Verbrennungsprozesse“) n Diradikal n Paramagnetisch Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 5
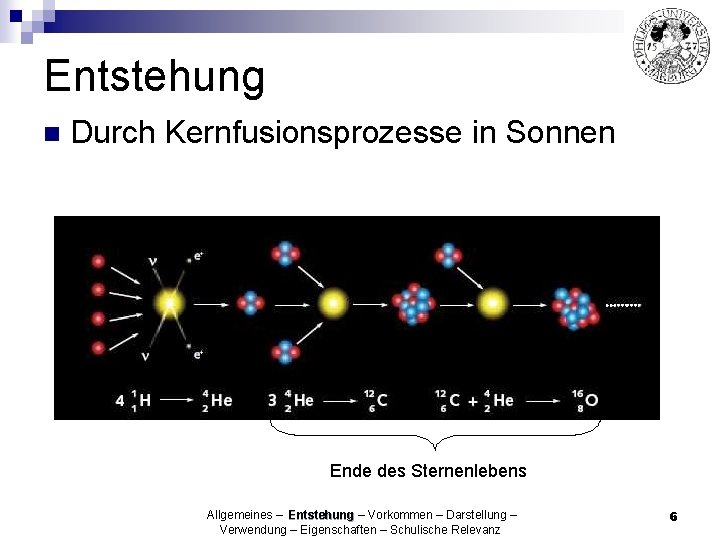
Entstehung n Durch Kernfusionsprozesse in Sonnen Ende des Sternenlebens Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 6

Verteilung der Elemente im Weltraum: Durch Sonneneruptionen Durch Supernovae Explosionen Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 7

Vorkommen Am häufigsten vorkommendes Element (48, 9%) Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 8

§ Bsp. : Erdkruste Massenanteil: 50, 5 % § Bsp. : Wasser Massenanteil: 88, 8 % § Bsp. : Atmosphäre Massenanteil: 23, 16 % Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 9
![Bsp. : Atmosphäre: Prozent Name 78, 08 Stickstoff [N 2] 20, 95 Sauerstoff [O Bsp. : Atmosphäre: Prozent Name 78, 08 Stickstoff [N 2] 20, 95 Sauerstoff [O](http://slidetodoc.com/presentation_image/4cce7be8891894ede3ecdff02885f0b4/image-10.jpg)
Bsp. : Atmosphäre: Prozent Name 78, 08 Stickstoff [N 2] 20, 95 Sauerstoff [O 2] 0, 93 Argon [Ar] 0, 34 Kohlendioxid [CO 2] 0, 0018 Neon [Ne] 0, 0005 Helium [He] Volumenprozent Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 10
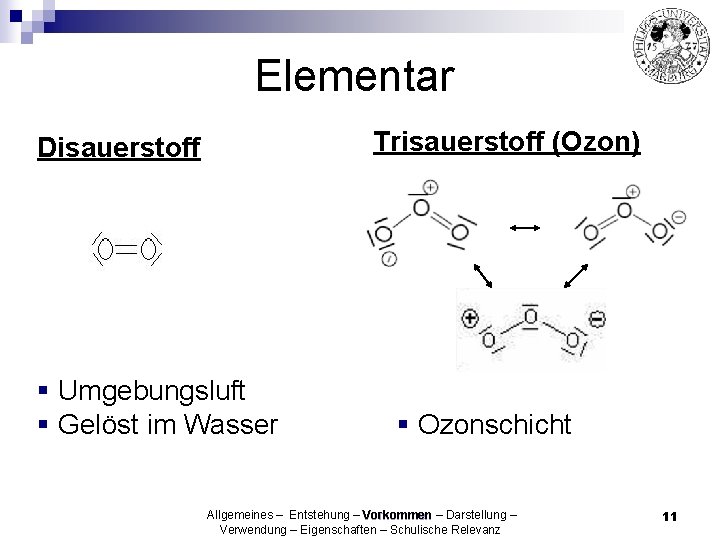
Elementar Trisauerstoff (Ozon) Disauerstoff § Umgebungsluft § Gelöst im Wasser § Ozonschicht Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 11

Disauerstoff Singulett Sauerstoff Triplett Sauerstoff 3 O 2 ( ) 1 O Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 2 ( ) 12
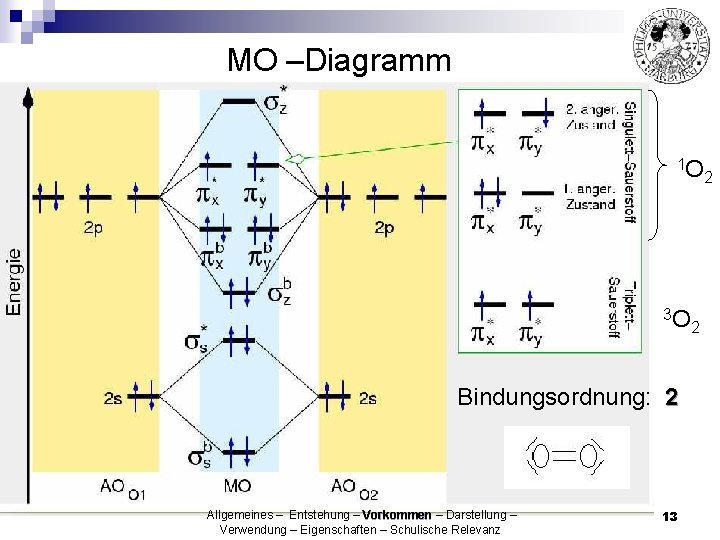
MO –Diagramm 1 O 3 O Bindungsordnung: 2 Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften - Schulische Relevanz Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 13 2 2

Sauerstoff Woher stammen die Namen? Namensgebung durch Formel zur Spinmultiplizität (2 * n + 1) Singulett: ( Triplett: ( ) ) 1 O 3 O 2, da Gesamtspin = 2 * [+½ + (-½)] +1 = 1 2, da Gesamtspin = 2 * [+½ + (+½)] +1 = 3 Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 14

Versuch 1: 1 Darstellung von Singulett - Sauerstoff Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 15
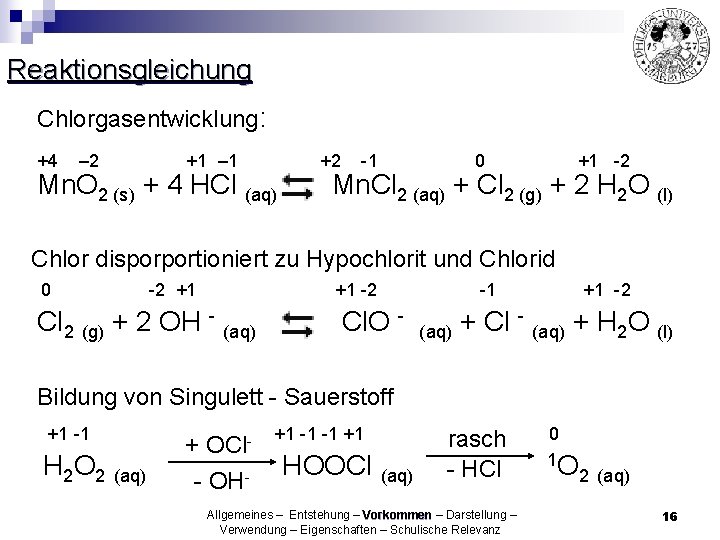
Reaktionsgleichung Chlorgasentwicklung: +4 – 2 +1 – 1 Mn. O 2 (s) + 4 HCl (aq) +2 -1 0 +1 -2 Mn. Cl 2 (aq) + Cl 2 (g) + 2 H 2 O (l) Chlor disporportioniert zu Hypochlorit und Chlorid 0 -2 +1 +1 -2 Cl 2 (g) + 2 OH - (aq) Cl. O - -1 +1 -2 + Cl (aq) + H 2 O (l) Bildung von Singulett - Sauerstoff +1 -1 H 2 O 2 (aq) OCl- + - OH- +1 -1 -1 +1 HOOCl (aq) rasch - HCl Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 0 1 O 2 (aq) 16
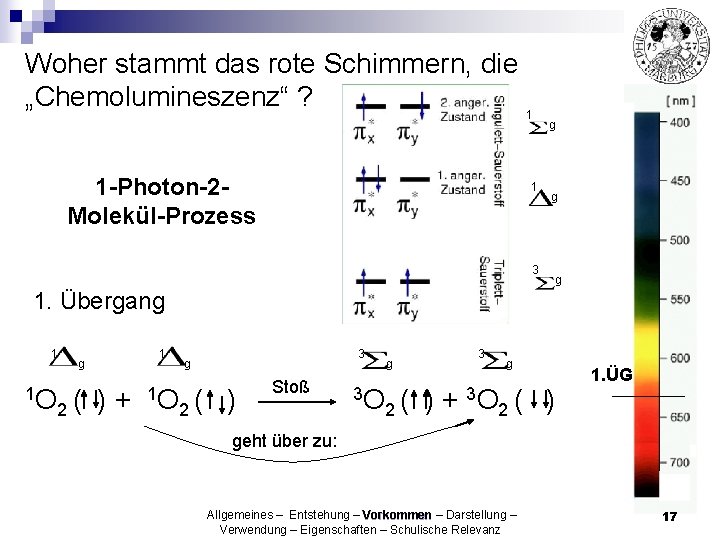
Woher stammt das rote Schimmern, die „Chemolumineszenz“ ? 1 1 -Photon-2 Molekül-Prozess 1 3 g g g 1. Übergang 1 1 O g 2( 1 3 g ) + 1 O 2 ( ) Stoß 3 O g 2( 3 g ) + 3 O 2 ( ) 1. ÜG geht über zu: Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 17
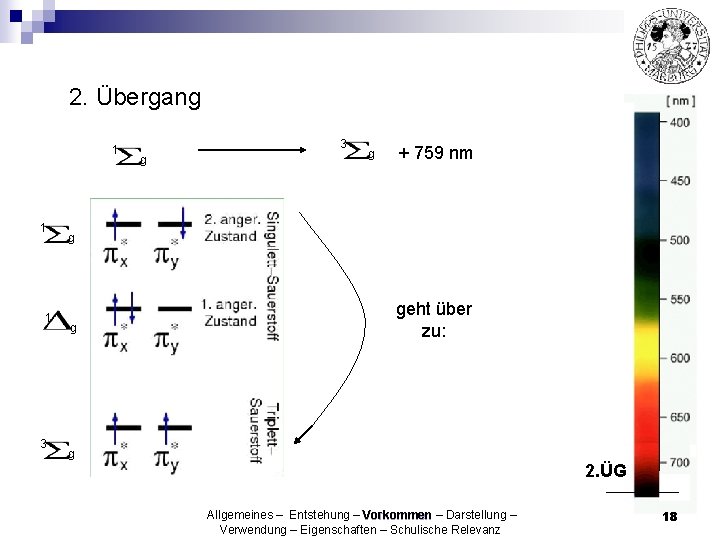
2. Übergang 1 1 1 3 3 g g + 759 nm g g geht über zu: g 2. ÜG Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 18

Gebunden: Oxide (H 2 O, CO 2, Si. O 2) n Carbonate (CO 32 -) n Silikate (Sx. Oyz-) n Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 19

Versuch 2: 2 Luftanalyse Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 20
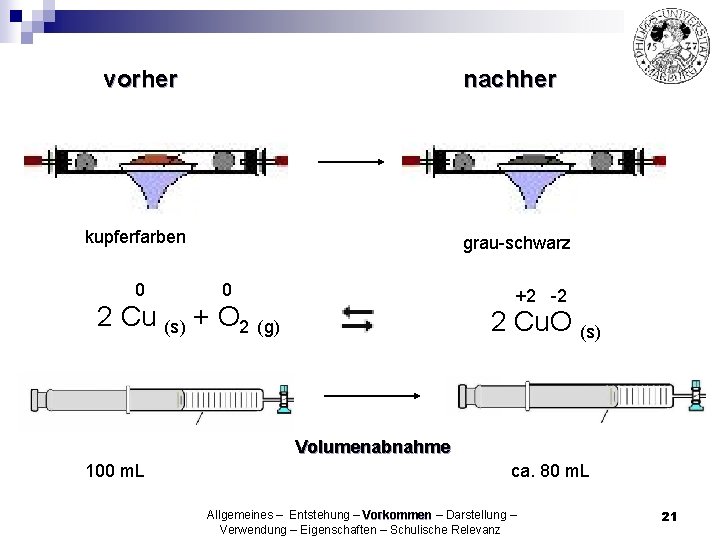
vorher nachher kupferfarben 0 grau-schwarz 0 +2 -2 2 Cu (s) + O 2 (g) 2 Cu. O (s) Volumenabnahme 100 m. L ca. 80 m. L Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 21

ca. 20 % O 2 in der Umgebungsluft Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 22

Woher dieser hohe Massenanteil Sauerstoff in der Umgebungsluft? Aus Photosyntheseprozessen Durch chlorophyllhaltige Pflanzen aus CO 2 und H 2 O gewonnen Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 23

Photosynthese Bsp. : Bildung von Glucose (schematisch) 6 H 2 O + 6 CO 2 Lichteinwirkung Chlorophyll C 6 H 12 O 6 + 6 O 2 Ein Baum (200. 000 Blättern) produziert pro Sonnentag: 9, 4 m 3 O 2 Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 24
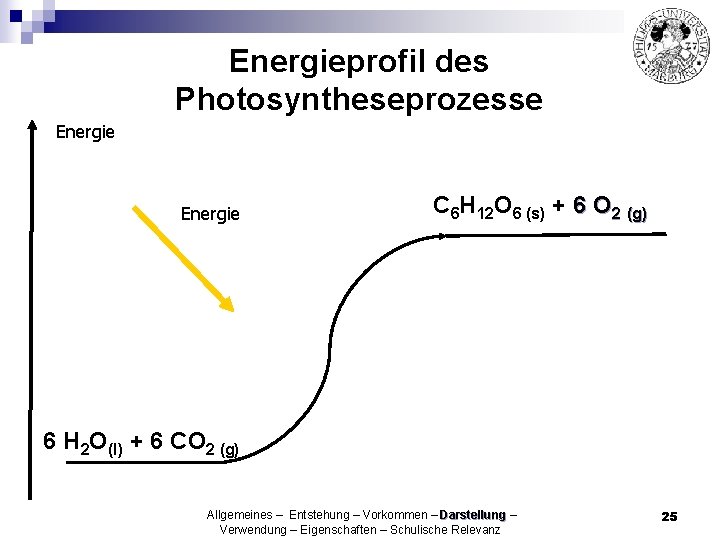
Energieprofil des Photosyntheseprozesse Energie C 6 H 12 O 6 (s) + 6 O 2 (g) 6 H 2 O(l) + 6 CO 2 (g) Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 25

Demo 1: 1 Photosyntheseprozess bei Wasserpest Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 26

Sauerstoffgewinnung n Großtechnisch: ¨ n Linde Verfahren zur Luftverflüssigung + fraktionierte Destillation Im Labor: Katalytische Zersetzung von H 2 O 2 ¨ Thermische Zersetzung von Oxiden ¨ Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 27
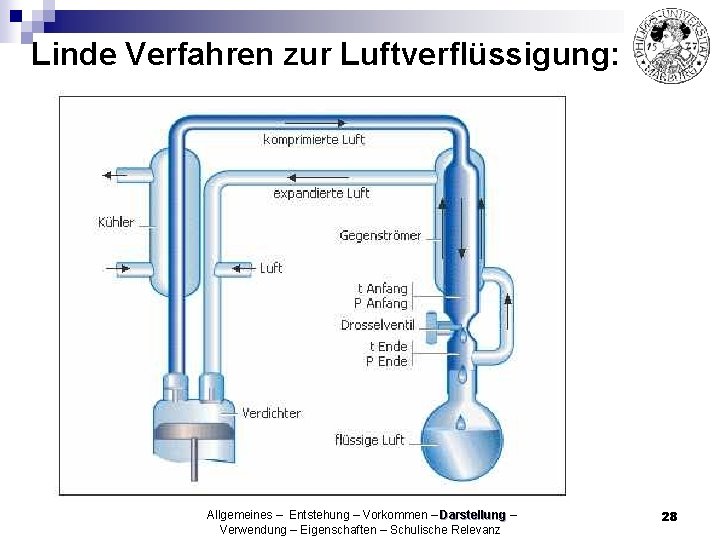
Linde Verfahren zur Luftverflüssigung: Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 28
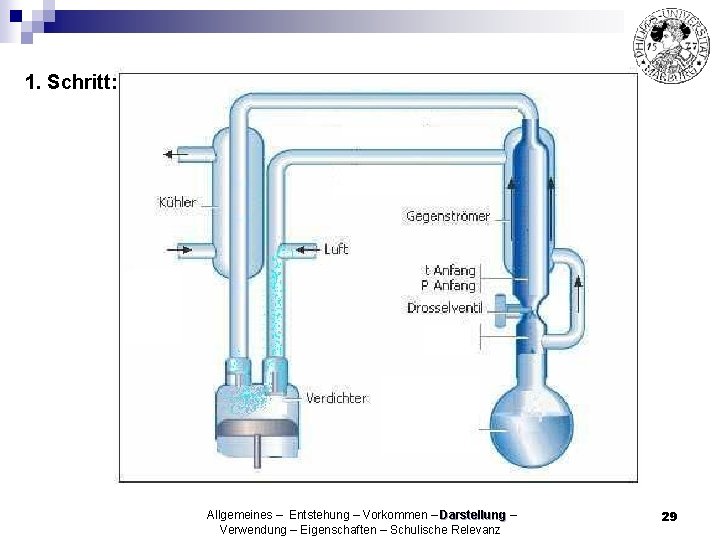
1. Schritt: Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 29
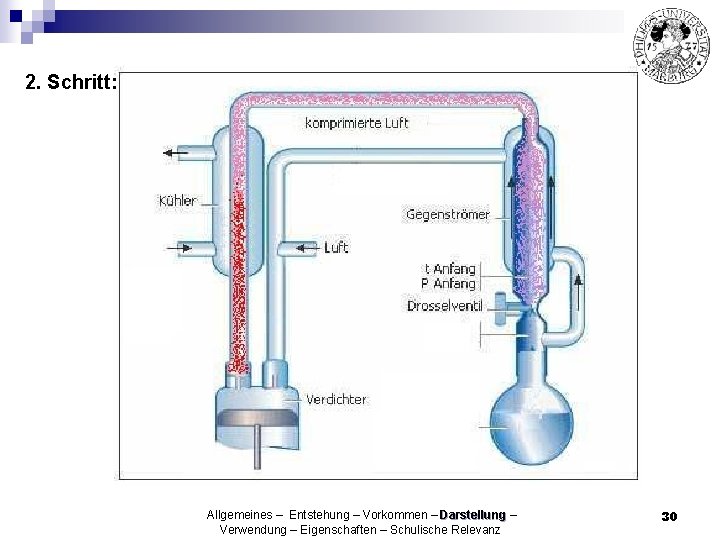
2. Schritt: Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 30
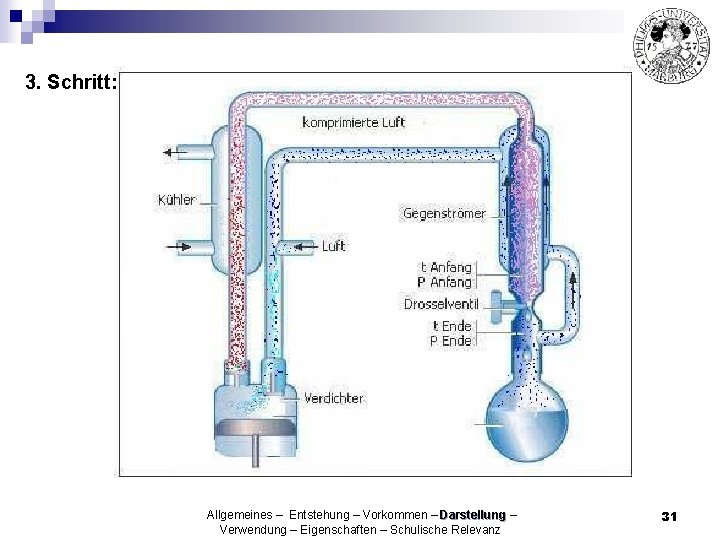
3. Schritt: Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 31
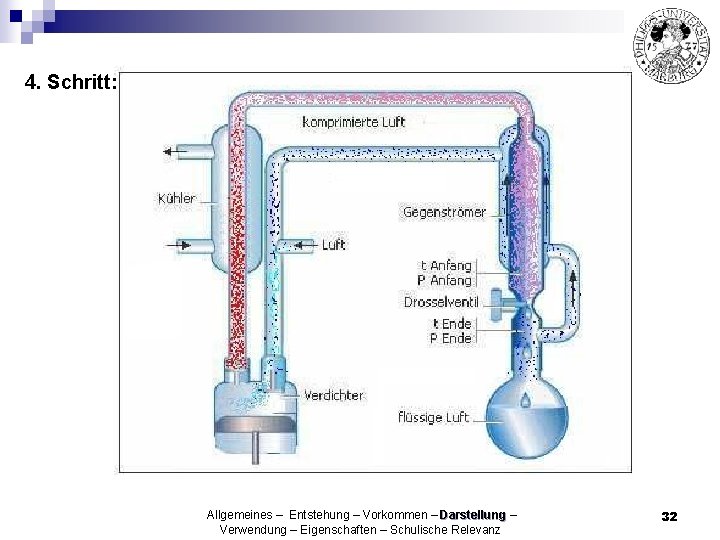
4. Schritt: Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 32
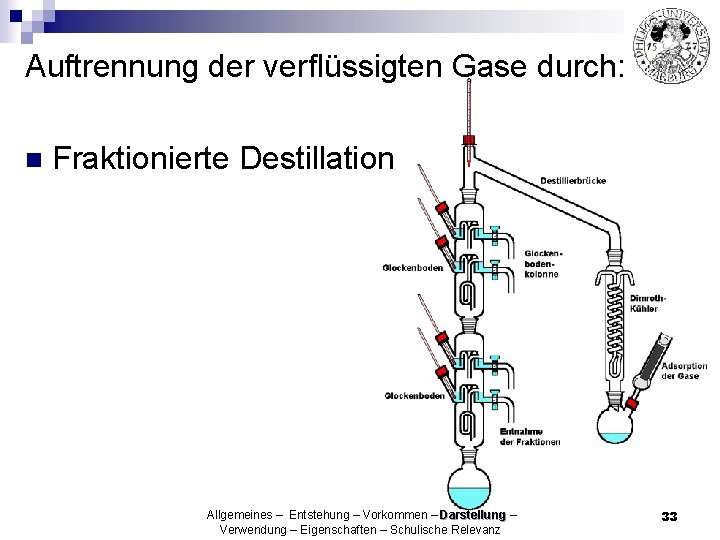
Auftrennung der verflüssigten Gase durch: n Fraktionierte Destillation Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 33

Darstellung im Labor: Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 34

Versuch 3: 3 Katalytische Zersetzung von Wasserstoffperoxid Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 35
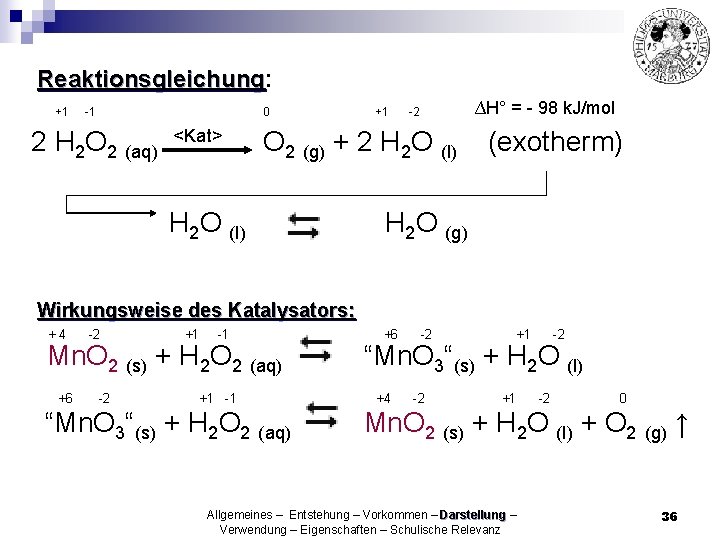
Reaktionsgleichung: Reaktionsgleichung +1 -1 0 2 H 2 O 2 (aq) <Kat> +1 ∆H° = - 98 k. J/mol -2 O 2 (g) + 2 H 2 O (l) (exotherm) H 2 O (g) Wirkungsweise des Katalysators: +4 -2 +1 -1 Mn. O 2 (s) + H 2 O 2 (aq) +6 -2 +1 -1 “Mn. O 3“(s) + H 2 O 2 (aq) +6 -2 +1 -2 “Mn. O 3“(s) + H 2 O (l) +4 -2 +1 -2 0 Mn. O 2 (s) + H 2 O (l) + O 2 (g) ↑ Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 36
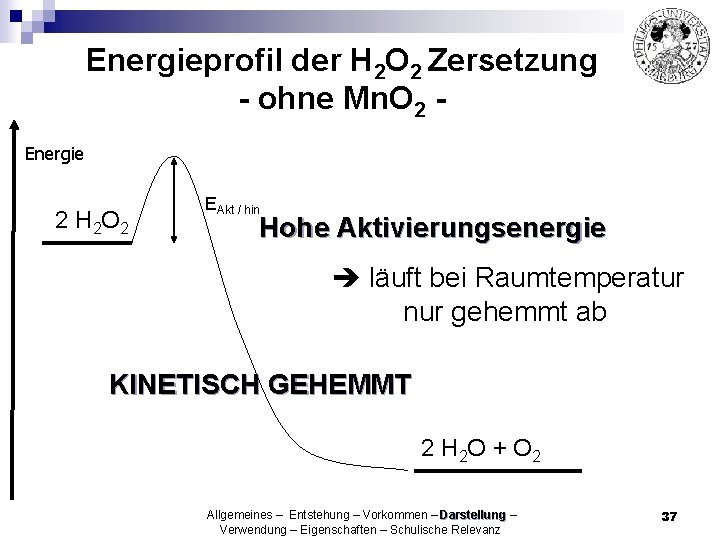
Energieprofil der H 2 O 2 Zersetzung - ohne Mn. O 2 Energie 2 H 2 O 2 EAkt / hin Hohe Aktivierungsenergie läuft bei Raumtemperatur nur gehemmt ab KINETISCH GEHEMMT 2 H 2 O + O 2 Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 37
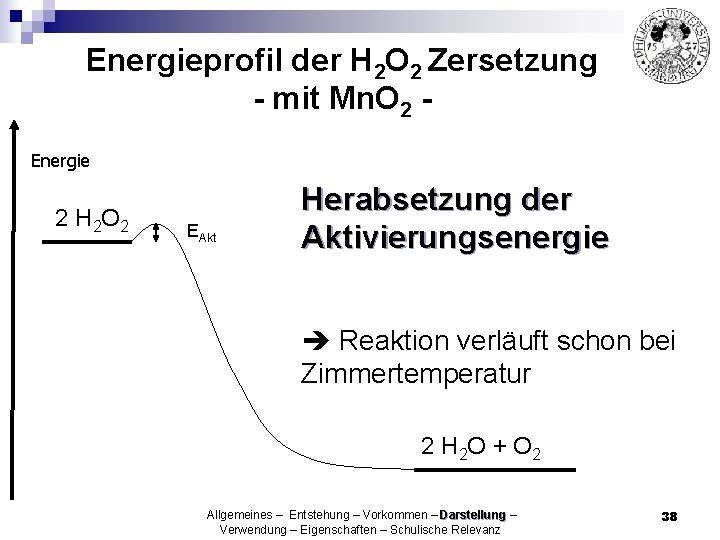
Energieprofil der H 2 O 2 Zersetzung - mit Mn. O 2 Energie 2 H 2 O 2 EAkt Herabsetzung der Aktivierungsenergie Reaktion verläuft schon bei Zimmertemperatur 2 H 2 O + O 2 Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 38

Sauerstoffnachweis Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 39

Demo 2: 2 Verbrennung eines glimmenden Spanes Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 40

Verwendung n Energiegewinnung in Organismen n Stahlerzeugung n Schweißtechnik n Medizinischen Zwecken Erzeugung hoher Temperaturen Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 41

Verwendung: Atmung Verbrauch eines Menschen n Pro Atemzug: 0, 5 – 2, 0 L (Luft) n Atemvolumen / min: 4, 7 L (Schlaf) – 60 L (Sport) (Luft) 12. 000 L Luft pro Tag = 2. 500 Liter O 2 am Tag Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 42

Oxidationsvermögen: Schnelle, heftige Prozesse mit großer Energieabgabe Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 43

Versuch 4: 4 Verbrennung von Stahlwolle Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 44
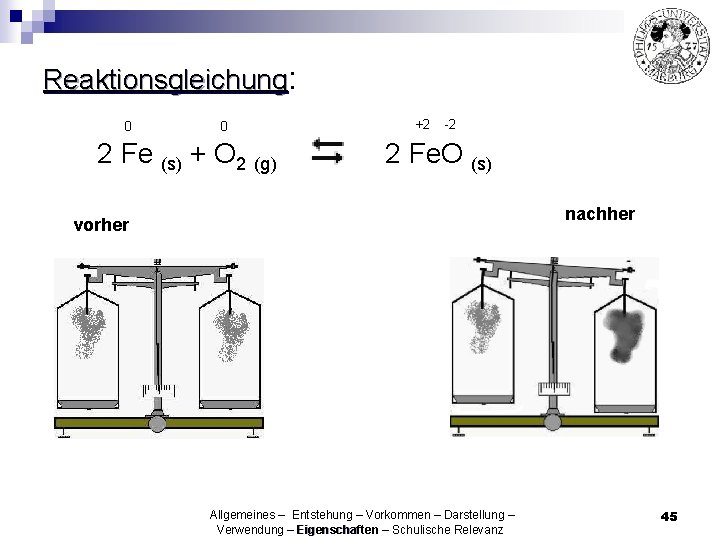
Reaktionsgleichung: 0 0 2 Fe (s) + O 2 (g) +2 -2 2 Fe. O (s) nachher vorher Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 45

Oxidationsvermögen: Langsame Oxidationsprozesse Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 46

Versuch 5: 5 Stille Verbrennung (Sauerstoffkorrosion) Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 47
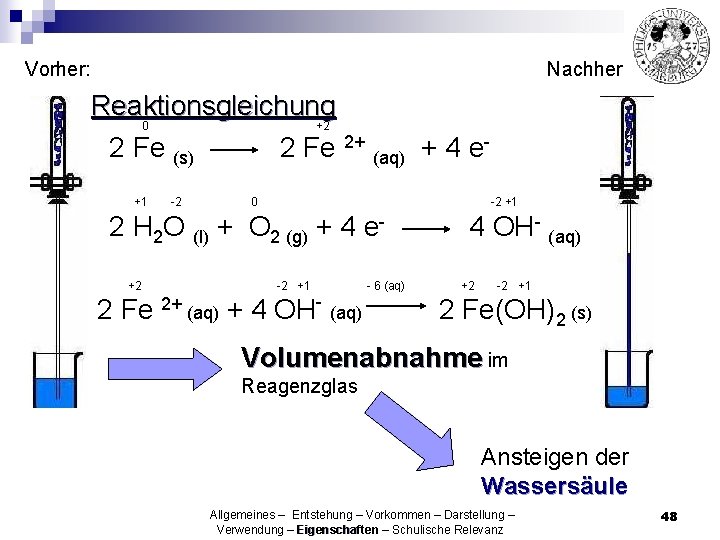
Vorher: Nachher: Reaktionsgleichung 0 +2 2 Fe (s) 2 Fe 2+ (aq) + 4 e+1 -2 0 -2 +1 2 H 2 O (l) + O 2 (g) + 4 e+2 -2 +1 2 Fe 2+ (aq) + 4 OH- (aq) - 6 (aq) 4 OH- (aq) +2 -2 +1 2 Fe(OH)2 (s) Volumenabnahme im Reagenzglas Ansteigen der Wassersäule Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 48

Folgereaktion: +2 -2 +1 0 +1 -2 4 Fe(OH)2 (s) + O 2 (g) + 2 H 2 O (l) +3 -2 +1 Fe(OH)3 (aq) +3 -2 -2 +1 +3 -2 +1 4 Fe(OH)3 (s) +1 -2 Fe. O(OH) (s) + H 2 O (l) Rostbildung: 2 Fe. O(OH) (s) „Fe 2 O 3* H 2 O“ (s) rotbraun Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 49

Flugzeugpark, Mojave Wüste Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 50

Grund für die langsam ablaufende Oxidation: Hohe Dissoziationsenergie (498, 34 k. J / mol) „Zündungsenergie“ fehlt Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 51

Demo 3: 3 Flüssiger Sauerstoff Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 52

Magnetische Eigenschaften von Sauerstoff? Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 53

Versuch 6: 6 Paramagnetismus von Sauerstoff Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 54
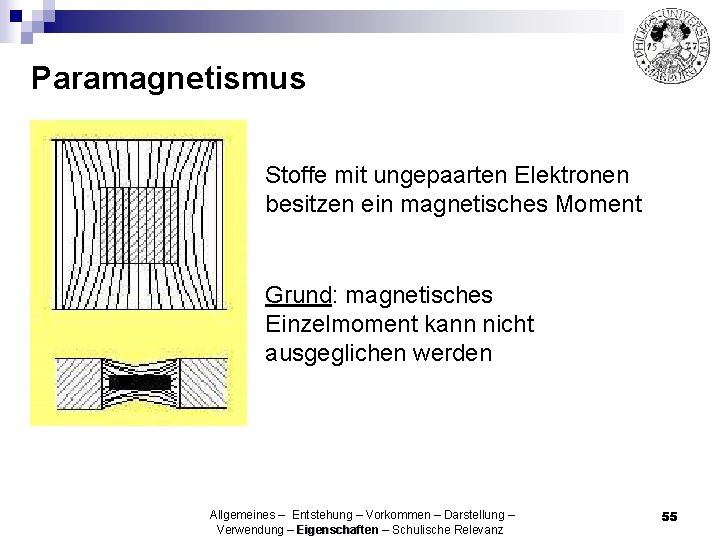
Paramagnetismus Stoffe mit ungepaarten Elektronen besitzen ein magnetisches Moment Grund: magnetisches Einzelmoment kann nicht ausgeglichen werden Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 55

Daraus folgt: Vergrößerung der Kraftflussdichte der Feldlinien im Inneren Stoff wird in ein Magnetfeld hineingezogen Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 56
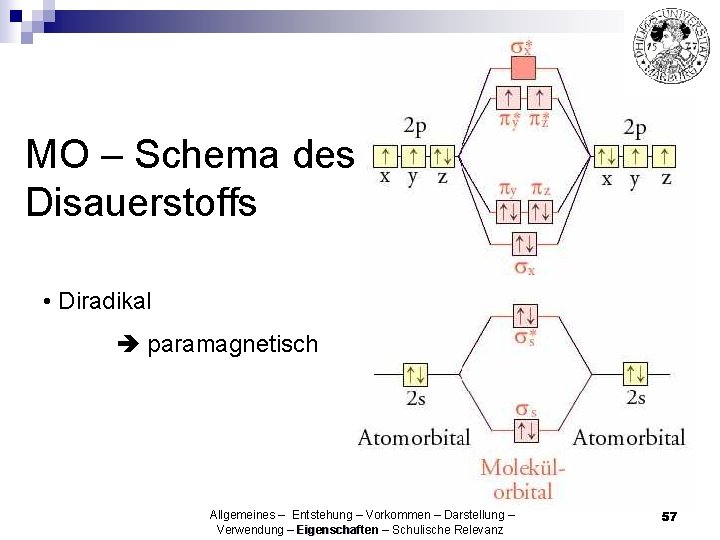
MO – Schema des Disauerstoffs • Diradikal paramagnetisch Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 57

Reaktion mit flüssigem Sauerstoff Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 58

Demo 4: 4 Verbrennung einer sauerstoffgetränkten Zigarre Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 59

Schulische Relevanz n Jahrgangsstufe 7: Einführung in die Chemischen Reaktionen (V 2, V 3, V 4) ¨ Reaktionen von Metallen und Nichtmetallen mit Sauerstoff (V 2, V 4, V 5, Demo 4) ¨ Gesetz zur Erhaltung der Masse (V 4) ¨ Quantitative Zusammensetzung der Luft (V 2) n Jahrgangsstufe 10: Redoxreaktionen (V 2, V 3, V 4, V 5) ¨ Ausgewählte Redoxreaktionen (V 4) (V 5) Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 60

Schulische Relevanz n Jahrgangsstufe 12: ¨ Geschwindigkeit chemischer Reaktionen (Anwendung von Katalysatoren (V 3)) n Jahrgangsstufe 12: GK / LK Wahlthema angewandte Chemie ¨ Korrosion (V 5) Allgemeines – Entstehung – Vorkommen – Darstellung – Verwendung – Eigenschaften – Schulische Relevanz 61

Vielen Dank für Ihre Aufmerksamkeit! -Ende- 62
- Slides: 62