Anorganische Chemie in Prinzipien und Methoden der Chemie





- Slides: 9

Anorganische Chemie in Prinzipien und Methoden der Chemie

Die wissenschaftliche Methodik I. Beobachtung II. Theorie (Erklärung der Beobachtung) III. Experimentelle Überprüfung (Planung, Durchführung, Auswertung) Erkennen fehlerhafter Theorien: a) Reproduzierbarkeit des Experiments b) statistische Überprüfung If it disagrees with experiment, it is wrong ! (R. Feynman)

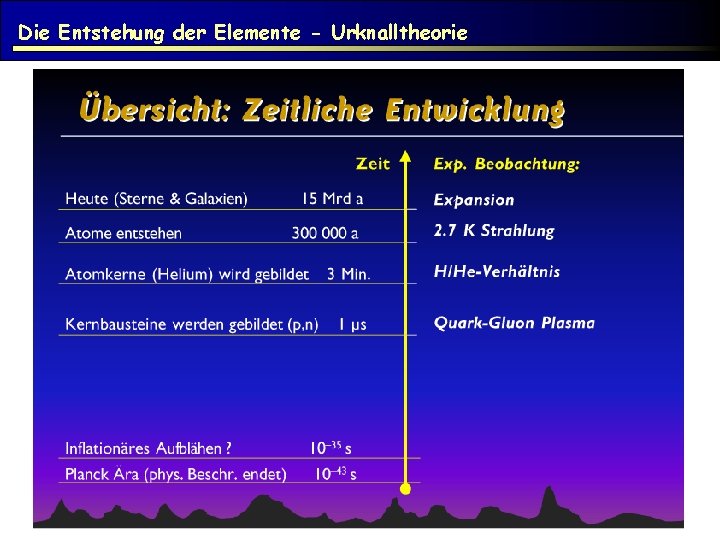
Die Entstehung der Elemente - Urknalltheorie

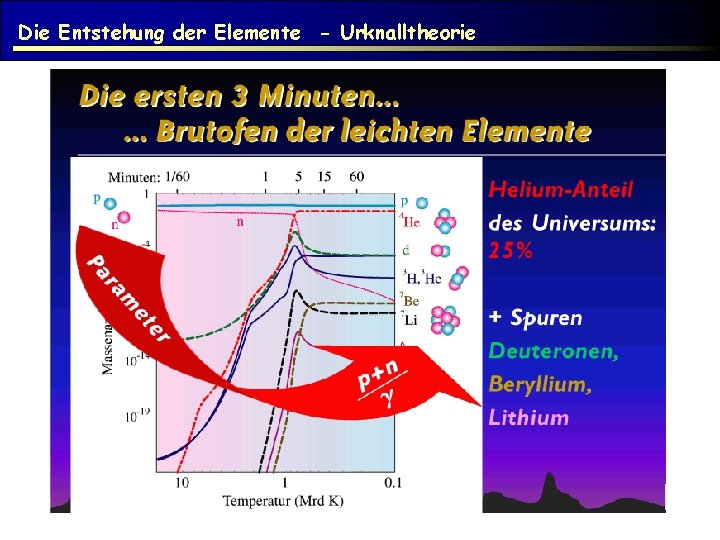
Die Entstehung der Elemente - Urknalltheorie

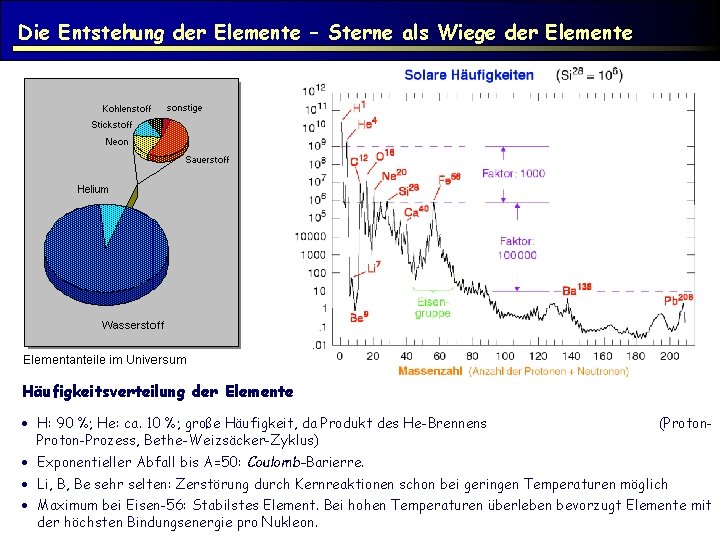
Die Entstehung der Elemente – Sterne als Wiege der Elemente Häufigkeitsverteilung der Elemente H: 90 %; He: ca. 10 %; große Häufigkeit, da Produkt des He-Brennens Proton-Prozess, Bethe-Weizsäcker-Zyklus) (Proton- Exponentieller Abfall bis A=50: Coulomb-Barierre. Li, B, Be sehr selten: Zerstörung durch Kernreaktionen schon bei geringen Temperaturen möglich Maximum bei Eisen-56: Stabilstes Element. Bei hohen Temperaturen überleben bevorzugt Elemente mit der höchsten Bindungsenergie pro Nukleon.

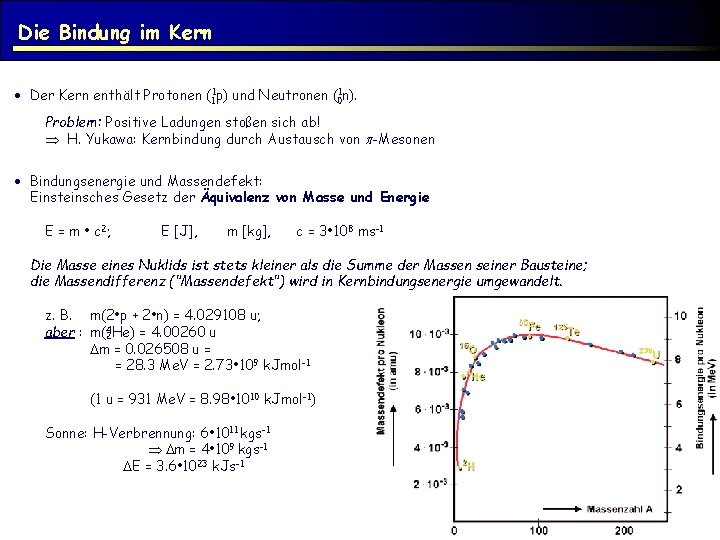
Die Bindung im Kern Der Kern enthält Protonen (11 p) und Neutronen (01 n). Problem: Positive Ladungen stoßen sich ab! H. Yukawa: Kernbindung durch Austausch von p-Mesonen Bindungsenergie und Massendefekt: Einsteinsches Gesetz der Äquivalenz von Masse und Energie E = m • c 2; E [J], m [kg], c = 3 • 10 8 ms-1 Die Masse eines Nuklids ist stets kleiner als die Summe der Massen seiner Bausteine; die Massendifferenz ("Massendefekt") wird in Kernbindungsenergie umgewandelt. z. B. m(2 • p + 2 • n) = 4. 029108 u; aber : m(42 He) = 4. 00260 u Dm = 0. 026508 u = = 28. 3 Me. V = 2. 73 • 109 k. Jmol-1 (1 u = 931 Me. V = 8. 98 • 1010 k. Jmol-1) Sonne: H-Verbrennung: 6 • 1011 kgs-1 Dm = 4 • 109 kgs-1 DE = 3. 6 • 1023 k. Js-1

Nuklide 112 Elemente ca. 1900 Nuklide ( = unterschiedliche Atomkerne) davon: 340 natürliche 270 stabil Indizierung Die meisten Elemente sind Mischelemente! 20 Reinelemente (alle außer Beryllium besitzen ungerade Ordnungszahlen): Be, F, Na, Al, Sc, Mn, Co, As, Y, Nb, Rh, I, Cs, Pr, Tb, Ho, Tm, Au, Bi Einteilung von Nukliden: Protonenzahl (p) Neutronenzahl (n) Nukleonenzahl (m = p+n) Bezeichnung gleich verschieden Isotope gleich Isomere verschieden gleich Isobare verschieden gleich verschieden Isotone

Isotopie-Effekte a) physikalische Gravitationswirkung auf höhere Masse, z. B. H 20 0. 00 °C D 2 O 3. 82 °C Fp. 100. 0 °C 101. 42 °C Kp. Anteil leichterer Nuklide (1 H; 16 O) im Dampf größer als im flüssigen Wasser Mit grösserer geograph. Breite/Distanz zum Meer sind Niederschläge verarmt an schweren Isotopen. b) chemische Masse bestimmt harmonische Schwingungsfrequenz leichtere Nuklide eines Elements zeigen höhere Reaktionsfähigkeit Geochemisches Beispiel: Schwefellagerstätten in Texas, besitzen überdurchschnittlich hohes 32 S/34 S - Verhältnis. Grund: bakteriell reduziertes Sulfatsediment. Generell Variation der Isotopenmasse bei Mischelementen: natürlich: künstlich: O, S, Ar, Cu, Pb H, Li, B, C, N, Ne, Kr, Xe, U

Isotopentrennung Wichtige Isotope: Anreicherung eines bestimmten Isotops für spezielle Anwendungen (Tracer-Technik, NMR-Experimente, Kernspaltung, Kernfusion) fraktionierte Destillation (H 2 O/D 2 O) Elektrolyse (H 2/D 2) Diffusion (Uran als UF 6) Druckdiffusion " Trennsäule " Gaszentrifuge " Im allgemeinen jeweils mehrere Trenngänge notwending! Einzig komplette Trennung: Massenspektrometrie!