U organska jedinjenja koja pored C O spadaju





















- Slides: 25

U organska jedinjenja koja pored C O spadaju : • ALKOHOLI • ALDEHIDI i KETONI • Karboksilne KISELINE • ESTRI i H sadržei


ALKOHOLI su jedinjenja kod kojih je za ugljovodoniĉni niz vezana jedna ili više OH grupa je FUNKCIONALNA grupa alkohola i naziva se HIDROKSILNA GRUPA

Hidroksilna grupa je funkcionalna grupa alkohola što znači da je imaju svi alkoholi i da ona određuje njihova svojstva. U OH grupi atom kiseonika je jednom jednostrukom kovalentnom vezan za atom ugljenika, a drugom jednostrukom kovalentnom vezom za atom vodonika. *U HIDROKSIDNOJ grupi koju sadrže hidroksidi, atom kiseonika je kovalentnom vezan za vodonik, a jonskom vezom za metal(razlika hidroksidne od hidroksilne). Hidroksilna grupa je uvek vezana za zasićeni C-atom.

Opšta formula alkohola je R ─ OH R može biti bilo koja alkil grupa ( Cn. H 2 n+1) ALKAN /alkilgrupa ALKOHOL METAN CH 4 METIL ─ CH 3 ─ OH METANOL ETAN C 2 H 6 ETIL C 2 H 5 ─ OH ETANOL ─ C 2 H 5 PROPAN C 3 H 8 PROPIL ─ C 3 H 7 BUTAN BUTIL C 4 H 10 ─ C 4 H 9 C 3 H 7 ─ OH PROPANOL C 4 H 9 ─ OH BUTANOL

Nazivi alkohola izvode se iz naziva ugljovodonika sa istim brojem ugljenikovih atoma dodavanjem nastavka OL. Obeležavanje C-atoma u ugljovodoniĉnom nizu poĉinje od kraja kome je bliža OH grupa. Alkoholi koji imaju više hidroksilnih grupa dobijaju nastavak DIOL, TRIOL itd.

Prema broju hidroksilnih grupa, alkoholi se dele na: MONOHIDROKSILNE (sadrže jednu OH grupu) i POLIHIDROKSILNE (sadrže dve ili više OH grupa)

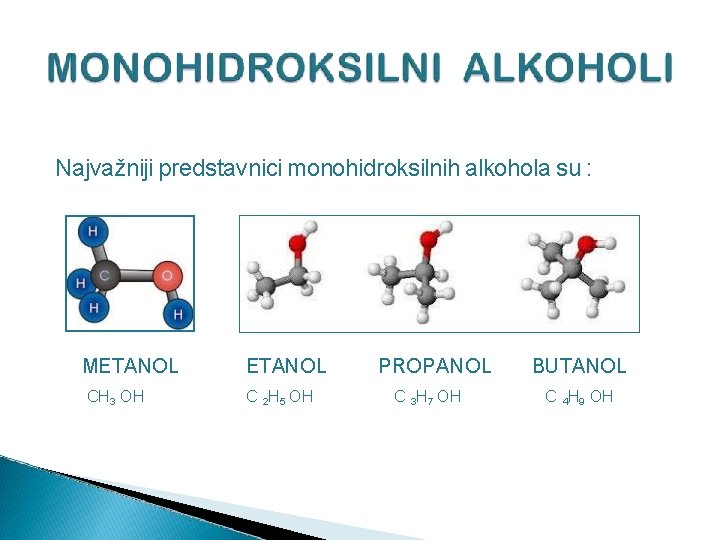
Najvažniji predstavnici monohidroksilnih alkohola su : METANOL CH 3 OH ETANOL C 2 H 5 OH PROPANOL C 3 H 7 OH BUTANOL C 4 H 9 OH

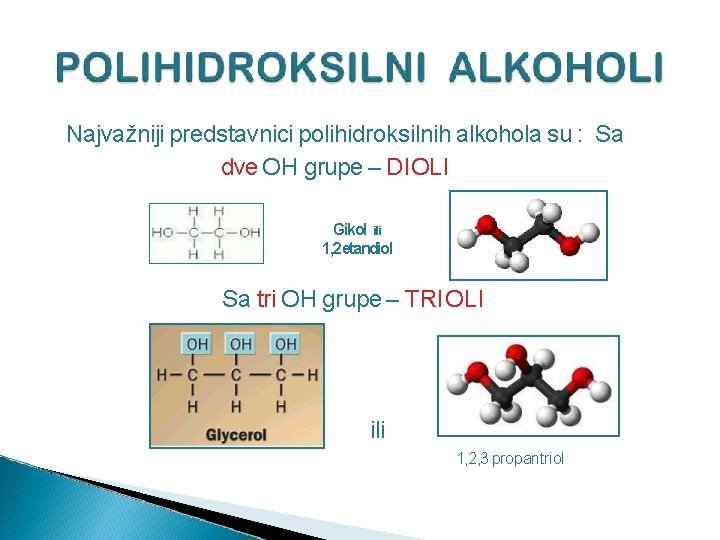
Najvažniji predstavnici polihidroksilnih alkohola su : Sa dve OH grupe – DIOLI Gikol ili 1, 2 etandiol Sa tri OH grupe – TRIOLI ili 1, 2, 3 propantriol

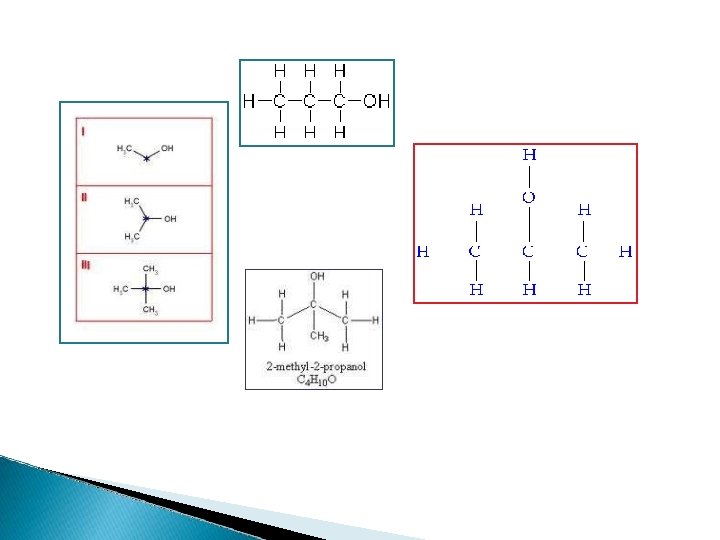
PRIMARNI ALKOHOLI – oni kod kojih je OH grupa vezana za primarni C-atom metanol, 1 -butanol SEKUNDARNI ALKOHOLI – oni kod kojih je OH grupa vezana za sekundarni C-atom 2 -butanol, 2 -propanol TERCIJARNI ALKOHOLI - oni kod kojih je OH grupa vezana za tercijarni C-atom. 2 -metil- 2 -propanol


• Postoji više naĉina za dobijanje alkohola ADICIJOM VODE na ALKENE • ALKOHOLNIM VRENJEM ŠEĆERA C 6 H 12 O 6 glukoza → 2 C 2 H 5 OH +2 CO 2 etanol

Fiziĉka svojstva alkohola određuje njegova funkcionalna grupa OH, ali i dužina i oblik samog ugljovodoničnog niza. OH grupa zbog polarnosti veze izmeĊu O i H, ĉini molekul alkohola polarnim. Polarne osobine su izraženije ukoliko je broj OH grupa veći. Ugljovodoniĉni niz je nepolarni deo molekula alkohola. Sa povećanjem broja C atoma u ugljovodoniĉnom nizu alkohola, izraženije su i fizičke osobinekarakteristiĉne za nepolarna organska jedinjenja.

AGREGATNO STANJE TEČNO – alkoholi sa manje od 11 C-atoma ČVRSTO – alkoholi sa više od 11 C-atoma. Imaju više temperature kljuĉanja od alkana sa istim brojem C – atoma, zbog prisustva polarne OH grupe i međumolekulskih privlačnih sila između njih.




Špiritus- gorivo za špiritusne lampe. Nastaje od etanola kome se dodaju neke supstance zbog kojih je neupotrebljiv za piće. Naziva se i DENATURISANI ALKOHOL.

U ovoj reakciji učestvuje vodonik iz hidroksilne grupe. To je reakcija supstitucije jer se dešava zamena tog H nekim izrazitim metalom. Proizvodi reakcije su ALKOKSIDI ili ALKOHOLATI, tj. soli alkohola i izrazitih metala. 2 R-OH +2 M → 2 RO- M ++H 2 alkohol metal alkoksid

Ovo je reakcija ELIMINACIJE. U njoj uĉestvuje OH grupa sa jednog C-atoma i H sa susednog Catoma. Izdvaja se voda i nastaje ALKEN. Da bi došlo do reakcije potrebno je neko dehidrataciono sredstvo (supstanca koja vezuje vodu, kao što je sumporna kiselina).

Blaga oksidacija alkohola odvija se pod dejstvom OKSIDACIONIH SREDSTAVA. Ovakvomoksidacijom alkohola dobijaju se KARBONILNA JEDINJENJA. Karbonilna jedinjenja su organska jedinjenja kod kojih je atom kiseonika vezan za ugljenik dvostrukom vezom. Funkcionalna grupa karbonilnih jedinjenja je KARBONILNA GRUPA C=O

Najvažniji alkohol je ETANOL. To je lako isparljiva, zapaljiva, bezbojna tečnost karakteristiĉnog mirisa i ukusa. Gori svetloplavim plamenom. Ključa na 78 C 0. Dobar je polarni rastvarač. Hemijski je vrlo reaktivan. Proizvodi se kao apsolutni alkohol (99, 9%). U medicini se za dezinfekciju i obloge koristi razblaženi 70%alkohol. Kao dobar rastvarač, etanol je sastojak parfema, losiona, dezodoranasa i drugih kozmetičkih preparata. Koristi se i za pravljenje tinktura (npr. tinkzura propolisa).

Ostali alkoholi se koriste: • METANOL – kao gorivo. Njegova upotreba je ograničena jer je veoma otrovan. • • • GLICEROL - proizvodnja lekova za bolesti srca-nitroglicerin za dobijanje eksploziva - nitroglicerin od koga je Alfred Nobel napravio DINAMIT. GLIKOL – 40% vodeni rastvor ovog alkohola koristi se kao ANTIFRIZ jer snižava tačku mržnjenja vode.

Nažalost, alkohol je uzročnik bolesti zavisnosti – ALKOHOLIZMA. Alkoholna pića se prave od različitih biljnih sirovina – voća, povrća i žitarica. Njihova prekomerna upotreba dovodi do brojnih štetnih posledica po zdravlje.

Pitanja za domaći: 1. Ispiši fizičke osobine metanola i etanola 1. a) b) c) Napiši formule: 3 -metil-2 -butanol 4 -metil-2 -pentanol 4, 4 -dimetil-(1)-pentanol 3. Napiši izomere C 5 H 11 O 4. Koja je primjena metanola, acetona? 5. Šta su antifriz i formaldehid