NASTAVNA TEMA BIOLOKI VANA ORGANSKA JEDINJENJA NASTAVNA JEDINICA

NASTAVNA TEMA: BIOLOŠKI VAŽNA ORGANSKA JEDINJENJA NASTAVNA JEDINICA: AMINOKISELINE I PROTEINI Zorica Bolović

SAZNAĆETE: -da su proteini biološki važna organska jedinjenja -njihovu strukturu i funkciju -značaj proteina za živi organizam -da je osnovna jedinica građe proteina aminokiselina -strukturu, fizičke i hemijske osobine aminokiselina

PROTEIOS- PRVI, PRVI PO VAŽNOSTI PRIRODNI POLIMERI- makromolekuli izgrađeni od velikog broja monomernih jedinica– aminokiselina. Jedinjenja su velike relativne molekulske mase ( 10 000 do 1000 000) i od svih biološki važnih organskih jedinjenja vrše najviše funkcija u živom organizmu.

Funkcionalne grupe AMINOKISELINE - organska jedinjenja koja u svom molekulu pored karboksilne –COOH sadrže još jednu funkcionalnu grupu: amino grupu – NH 2. Amino grupa je jednovalentni ostatak amonijaka. NH 3 ili H-NH 2 Mogu se smatrati amino derivatima karboksilnih kiselina. (nastale zamenom jednog atoma vodonika amino gripom).

PROTEINSKE AMINOKISELINE U sastav proteina ulaze aminokiseline kod kojih su obe funkcionalne grupe vezane za isti ugljenikov atom.

Opšta formula proteinskih aminokiselina 1 R - СН – СООН │ NH 2 -R -bočna grupa( obično alkil) Po IUPAC nomenklaturi aminokiseline su 2 -amino derivati karboksilnih kiselina, jer se ugljenikov atom –COOH numeriše kao prvi. Ovaj C atom obeležava se sa α pa se nazivaju i α-aminokiseline. СН 2 – СООН │ NH 2 amino-etanska GLICIN (najjednostavnija) СН 3 -СН – СООН │ NH 2 2 -amino-propanska kiselina ALANIN

20 proteinskih aminokiselina (nastaju hidrolizom proteina): -esencijalne (bitne) -nenesencijalne Biljke mogu da izvrše sintezu svih proteinskih aminokiselina (i neki mikroorganizmi). Životinjski organizam može da sintetiše 10 proteinskih aminokiselina. Te kiseline nazivamo neesencijalne. Preostale( esencijalne) moraju se uneti hranom. Namirnice bogate esencijalnim aminokiselinama

Fizičke osobine: bele kristalne supstance dobro rastvorne u vodi

Hemijska svojstva određena su prisustvom dve funkcionalne grupe: -COOH i NH 2 Pokazuju sve reakcije karakteristične za karboksilne kiseline ( građenje soli, dekarboksilacije, esterifikacije). Građenje peptidne veze- reakcija u kojoj učestvuju karboksilna grupa jedne aminokiseline i amino grupa druge amino kiseline. ( uz eliminisanje vode) O ║ R -СН – С – N – CH - COOH │ │ │ NH 2 Н R
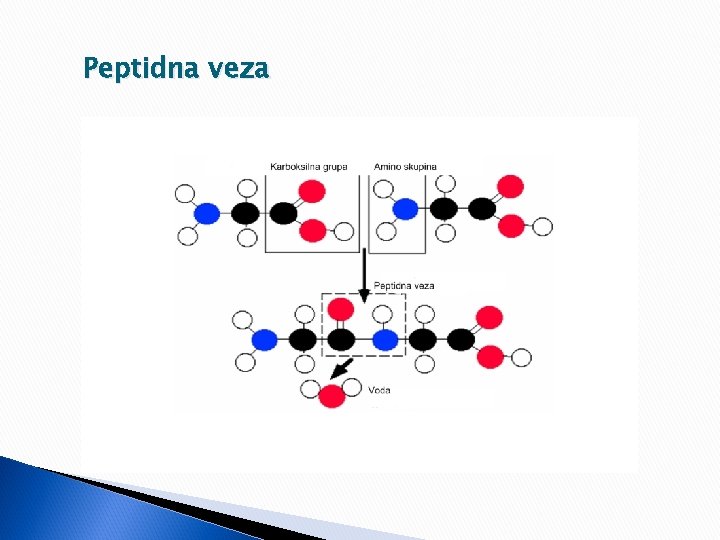
Peptidna veza

Dipeptid-molekul nastao povezivanjem dve aminokiseline peptidnom vezom О ║ СН 3 -СН – С – N – CH 2 – COOH alanil-glicin │ │ NH 2 Н Dve aminokiseline mogu se povezati peptidnom vezom na dva načina. О ║ СН 2 – С – N – CH - COOH │ │ │ glicil-alanin NH 2 Н СН 3

Polipeptidi –nastaju povezivanjem od 100 do nekoliko hiljada ostataka aminokiselina peptidnom vezom. Nazivaju se proteini (belančevine). Redosled kojim su aminokiseline međusobno povezane u polipeptidnom lancu tačno je određen i nepromenljiv. Naziva se sekvenca. Polipeptidni lanac može imati različit prostorni oblik tj. proteini imaju različitu strukturu. Različita struktura uzrok je različitih fizičkih osobina i različite funkcije koju vrše u organizmu.

Prema strukturi i funkciji koju vrše u organizmu proteini se dele na: Vlaknaste (fibrilarne)čvrsti i nerastvorni u vodi pa imaju gradivnu funkciju (kosa, koža, nokti, mišići) Globularne (loptaste) Funkcija: -transportna (hemoglobin) -katalitička (enzimi) -regulatorska( hormoni) -zaštitna (imunoglobulini)
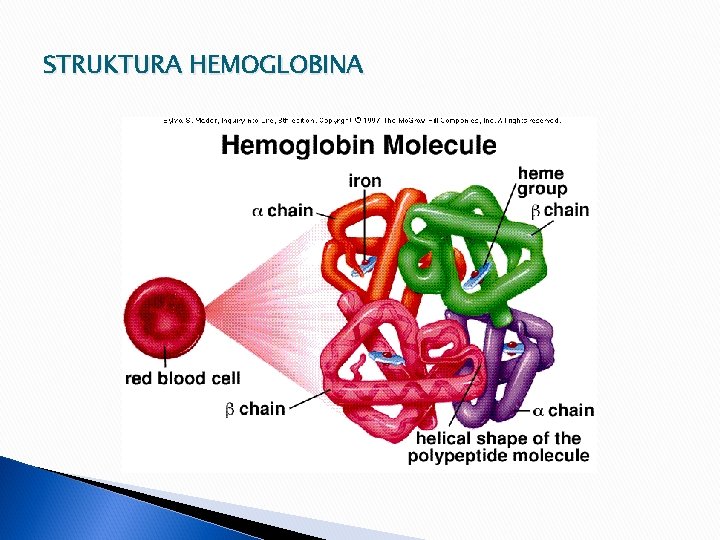
STRUKTURA HEMOGLOBINA

Denaturacija- narušavanje strukture proteina koje dovodi do smanjenja ili potpunog gubitka njegove biološke aktivnosti. Denaturacija protena se može postići dejstvom: - kiselina - baza -soli -nepolarnih rastvarača -zagrevanjem

HVALA VAM NA PAŽNJI
- Slides: 16