Ressonncia Paramagntica Eletrnica RPE Prof Claudio Jos Magon


























- Slides: 71

Ressonância Paramagnética Eletrônica RPE Prof. Claudio José Magon

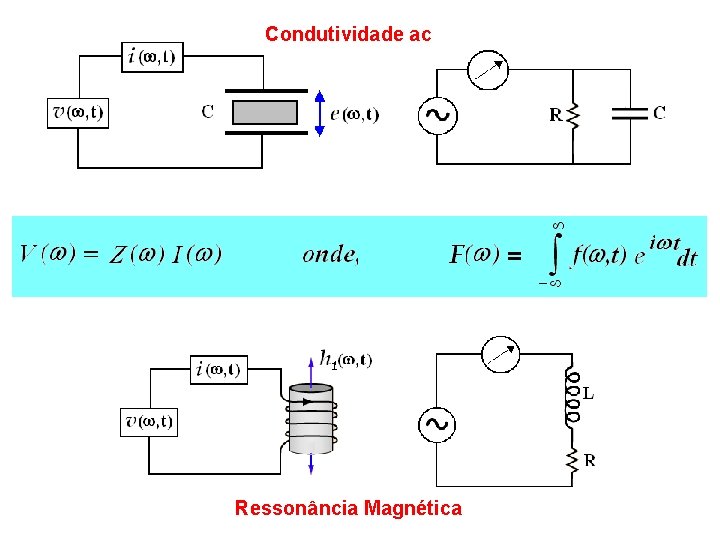
Condutividade ac Ressonância Magnética

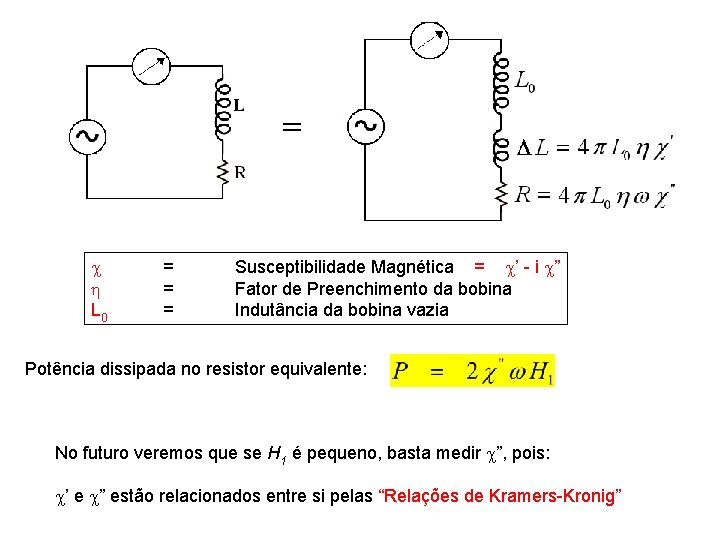
L 0 = = = Susceptibilidade Magnética = ’ - i ” Fator de Preenchimento da bobina Indutância da bobina vazia Potência dissipada no resistor equivalente: No futuro veremos que se H 1 é pequeno, basta medir ”, pois: ’ e ” estão relacionados entre si pelas “Relações de Kramers-Kronig”

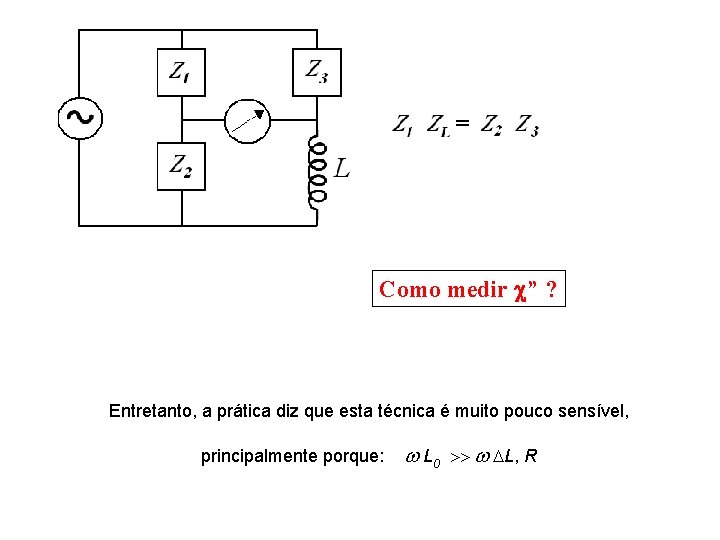
Como medir ” ? Entretanto, a prática diz que esta técnica é muito pouco sensível, principalmente porque: L 0 L, R

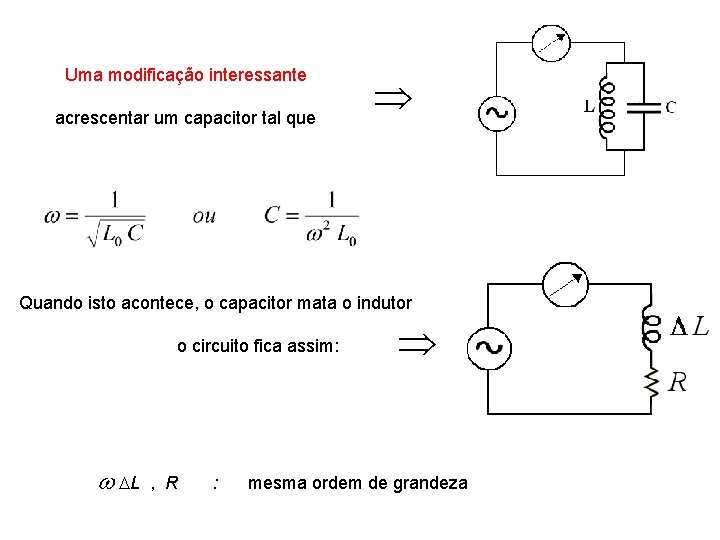
Uma modificação interessante acrescentar um capacitor tal que Quando isto acontece, o capacitor mata o indutor o circuito fica assim: L , R : mesma ordem de grandeza

E daí, é só isso? Infelizmente não! A prática diz que o experimento fica interessante quando: / 2 109 Hz = 1 GHz Problema Em altas frequências os “fios” do circuito não se comportam mais como fios. Fios se comportam como “linhas de transmissão”. Isto acontece porque o comprimento de onda associado a : se torna comparável ao comprimento dos fios, por exemplo:

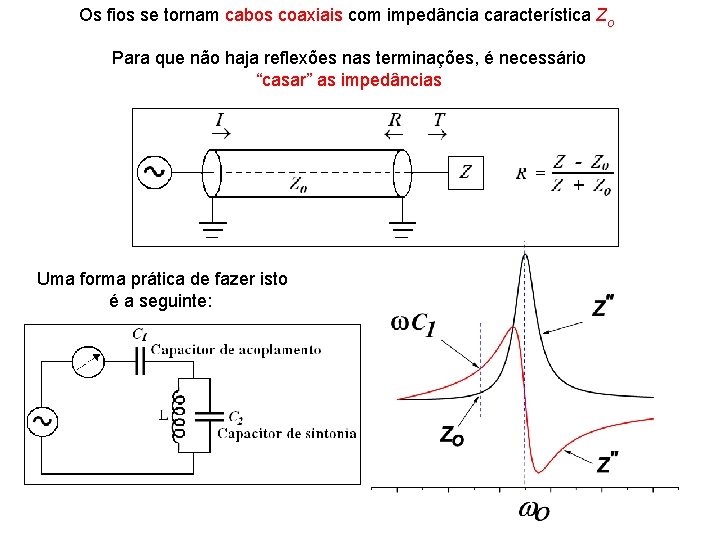
Os fios se tornam cabos coaxiais com impedância característica Zo Para que não haja reflexões nas terminações, é necessário “casar” as impedâncias Uma forma prática de fazer isto é a seguinte:

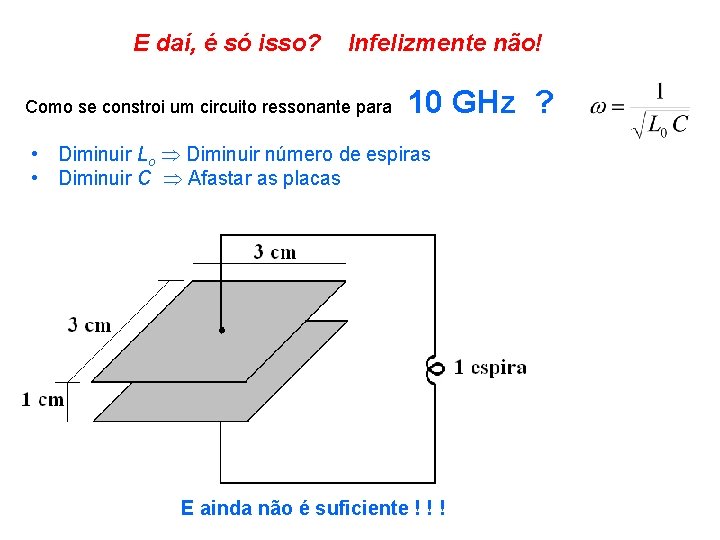
E daí, é só isso? Infelizmente não! Como se constroi um circuito ressonante para 10 GHz ? • Diminuir Lo Diminuir número de espiras • Diminuir C Afastar as placas E ainda não é suficiente ! ! !

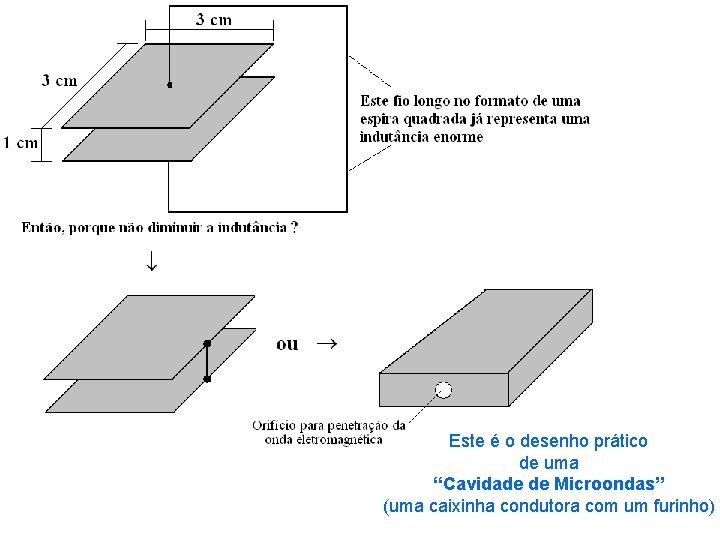
Este é o desenho prático de uma “Cavidade de Microondas” (uma caixinha condutora com um furinho)

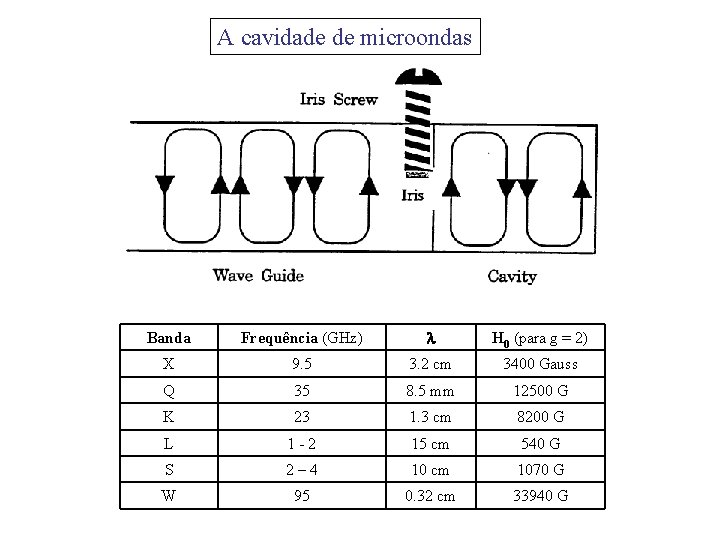
A cavidade de microondas Banda Frequência (GHz) H 0 (para g = 2) X 9. 5 3. 2 cm 3400 Gauss Q 35 8. 5 mm 12500 G K 23 1. 3 cm 8200 G L 1 -2 15 cm 540 G S 2– 4 10 cm 1070 G W 95 0. 32 cm 33940 G

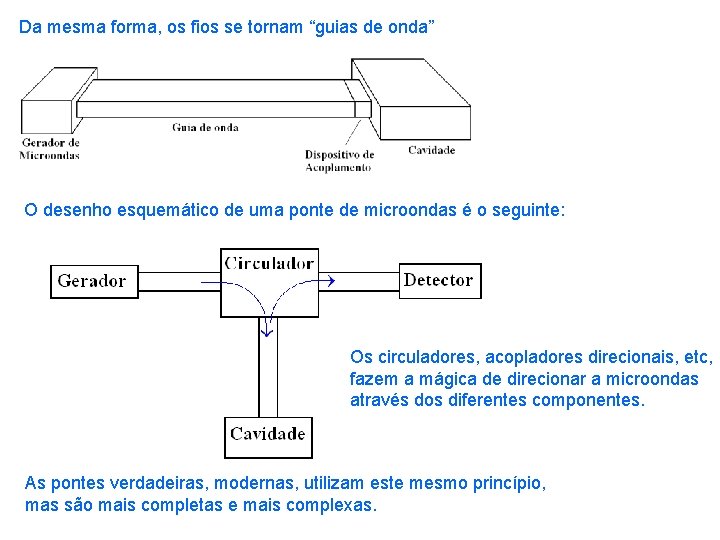
Da mesma forma, os fios se tornam “guias de onda” O desenho esquemático de uma ponte de microondas é o seguinte: Os circuladores, acopladores direcionais, etc, fazem a mágica de direcionar a microondas através dos diferentes componentes. As pontes verdadeiras, modernas, utilizam este mesmo princípio, mas são mais completas e mais complexas.

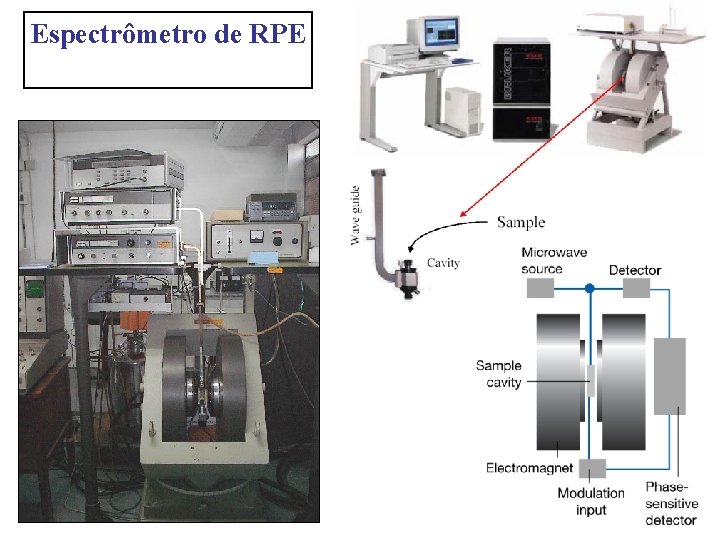
Espectrômetro de RPE

Espectrômetro RPE cw Varian adquirido em 1980 Espectrômetro RPE pulsado Bruker adquirido em 2000 IFSC – Grupo de Biofísica

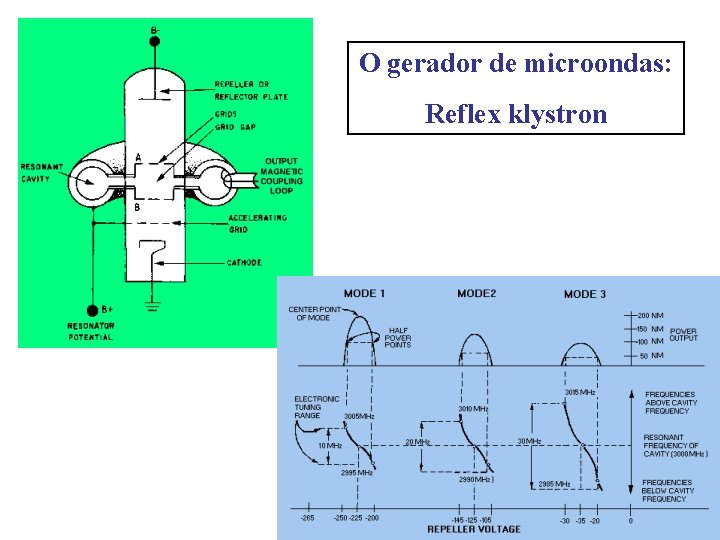
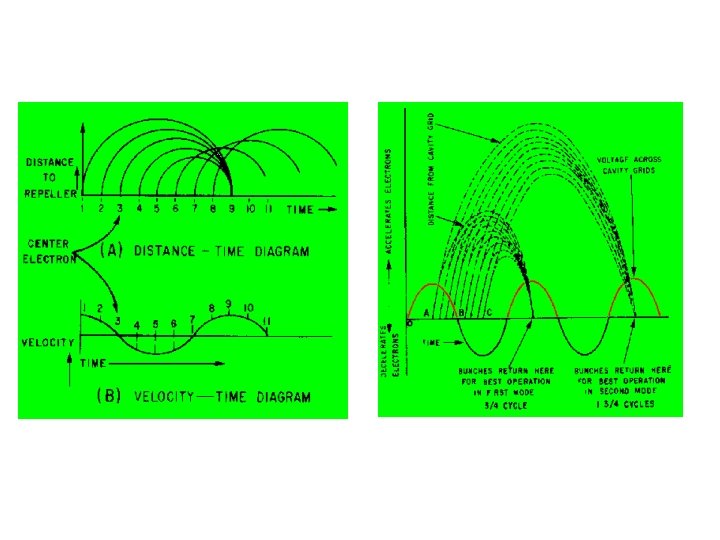
O gerador de microondas: Reflex klystron


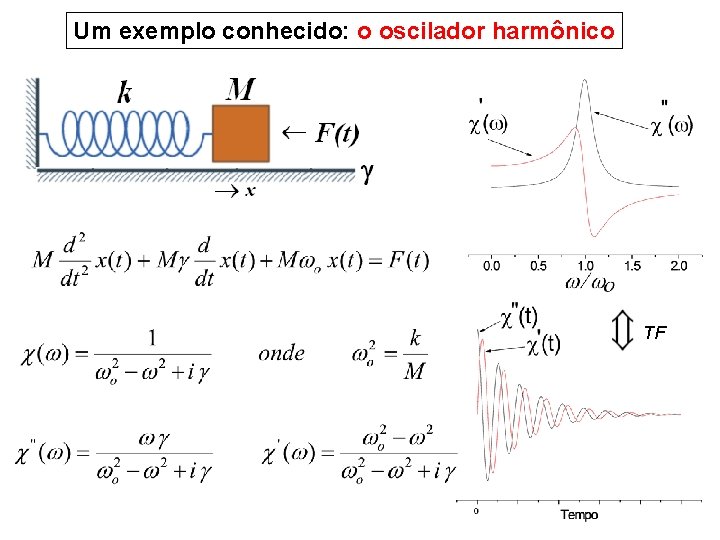
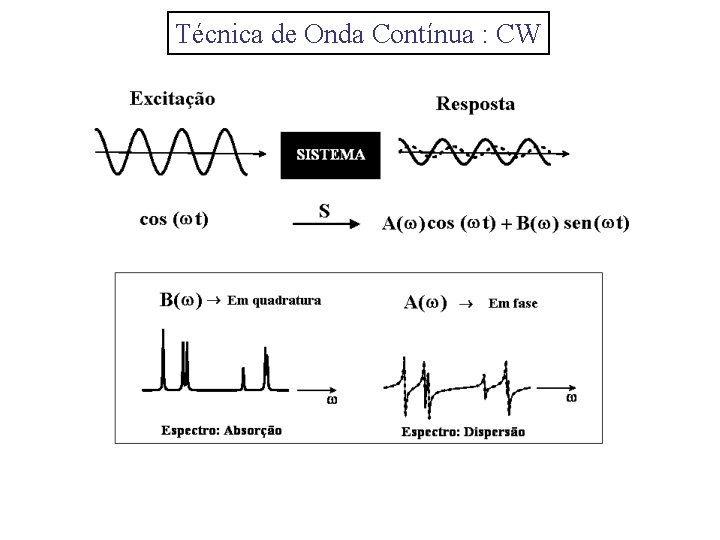
Um conceito importante: a teoria da “Resposta Linear” A magnetização da amostra é a resposta ao campo de excitação Parte imaginária ” Absorção (ou componente em quadratura) Parte real ’ Dispersão (ou componente em fase)

Um exemplo conhecido: o oscilador harmônico TF

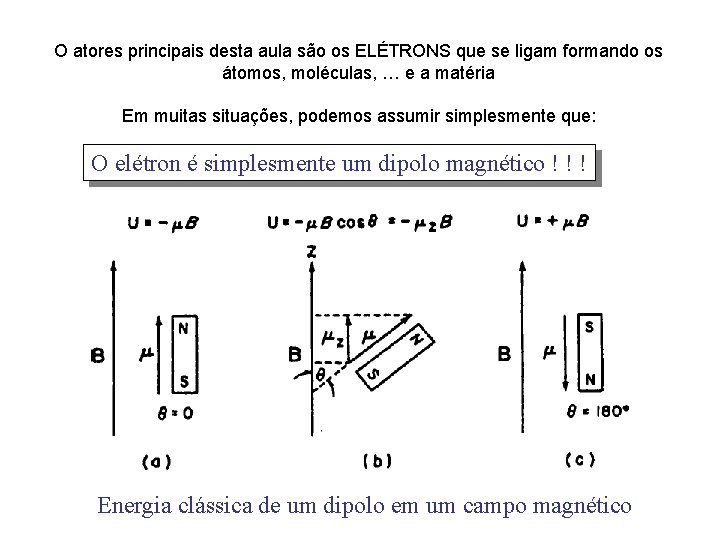
O atores principais desta aula são os ELÉTRONS que se ligam formando os átomos, moléculas, … e a matéria Em muitas situações, podemos assumir simplesmente que: O elétron é simplesmente um dipolo magnético ! ! ! Energia clássica de um dipolo em um campo magnético

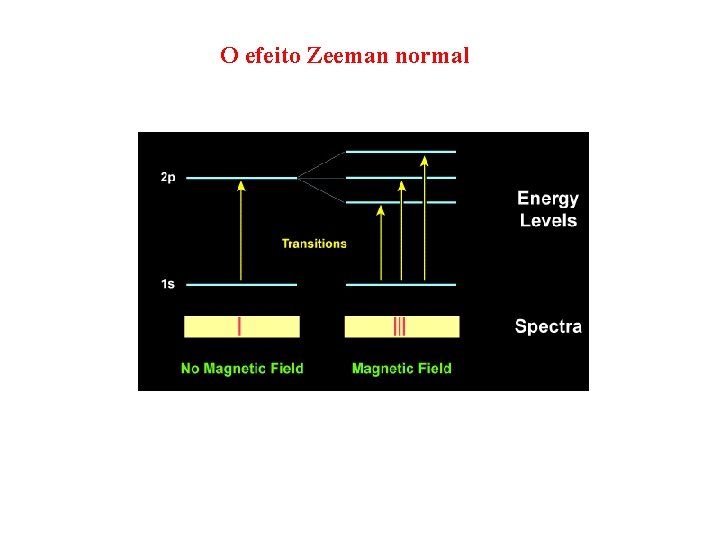
O efeito Zeeman normal

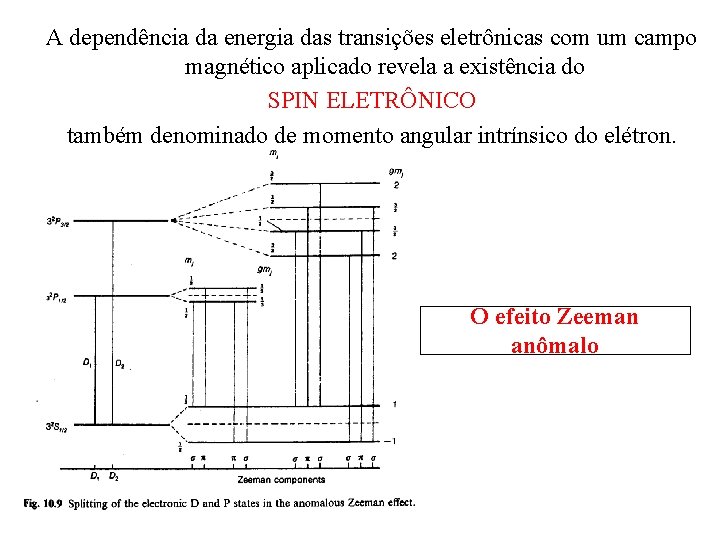
A dependência da energia das transições eletrônicas com um campo magnético aplicado revela a existência do SPIN ELETRÔNICO também denominado de momento angular intrínsico do elétron. O efeito Zeeman anômalo

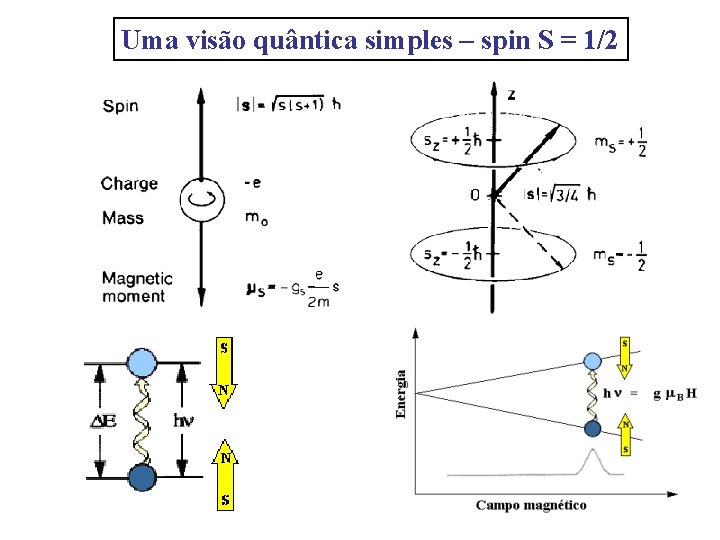
Uma visão quântica simples – spin S = 1/2

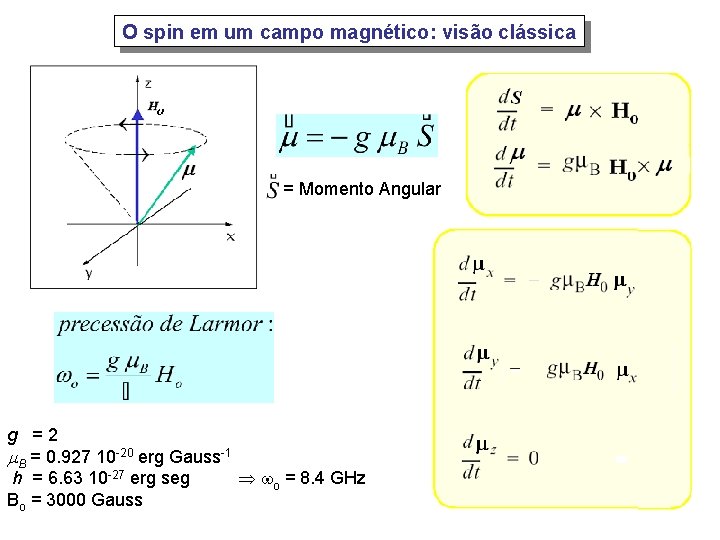
O spin em um campo magnético: visão clássica = Momento Angular g = 2 B = 0. 927 10 -20 erg Gauss-1 h = 6. 63 10 -27 erg seg o = 8. 4 GHz Bo = 3000 Gauss

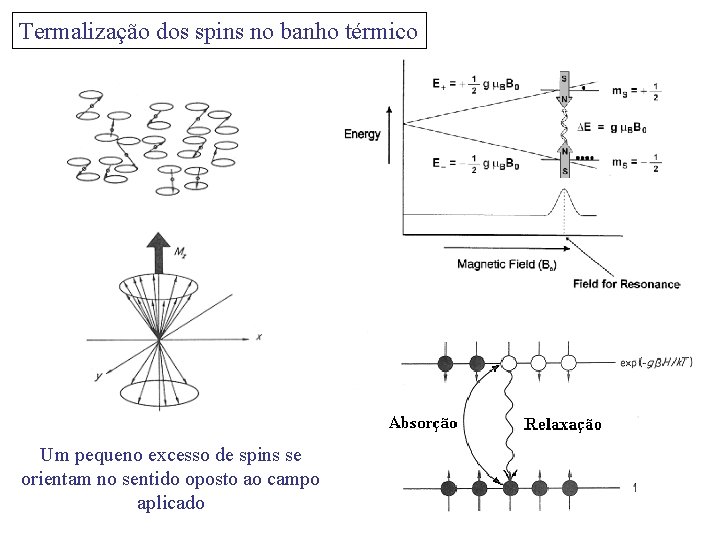
Termalização dos spins no banho térmico Um pequeno excesso de spins se orientam no sentido oposto ao campo aplicado

Paramagnetismo M : momento magnético / unidade de volume Ho : intensidade do campo macroscópico aplicado o : susceptibilidade por unidade de volume âSomente se manifesta na presença de um campo externo. âSomente é observado em átomos, moléculas com spins desemparelhados. âA orientação de cada momento é perturbada pelo efeito térmico. âAlinhamento parcial é induzido pelo campo aplicado. âParamagnetismo ideal é caracterizado por uma susceptibilidade de Curie.

Na maioria dos experimentos de ressonância magnética um campo magnético estático é aplicado (em adição ao campo de radiação eletromagnética), a fim de promover o alinhamento dos spins e desdobrar os níveis de energia, possibilitando assim a absorção e emissão de um quantum da radiação eletromagnética: um fenômeno conhecido por “RESSON NCIA do spin eletrônico”.

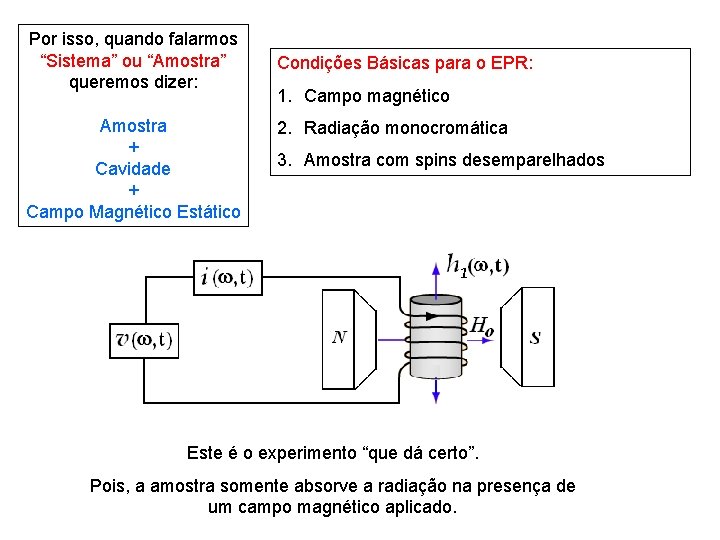
Por isso, quando falarmos “Sistema” ou “Amostra” queremos dizer: Amostra + Cavidade + Campo Magnético Estático Condições Básicas para o EPR: 1. Campo magnético 2. Radiação monocromática 3. Amostra com spins desemparelhados Este é o experimento “que dá certo”. Pois, a amostra somente absorve a radiação na presença de um campo magnético aplicado.

Técnica de Onda Contínua : CW

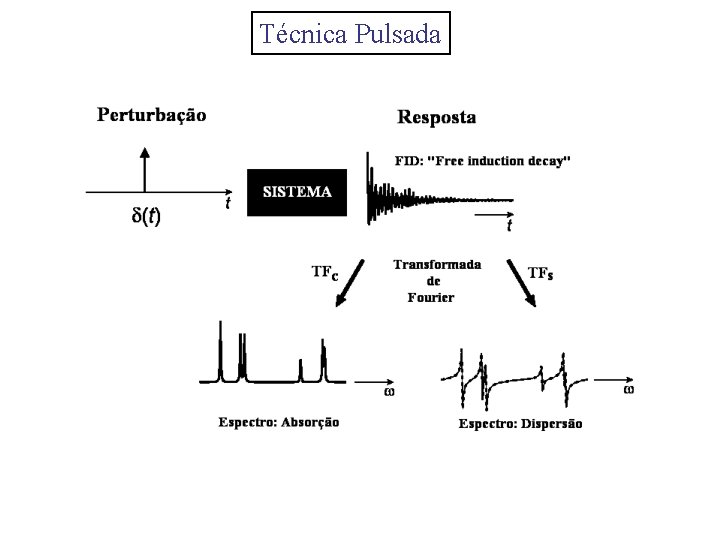
Técnica Pulsada

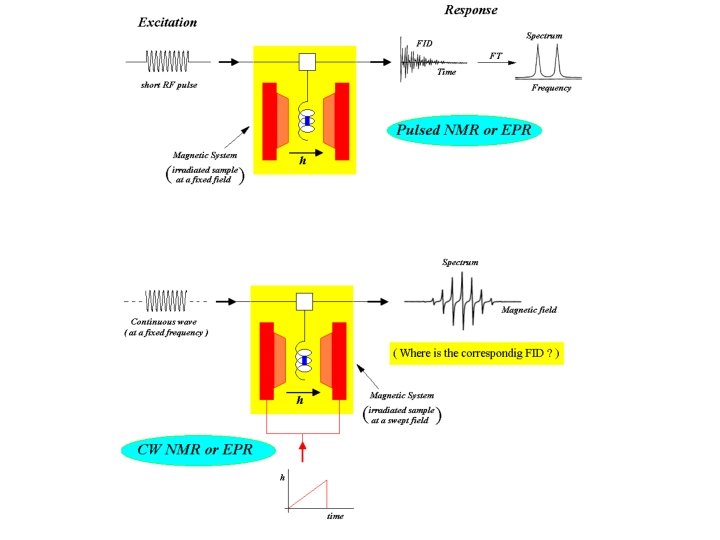
E daí, é só isso? Infelizmente não! Os engenheiros dizem que: Variar a frequência da microoonda, mantendo a mesma sensibilidade, com a cavidade sintonizada e acoplada: NEM PENSAR ! ! ! Solução: Fazer o que? Nesta parte são os engenheiros que dão as ordens. O único jeito é “dar um jeito”. Se é para o bem de todos: manteremos a frequência fixa, mas, VAMOS VARIAR O CAMPO MAGNÉTICO (lentamente)


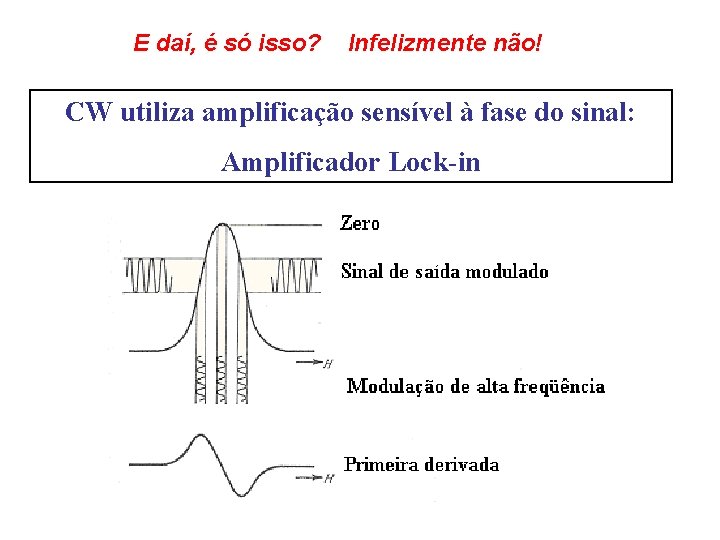
E daí, é só isso? Infelizmente não! CW utiliza amplificação sensível à fase do sinal: Amplificador Lock-in

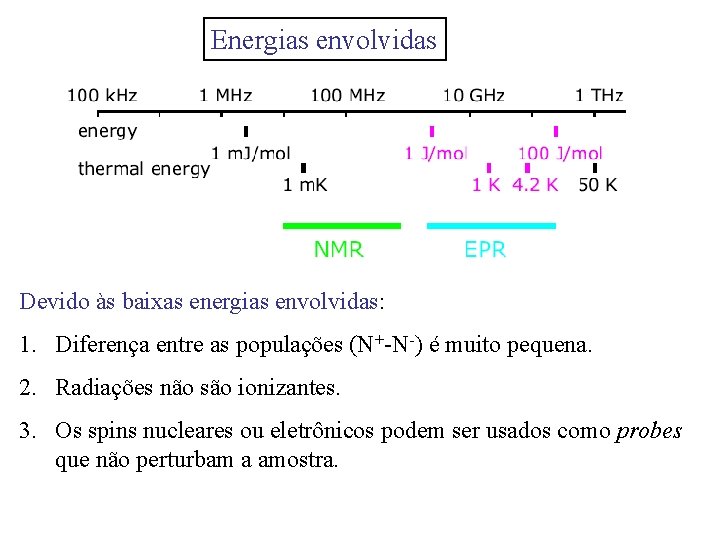
Energias envolvidas Devido às baixas energias envolvidas: 1. Diferença entre as populações (N+-N-) é muito pequena. 2. Radiações não são ionizantes. 3. Os spins nucleares ou eletrônicos podem ser usados como probes que não perturbam a amostra.

Parâmetros característicos do espectro de RPE • fator-g • acoplamentos hiperfinos • formas de linha • Intensidades • Tempos de relaxação



Outro tipo de Magnetismo: Diamagnetismo M : momento magnético / unidade de volume B : intensidade do campo macroscópico aplicado : susceptibilidade por unidade de volume âSomente se manifesta na presença de um campo externo. âDiamagnetismo é comum a quase todos os materiais mas é normalmente pequeno comparado com outros tipos de magnetismo. âSua origem é orbital (blindagem): NÃO PRECISA DO SPIN DO ELÉTRON! âÉ caracterizado por uma susceptibilidade magnética negativa e independente da temperatura.

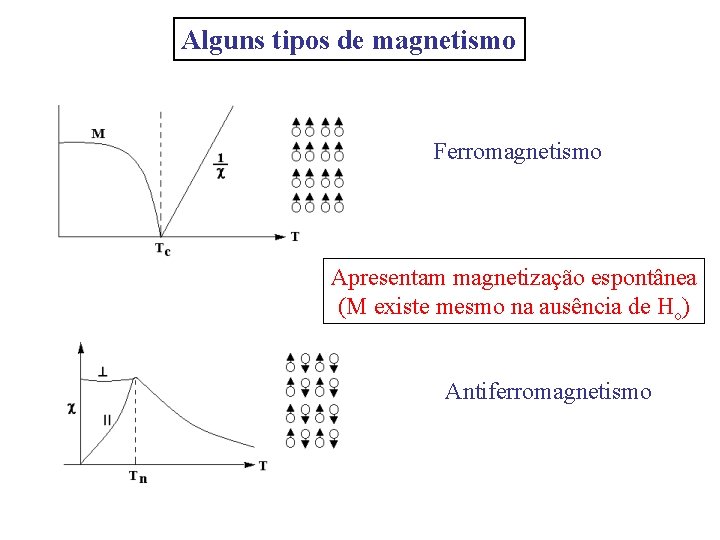
Alguns tipos de magnetismo Ferromagnetismo Apresentam magnetização espontânea (M existe mesmo na ausência de Ho) Antiferromagnetismo

O átomo tem muitos elétrons • Os elétrons interagem não somente com o núcleo mas também entre si, e consigo mesmo (interação spin-órbita) É difícil calcular a função de onda. • Configuração eletrônica: Como os elétrons preenchem as camadas? Como encontrar o estado fundamental?

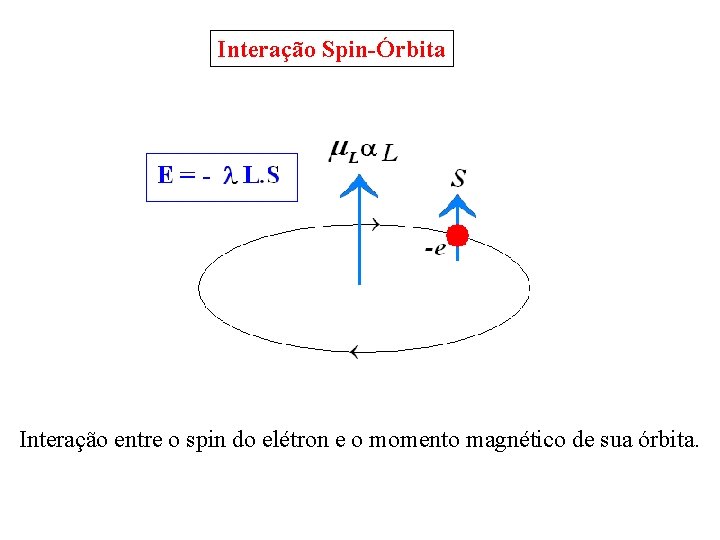
Interação Spin-Órbita Interação entre o spin do elétron e o momento magnético de sua órbita.

O princípio de exclusão de Pauli • O princípio de exclusão de Pauli requer que somente um elétron possa estar em um dado estado, (n, l, ms). • Este princípio se aplica para fermions (próximo slide). • No estado fundamental dos átomos, elétrons ocupam os estados de mais baixa energia, disponíveis e consistentes com o princípio de exclusão.

Fermions e Bosons Partículas com spin semi-inteiro são chamadas de “Partículas de Fermi” ou “Fermions” (protons, elétrons e neutrons) Suas funções de onda são antissimétricas com relação à troca pares de partículas: Partículas com spin inteiro (ou nulo) são chamadas de “Partículas de Bose” ou “Bosons” (fotons, partícula α, atomos de Hélio). Suas funções de onda são simétricas com relação à troca pares de partículas:

Configuração eletrônica • Duas regras básicas determinam a estrutura eletrônica de um átomo de muitos elétrons. – O sistema de partículas é estável se a energia total é mínima. – Somente um elétron pode existir em qualquer estado quântico. • Camadas atômicas com números quânticos principais, n, são denotados por letras maiúsculas: n=1 (K), n=2 (L), n=3 (M), n=4 (N), n=5 (O), • Cada sub-camada é identificada pelo seu número quântico principal, n, seguido da letra correspondente ao número quântico orbital, l, denotado por s, p, d, f, g, h …

O estado do átomo • Cada camada pode conter, no máximo, 2(2 l+1) elétrons, s(2), p(6), d(10)… • O índice acima da letra, à direita, indica o número de elétrons em cada sub-camada. Por exemplo, a configuração do sódio é expressa por: 1 s 22 p 63 s 1. • O número máximo de elétrons em uma camada é igual ao número de elétrons em todas sub-camadas fechadas. Por exemplo, na camada n é igual a 2 n 2: n=1 (2), n=2(8), n=3(18)… • Para uma dada configuração: Como se determinam os estados atômicos e o estado fundamental?

O momento angular total • Cada elétron no átomo tem um certo momento angular orbital L e um certo momento angular de spin S. Ambos contribuem para o momento angular total J do átomo. Como? • Em termos da soma de momentos angulares existe diversas maneiras de se obter o momento angular total. As duas principais são: “Acoplamento LS” e “Acoplamento JJ”.

Acoplamento LS • Quando o acoplamento spin-órbita em um elétron individual é menor do que as interações eletrostáticas elétron-eletron, o acoplamento LS se aplica. • O momento angular orbital individual, Li dos diversos elétrons se acoplam em um único resultante L. Assim também acontece com os momentos Si em um resultante S. Quando a interação spin-orbita atua, L e S interagem magneticamente para formar o momento angular total:

O estado do átomo, sob acoplamento LS Por examplo, 2 P 3/2 S = 1/2, L = 1, J = 3/2.

Acoplamento JJ • Quando as interações spin-órbita individuais são mais fortes do que as interações eletrostáticas mútuas o acoplamento J se aplica. • Cada elétron tem um momento angular Ji resultante da soma vetorial de Li e Si. Daí, os Ji se combinam para formar o momento angular total do átomo, J.

Exemplo • Problema: Encontrar os valores possíveis do momento angular total, sob acoplamento LS, de dois elétrons cujos números quânticos orbitais são l 1=1 and l 2=2. • Solução: Existem três maneiras de se combinar L 1 e L 2 em um único vetor L: L = 3, 2, 1. Da mesma maneira, existem duas maneiras de se combinar S 1 e S 2, S = 1, 0. Como mostra a tabela, os 5 valores possíveis de J são: J = 0, 1, 2, 3, 4. S L 3 2 1 1 4, 3, 2, 1, 0 0 3 1 2

As regras de Hund determinam o estado fundamental do átomo: Para uma dada configuração eletrônica, o estado com maior multiplicidade (2 S+1) tem a energia mais baixa. Para uma dada multiplicidade, (S), o estado com maior valor de L tem energia mais baixa. Para elétrons equivalentes, os estados com menor valor de J tem a energia mais baixa em multipletos “normais”, (valendo a reversa). “Normal” significa que as sub-camadas estão menos que a metade cheias.

Exemplo Problem: A configuração de um átomo é 1 s 22 p 3. Solução: L 1 = 1, L 2 = 1 L = 2, 1, 0. S 1 = 1/2, S 2 = 1/2 S = 1, 0. 3 D 3, 3 D 2, 3 D 1, 1 D 2, 3 P 1, 3 P 0, 1 P 1, 3 S 1, 1 S 0 Princípio de exclusão proíbe D 3 P 2, 3 P 1, 3 P 0, 1 P 1, 3 S 1, 1 S 0 Maior multiplicidade 3 P, 3 S Maior L 3 P Camada menos da metade cheia 3 P 0

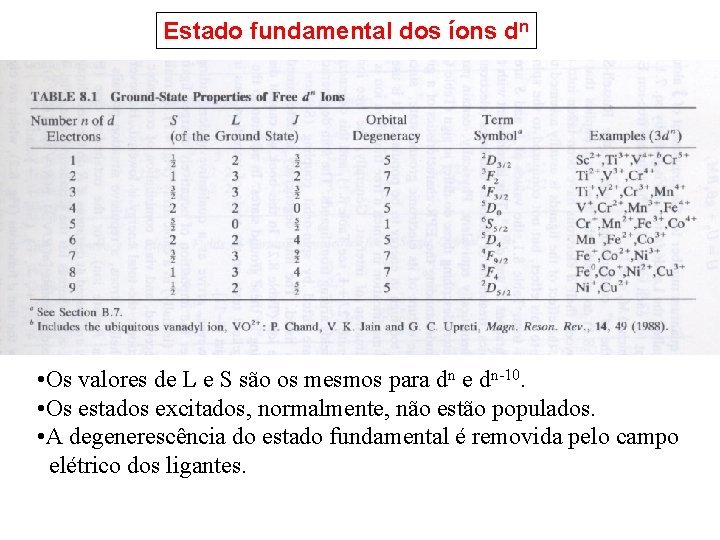
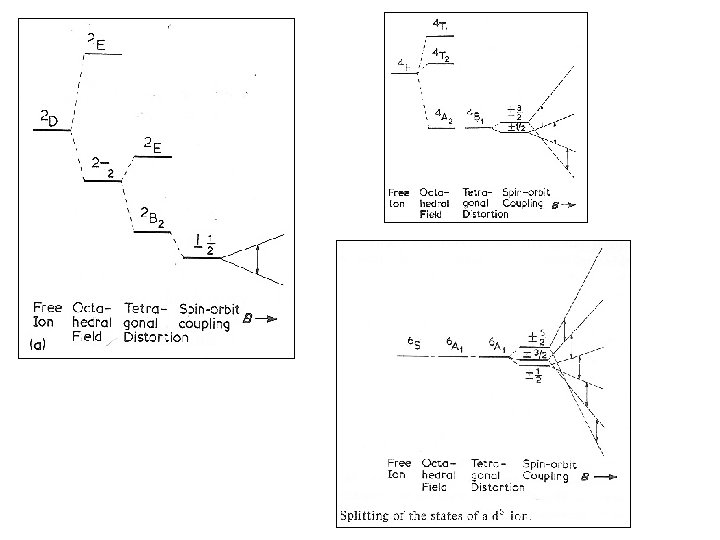
Estado fundamental dos íons dn • Os valores de L e S são os mesmos para dn e dn-10. • Os estados excitados, normalmente, não estão populados. • A degenerescência do estado fundamental é removida pelo campo elétrico dos ligantes.

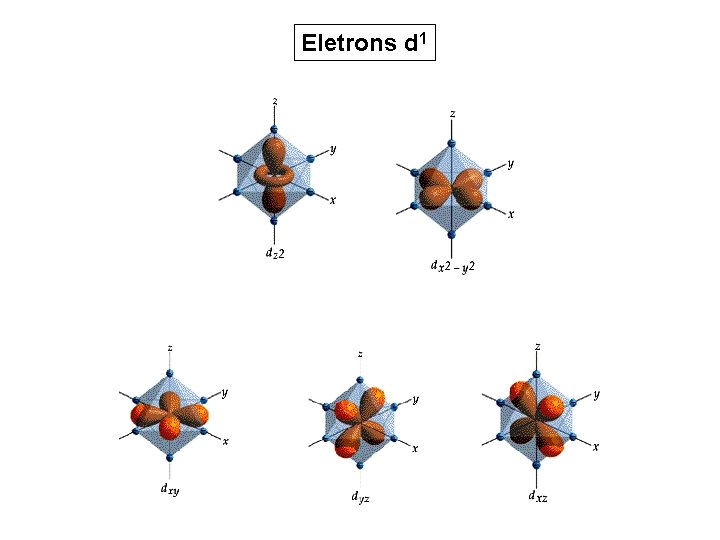
Eletrons d 1


Hamiltoniano de spin Para o caso do acoplamento LS, a teoria preve que o estado fundamental do íon, na presença do campo cristalino e do campo externo, B, pode ser descrita por um Hamiltoniano efetivo: “matriz g” caracterizada por gx , gy , gz “matriz de campo nulo” caracterizada por Dx , Dy , Dz G : estado fundamental de energia EG n : estados excitados de energia En O primeiro termo de H é a interação Zeeman efetiva. O segundo termo de H é chamado de “termo de campo nulo”

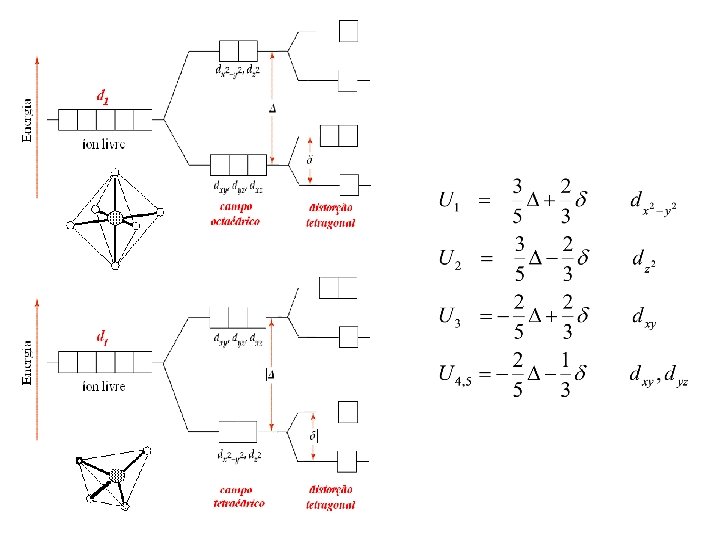
O parâmetro de campo cristalino Aplicando-se a teoria do hamiltoniano de spin para o caso do íon d 1 em um campo octaédrico, obtem-se: Portanto, a medida experimental do tensor g permite o cálculo de e .

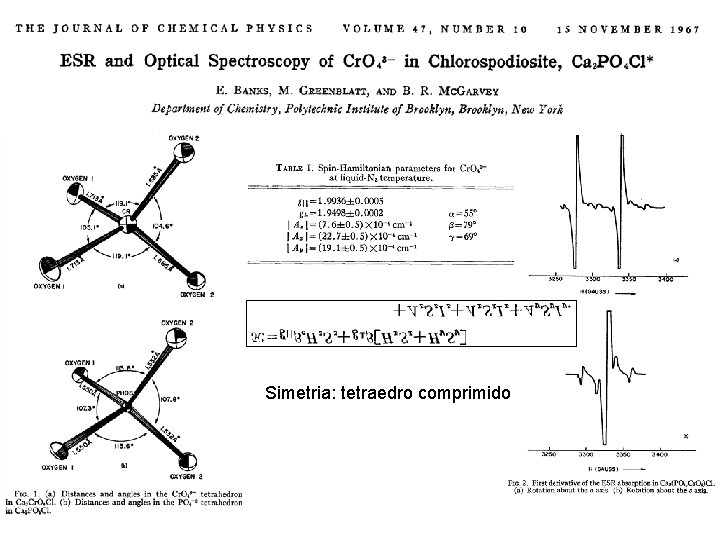
Simetria: tetraedro comprimido

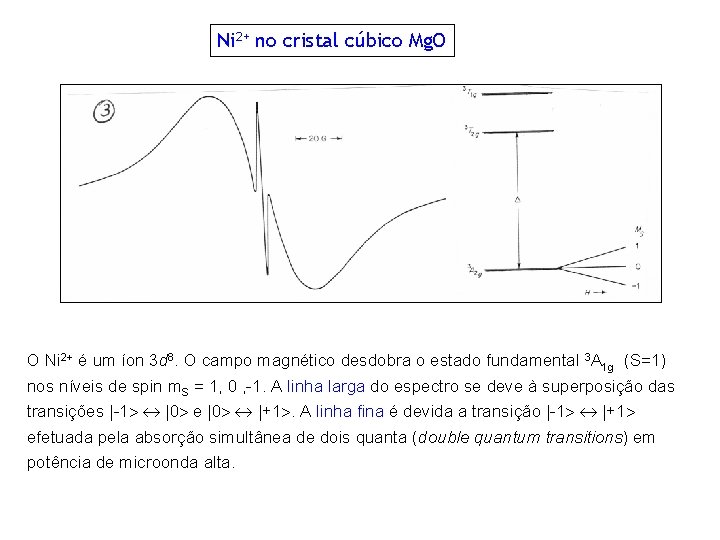
Ni 2+ no cristal cúbico Mg. O O Ni 2+ é um íon 3 d 8. O campo magnético desdobra o estado fundamental 3 A 1 g (S=1) nos níveis de spin m. S = 1, 0 , -1. A linha larga do espectro se deve à superposição das transições |-1 |0 e |0 |+1. A linha fina é devida a transição |-1 |+1 efetuada pela absorção simultânea de dois quanta (double quantum transitions) em potência de microonda alta.


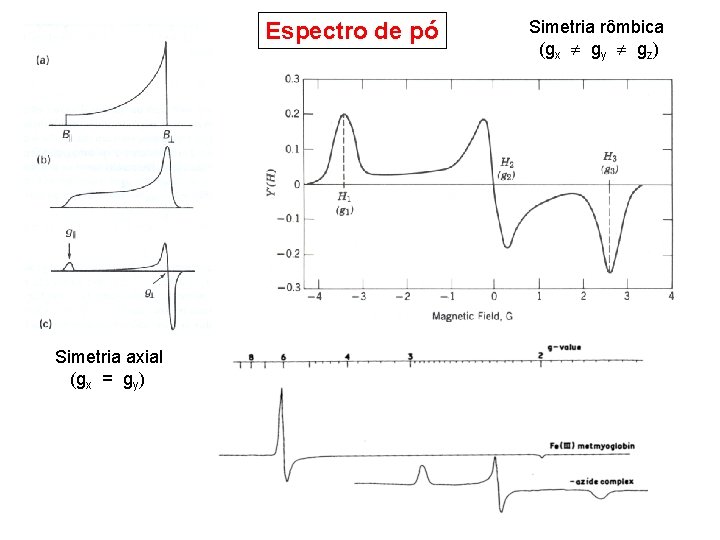
Espectro de pó Simetria axial (gx = gy) Simetria rômbica (gx gy gz)

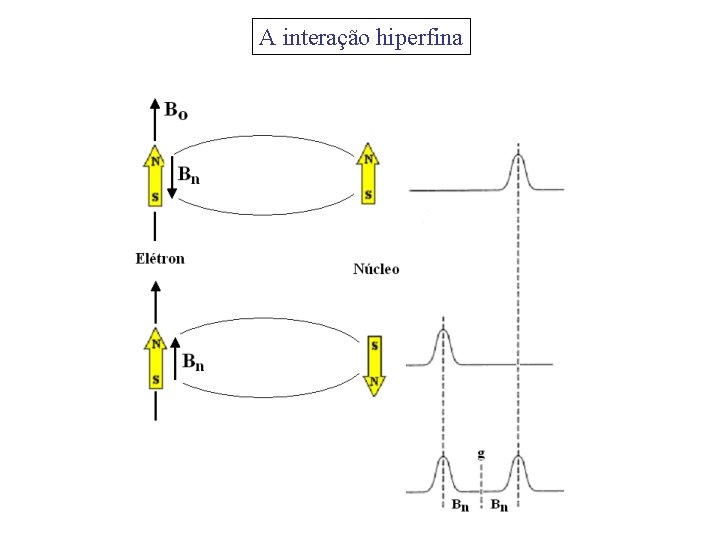
A interação hiperfina

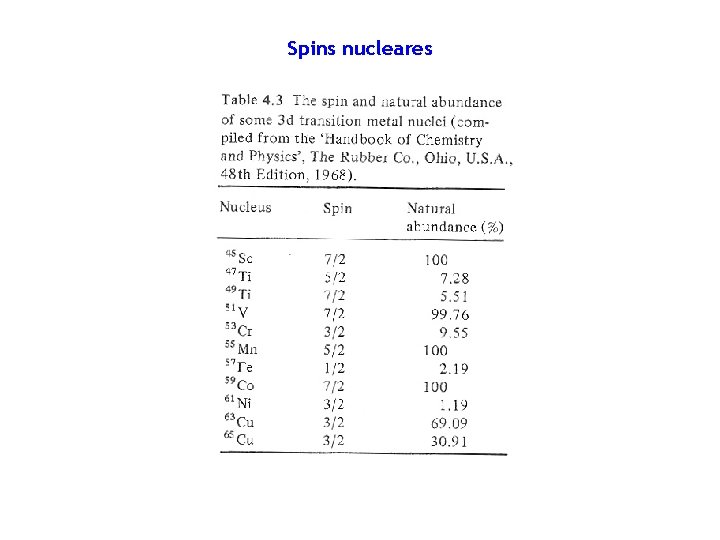
Spins nucleares

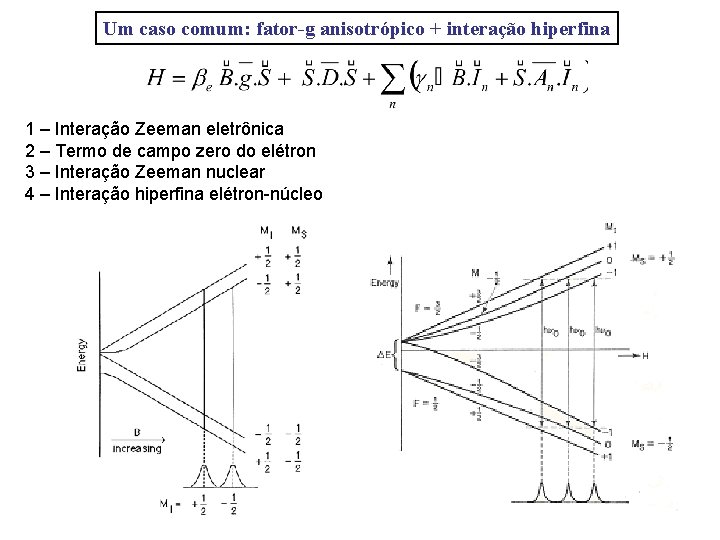
Um caso comum: fator-g anisotrópico + interação hiperfina 1 – Interação Zeeman eletrônica 2 – Termo de campo zero do elétron 3 – Interação Zeeman nuclear 4 – Interação hiperfina elétron-núcleo

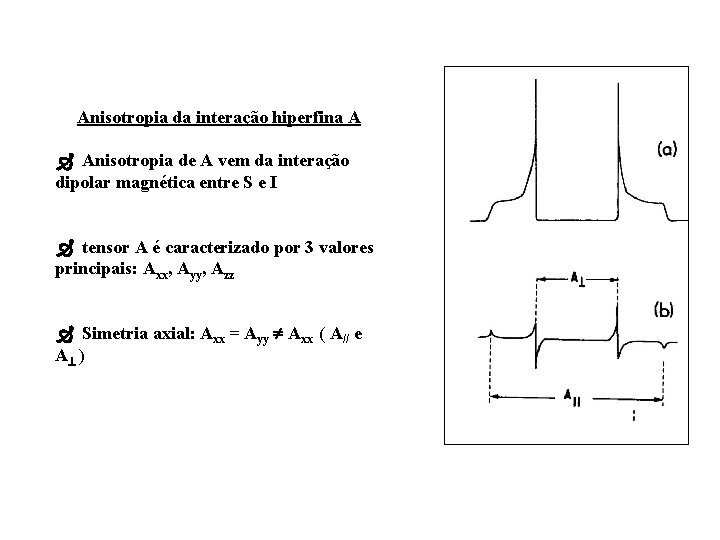
Anisotropia da interação hiperfina A Anisotropia de A vem da interação dipolar magnética entre S e I tensor A é caracterizado por 3 valores principais: Axx, Ayy, Azz Simetria axial: Axx = Ayy Axx ( A// e A )

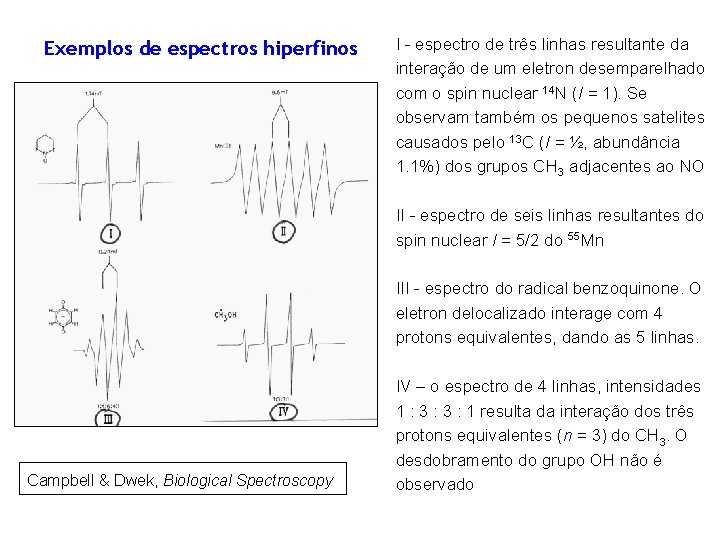
Exemplos de espectros hiperfinos I - espectro de três linhas resultante da interação de um eletron desemparelhado com o spin nuclear 14 N (I = 1). Se observam também os pequenos satelites causados pelo 13 C (I = ½, abundância 1. 1%) dos grupos CH 3 adjacentes ao NO II - espectro de seis linhas resultantes do spin nuclear I = 5/2 do 55 Mn III - espectro do radical benzoquinone. O eletron delocalizado interage com 4 protons equivalentes, dando as 5 linhas. Campbell & Dwek, Biological Spectroscopy IV – o espectro de 4 linhas, intensidades 1 : 3 : 1 resulta da interação dos três protons equivalentes (n = 3) do CH 3. O desdobramento do grupo OH não é observado

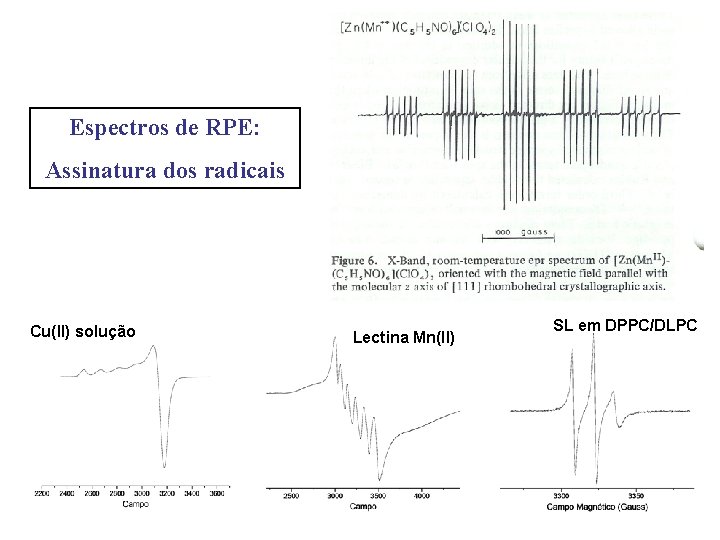
Espectros de RPE: Assinatura dos radicais Cu(II) solução Lectina Mn(II) SL em DPPC/DLPC

Movimento: escala de Tempo em RPE Um marcador de spin é um radical que interage com um biopolímero. O seu espectro reflete as propriedades dinâmicas do biopolímero. Marcadores de spin de nitróxido (estáveis até 80 o. C e p. H de 3 a 10) tem sido utilizados para estudar a dinâmica de membranas biológicas e de cadeias poliméricas. O marcador pode ser ligado um grupo funcional específico da macromolécula

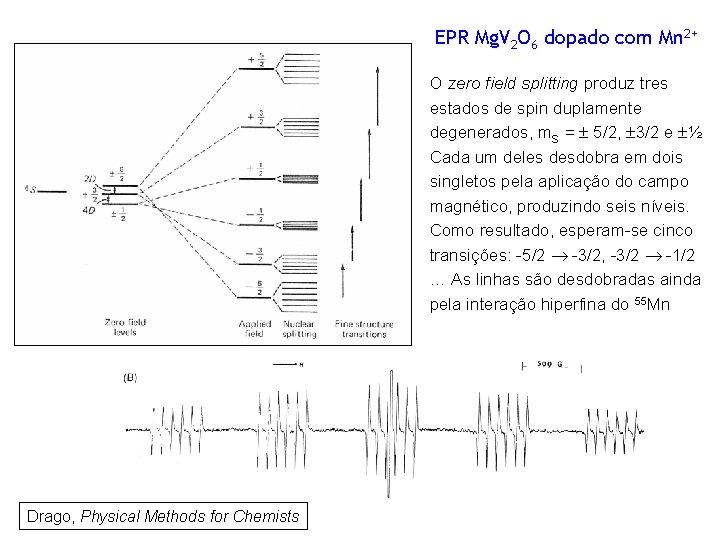
EPR Mg. V 2 O 6 dopado com Mn 2+ O zero field splitting produz tres estados de spin duplamente degenerados, m. S = 5/2, 3/2 e ½ Cada um deles desdobra em dois singletos pela aplicação do campo magnético, produzindo seis níveis. Como resultado, esperam-se cinco transições: -5/2 -3/2, -3/2 -1/2 … As linhas são desdobradas ainda pela interação hiperfina do 55 Mn Drago, Physical Methods for Chemists

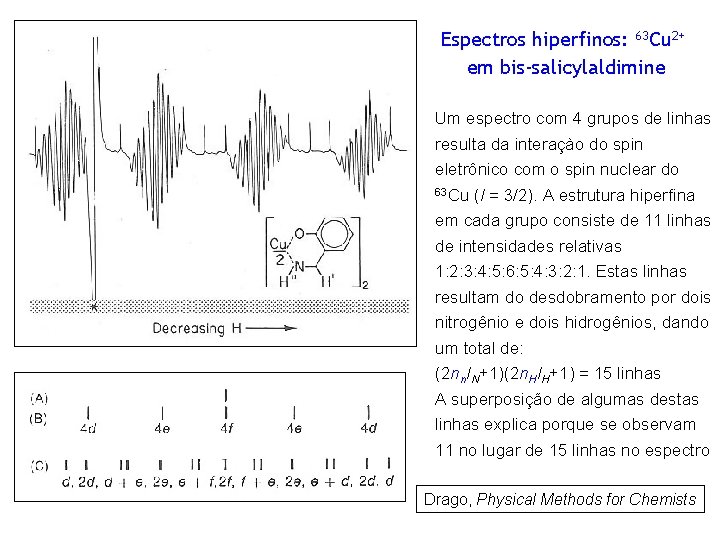
Espectros hiperfinos: 63 Cu 2+ em bis-salicylaldimine Um espectro com 4 grupos de linhas resulta da interaçào do spin eletrônico com o spin nuclear do 63 Cu (I = 3/2). A estrutura hiperfina em cada grupo consiste de 11 linhas de intensidades relativas 1: 2: 3: 4: 5: 6: 5: 4: 3: 2: 1. Estas linhas resultam do desdobramento por dois nitrogênio e dois hidrogênios, dando um total de: (2 nn. IN+1)(2 n. HIH+1) = 15 linhas A superposição de algumas destas linhas explica porque se observam 11 no lugar de 15 linhas no espectro Drago, Physical Methods for Chemists

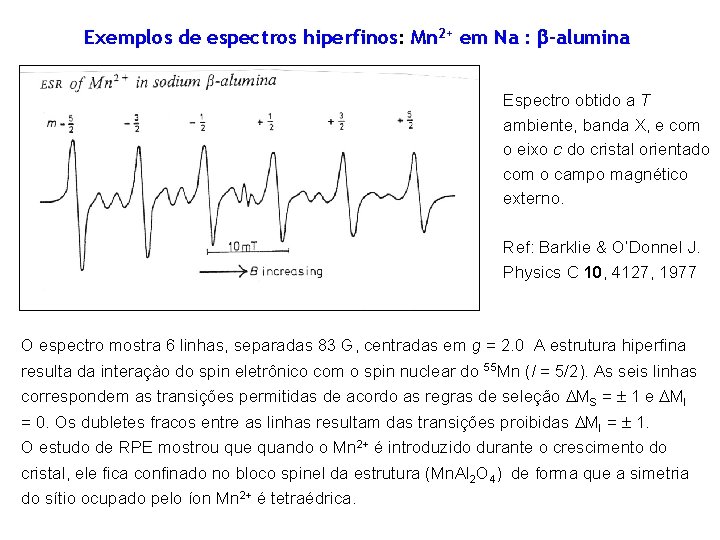
Exemplos de espectros hiperfinos: Mn 2+ em Na : -alumina Espectro obtido a T ambiente, banda X, e com o eixo c do cristal orientado com o campo magnético externo. Ref: Barklie & O’Donnel J. Physics C 10, 4127, 1977 O espectro mostra 6 linhas, separadas 83 G, centradas em g = 2. 0 A estrutura hiperfina resulta da interaçào do spin eletrônico com o spin nuclear do 55 Mn (I = 5/2). As seis linhas correspondem as transições permitidas de acordo as regras de seleção MS = 1 e MI = 0. Os dubletes fracos entre as linhas resultam das transições proibidas MI = 1. O estudo de RPE mostrou que quando o Mn 2+ é introduzido durante o crescimento do cristal, ele fica confinado no bloco spinel da estrutura (Mn. Al 2 O 4) de forma que a simetria do sítio ocupado pelo íon Mn 2+ é tetraédrica.

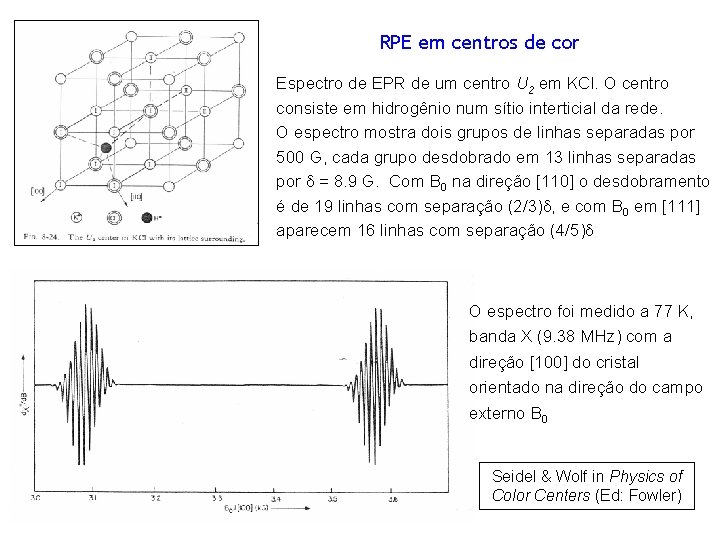
RPE em centros de cor Espectro de EPR de um centro U 2 em KCl. O centro consiste em hidrogênio num sítio interticial da rede. O espectro mostra dois grupos de linhas separadas por 500 G, cada grupo desdobrado em 13 linhas separadas por = 8. 9 G. Com B 0 na direção [110] o desdobramento é de 19 linhas com separação (2/3) , e com B 0 em [111] aparecem 16 linhas com separação (4/5) O espectro foi medido a 77 K, banda X (9. 38 MHz) com a direção [100] do cristal orientado na direção do campo externo B 0 Seidel & Wolf in Physics of Color Centers (Ed: Fowler)

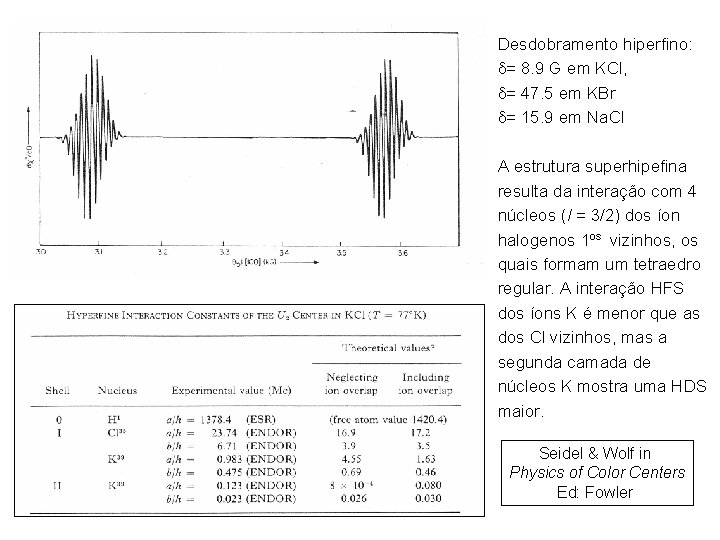
Desdobramento hiperfino: = 8. 9 G em KCl, = 47. 5 em KBr = 15. 9 em Na. Cl A estrutura superhipefina resulta da interação com 4 núcleos (I = 3/2) dos íon halogenos 1 os vizinhos, os quais formam um tetraedro regular. A interação HFS dos íons K é menor que as dos Cl vizinhos, mas a segunda camada de núcleos K mostra uma HDS maior. Seidel & Wolf in Physics of Color Centers Ed: Fowler