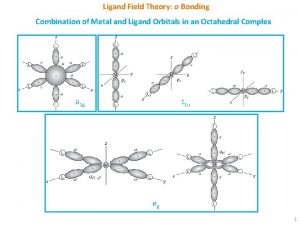
Radiofarmacja Radiofarmacja ligand cznik biomolekua Chemia organiczna Radiochemia
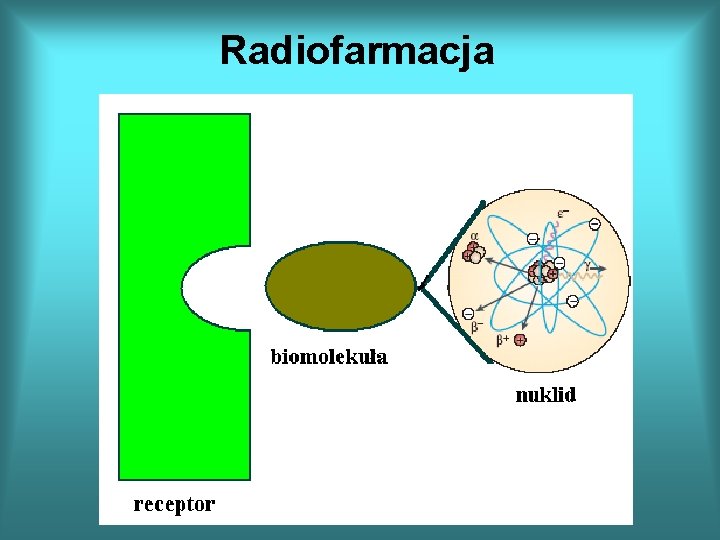
Radiofarmacja
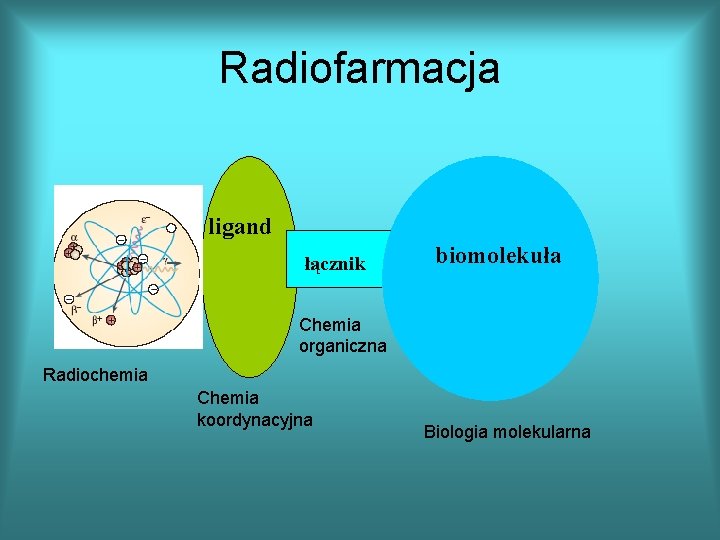
Radiofarmacja ligand łącznik biomolekuła Chemia organiczna Radiochemia Chemia koordynacyjna Biologia molekularna

Rodzaje rozpadow Rozpad g, EC a bb+ Auger przyklad 99 m. Tc 211 At 90 Y 18 F 125 I zastosowanie diagnostyczne terapeutyczne diagnostyczne (PET) terapeutyczne

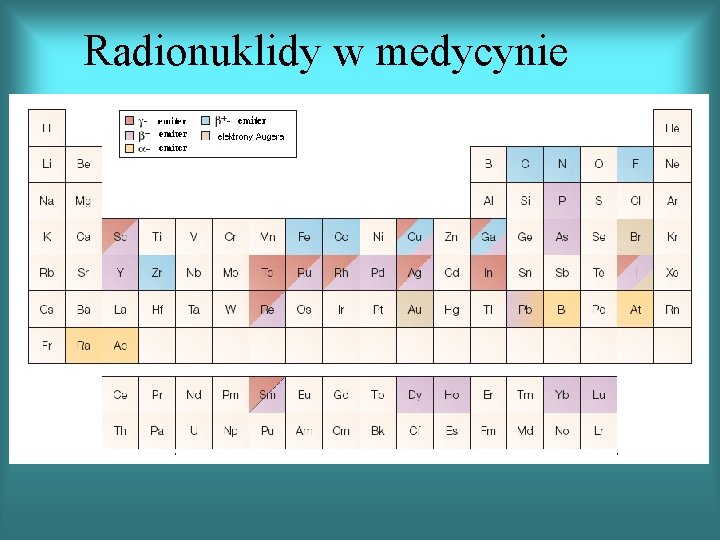
Radionuklidy w medycynie

Otrzymywanie radionuklidów Naturalne np. 226 Ra Reaktor jądrowy Cyklotron Generatory radionuklidów

Reaktor jądrowy jest źródłem neutronów - termicznych - wolnych - niskoenergetycznych 59 Co + n 60 Co - szybkich - wysokoenergetycznych 47 Ti + n 47 Sc + p
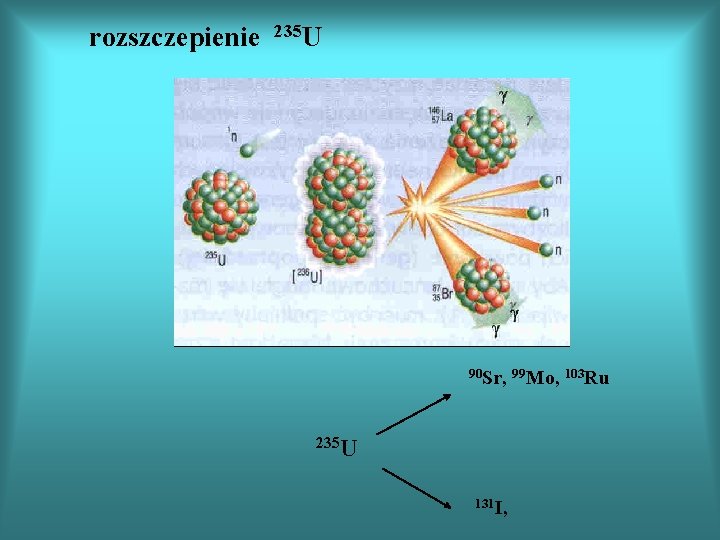
rozszczepienie 235 U 90 Sr, 99 Mo, 103 Ru 235 U 131 I,
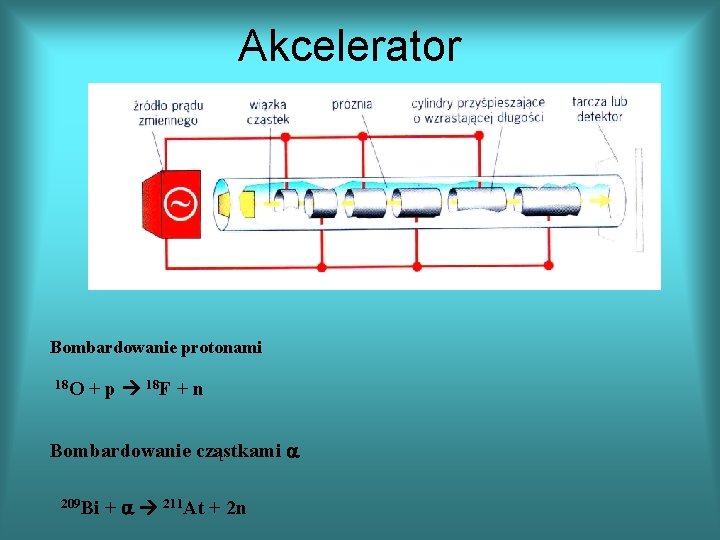
Akcelerator Bombardowanie protonami 18 O + p 18 F + n Bombardowanie cząstkami a 209 Bi + a 211 At + 2 n

Generatory radionuklidów 99 Mo 99 m. Tc 99 Tc Dojenie radionuklidów
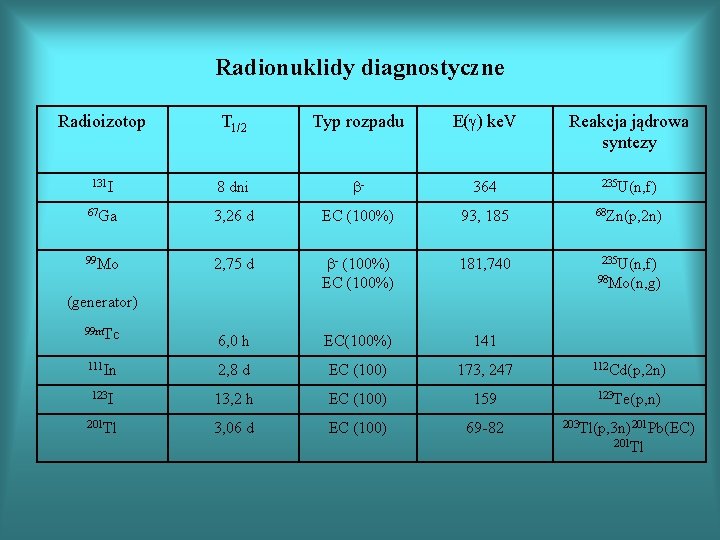
Radionuklidy diagnostyczne Radioizotop T 1/2 Typ rozpadu E(g) ke. V Reakcja jądrowa syntezy 131 I 8 dni b- 364 235 U(n, f) 67 Ga 3, 26 d EC (100%) 93, 185 68 Zn(p, 2 n) 99 Mo 2, 75 d b- (100%) EC (100%) 181, 740 235 U(n, f) 6, 0 h EC(100%) 141 111 In 2, 8 d EC (100) 173, 247 112 Cd(p, 2 n) 123 I 13, 2 h EC (100) 159 123 Te(p, n) 201 Tl 3, 06 d EC (100) 69 -82 203 Tl(p, 3 n)201 Pb(EC) 98 Mo(n, g) (generator) 99 m. Tc 201 Tl
Diagnostyczna medycyna nuklearna
![Chemia technetu [99 m. Tc. O 4]- redukcja 4 ]- Gamma [99 Tc. O Chemia technetu [99 m. Tc. O 4]- redukcja 4 ]- Gamma [99 Tc. O](http://slidetodoc.com/presentation_image_h/ec21cf035eca768da5dbd5464de003cb/image-13.jpg)
Chemia technetu [99 m. Tc. O 4]- redukcja 4 ]- Gamma [99 Tc. O 4]redukcja [99 m. Tc. O 3+] [99 m. Tc 3+] Tc -cysteina
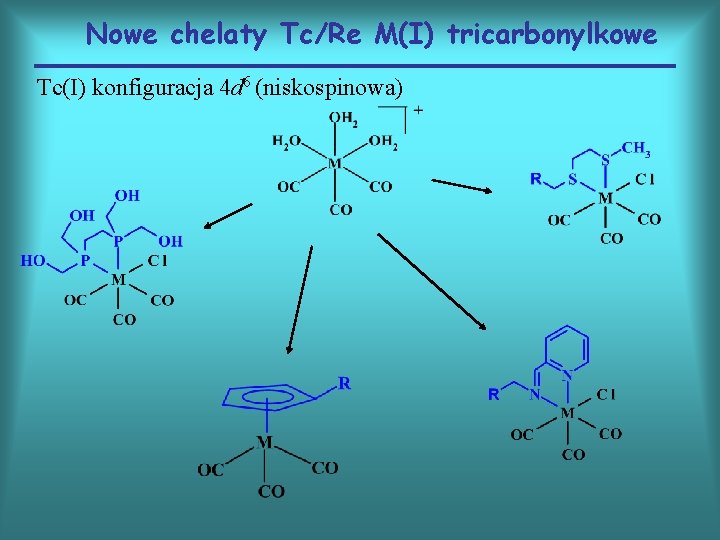
Nowe chelaty Tc/Re M(I) tricarbonylkowe Tc(I) konfiguracja 4 d 6 (niskospinowa)
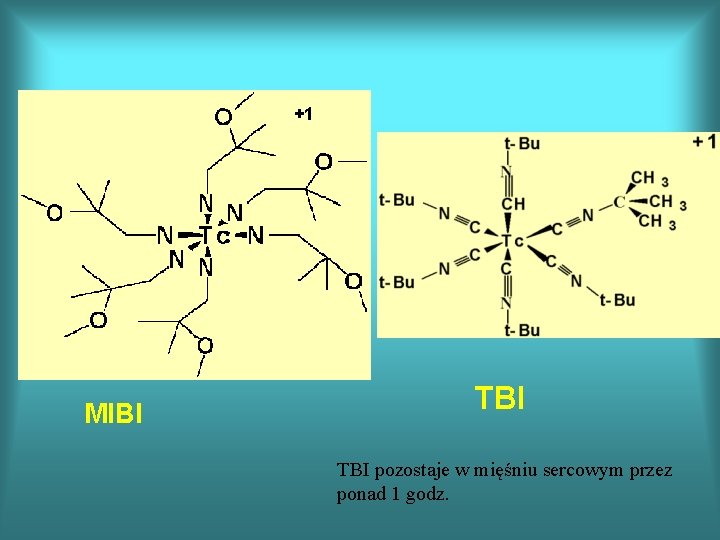
+1 MIBI TBI pozostaje w mięśniu sercowym przez ponad 1 godz.
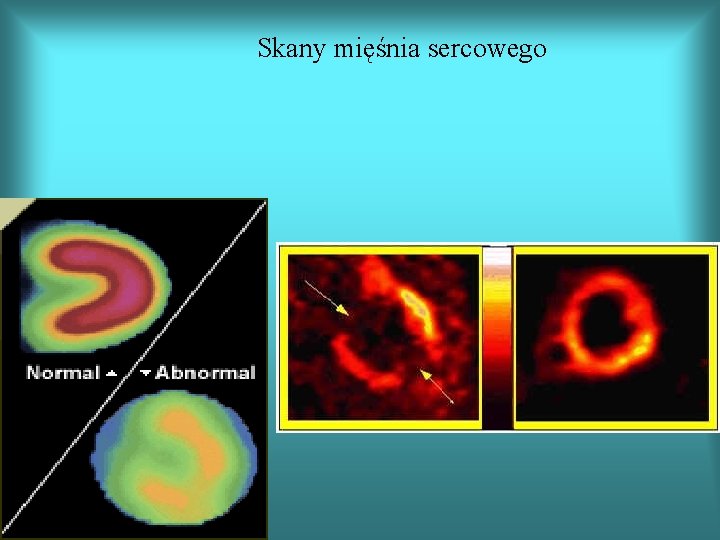
Skany mięśnia sercowego

Jak działa pozytonowa tomografia emisyjna (PET) W PET wykorzystuje się nuklidy z niedomiarem neutronów rozpadające się według rozpadu b+. Pozyton emitowany przez nuklid jest natychmiast anihilowany z elektronem e+ + e- 2 x 511 ke. V

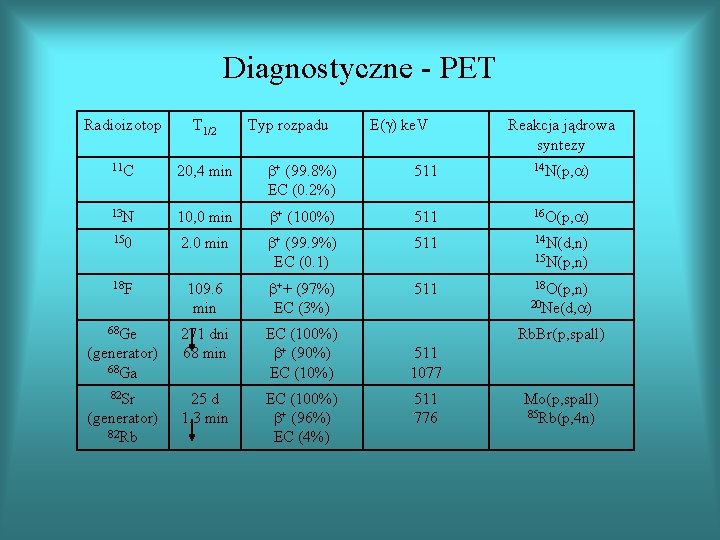
Diagnostyczne - PET Radioizotop T 1/2 11 C 20, 4 min b+ (99. 8%) EC (0. 2%) 511 14 N(p, a) 13 N 10, 0 min b+ (100%) 511 16 O(p, a) 150 2. 0 min b+ (99. 9%) EC (0. 1) 511 14 N(d, n) 109. 6 min b++ (97%) EC (3%) 511 271 dni 68 min EC (100%) b+ (90%) EC (10%) 25 d 1. 3 min EC (100%) b+ (96%) EC (4%) 18 F 68 Ge (generator) 68 Ga 82 Sr (generator) 82 Rb Typ rozpadu E(g) ke. V Reakcja jądrowa syntezy 15 N(p, n) 18 O(p, n) 20 Ne(d, a) Rb. Br(p, spall) 511 1077 511 776 Mo(p, spall) 85 Rb(p, 4 n)

2 -Deoxyglucose C 2
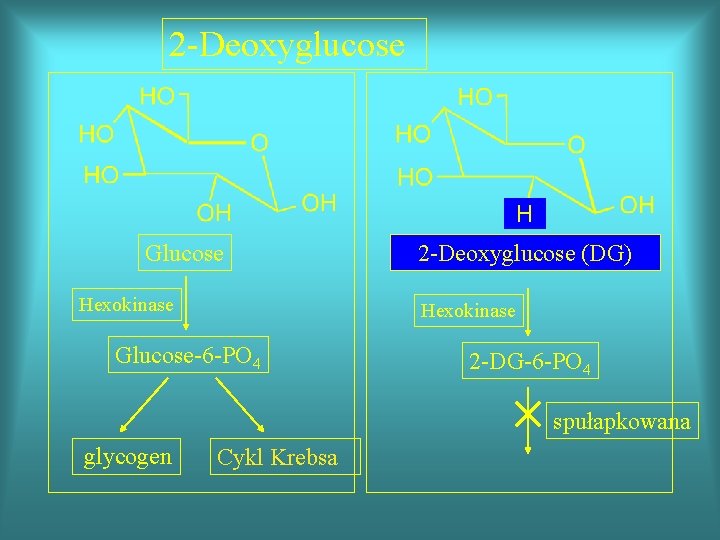
2 -Deoxyglucose H Glucose Hexokinase 2 -Deoxyglucose (DG) Hexokinase Glucose-6 -PO 4 2 -DG-6 -PO 4 spułapkowana glycogen Cykl Krebsa

Metabolizm glukozy C 6 H 12 O 6 HEXOKINASE C 6 H 11 O 6 -6 -PO 4 Glucose C 6 H 12 O 5 F HEXOKINASE [18 F]fluorodeoxyglucose FDG C 6 H 11 O 5 F-6 -PO 4 [18 F]fluorodeoxyglucose-6 -PO 4 FDG glycolysis + TCA cycle (36 -38 ATP) glycogen pentose shunt X spułapkowana
![Podstawienie nukleofilowe 18 F Ac. O OTf 18 O F[F-], K 222 Ac. O Podstawienie nukleofilowe 18 F Ac. O OTf 18 O F[F-], K 222 Ac. O](http://slidetodoc.com/presentation_image_h/ec21cf035eca768da5dbd5464de003cb/image-23.jpg)
Podstawienie nukleofilowe 18 F Ac. O OTf 18 O F[F-], K 222 Ac. O OAc HO Ac. O O 18 F HCl OAc HO O HO 18 F FDG OH

Bioscan FDG aparat do automatycznej syntezy
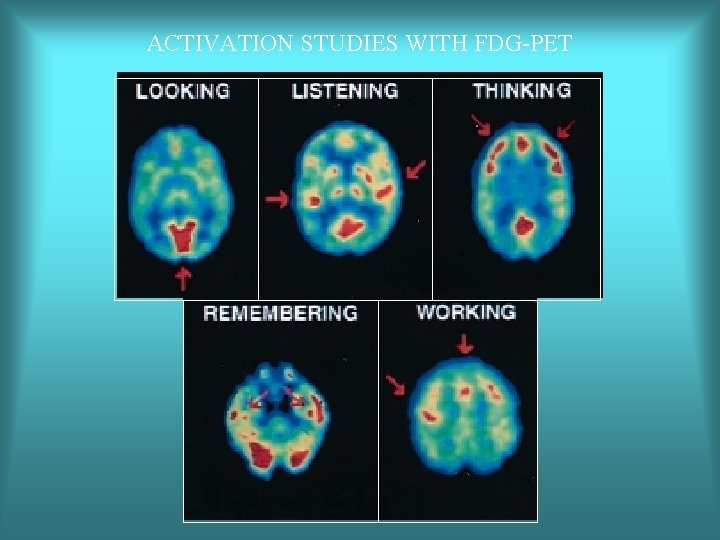
ACTIVATION STUDIES WITH FDG-PET
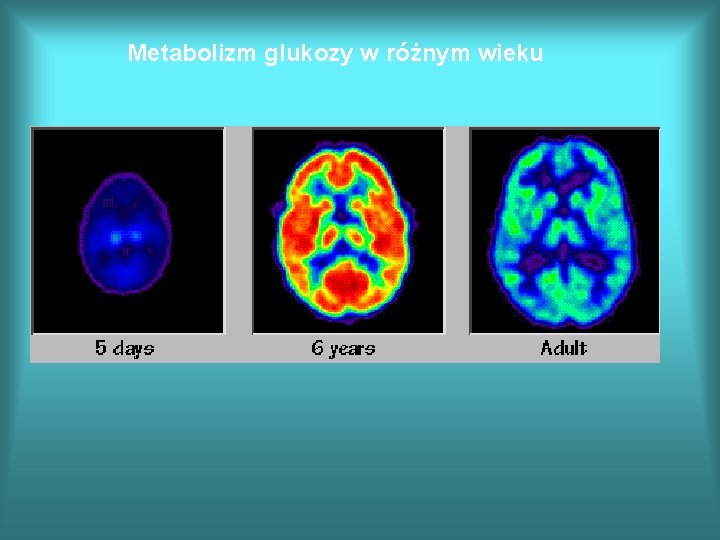
Metabolizm glukozy w różnym wieku
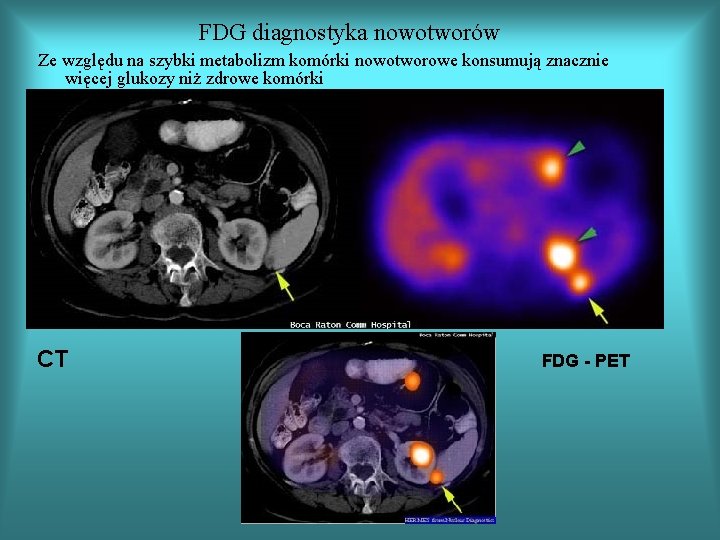
FDG diagnostyka nowotworów Ze względu na szybki metabolizm komórki nowotworowe konsumują znacznie więcej glukozy niż zdrowe komórki CT FDG - PET

67 Ga - cytryniany • W komórkach nowotworowych jest więcej receptorów transferyny niż w zdrowych • Fe 3+/Fe 2+ Ga 3+ • O ile Fe 3+(z transferyną) jest pochłaniany przez komórki to jest także łatwo wydalany w postaci Fe 2+ • Ga nie ma stopnia utl 2+ i nie może być wydalony
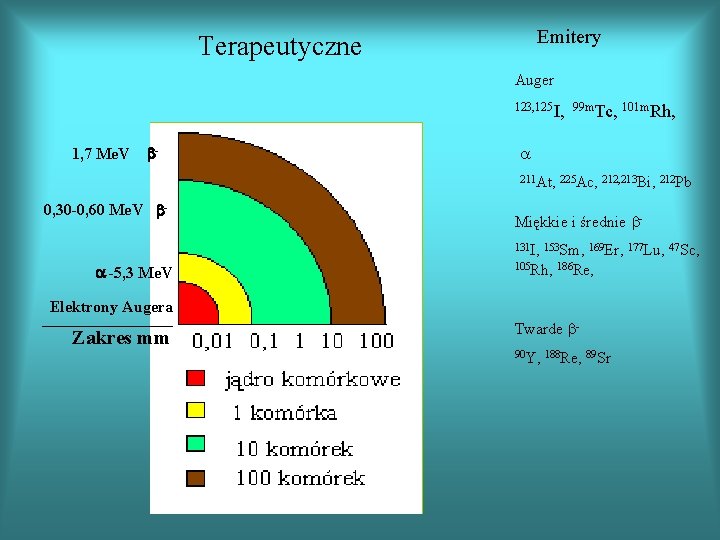
Emitery Terapeutyczne Auger 123, 125 I, 99 m. Tc, 101 m. Rh, 1, 7 Me. V b- a 211 At, 225 Ac, 212, 213 Bi, 212 Pb 0, 30 -0, 60 Me. V b- Miękkie i średnie b 131 I, 153 Sm, 169 Er, 177 Lu, 47 Sc, a -5, 3 Me. V 105 Rh, 186 Re, Elektrony Augera Zakres mm Twarde b 90 Y, 188 Re, 89 Sr


Radionuklidy terapeutyczne radionuklid T 1/2 typ rozpadu (Me. V) max. zasięg

Jakie wymagania musi spełnić radionuklid terapeutyczny? 1. odpowiednia energia emitowanej cząstki, 2. T 1/2 między 1 godz. a 10 dni, 3. duży przekrój czynny reakcji jądrowej syntezy, 4. dobrze, gdy można go otrzymać w reaktorze jądrowym, 5. łatwe wydzielenie z tarczy, 6. możliwość otrzymania w formie beznośnikowej, 7. łatwość wydzielenia z tarczy

radionuklidy beznośnikowe 176 Lu + n 177 Lu - nośnikowy 176 Yb +n 177 Yb 177 Lu - beznośnikowy Zalety radionuklidów beznośnikowych - duża aktywność właściwa, - znakowanie wszystkich centrów aktywnych biomolekuły - duży efekt terapeutyczny
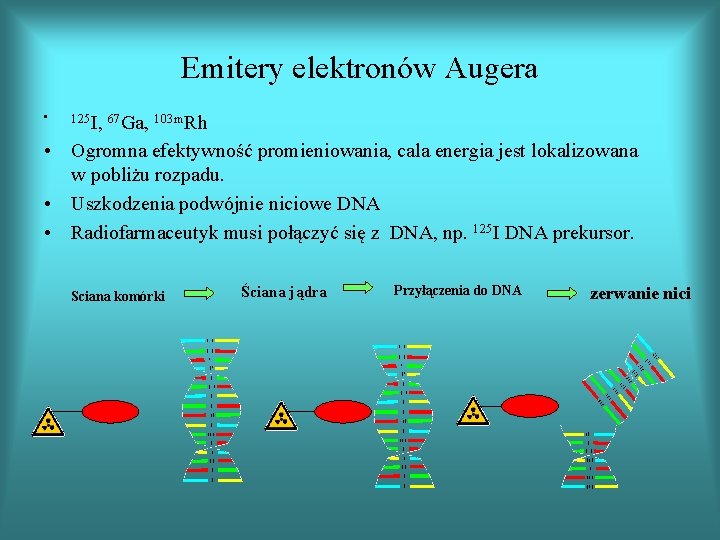
Emitery elektronów Augera • 125 I, 67 Ga, 103 m. Rh • Ogromna efektywność promieniowania, cala energia jest lokalizowana w pobliżu rozpadu. • Uszkodzenia podwójnie niciowe DNA • Radiofarmaceutyk musi połączyć się z DNA, np. 125 I DNA prekursor. Sciana komórki Ściana jądra Przyłączenia do DNA zerwanie nici

Emitery a • 211 At • • otrzymywany w cyklotronie 209 Bi + a 211 At + 2 n 212 Bi, 213 Bi otrzymane z generatorów • Bardzo duży efekt terapeutyczny

Emitery b Grupa 3 + lantanowce oraz 105 Rh, 186, 188 Re Zasięg od 1 do 12 mm
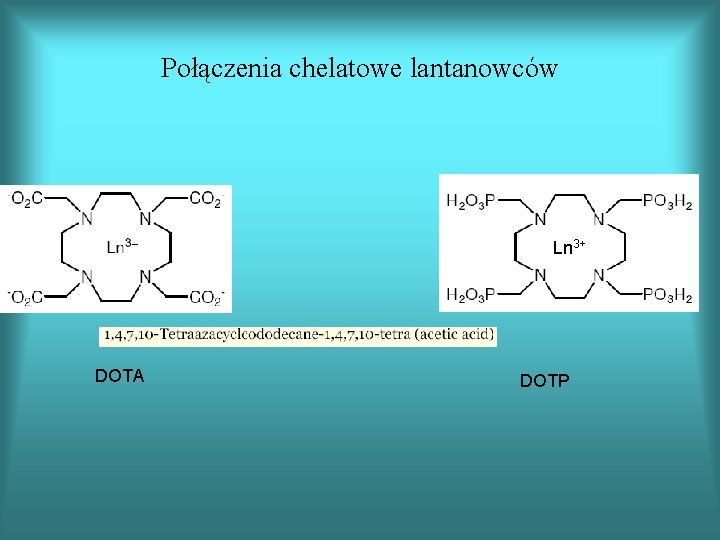
Połączenia chelatowe lantanowców Ln 3+ DOTA DOTP
![Radionuklidy w formie prostych jonów • 131 I – terapia tarczycy, • [32 P]PO Radionuklidy w formie prostych jonów • 131 I – terapia tarczycy, • [32 P]PO](http://slidetodoc.com/presentation_image_h/ec21cf035eca768da5dbd5464de003cb/image-38.jpg)
Radionuklidy w formie prostych jonów • 131 I – terapia tarczycy, • [32 P]PO 4 -, [89 Sr]Sr 2+, [90 Y]Y 3+, terapia kości • Radionuklidy wbudowują się w strukturę hydroksyapatytów Ca 10(PO 4)6(OH)2
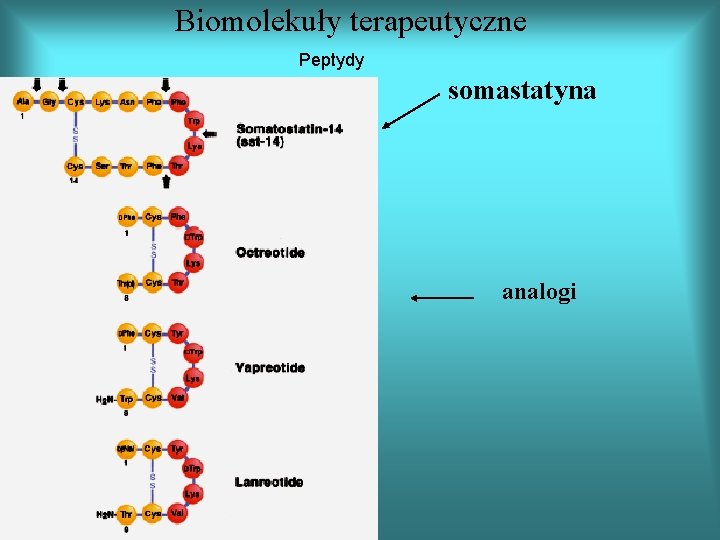
Biomolekuły terapeutyczne Peptydy somastatyna analogi
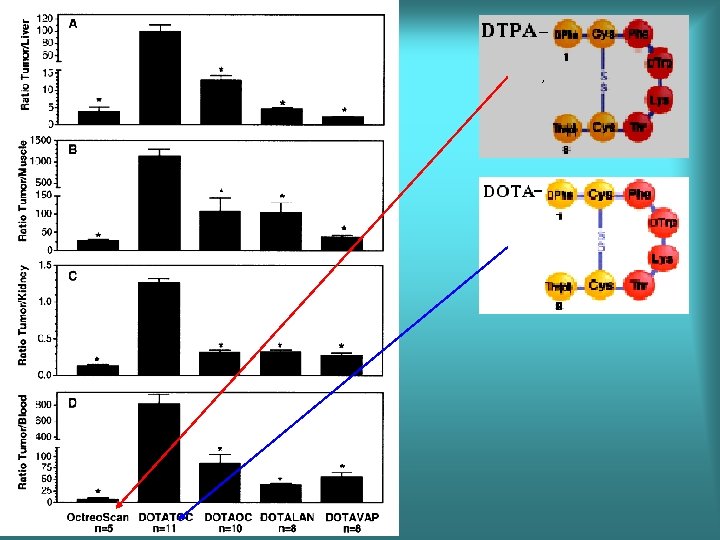
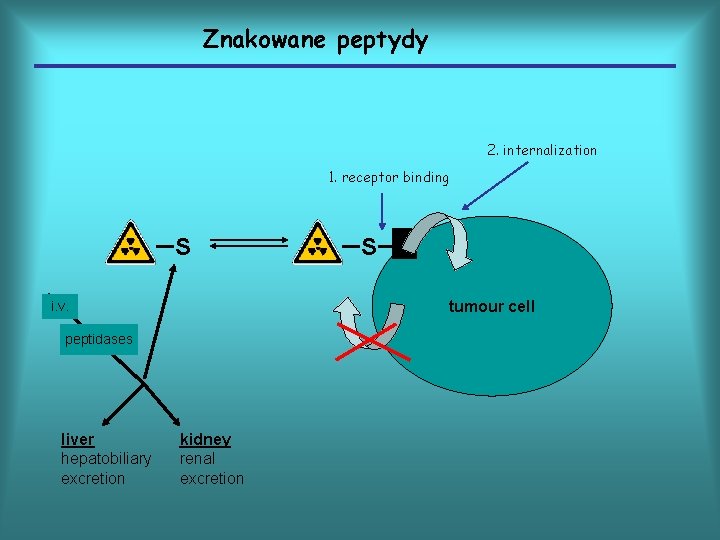
Znakowane peptydy 2. internalization 1. receptor binding S tumour cell i. v. peptidases liver hepatobiliary excretion S kidney renal excretion
Przeciwcialo monoklonalne z przyczepionym radioizotopem

Terapia wychwytu neutronów Niektóre stabilne izotopy wykazują ogromny przekrój czynny dla neutronów. W medycynie znalazły zastosowanie dwa izotopy 10 B (przekrój czynny 3838 barnów) i 157 Gd (255000 barnów). Przeciwciała znakuje się tymi nuklidami i akumulują się one w chorej tkance. Następnie naświetla się organizm strumieniem neutronów o takiej wielkości aby głównie były pochłaniane przez 10 B lub 157 Gd. Następują reakcje: Gd +n 158 Gd +g lub 157 Po pochłonięciu neutronu emitowana jest cząstka a i 7 Li o dużej sile niszczącej chore komórki lub wysoenergetyczny kwant g w przypadku 157 Gd. Metoda terapii 157 Gd może być połączona z obrazowaniem NMR co zwiększa jej efektywność.
- Slides: 43









![Complexes of the type [m(aa)3]±n show Complexes of the type [m(aa)3]±n show](https://slidetodoc.com/wp-content/uploads/2020/12/3015715_d8412bc28f0c7b6a8c2ea3744ce60d97-300x225.jpg)