Spectroscopy of Proteins Proteins The final product of





- Slides: 26

Spectroscopy of Proteins

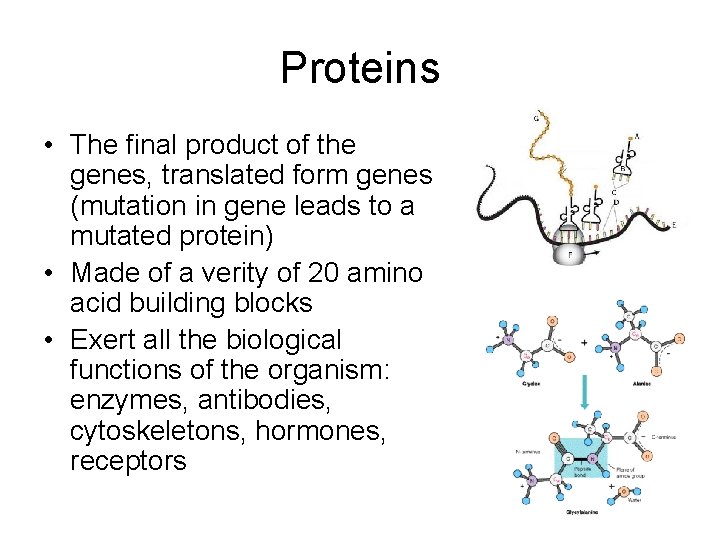
Proteins • The final product of the genes, translated form genes (mutation in gene leads to a mutated protein) • Made of a verity of 20 amino acid building blocks • Exert all the biological functions of the organism: enzymes, antibodies, cytoskeletons, hormones, receptors

Protein characteristics • Unbranched polymer • Folds into an accurate three dimensional structure (globular structure) • Correct folding is essential for the protein to exert its functions- tight structure-function relationship

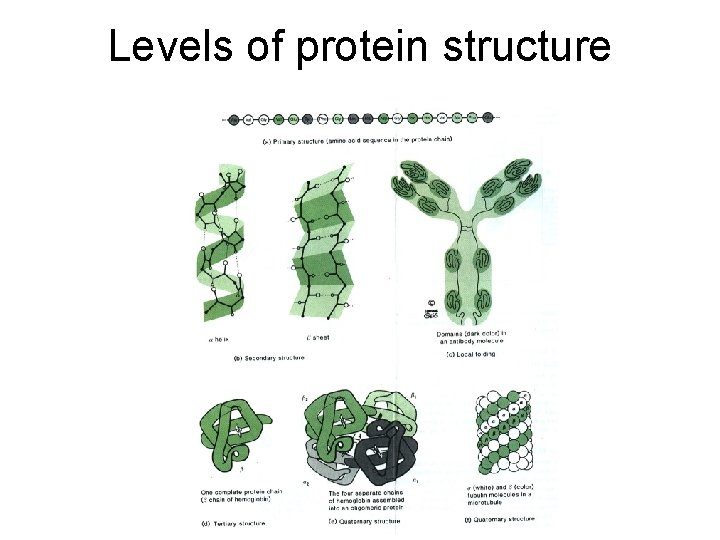
Levels of protein structure

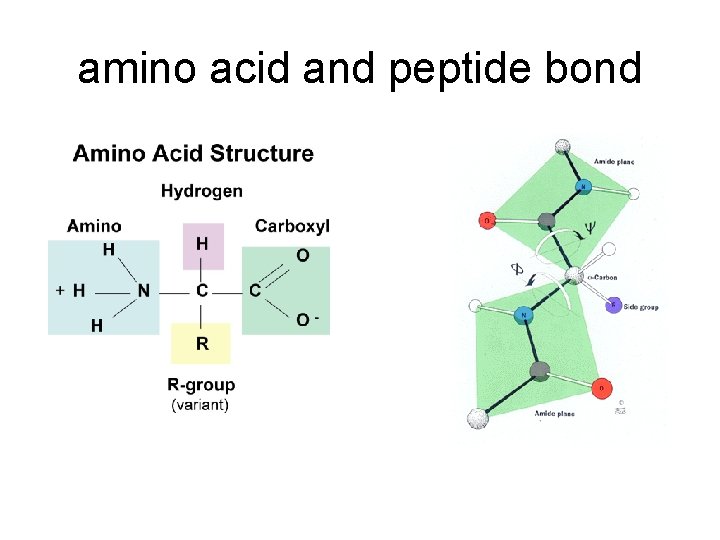
amino acid and peptide bond

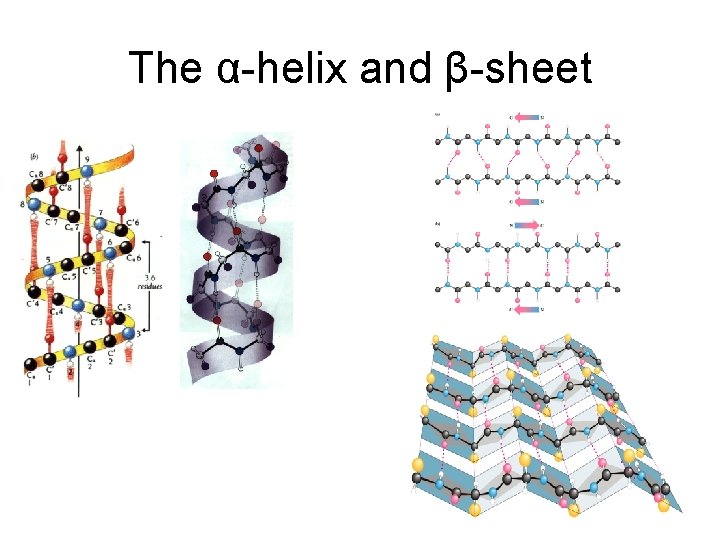
The α-helix and β-sheet

? Protein spectroscopy- what for • Structural analysis- Shape, size and formsecondary and tertiary conforamtions • quantification • Interaction with other molecules (proteins, ligands and solutes).

Spectroscopic methods • • • Absorbance- UV-vis, FTIR Circular Dichroism (CD) Fluorescence- internal, labeling, polarization Light scattering- DLS, SAXS NMR X-ray diffraction (crystallography) Resolution of Structural analysis methods • Low: UV-vis absorbance, DLS, fluorescence • Medium: FTIR, CD, SAXS • High: X-ray diffraction, NMR

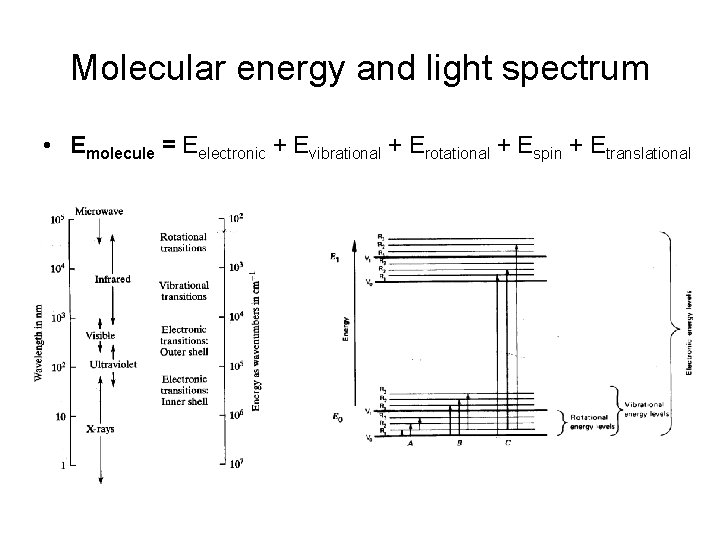
Molecular energy and light spectrum • Emolecule = Eelectronic + Evibrational + Erotational + Espin + Etranslational

Absorbance (and transmittance) Beer-Lambert’s law Chromophors in proteins • Peptidic bond (UV-CD and FTIR) • Aromatic amino acids (260 -300 nm) • Attached probe (varies, mostly vis)

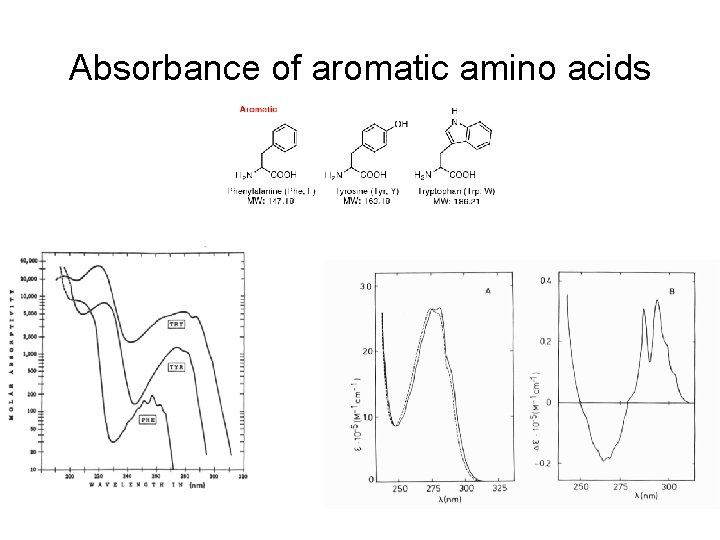
Absorbance of aromatic amino acids

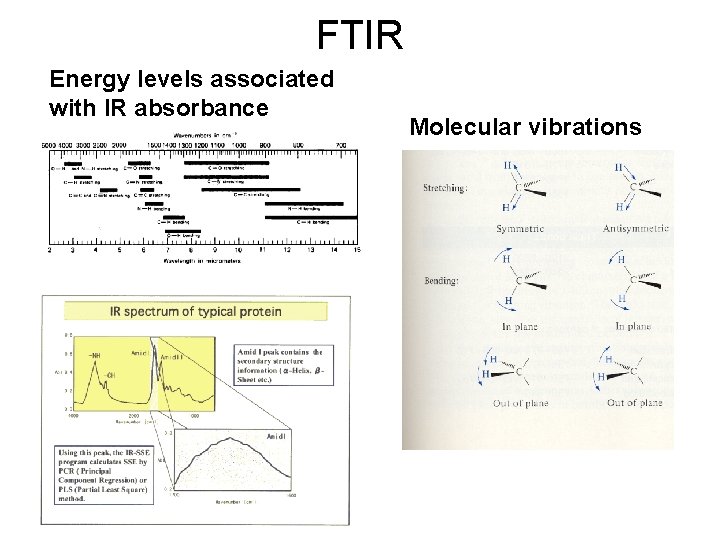
FTIR Energy levels associated with IR absorbance Molecular vibrations

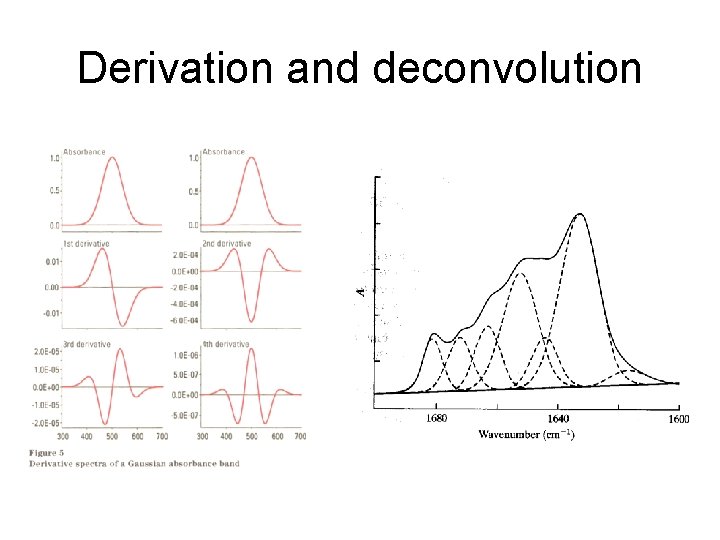
Derivation and deconvolution

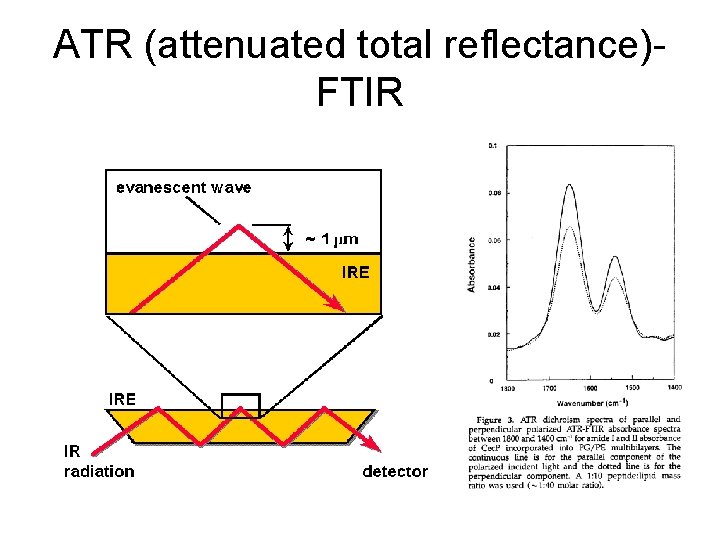
ATR (attenuated total reflectance)FTIR

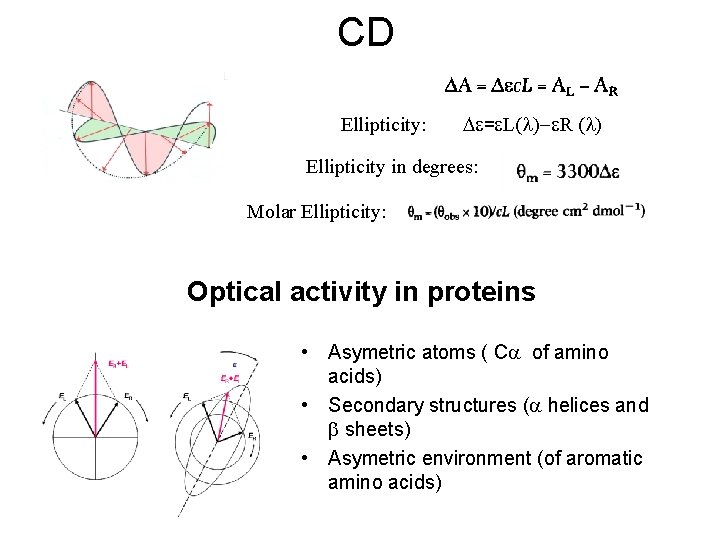
CD Ellipticity: = L(l)- R (l) Ellipticity in degrees: Molar Ellipticity: Optical activity in proteins • Asymetric atoms ( C of amino acids) • Secondary structures ( helices and sheets) • Asymetric environment (of aromatic amino acids)

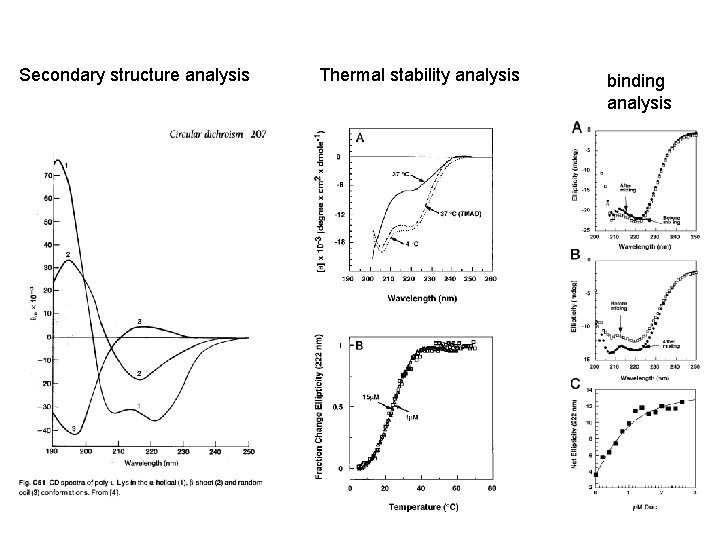
Secondary structure analysis Thermal stability analysis binding analysis

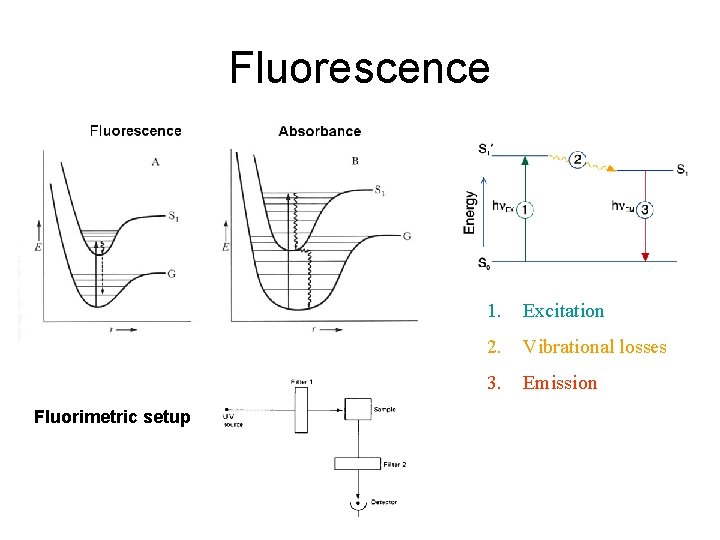
Fluorescence Fluorimetric setup 1. Excitation 2. Vibrational losses 3. Emission

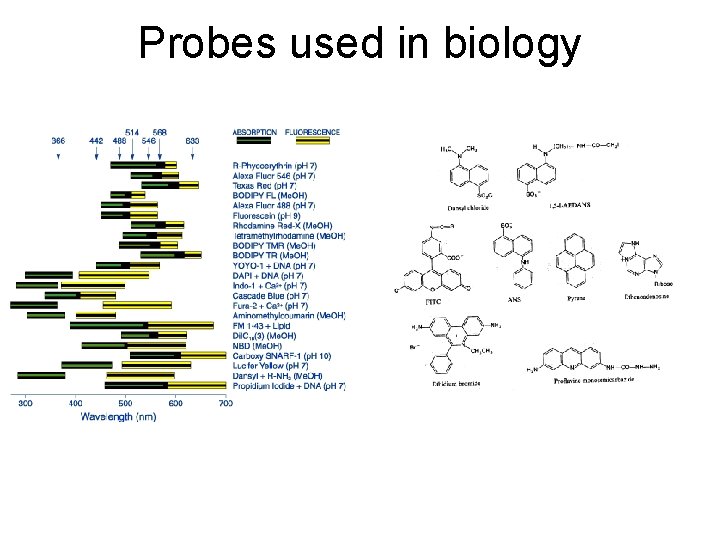
Probes used in biology

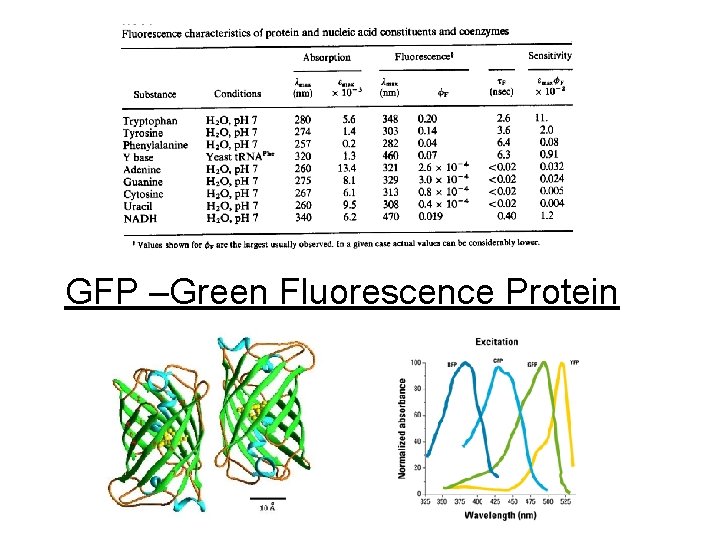
GFP –Green Fluorescence Protein

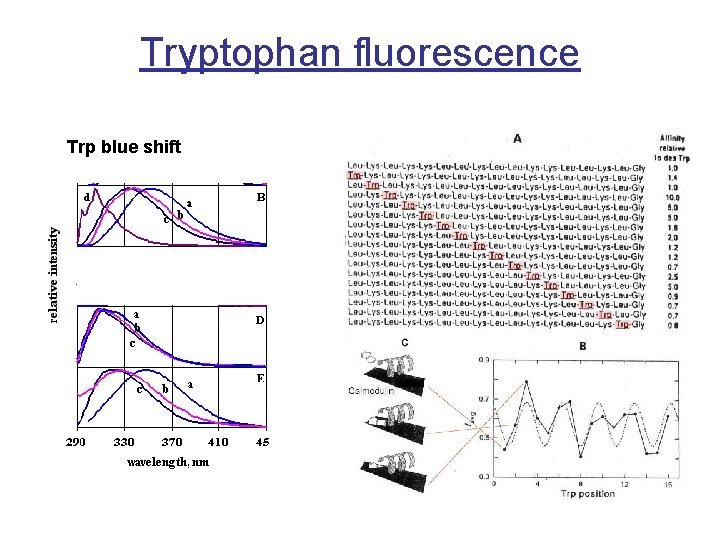
Tryptophan fluorescence Trp blue shift

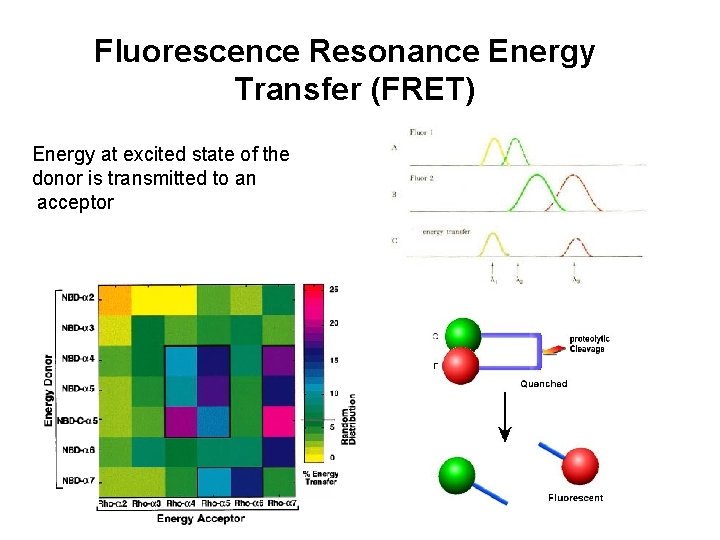
Fluorescence Resonance Energy Transfer (FRET) Energy at excited state of the donor is transmitted to an acceptor

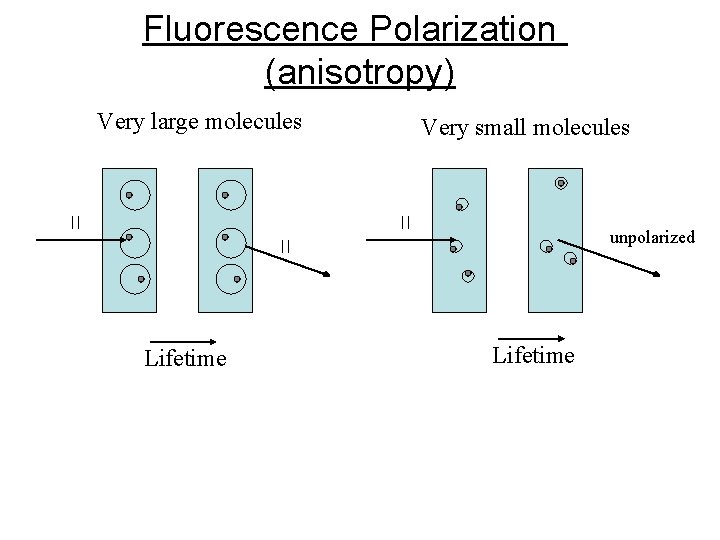
Fluorescence Polarization (anisotropy) Very large molecules Very small molecules unpolarized Lifetime

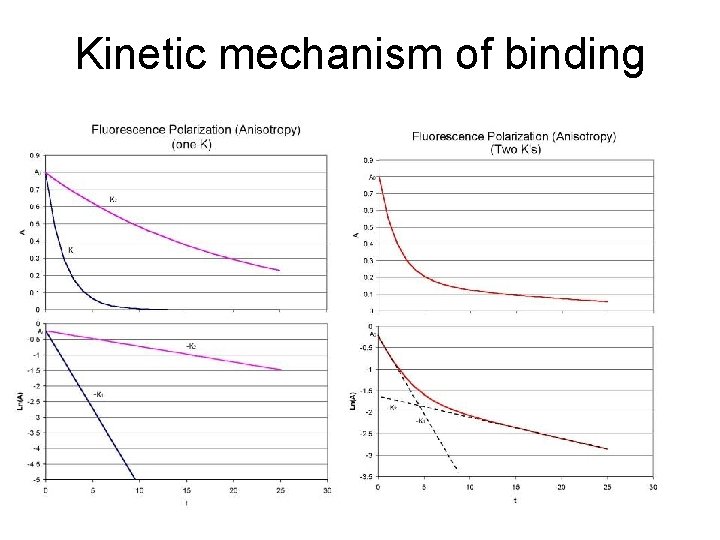
Kinetic mechanism of binding

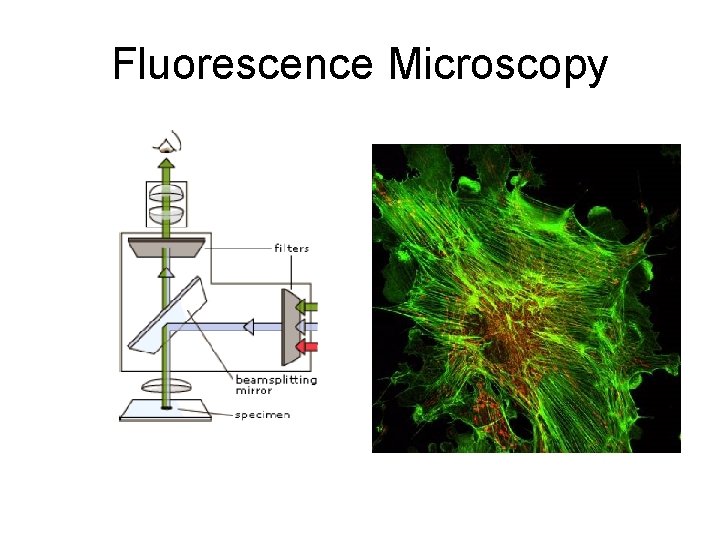
Fluorescence Microscopy

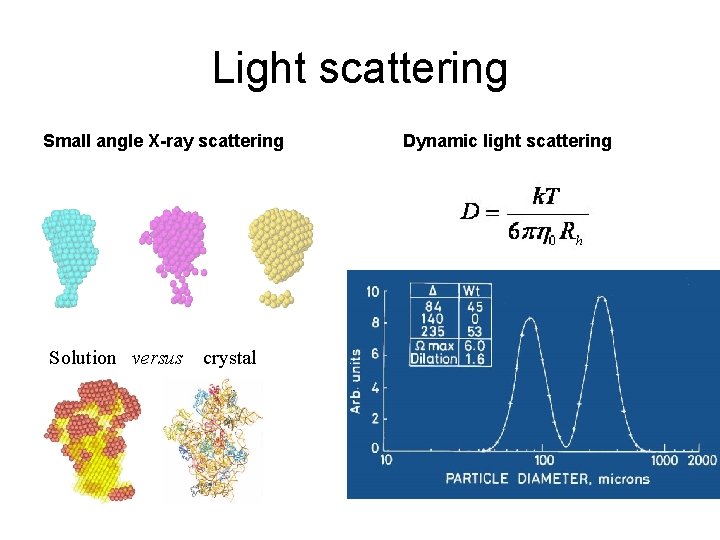
Light scattering Small angle X-ray scattering Solution versus crystal Dynamic light scattering

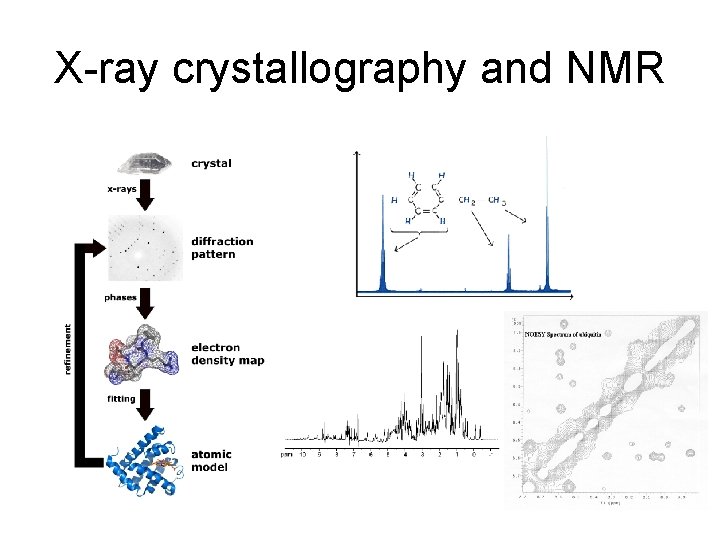
X-ray crystallography and NMR