QUMICA DESCRITIVA Parte I Composio Qumica da Terra



























- Slides: 39

QUÍMICA DESCRITIVA

Parte I Composição Química da Terra

Parte I - Composição Química da Terra Atmosfera Litosfera Hidrosfera

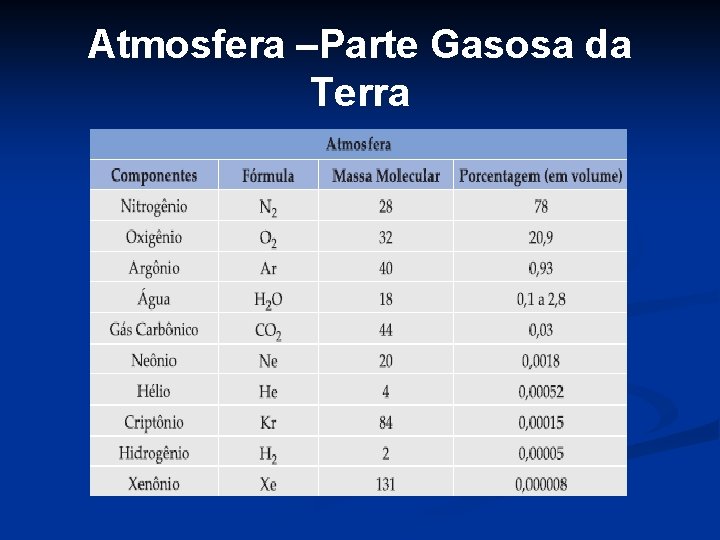
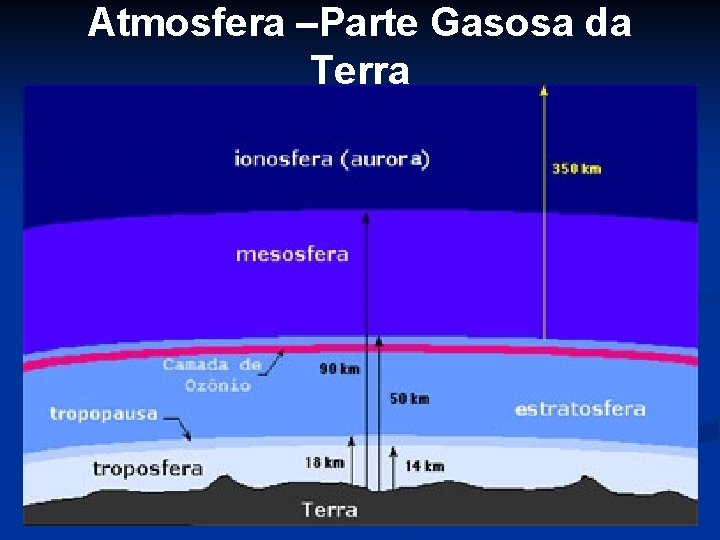
Atmosfera –Parte Gasosa da Terra

Atmosfera –Parte Gasosa da Terra

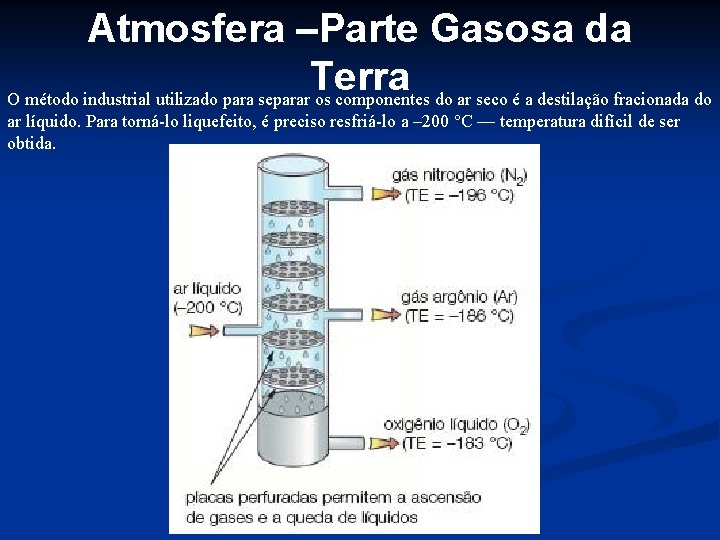
Atmosfera –Parte Gasosa da Terra O método industrial utilizado para separar os componentes do ar seco é a destilação fracionada do ar líquido. Para torná-lo liquefeito, é preciso resfriá-lo a – 200 °C — temperatura difícil de ser obtida.

Atmosfera –Parte Gasosa da Terra Usos de alguns gases purificados da atmosfera: O 2 - alimentação de combustão (queima), aparelhos de respiração artificial, produção de aço; N 2 - produção de amônia, ácido nítrico e fertilizantes; Ar - preenchimento de lâmpadas de filamento.

Litosfera – Parte Sólida da Terra n n n Elementos mais comuns na crosta terrestre (porcentagem em massa) O > Si > Al > Fe> Ca Minerais: são substâncias de origem inorgânica e natural que ocorrem na natureza no estado sólido, com uma composição química definida e uma estrutura interna de átomos na forma de arranjo geométrico. Apresentam-se geralmente na forma de cristais. Rochas: São agregados de minerais que formam toda a crosta terrestre e as partes mais profundas do planeta (com exceção do núcleo externo, que é a única parte líquida existente no interior da Terra).

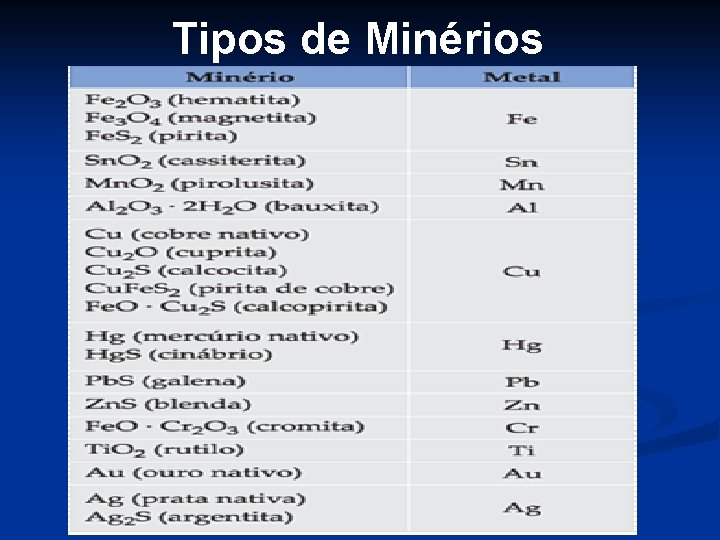
Tipos de Minérios

Litosfera – Parte Sólida da Terra HEMATITA MAGNETITA

Litosfera – Parte Sólida da Terra PIRITA BLENDA

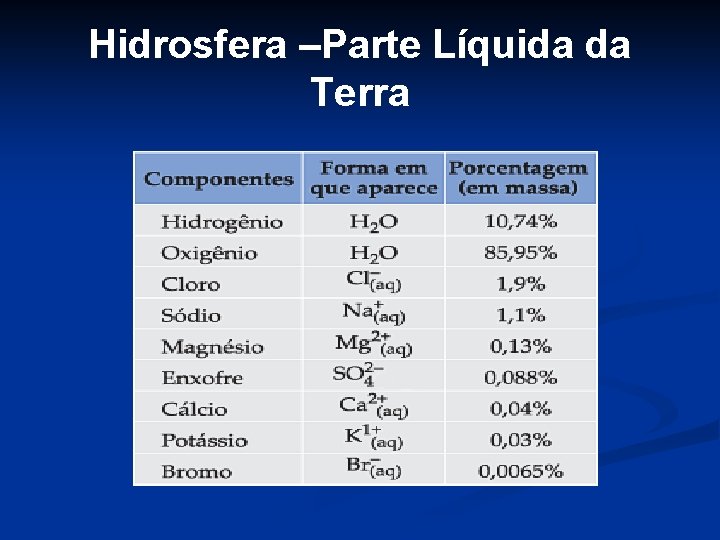
Hidrosfera –Parte Líquida da Terra

Parte II – Obtenção de substâncias

Metais

Metais Família 1 A - Grupo 1 – Metais alcalinos. Césio Sódio Potássio Lítio

Metais Família 1 A - Grupo 1 – Metais alcalinos. Os metais alcalinos apresentam alta reatividade (potencial de oxidação) e, portanto, na natureza são encontrados na forma de cátions monovalentes: Li + , Na + , K + , Rb + , Cs +

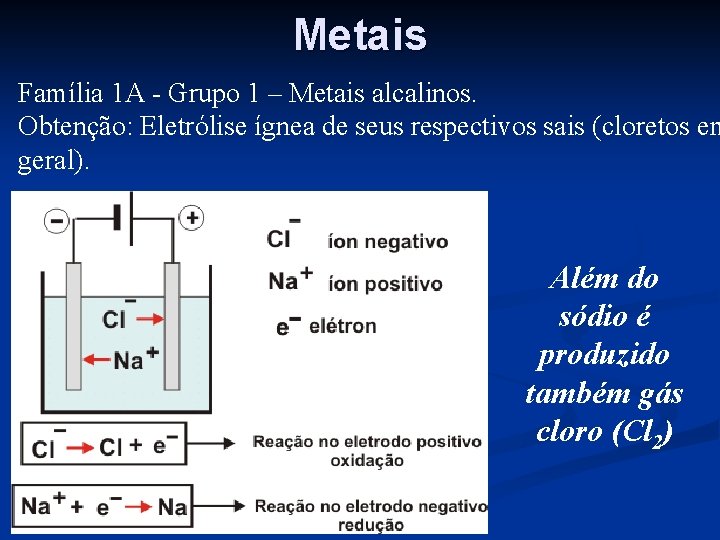
Metais Família 1 A - Grupo 1 – Metais alcalinos. Obtenção: Eletrólise ígnea de seus respectivos sais (cloretos em geral). Além do sódio é produzido também gás cloro (Cl 2)

Metais Família 2 A - Grupo 2 – Metais alcalino-terrosos Assim como os metais do grupo 1, também são reativos. Magnésio Bário

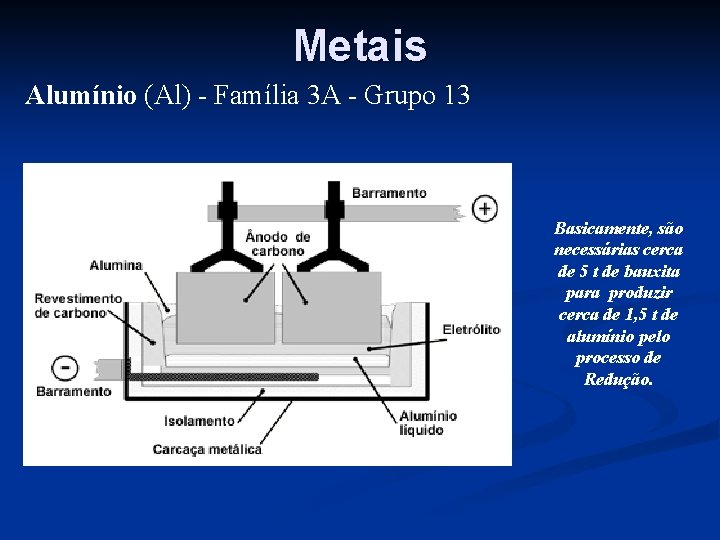
Metais Alumínio (Al) - Família 3 A - Grupo 13

Metais Alumínio (Al) - Família 3 A - Grupo 13 Devido sua relativa eletropositividade encontra-se na natureza em sua forma oxidada (Al+3 ). Fonte principal de obtenção – Bauxita A produção de bauxita brasileira concentra-se nos Estados do Para e Minas Gerais cujas reservas totais são de aproximadamente 11% das reservas mundiais O Brasil é a terceira reserva mundial de bauxita.

Metais Alumínio (Al) - Família 3 A - Grupo 13 Obtenção do Alumínio – Eletrólise ígnea do óxido de alumínio (Al 2 O 3).

Metais Alumínio (Al) - Família 3 A - Grupo 13 Basicamente, são necessárias cerca de 5 t de bauxita para produzir cerca de 1, 5 t de alumínio pelo processo de Redução.

Metais Reações envolvidas na produção do alumínio: Dissolução do óxido em criolita: Al 2 O 3 => 2 Al 3+ + 3 O 2 Em meio fortemente básico (Na. OH) No pólo negativo: 4 Al 3+ + 12 e- => 4 Al 0 No pólo positivo: 6 O 2 - => 3 O 2 + 12 e. Equação global: 2 Al 2 O 3 => 4 Al 3+ + 6 O 2 - Al 3+ + 12 e- => 4 Al 0 6 O 2 - => 3 O 2 + 12 e 2 Al 2 O 3 => 4 Al 0 + 3 O 2

Metais Ferro (Fe) – Metal de transição – Grupo 8 Ocorre na natureza na suas formas oxidadas (Fe+2 , Fe+3 ). As principais matérias primas são a hematita (Fe 2 O 3), magnetita (Fe 3 O 4) e a pirita (Fe. S). HEMATITA MAGNETITA

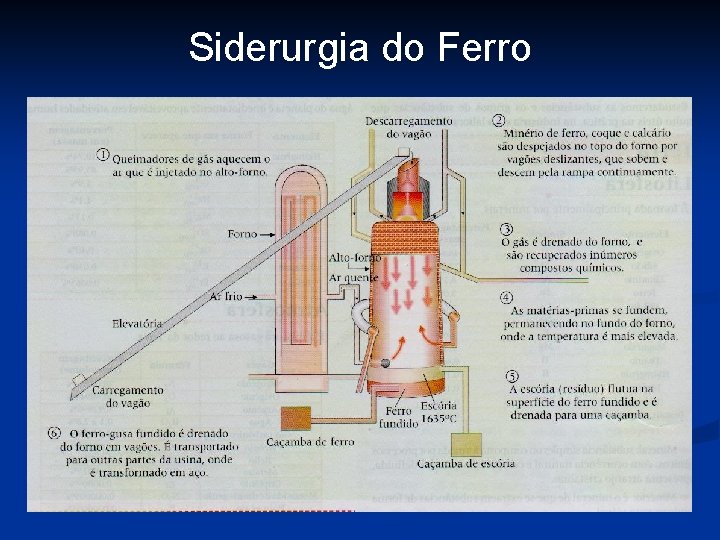
Siderurgia do Ferro

Siderurgia do Ferro Alto forno utilizado para siderurgia do ferro em Volta Redonda - RJ (CSN)

Reações ocorridas na obtenção do Fe Se o minério for Fe 2 O 3, ele é reduzido pelo CO a Fe 3 O 4 na parte superior do forno (300 °C). CO(g) + 3 Fe 2 O 3 (s) 2 Fe 3 O 4 (s) + CO 2(g) O Fe 3 O 4 vai aos poucos descendo para a parte inferior do forno onde é reduzido a Fe. O (600 °C) por diferença de densidade. CO(g) + Fe 3 O 4 (s) 3 Fe. O(s) + CO 2(g) Na parte mais baixa do forno, Fe. O é reduzido a ferro (Fe) (de 800 a 1600 °C). CO(g) + Fe. O(s) Fe(l) + CO 2(g)

Ferro como matéria prima do aço

Ferro como matéria prima do aço

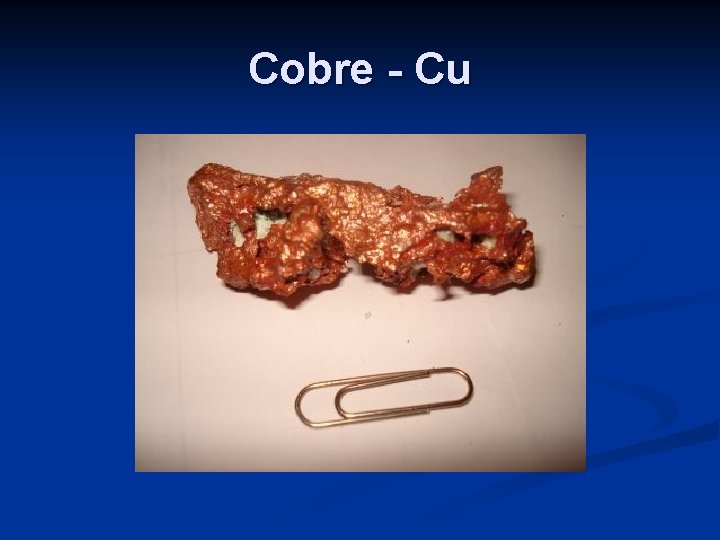
Cobre - Cu

Cobre - Cu

Ametais

Oxigênio – O 2 O oxigênio líquido é obtido à temperatura inferior a – 180º C.

Oxigênio– O 2 Gás incolor, inodoro usado comburente (substância que alimenta as combustões). Ocorre livre na atmosfera, combinado com hidrogênio na hidrosfera e na forma de diversos óxidos , sulfatos , fosfatos e outros compostos de diferentes elementos na crosta terrestre.

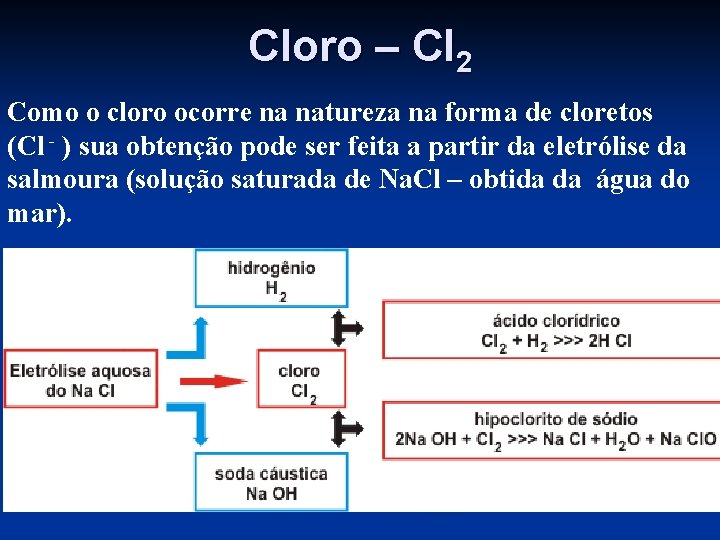
Cloro – Cl 2 Nas condições ambientes o cloro encontra-se na forma de um gás amarelo - esverdeado, de odor fortemente irritante e altamente tóxico.

Cloro – Cl 2 Como o cloro ocorre na natureza na forma de cloretos (Cl - ) sua obtenção pode ser feita a partir da eletrólise da salmoura (solução saturada de Na. Cl – obtida da água do mar).

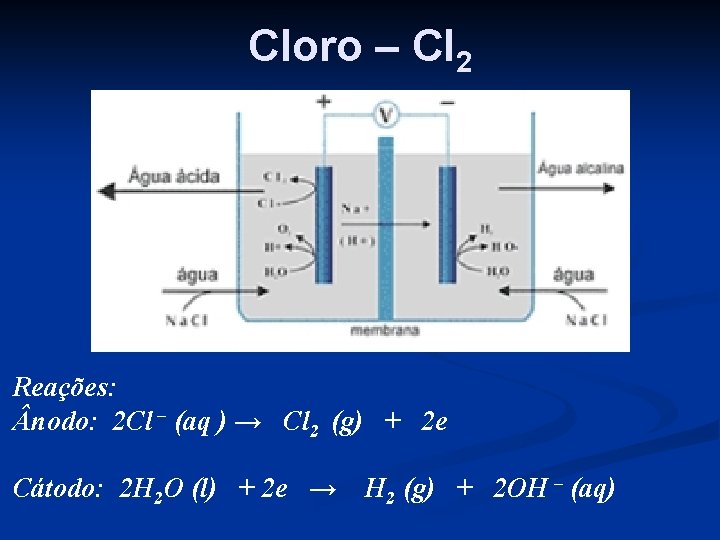
Cloro – Cl 2 Reações: nodo: 2 Cl – (aq ) → Cl 2 (g) + 2 e Cátodo: 2 H 2 O (l) + 2 e → H 2 (g) + 2 OH – (aq)

Bromo e Iodo O bromo é um líquido avermelhado relativamente volátil, enquanto que o iodo é um sólido púrpura que sublima em condições ambiente.

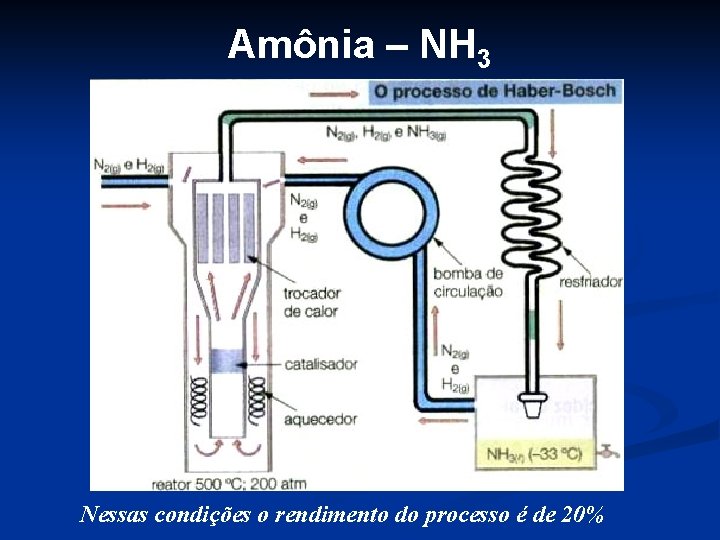
Amônia – NH 3 Nessas condições o rendimento do processo é de 20%