MATEREI SELANJUTNYA KIMIA TANAH KIMIA TANAH TIU Setelah







































- Slides: 50

MATEREI SELANJUTNYA KIMIA TANAH

KIMIA TANAH TIU : Setelah mempelajari Materi Sifat Kimia Tanah, mahasiswa diharapkan mampu memahami dan menjelaskan sifat kimia tanah, yang meliputi : (a) dasar jerapan dalam tanah, (b) koloid tanah, (c) kapasitas tukar kation, (d) kejenuhan basa, (e) reaksi tanah (p. H), (f) pengaruh reaksi tanah pada pertumbuhan dan perkembangan tanaman, dan (g) mengubah p. H tanah

• Komponen kimia tanah mempengaruhi sifat dan ciri tanah (umumnya) dan kesuburan tanah (khususnya)

DASAR-DASAR JERAPAN KATION • Fenomena jerapan (adsorpsi) dan pertukaran ion ditemukan pertama kali oleh Thomas Way (1852) - Bau tidak sedap dari pupuk kandang bisa hilang jika dicampur dengan tanah - Kehilangan amonia dari pupuk kandang dapat dikurangi bila dicampur dengan tanah • Timbul pertanyaan : Bahan apa dari tanah yang dapat menjerap amonia tsb? • Bahan aktif dari tanah yang dapat menjerap dan mempertukarkan ion adalah bahan yang berada dalam bentuk koloidal, yaitu liat dan bahan organik

Dua bahan penting yang diabsorbsi tanaman dipindahkan dari tanah adalah air dan unsur hara. Tanaman dapat mengalami defisiensi unsur essensial, bila : 1. Unsur tidak terdapat di dalam tanah 2. Terdapat dalam kuantitas yang besar dalam tanah, tetapi sangat sedikit terlarut atau tersedia untuk menopang kebutuhan tanaman. 1. Koloid Tanah Koloid tanah adalah bahan mineral dan bahan organik yang sangat halus sehingga mempunyai luas permukaan yang sangat tinggi persatuan berat (massa).

Koloid tanah yang berperan yaitu koloid anorganik (koloid liat atau mineral) dan koloid organik (humus). Kedua koloid ini mempunyai sifat dan ciri yang jauh berbeda. Menurut Brady (1974), bahwa koloid berukuran < 1 sehingga tidak semua fraksi liat termasuk koloid. Koloid merupakan bagian tanah yang sangat aktif dalam reaksi-reaksi fisikokimia di dalam tanah. Partikel-partikel koloid yang sangat halus yang disebut micell (microcell), umumnya bermuatan negatif, karena itu ion-ion bermuatan positif (kation) tertarik pada koloid tersebut sehingga terbentuk lapisan ganda ion. Bagian dalam dari lapisan ganda ion ini terdiri dari partikel koloid yang bermuatan negatif (anion) sedang bagian luar merupakan kumpulan kation yang tertarik oleh partikel-partikel koloid tersebut. 6

A. Koloid Liat Ukuran fraksi liat (mineral liat) adalah kurang dari 2 sedangkan liat yang bersifat koloid berukuran < 2 , berarti tidak semua fraksi liat dapat dikatakan koloid. Mineral liat dalam tanah terbentuk karena : 1. Rekristalisasi sintesis dari senyawa-senyawa hasil pelapukan mineral primer atau 2. Alterasi (perubahan) langsung dari mineral primer yang telah ada (misal mika menjadi ilit).

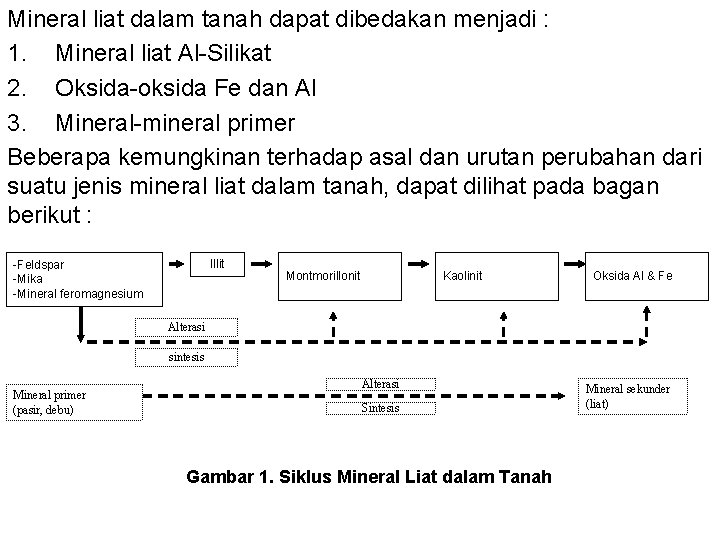
Mineral liat dalam tanah dapat dibedakan menjadi : 1. Mineral liat Al-Silikat 2. Oksida-oksida Fe dan Al 3. Mineral-mineral primer Beberapa kemungkinan terhadap asal dan urutan perubahan dari suatu jenis mineral liat dalam tanah, dapat dilihat pada bagan berikut : Illit -Feldspar -Mika -Mineral feromagnesium Montmorillonit Kaolinit Oksida Al & Fe Alterasi sintesis Mineral primer (pasir, debu) Alterasi Sintesis Gambar 1. Siklus Mineral Liat dalam Tanah Mineral sekunder (liat)

• Mineral liat Al-silikat : Mineral liat Al-silikat dapat dibedakan menjadi : a. Mineral liat Al-silikat yang mempunyai bentuk kristal yang baik (kristalin) misalnya kaolinit, haloisit, montmorilonit dan Illit. b. Mineral liat Al-silikat amorf. Misalnya alofon, yang banyak ditemukan pada tanah yang berasal dari abu volkan seperti tanah Andisols. Mineral liat Al-silikat mempunyai struktur berlapis, setiap unit terdiri dari lapisan Si-tetrahedron dan Al-oktahedron. Berdasarkan atas banyaknya lapisan Si-tetrahedron dan Al-oktahedron dalam setiap unit mineral, maka mineral liat silikat dibedakan menjadi :

• Mineral liat 1 : 1 • Mineral liat 2 : 2 Mineral liat 1 : 1 adalah mineral liat dimana setiap unitnya terdiri dari satu lapis Si-tetrahedron dan satu lapis Al-oktahedron Mineral liat 2 : 1 adalah mineral liat dimana setiap unitnya terdiri dari dua lapis Si-tetrahedron yang mengapit satu lapis Al-oktahedron Mineral liat 2 : 2 adalah mineral liat dimana setiap unitnya terdiri dari dua lapis Si-tetrahedron dan dua lapis Al-oktahedron yang letaknya berselangseling.

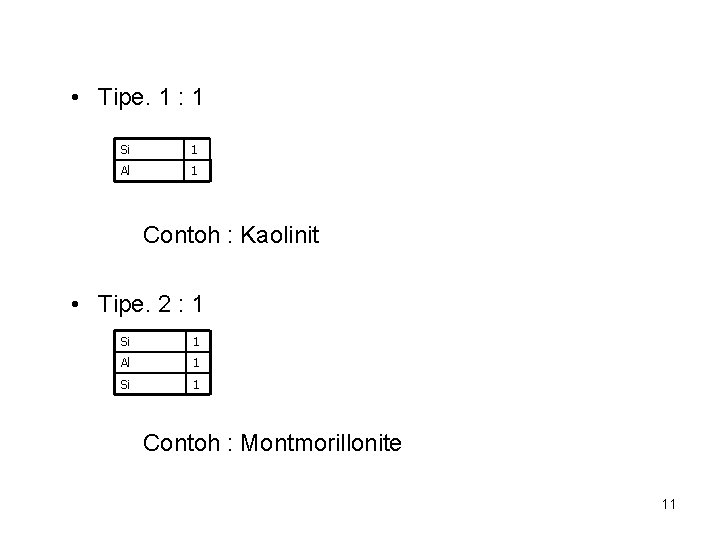
• Tipe. 1 : 1 Si 1 Al 1 Contoh : Kaolinit • Tipe. 2 : 1 Si 1 Al 1 Si 1 Contoh : Montmorillonite 11

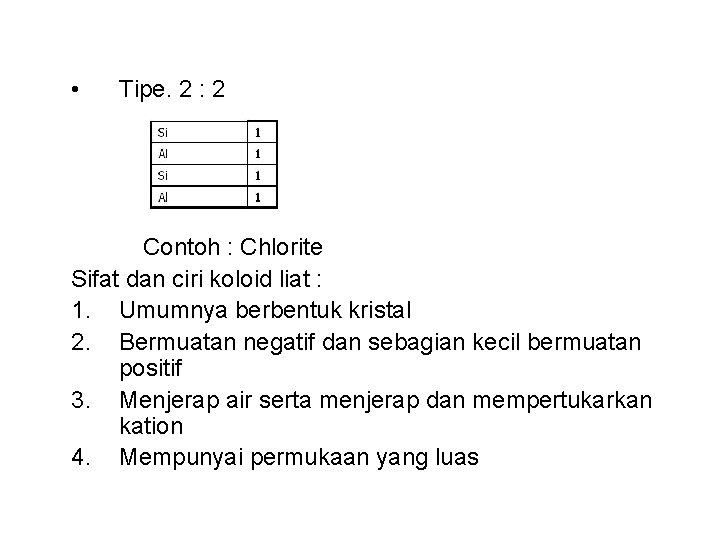
• Tipe. 2 : 2 Contoh : Chlorite Sifat dan ciri koloid liat : 1. Umumnya berbentuk kristal 2. Bermuatan negatif dan sebagian kecil bermuatan positif 3. Menjerap air serta menjerap dan mempertukarkan kation 4. Mempunyai permukaan yang luas

Adanya muatan negatif pada liat silikat disebabkan oleh beberapa hal (Brady, 1974) ; 1. Kelebihan muatan negatif pada ujung-ujung patahan kristal baik pada Si-tetrahedron maupun Al-oktahedron 2. Disosiasi H+ dari gugus OH yang terdapat pada tepi atau ujung kristal -OH+ -O+H+ Pada p. H rendah (masam) ion H+ terikat erat tetapi bila p. H Naik, ion H menjadi mudah lepas sehingga muatan negatif meningkat, muatan ini disebut muatan tergantung p. H.

3. Subtitusi Isomorfik, yaitu penggantian kation struktur oleh dalam kristal dalam struktur kristal oleh kation lain yang mempunyai ukuran yang sama dengan muatan (valensi) berbeda. Pada umumnya kation yang menggantikan mempunyai valensi lebih rendah daripada yang digantikan, misalnya Mg 2+ menggantikan Al 3+ dalam Al-oktahedron atau Al 3+ menggantikan Si 4+ dalam Sitetrahedron, sehingga terjadi kelebihan muatan negatif pada liat.

SIFAT DAN CIRI KOLOID LIAT 1. Umumnya berbentuk kristal 2. Mudah mengalami substitusi isomorfik 3. Bermuatan negatif umumnya 4. Sebagian kecil bermuatan positif 5. Menjerap air 6. Menjerap dan mempertukarkan kation 7. Mempunyai permukaan yang luas 8. Merupakan suatu garam yang bersifat masam

B. Koloid organik Bahan organik yang bersifat koloid adalah humus Koloid humus seperti halnya koloid liat bermuatan negatif. Perbedaan utama dari koloid organik dengan koloid anorganik adalah bahwa humus tersusun dari: C, H dan O; sedangkan liat tersusun dari : Al, Si, dan O. Humus bersifat amorft, mempunyai KTK yang lebih tinggi dari mineral liat, sumber muatan negatif ini diduga berasal dari karboksil (-COOH) dan Fenolik ( --OH). Muatan dalam humus adalah muatan tergantung p. H, dalam keadaan masam H+ diikat kuat dalam gugus karboksil atau phenol, tetapi ikatan tersebut menjadi lemah apabila p. H menjadi lebih tinggi, akibatnya disosialisasi H+ meningkat dengan naiknya p. H tanah,

sehingga muatan negatif dalam koloid humus yang dihasilkan meningkat pula. Humus diperkirakan disusun oleh 3 jenis bagian utama yaitu: 1. warna terang, larut dalam asam maupun alkali, serta aktif dalam reaksi kimia. 2. tidak terlalu terang dan tidak terlalu gelap, larut dalam alkali tetapi tidak dalam asam, aktif dalam reaksi kimia. 3. paling kelam, tidak larut baik dalam asam maupun alkali, tidak aktif dalam reaksi kimia.

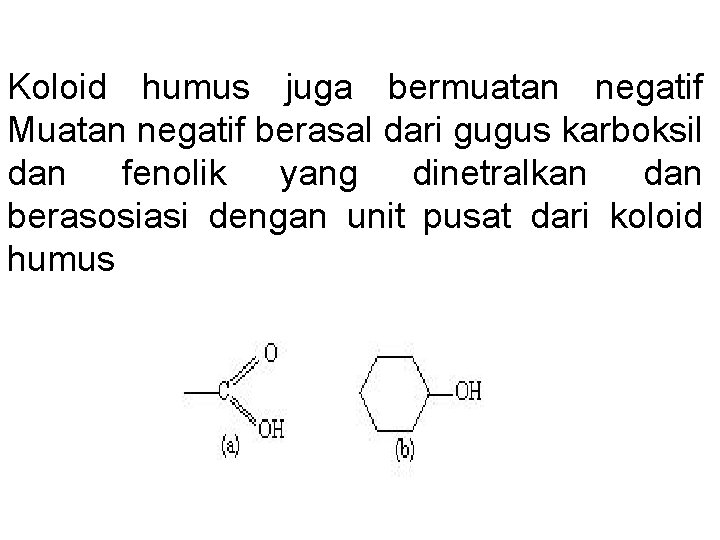
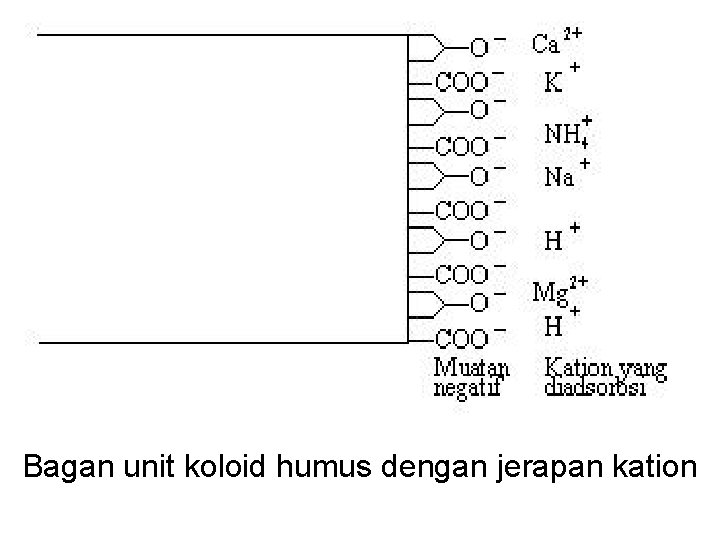
Koloid humus juga bermuatan negatif Muatan negatif berasal dari gugus karboksil dan fenolik yang dinetralkan dan berasosiasi dengan unit pusat dari koloid humus

Bagan unit koloid humus dengan jerapan kation

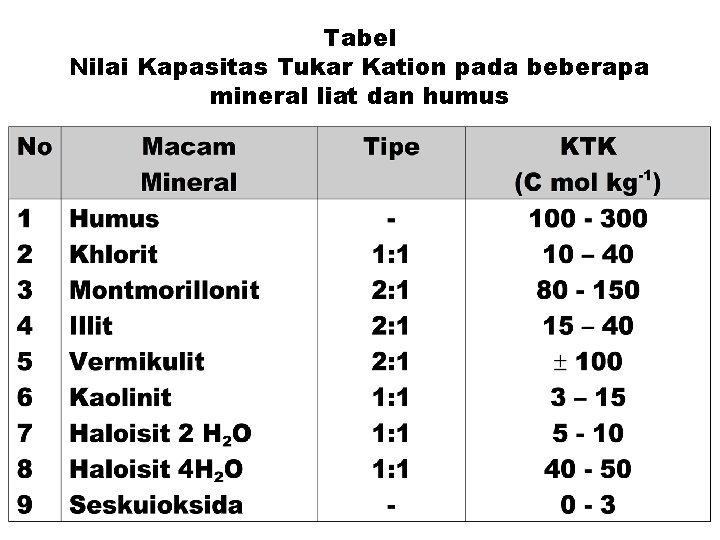
2. Kapasitas Tukar Kation (KTK) • KTK tanah adalah suatu kemampuan koloid tanah menjerap dan mempertukarkan kation. • KTK berbagai tanah sangat beragam, bahkan tanah sejenispun berbeda KTKnya • Besarnya KTK tanah dipengaruhi oleh sifat dan ciri tanah antara lain adalah : - Reaksi tanah atau p. H - Tekstur tanah atau jumlah liat - Jenis mineral liat - Bahan organik - Pengapuran dan pemupukan

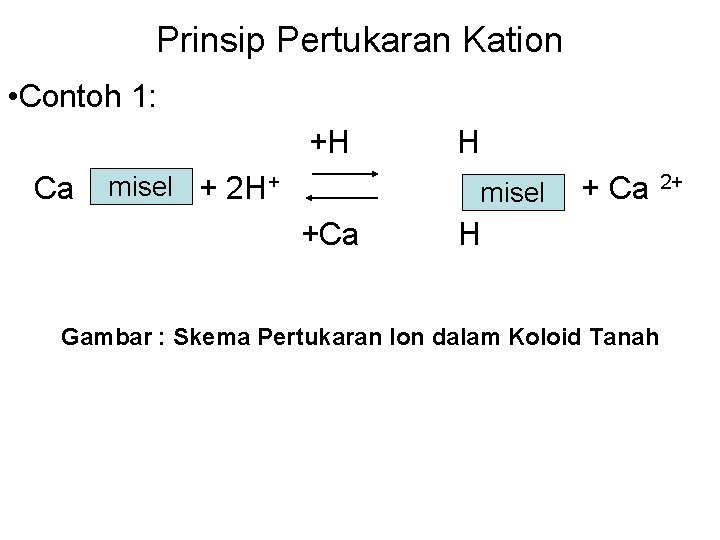
Prinsip Pertukaran Kation • Contoh 1: +H Ca misel + 2 H+ H misel +Ca + Ca H Gambar : Skema Pertukaran Ion dalam Koloid Tanah 2+

• Reaksi diatas terjadi pada tanah mineral dilapisan olah yang banyak Ca terjerap dan berada di daerah humid. • Sejumlah asam karbonat dan asam lainnya dibentuk bersamaan dengan proses dekomposisi bahan organik • Ion H yang terbentuk mulai menggantikan ion Ca yang berada pada kompleks jerapan. Pertukaran ini terjadi sebagai akibat aksi massa, disamping itu juga karena ion H dijerap lebih kuat oleh koloid tanah daripadaion Ca • Pertukaran ion Ca dengan H berlangsung secara ekuivalen. Apabila terjadi penurunan ion H atau penambahan ion Ca , reaksi akan beralih kekiri. Sebaliknya jika H bertambah, atau ion ca berkurang, reaksi akan berali kekanan

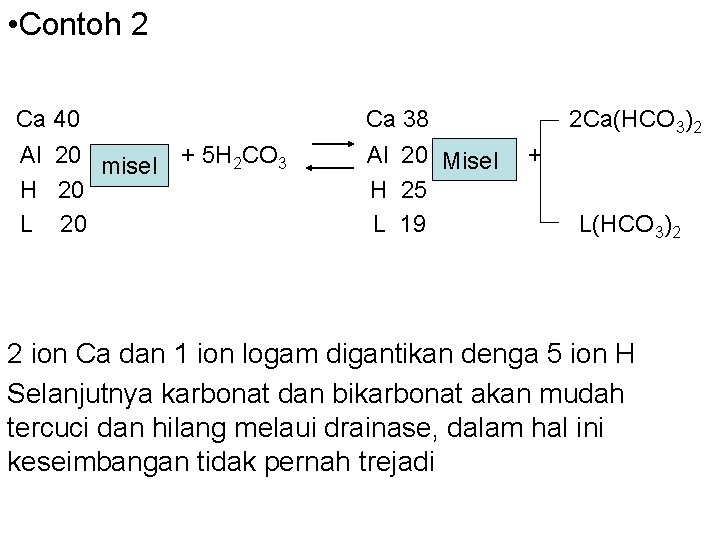
• Contoh 2 Ca 40 Al 20 misel H 20 L 20 Ca 38 + 5 H 2 CO 3 Al 20 Misel H 25 L 19 2 Ca(HCO 3)2 + L(HCO 3)2 2 ion Ca dan 1 ion logam digantikan denga 5 ion H Selanjutnya karbonat dan bikarbonat akan mudah tercuci dan hilang melaui drainase, dalam hal ini keseimbangan tidak pernah trejadi

• p. H mempunyai hubungan yang linier dengan KTK, p. H rendah (asam) KTK rendah sedangkan p. H Tanah tinggi (netral atau alkalis) KTK tanah akan tinggi • Tekstur tanah atau jumlah liat - KTK tanah berbanding lurus dengan jumlah butir liat - KTK berbanding terbalik dengan besar butir liat • Jenis mineral liat - Jenis koloid mempunyai muatan yang beragam, maka jenis koloid juga mempunyai KTK yang beragam

Tabel Nilai Kapasitas Tukar Kation pada beberapa mineral liat dan humus

• Bahan Organik - Bahan organik mempunyai daya jerap kationyang lebih besar daripada koloid liat - Makin tinggi kandungan bahan organik suatu tanah makin tinggi pula KTK • Pengapuran dan pemupukan - Pada tanah yang bermuatan tergantung p. H (montmorilonit atau koloid organik), maka KTK akan meningkat dengan pengapuran

• Besarnya KTK dinyatakan dengan satuan mili ekuivalen (me) yang berarti, satu mili ekuivalen adalah suatu jumlah yang setara dengan 1 mg hidrogen atau sejumlah ion lain yang dapat berkombinasi atau menggantikan ion hidrogen. • Jumlah atom dalam setiap ekuivalen adalah 6, 02 x 10 (bilangan avogadro). Dengan demikian 1 miliekuivalen setara dengan 1 mg hidrogen dan terdiri atas 6, 02 x 10 atom hidrogen. • Untuk memudahkan satuan ini digunakan yang dapat dirubah menjadi ppm. • Ekuivalen atau kesetaraan bobot suatu unsur adalah perbandingan antara berat molekul atau berat atom unsur tersebut dengan valensinya: me = BA/Valensi mg = (BA/V) x me ppm = me x 10


3. Kejenuhan Basa (KB) Kejenuhan basa merupakan perbandingan antara jumlah kation basa dengan semua kation (kation basa dan kation asam) yang terdapat dalam kompleks jerapan tanah. Jumlah maksimum kation yang dapat dijerap tanah menunjukan besarnya nilai kapasitas tukar kation tanah tersebut. me kation • % KB = x 100 % KTK • Bila % KB 40 artinya : 40/100 =2/5 bagian dari seluruh KTK ditempati oleh kation basa (Ca, Mg, K, Na) Kation Al 3+ dan H+ merupakan kation lain yang mudah terjerap, sedangkan kation lain kurang berarti Jadi tanah yang ber KB 40% artinya: 40% kation basa (Ca, Mg, K, Na) dan 60 % adalah Al 3+ dan H+, oleh karenanya p. Hnya rendah

• Contoh, Hasil analisis tanah diperoleh basa-basa dapat dipertukarkan (me/100 g) adalah sbb: Ca = 10, Mg = 5, K = 10 dan Na = 5 serta hasil pengukuran KTK tanah tersebut adalah 50 me/100 g. Kejenuhan basa tanah tersebut adalah: KB = ((10+5+10+5)/50) x 100 % = (30/50) x 100 % = 60%

• KB berhubungan erat dengan p. H tanah, dimana tanah-tanah dengan p. H rendah umumnya mempunyai KB rendah, sedangkan tanah-tanah dengan p. H tinggi mempunyai KB tinggi pula. • Hubungan p. H dengan KB pada p. H 5, 5 -6, 5 hampir merupakan suatu garis. • Tanah-tanah dengan KB rendah berarti komplek jerapan lebih banyak diisi oleh kation-kation asam yaitu H dan Al. • Tanah-tanah dengan KB yang sama dan komposisi mineral liat berlainan akan memberikan nilai p. H yang berbeda. Hal ini disebabkan oleh perbedaan derajat dissosiasi ion H yang dijerap pada permukaan koloid tanah. Ion H yang dijerap oleh komplek organik (humus) akan lebih mudah mengalami dissosiasi hingga p. H tanah organik dengan KB tertentu akan lebih rendah dari pada p. H tanah mineral dengan KB yang sama.

• KB selalu dihubungkan sebagai petunjuk mengenai kesuburan tanah. Kemudahan dalam melepaskan ion yang dapat diserap tanaman tergantung pada KB. • Tanah dapat digolongkan sangat subur bila mempunyai nilai KB > 80 %, tingkat kesuburan sedang jika KB 50 - 80 % dan tidak subur jika KB kurang dari 50%. • Hal ini didasarkan pada sifat tanah dengan kejenuhan basa 80 % akan mampu membebaskan kation basa dapat dipertukarkan untuk tanaman jauh lebih mudah dari tanah dengan nilai KB 50 %. • Nilai KB 80 % berarti 4/5 bagian tempat pertukaran dijenuhi oleh basa-basa K, Ca, Mg dan Na serta 1/5 bagian komplek jerapan ditempati oleh Al dan H.

4. REAKSI TANAH (p. H) 1. Kapasitas Sangga dan Pengertian p. H Tanah Sanggaan Tanah • Untuk menciptakan pertumbuhan dan produksi optimal dari tanaman menghendaki p. H tertentu • Jarang sekali bisa menemukan p. H tanah yang sesusai dengan kebutuhan tanaman. Oleh karena tu diperlukan sutu tindakan untuk mengubah p. H sebelum ditanami • Tetapi p. H tanah tidak dapat diubah dengan mudah, karena tanah memiliki sanggaan (buffer), yang merupakan suatu sifat umum dari campuran asam basa dengan garamnya

Komponen tanah yang mempunyai sifat menyangga: • Gugus asam lemah (karbonat) • Kompleks koloidal tanah Suatu kenyataan di lapangan menunjukkan bahwa makin tinggi kandungan liat dan bahan organik tanah, makin banyak pula diperlukan kapur untuk menaiikan p. H tanah tsb Kapasitas sanggaan tanah berbanding lurus dengan KTK

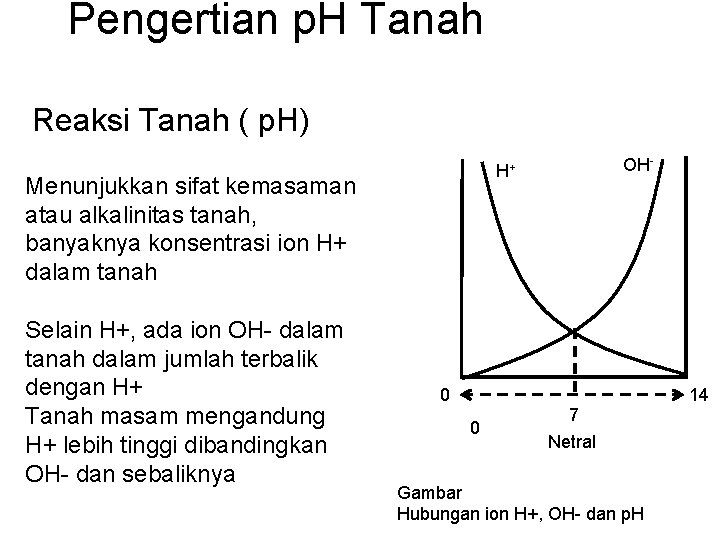
Pengertian p. H Tanah Reaksi Tanah ( p. H) Menunjukkan sifat kemasaman atau alkalinitas tanah, banyaknya konsentrasi ion H+ dalam tanah Selain H+, ada ion OH- dalam tanah dalam jumlah terbalik dengan H+ Tanah masam mengandung H+ lebih tinggi dibandingkan OH- dan sebaliknya OH- H+ 0 0 7 Netral Gambar Hubungan ion H+, OH- dan p. H 14



• Reaksi Tanah merupakan ukuran keasamaan dan kebasaan larutan tanah • p. H = - log (H+) • p. H tanah merupakan indikator pelapukan tanah, kandungan mineral dalam batuan induk, lama waktu dan intensitas pelapukan, terutama pelindihan kation-kation basa dari tanah • Tanah asam banyak mengandung H yang dapat ditukar, sedang tanah alkalis banyak mengandung basa dapat ditukar • p. H > 7 Ca dan Mg bebas; p. H>8. 5 pasti terdapat Na tertukar • Kandungan unsur-unsur hara seperti besi, copper, fosfor, Zn, dan hara lainnya serta substansi toksik (Al 3+, Pb 2+) dikontrol oleh p. H. Kandungan Al 3+, Pb 2+ akan berpengaruh sedikit bagi pertumbuhan tanaman pada tanah alkali calcareous tapi akan sangat serius pada tanah asam. • Nutrient seperti P banyak tersedia (optimum) pada p. H asam sampai netral, dan akan sedikit pada p. H dibawah atau diatas nilai optimum tersebut

Sumber Kemasaman Tanah Bahan induk • Bahan induk masam akan berkembang menjadi tanah masam • Bahan induk basa akan berkembang menjadi tanah basa/alkalin Iklim • tanah yang berkembang di daerah iklim lembab/basah akan bersifat asam • Curah hujan dan suhu sangat berpengaruh aktif terhadap asam – basanya tanah. Bahan Organik. • Bahan organik menghasilkan asam-asam organik hasil proses humifikasi. • Asam organik memiliki p. H nisbi yang rendah • Asam anorganik (H 2 CO 3 H 2 SO 4 HNO 3) hasil dekomposisi Pengaruh manusia • Pemupukan dengan pupuk fisiologis masam akan menyebabkan tanah bersifat masam • Pengapuran akan menyebabkan p. H akan naik Jenis lempung • Lempung silikat merupakan sumber muatan negatif yang bersifat tetap.

KENDALA TANAH MASAM BAGI TANAH DAN PERTUMBUHAN TANAMAN • • • Keracunan Al, Mn dan Fe Kekahatan Ca, Mg, Mo Pelapukan bahan organik lambat Ketersediaan N dan P kecil Aktivitas organisme rendah Produktivitas`tanah rendah Tidak semua tanaman dapat toleran Pertumbuhan tanaman terhambat tanah min bersifat tua Tanah organik belum matang

Klasifikasi p. H tanah berdasar bahan pengekstrak PH tanah aktual (p. H H 2 O) • menunjukkan konsentrasi H+ dalam larutan tanah, sesuai dengan kondisi alam sebenarnya. • Larutan pengekstrak adalah air suling (H 2 O) dengan perbandingan tanah dan H 2 O adalah 1: 2, 5 • Skema keseimbangannya : H+ H+ - H+ Na+ Ca H+ Ca++ K+ Mg++ K+Mg++ H 2 O - fase padat larutan tanah p. H tanah Potensial (p. H Kcl atau p. H Ca. Cl 2) • Menunjukkan nilai p. H tanah setelah H+ dalam kompleks jerapan/didesak keluar dan masuk ke dalam larutan tanah oleh kation lain. • Merupakan p. H tanah yang mungkin potensial dapat terjadi karena pengaruh lain • Larutan pengekstrak adalah KCl 1 N atau Ca. Cl 2 1 N (1: 2, 5) • Skema : H+H+H+ Na+ K+K+K+ H+ H+ K+Cl- K+ K+ H+H+Cl. Ca++ K+Ca++ H+ Na+ Ca++Mg++ Na+ Fase padat + larutan tanah fase padat + larutan tanah • Konsentrasi H+ dalam larutan tanah meningkat maka p. H turun

PH tanah Oksidatif (p. H H 2 O 2) • Menunjukkan nilai p. H tanah setelah tanah mengalami oksidasi • Larutan pengekstrak adalah H 2 O 2 30% atau karena proses`pengeringan pada udara terbuka. • Penting untuk daerah tergenang atau rawa untuk melihat potensi bahaya zat clay (lempung belang) karena dilakukan pengatusan. • Jika setelah oksidasi (pengatusan) nilai p. H <= 3, 5 maka mengandung pirit yang menghasilkan sulfat yang meracun. • Reaksi : 2 H+ Fe. S + On + H 2 O Fe (OH)3 + H 2 SO 4= • Pirit dlm tanah oksidator Fase padat Dlm lrtn tanah

Cara Pengukuran p. H • Elektrometrik : - menggunakan p. H meter (glass electrode) - Biasa dilakukan di laboratotium • Kolorimetrik : - Menggunakan indikator warna kertas p. H, p. H stick indikator, kertas`lakmus, kertas p. H universiil - Banyak digunakan di lapangan

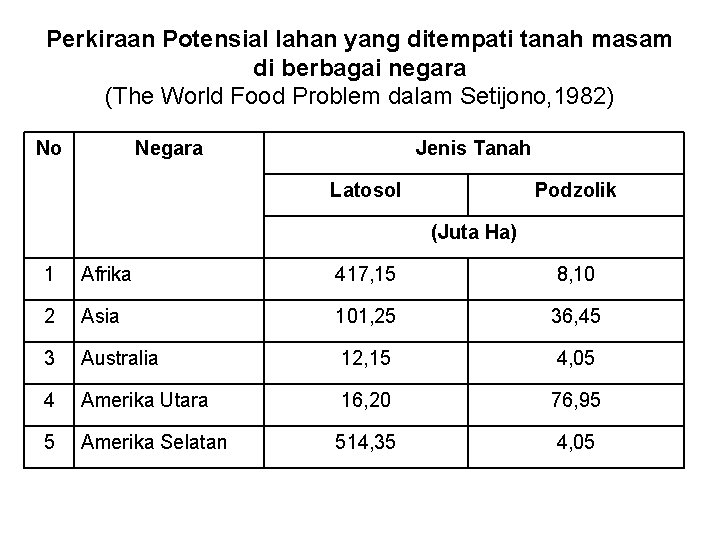
Perkiraan Potensial lahan yang ditempati tanah masam di berbagai negara (The World Food Problem dalam Setijono, 1982) No Negara Jenis Tanah Latosol Podzolik (Juta Ha) 1 Afrika 417, 15 8, 10 2 Asia 101, 25 36, 45 3 Australia 12, 15 4, 05 4 Amerika Utara 16, 20 76, 95 5 Amerika Selatan 514, 35 4, 05

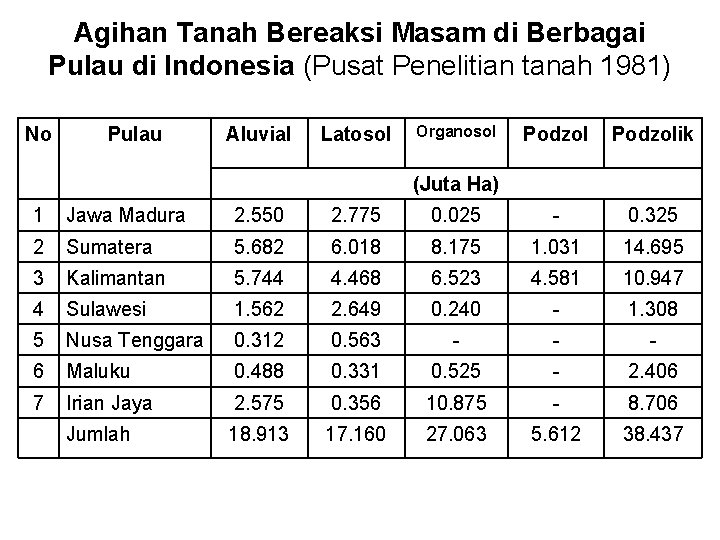
Agihan Tanah Bereaksi Masam di Berbagai Pulau di Indonesia (Pusat Penelitian tanah 1981) No Pulau Aluvial Latosol Organosol Podzolik (Juta Ha) 1 Jawa Madura 2. 550 2. 775 0. 025 - 0. 325 2 Sumatera 5. 682 6. 018 8. 175 1. 031 14. 695 3 Kalimantan 5. 744 4. 468 6. 523 4. 581 10. 947 4 Sulawesi 1. 562 2. 649 0. 240 - 1. 308 5 Nusa Tenggara 0. 312 0. 563 - - - 6 Maluku 0. 488 0. 331 0. 525 - 2. 406 7 Irian Jaya 2. 575 0. 356 10. 875 - 8. 706 Jumlah 18. 913 17. 160 27. 063 5. 612 38. 437

KONDISI KEHARAAN PADA BERBAGAI KISARAN p. H 1. Sangat Alkalis (diatas 8, 5) • Tanah alkali, sodik • Ca dan Mg, kemungkinan tidak tersedia • Fospat terjerap dalam bentuk Ca-P, Mg-P • Bila kadar Na Tinggi, P terjerap menjadi Na-P yang mudah larut • Keracunan Boron (B) pada tanah garaman dan Sodik • Persentase Na tertukar (ESP) di atas 15 dapat menyebabkan kerusakan struktur. • Aktivitas bakteri rendah • Proses nitrifikasi menurun • Ketersediaan hara mikro menurun, kecuali Mo 2. Alkalis ( 7, 5 – 8, 5 ) • Penurunan ketersediaan P dan B sehingga terjadi kekahatan hara P dan B • Kekahatan Co, Cu, Fe, Mn dan Zn • Kadar Ca dan Mg Tinggi • Tanah alkali

3. Netral (6, 5 – 7, 5) • Sifat netral • Kisaran p. H yang baik untuk sebagianj besar tanaman • Kadar hara (makro & mikro) optimum • Aktivitas mikroorganisme optimum) • Sifat kimia tanah optimum 4. Agak Masam, Masam sampai sangat masam (<6, 5) • Tanah masam • Ion Fosfat bersenyawa dengan Fe dan Al membentuk senyawa yang tidak cepat tersedia bagi tanaman. • Semua hara mikro (kecuali Mo) menjadi lebih tersedia dengan peningkatan kemasaman, • Ion Al dilepaskan dari mineral lempung pada nilai p. H di bawah 5, 5 dan • Aktivitas bakteri menurun • Proses nitrifikasi terhambat.

Exchangeable Al (Al tertukar/Aldd) • Trivalen aluminium merupakan kation basa lemah sehingga mampu menghidrolisa air menghasilkan ion hidrogen • Kombinasi Al 3+, hidrolisis, basa lemah tidak terlarut {Al(OH)3 s} merupakan buffer tanah pada p. H 4 -5. 5 • Bentuk : Soluble : Al 3+, Al. OH 2+, Al(OH)2+ • Soild : Al(OH)3 (amorf) Reaksi : Al(OH)3 (amorf) + H+ Al. OH 2+ + H 2 O K 1=10 -0. 081 Al. OH 2+ + H+ Al(OH)2+ + H 2 O K 2=104. 7 Al(OH)2+ + H+ Al 3+ + H 2 O K 3=105. 0 • Terlihat bahwa dissolusi Al dari bentuk padatan menjadi cair mengkonsumsi ion H+ dan berperanan sebagai buffer dalam memperlambat proses pengasaman. • Pada tanah p. H netral, keterlarutan aluminium padat sangat rendah. Misal pada p. H 7 konsentrasi keseimbangan (Kw) Al(OH)2+ dengan Al(OH)3 (amorf) adalah 8. 3 x 10 -7 M; jika p. H menjadi 5 maka konsentrasi Al(OH)2+ meningkat 8. 3 x 10 -5 M.

Mengubah p. H tanah Tanah masam dapat dinaikkan p. H dengan pengapuran (pemberian Ca. CO 3), sedangkan tanah alkalis dapat diturunkan p. Hnya dengan pemberian sulfur/gypsum (Pemberian Ca. SO 4)

 Types of drainage
Types of drainage Hilangnya sebagian kromosom karena patah
Hilangnya sebagian kromosom karena patah Nab adalah nilai ambang batas
Nab adalah nilai ambang batas Tiu medical analysis
Tiu medical analysis Interpretasi tiu 5
Interpretasi tiu 5 Streak plate method
Streak plate method Contoh tujuan instruksional umum
Contoh tujuan instruksional umum Lecture note tiu
Lecture note tiu C learning tiu
C learning tiu Anne laure wu tiu yen
Anne laure wu tiu yen Hitori futari selanjutnya adalah
Hitori futari selanjutnya adalah Prosedur audit selanjutnya
Prosedur audit selanjutnya Indonesia tanah airku tanah tumpah darahku
Indonesia tanah airku tanah tumpah darahku Klasifikasi tanah ppt bogor
Klasifikasi tanah ppt bogor Gumpalan tanah
Gumpalan tanah Yulvi zaika
Yulvi zaika Kapan sebuah kesimpulan dibuat
Kapan sebuah kesimpulan dibuat Kejadian setelah tanggal neraca
Kejadian setelah tanggal neraca Kelompok crinoidea
Kelompok crinoidea Indikator untuk ragam tulis
Indikator untuk ragam tulis Kas berkurang di debet atau kredit
Kas berkurang di debet atau kredit Titik hilang ditentukan setelah selesai membuat
Titik hilang ditentukan setelah selesai membuat Setelah mempelajari materi ini
Setelah mempelajari materi ini Keseimbangan pasar setelah pajak proporsional
Keseimbangan pasar setelah pajak proporsional Pengertian menulis surat
Pengertian menulis surat Cara mengusir jin kiriman orang
Cara mengusir jin kiriman orang Contoh kata hubung gabungan
Contoh kata hubung gabungan Visi menikah adalah
Visi menikah adalah Surat at tin diturunkan di
Surat at tin diturunkan di Sistem penyusunan formasi
Sistem penyusunan formasi Setelah mempelajari materi
Setelah mempelajari materi Sebuah petir terdengar 4 s setelah kilat terlihat di langit
Sebuah petir terdengar 4 s setelah kilat terlihat di langit Rencana setelah mengikuti pelatihan
Rencana setelah mengikuti pelatihan Kata sambung ayat
Kata sambung ayat Imbangan duga tidak seimbang
Imbangan duga tidak seimbang Pengertian menyundul bola
Pengertian menyundul bola Contoh gambar tekanan zat padat
Contoh gambar tekanan zat padat Setelah mempelajari materi tentang
Setelah mempelajari materi tentang Struktur organisasi dapur kecil
Struktur organisasi dapur kecil Psak 8 peristiwa setelah periode pelaporan
Psak 8 peristiwa setelah periode pelaporan Sistematika konstitusi ris
Sistematika konstitusi ris Tahapan pengolahan bahan pangan buah buahan menjadi makanan
Tahapan pengolahan bahan pangan buah buahan menjadi makanan Setelah mempelajari materi tentang
Setelah mempelajari materi tentang Contoh penggalan surat lamaran pekerjaan
Contoh penggalan surat lamaran pekerjaan Setelah mempelajari bab
Setelah mempelajari bab Cara mengindeks sistem abjad
Cara mengindeks sistem abjad Materi pendapatan akuntansi keuangan menengah 2
Materi pendapatan akuntansi keuangan menengah 2 Neraca saldo setelah penyesuaian
Neraca saldo setelah penyesuaian Amina aromatik
Amina aromatik Reaksi inti
Reaksi inti Contoh metode ilmiah kimia
Contoh metode ilmiah kimia









































































