Estereoqumica Tercera parte ESTEREOISOMEROS CONFIGURACIONALES Pedro Antonio Garca



































- Slides: 70

Estereoquímica Tercera parte ESTEREOISOMEROS CONFIGURACIONALES Pedro Antonio García Ruiz Catedrático de Escuela Universitaria Area Química analítica Profesor Titular de Universidad Area Química Orgánica Departamento de Química Orgánica - Universidad de Murcia

CONTENIDO TIPOS DE ISOMERIA ESTEREOISOMEROS COFORMACIONALES ESTEREOISOMEROS CONFIGURACIONALES NOMENCLATURA DE ESTEREOISOMEROS

CONFIGURACION - ESTEREOISOMEROS NO QUIRALES -ESTEREOISOMEROS QUIRALES SON SUPERPONIBLES CON SU IMAGEN EN EL ESPEJO DIFIEREN UNOS DE OTROS EN SU MAYOR PARTE EN LA ORDENACION DE GRUPOS EN UN PLANO

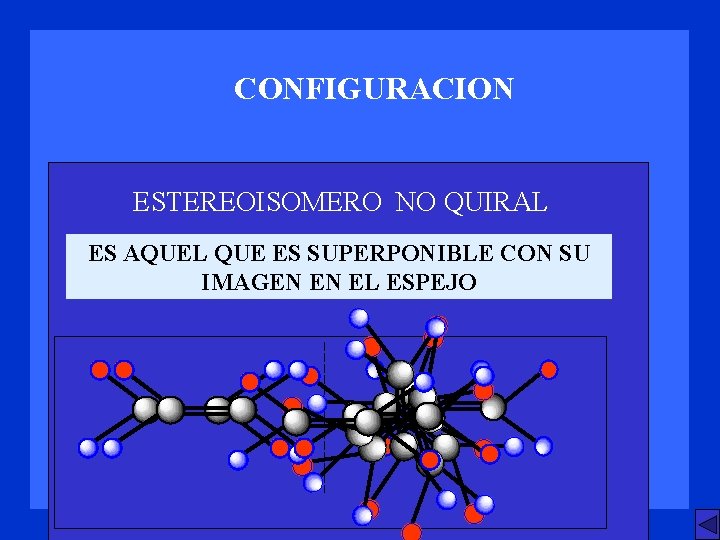
CONFIGURACION ESTEREOISOMERO NO QUIRAL ES AQUEL QUE ES SUPERPONIBLE CON SU IMAGEN EN EL ESPEJO Son superponibles

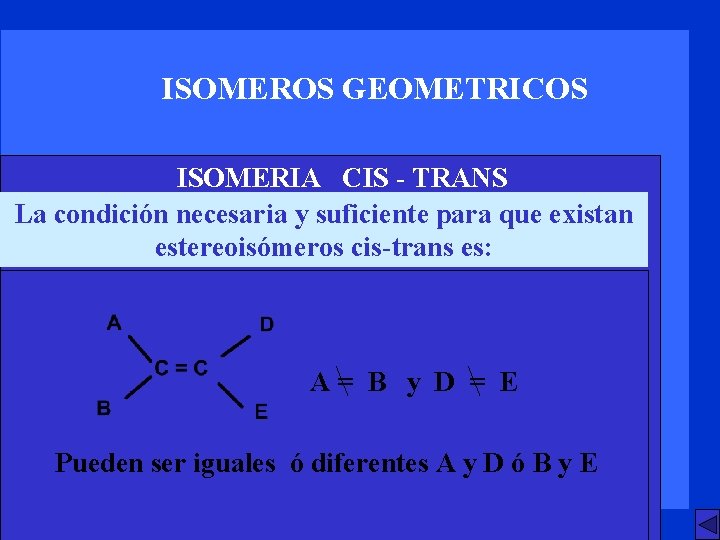
ISOMEROS GEOMETRICOS ISOMERIA CIS - TRANS La condición necesaria y suficiente para que existan estereoisómeros cis-trans es: A= B y D = E Pueden ser iguales ó diferentes A y D ó B y E

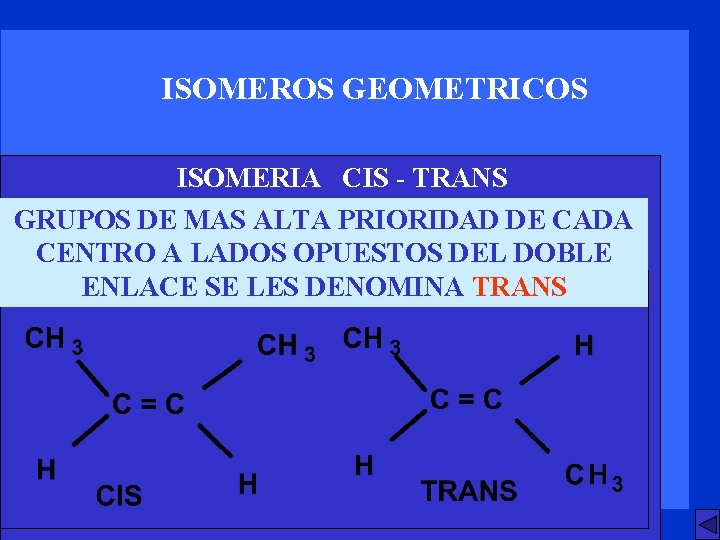
ISOMEROS GEOMETRICOS ISOMERIA CIS - TRANS GRUPOS DE MAS ALTA PRIORIDAD DE CADA CENTRO A AL LADOS MISMO OPUESTOS LADO DEL DOBLE ENLACE SESE LES DENOMINA TRANS CIS

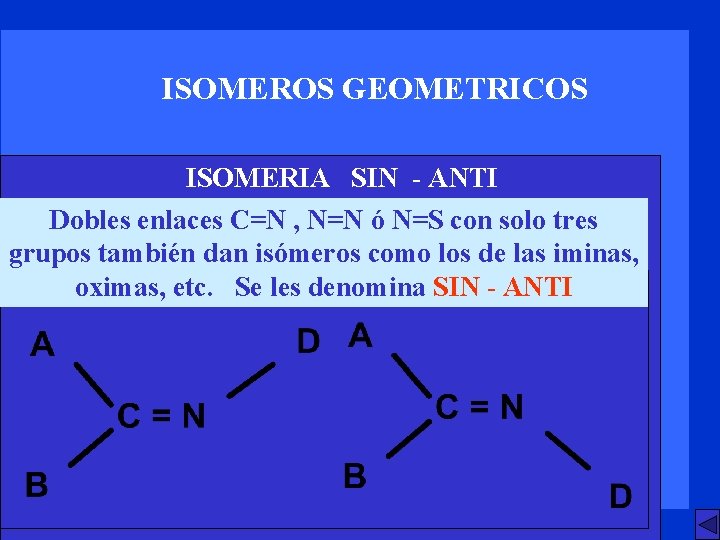
ISOMEROS GEOMETRICOS ISOMERIA SIN - ANTI GRUPOS Dobles enlaces DE MAS C=N ALTA , N=N PRIORIDAD ó N=S con solo DE CADA tres grupos CENTRO también A AL LADOS dan MISMO isómeros OPUESTOS LADO como. DEL los DEL de DOBLE las DOBLE iminas, oximas, ENLACE etc. SE SE Se. LES les LES denomina DENOMINA SIN ANTI -SIN ANTI

ISOMEROS GEOMETRICOS ISOMERIA SIN - ANTI Con GRUPOS solo dos. Agrupos AL LADOS MISMO también OPUESTOS LADO dan isómeros DEL DOBLE como los de los azocompuestos. ENLACESE SELES Se. DENOMINA les denomina. ANTI SIN - ANTI

ISOMEROS GEOMETRICOS DESIGNACION E -Z Según las Reglas de Cahn-Ingold-Prelog Si los sustituyentes de mayor prioridad están juntos se les denomina Z (del alemán Zusammen = Juntos), si están opuestos se les denomina E (de Engegen= de través)

ISOMEROS GEOMETRICOS ISOMERIA GEOMETRICA EN ANILLOS Cualquier anillo puede provocar restrinción de giro de un enlace y que cuatro grupos queden en un plano. Por ello en ciclos también se dá isomeria cis y trans ó E-Z

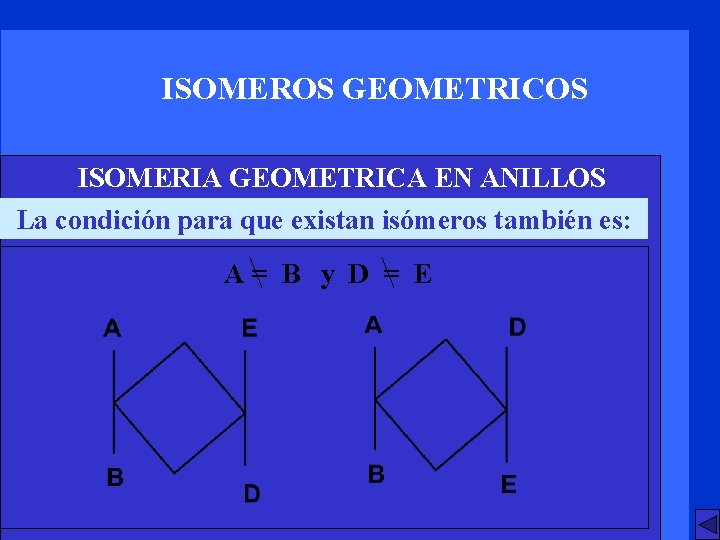
ISOMEROS GEOMETRICOS ISOMERIA GEOMETRICA EN ANILLOS La condición para que existan isómeros también es: A= B y D = E

ISOMEROS GEOMETRICOS ISOMERIA GEOMETRICA EN ANILLOS La condición para que existan isómeros también es: A= B y D = E

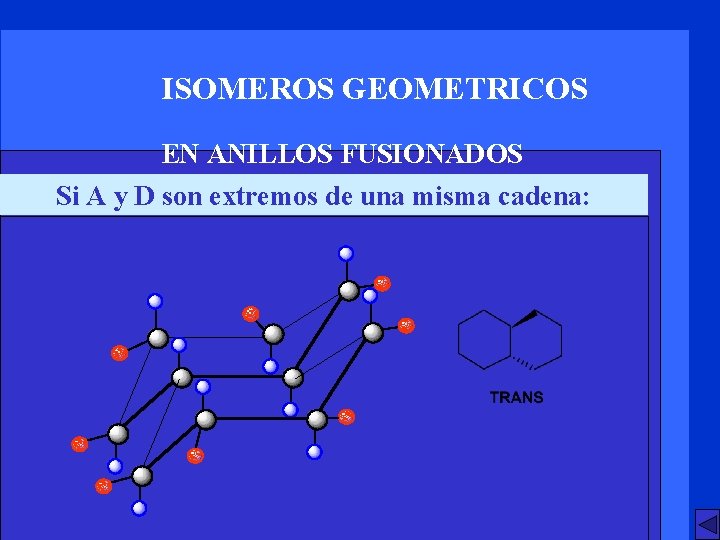
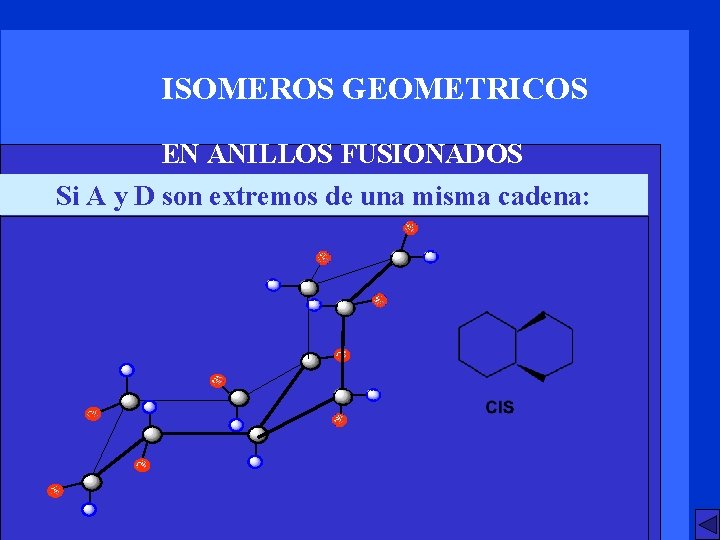
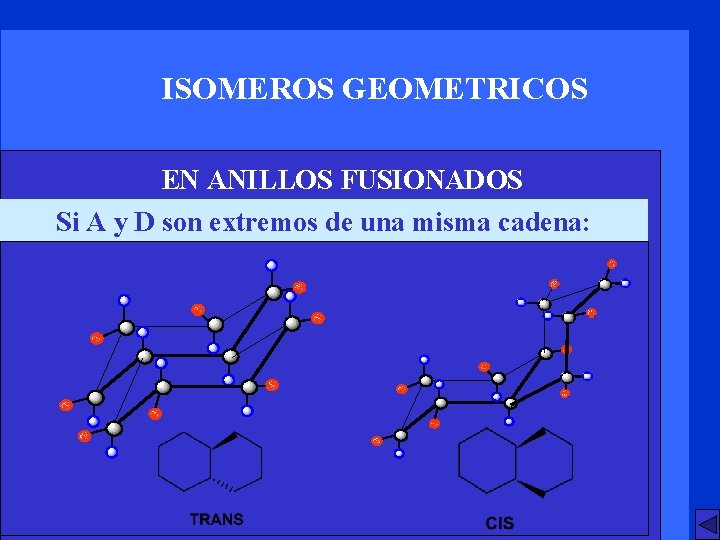
ISOMEROS GEOMETRICOS EN ANILLOS FUSIONADOS Si A y D son extremos de una misma cadena:

ISOMEROS GEOMETRICOS EN ANILLOS FUSIONADOS Si A y D son extremos de una misma cadena:

ISOMEROS GEOMETRICOS EN ANILLOS FUSIONADOS Si A y D son extremos de una misma cadena:

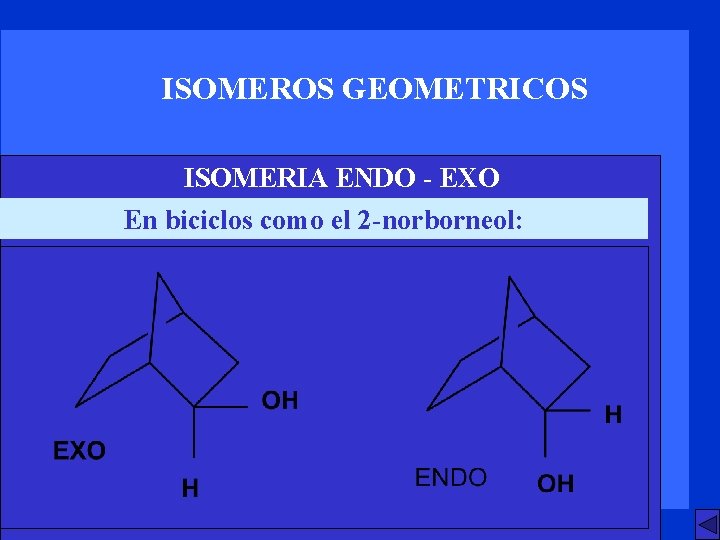
ISOMEROS GEOMETRICOS ISOMERIA ENDO - EXO En biciclos como el 2 -norborneol:

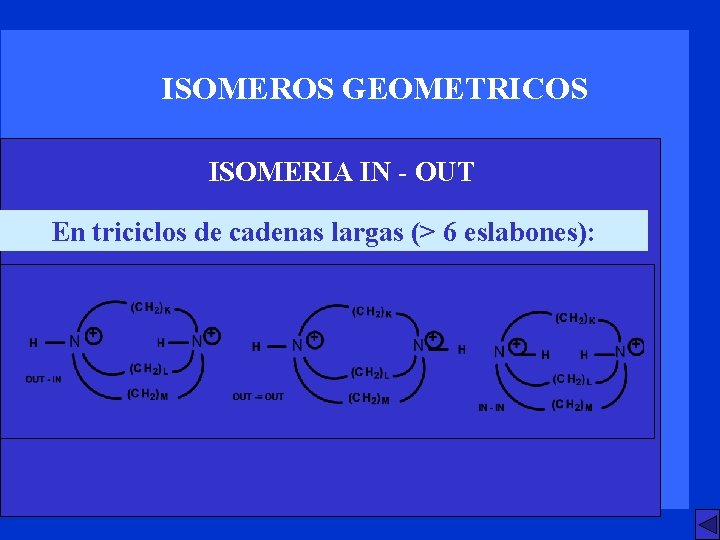
ISOMEROS GEOMETRICOS ISOMERIA IN - OUT En triciclos de cadenas largas (> 6 eslabones):

ISOMEROS GEOMETRICOS ISOMERIA EN COMPLEJOS INORGANICOS Complejos de número de coordinación cuatro cuadrado planares como los diamino dicloruro platino II dán isómeros cis y trans

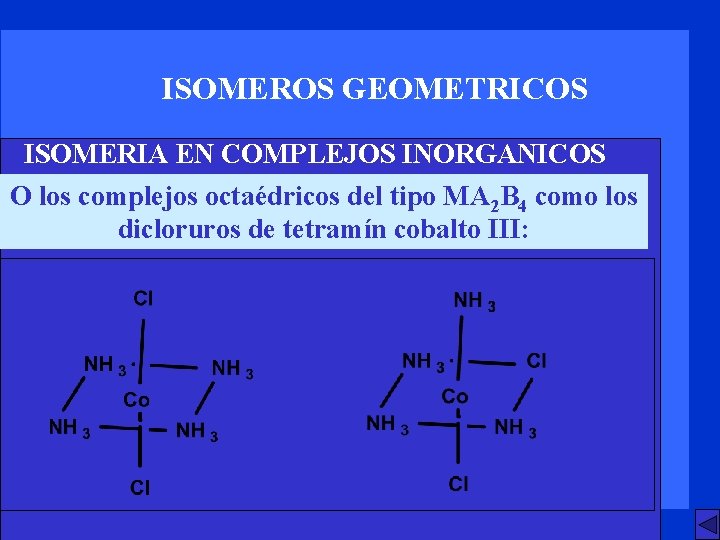
ISOMEROS GEOMETRICOS ISOMERIA EN COMPLEJOS INORGANICOS O los complejos octaédricos del tipo MA 2 B 4 como los dicloruros de tetramín cobalto III:

CONFIGURACION - ESTEREOISOMEROS NO QUIRALES -ESTEREOISOMEROS QUIRALES NO SON SUPERPONIBLES CON SU IMAGEN EN EL ESPEJO DIFIEREN UNOS DE OTROS EN LA ORDENACION DE GRUPOS EN EL ESPACIO

CONFIGURACION - ESTEREOISOMEROS NO QUIRALES -ESTEREOISOMEROS QUIRALES - ENANTIOMEROS - DIASTEROISOMEROS DOS ESTEREOISOMEROS SON ENANTIOMEROS CUANDO UNO ES LA IMAGEN EN EL ESPEJO DEL OTRO

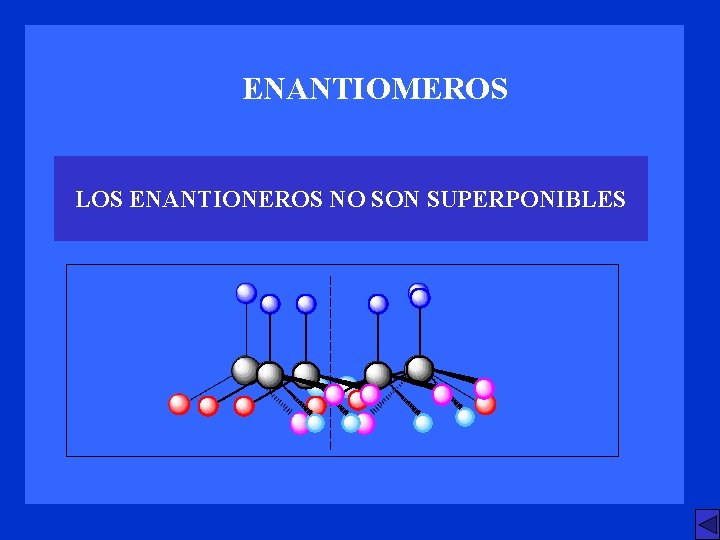
ENANTIOMEROS LOS ENANTIONEROS NO SON SUPERPONIBLES

ENANTIOMEROS LOS ENANTIOMEROS SE PARECEN COMO LA MANO DERECHA Y LA IZQUIERDA LOS ENANTIOMEROS TIENEN IDENTICAS PROPIEDADES FISICAS Y QUIMICAS EN CONDICIONES AQUIRALES

ENANTIOMEROS LOS ENANTIONEROS ROTAN EL PLANO DE LA LUZ POLARIZADA EN DIRECCIONES OPUESTAS PERO EN IGUAL CANTIDAD Al isómero que rota el plano de polarización de la luz en sentido contrario a las agujas del reloj (a la izquierda) se le denomina isómero levo y se nombra anteponiendo al nombre del compuesto el signo (-) ó también la letra l (l minúscula) LEVO (-) - l-

ENANTIOMEROS LOS ENANTIONEROS ROTAN EL PLANO DE LA LUZ POLARIZADA EN DIRECCIONES OPUESTAS PERO EN IGUAL CANTIDAD Al isómero que rota el plano de polarización de la luz en el sentido de las agujas del reloj (a la derecha) se le denomina isómero dextro y se nombra anteponiendo al nombre del compuesto el signo (+) ó también la letra d (d minúscula) DEXTRO (+) - d-

ENANTIOMEROS SUS PROPIEDADES FISICAS Y QUIMICAS SON DIFERENTES EN CONDICIONES QUIRALES Reaccionan con diferentes velocidades con otros compuestos quirales Diferentes velocidades de reacción y solubilidad si el catalizador o el disolvente es quiral También diferencias si la medida de una propiedad física o una reacción se hace en presencia de luz polarizada circularmente

ENANTIOMEROS RACEMICOS La mezcla en iguales proporciones (50%) de moléculas del isómero dextro y del isómero levo se denomina MEZCLA RACEMICA Una mezcla racémica o racemato no rota el plano de la luz polarizada La separación de los componentes de un racémico se denomina Resolución del racémico

ENANTIOMEROS RACEMICOS Las propiedades de las mezclas racémicas no son siempre las mismas que las de los enantiómeros por separado. En estado gas, líquido ó en disolución propiedades casi las mismas por mezcla casi ideal En estado sólido, puntos fusión, solubilidades, calores de fusión etc. diferentes

ENANTIOMEROS RACEMICOS En estado sólido, puntos fusión, solubilidades, calores de fusión etc. diferentes Acido tartárico Racémico -PF = 204 a 206ºC- Solubilidad en agua a 20º 206 gr/litro Enantiómero (+) ó el (-) -PF = 170ºC - Solubilidad en agua a 20º 1390 gr/litro

ROTACION Y ACTIVIDAD OPTICA LUZ POLARIZADA EN EL PLANO A un rayo luminoso cuyas vibraciones se dan en un solo plano se dice que es LUZ POLARIZADA EN EL PLANO

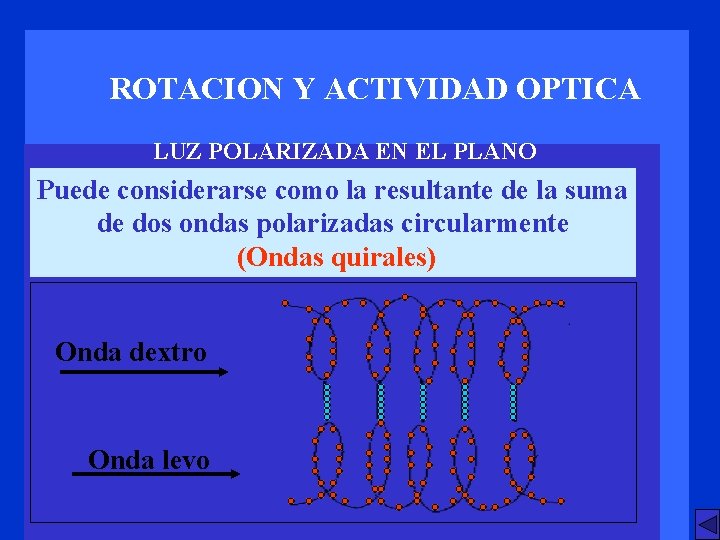
ROTACION Y ACTIVIDAD OPTICA LUZ POLARIZADA EN EL PLANO Puede considerarse como la resultante de la suma de dos ondas polarizadas circularmente (Ondas quirales) Onda dextro Onda levo

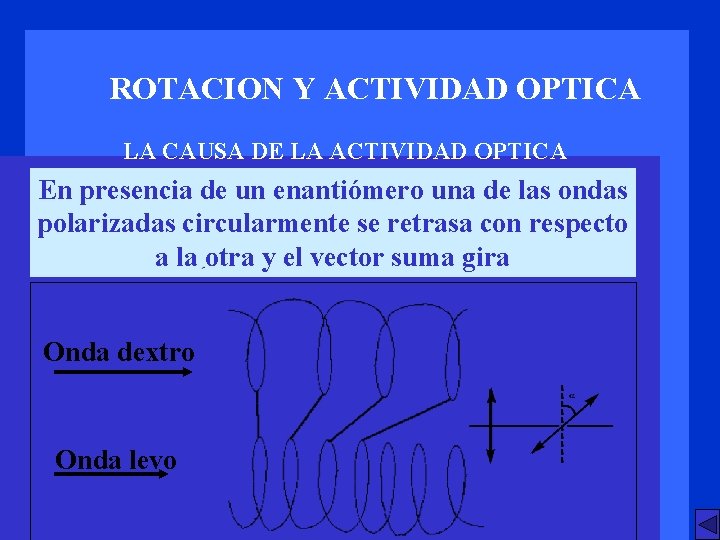
ROTACION Y ACTIVIDAD OPTICA LA CAUSA DE LA ACTIVIDAD OPTICA En presencia de un enantiómero una de las ondas polarizadas circularmente se retrasa con respecto a la otra y el vector suma gira Onda dextro Onda levo

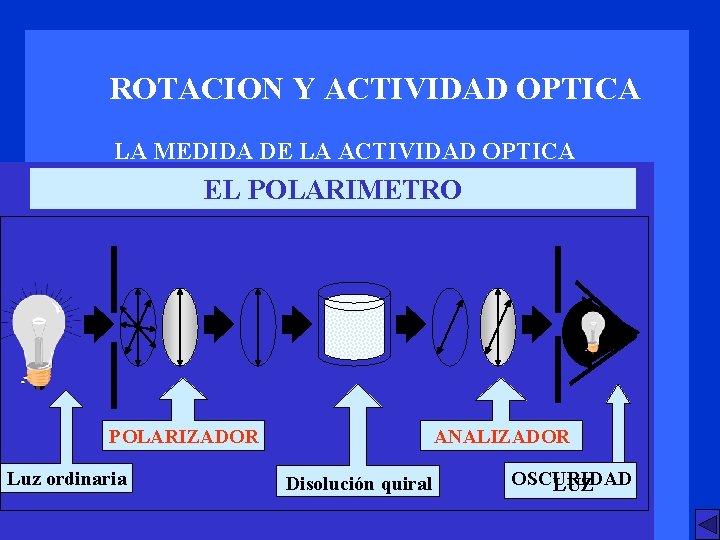
ROTACION Y ACTIVIDAD OPTICA LA MEDIDA DE LA ACTIVIDAD OPTICA Si se hace pasar un rayo luminoso por un filtro <Polarizador> (Prisma de Nicol; Cristales de espato de Islandia pegados con bálsamo de Canadá) emerge de él luz polarizada en el plano Si un rayo de luz polarizada en el plano se hace pasar por una nueva lente polarizadora <Analizador> emerge de él luz si ambos planos de polarización coinciden, si están girados 90º se observará oscuridad < Extinción>

ROTACION Y ACTIVIDAD OPTICA LA MEDIDA DE LA ACTIVIDAD OPTICA EL POLARIMETRO POLARIZADOR Luz ordinaria ANALIZADOR Disolución quiral OSCURIDAD LUZ

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sandwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sandwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

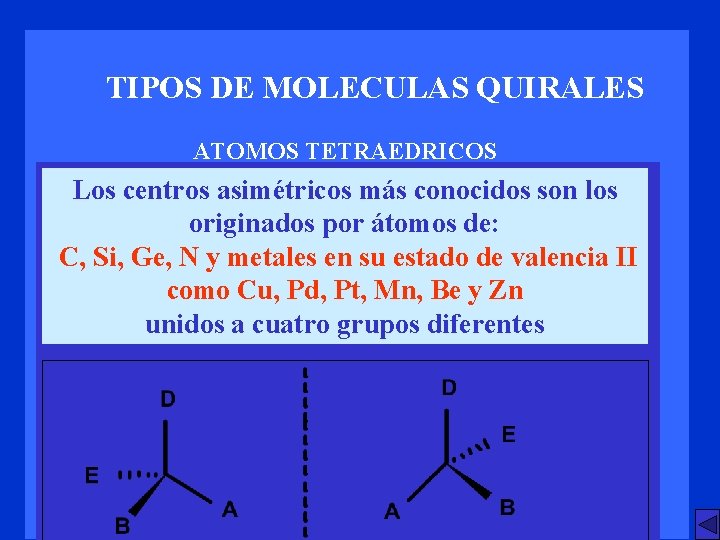
TIPOS DE MOLECULAS QUIRALES ATOMOS TETRAEDRICOS Los centros asimétricos más conocidos son los originados por átomos de: C, Si, Ge, N y metales en su estado de valencia II como Cu, Pd, Pt, Mn, Be y Zn unidos a cuatro grupos diferentes

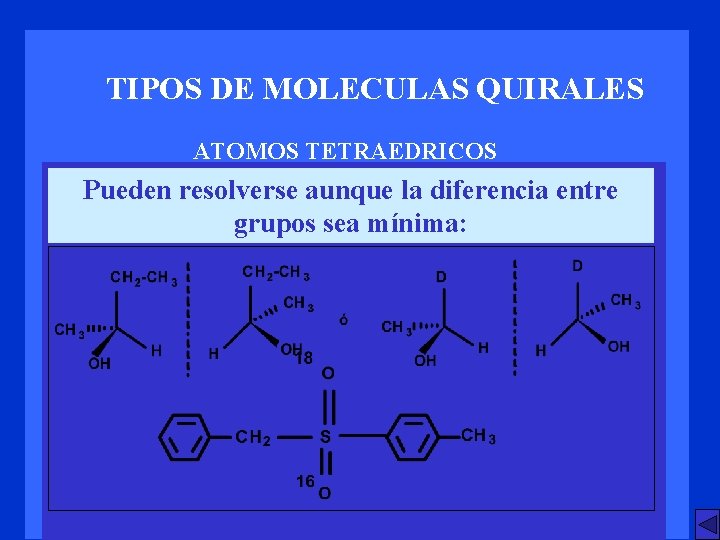
TIPOS DE MOLECULAS QUIRALES ATOMOS TETRAEDRICOS Pueden resolverse aunque la diferencia entre grupos sea mínima:

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

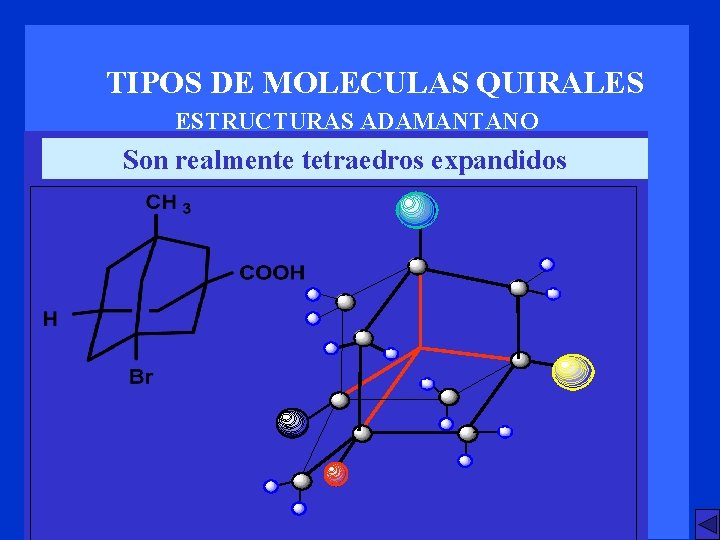
TIPOS DE MOLECULAS QUIRALES ESTRUCTURAS ADAMANTANO Son realmente tetraedros expandidos

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

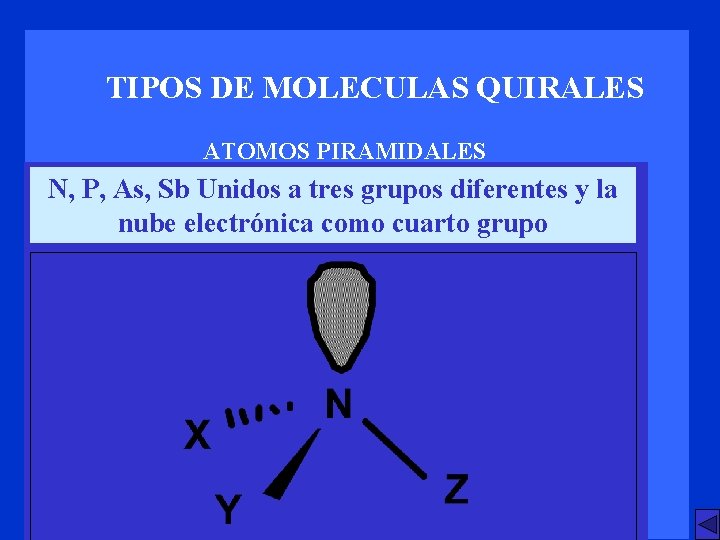
TIPOS DE MOLECULAS QUIRALES ATOMOS PIRAMIDALES N, P, As, Sb Unidos a tres grupos diferentes y la nube electrónica como cuarto grupo

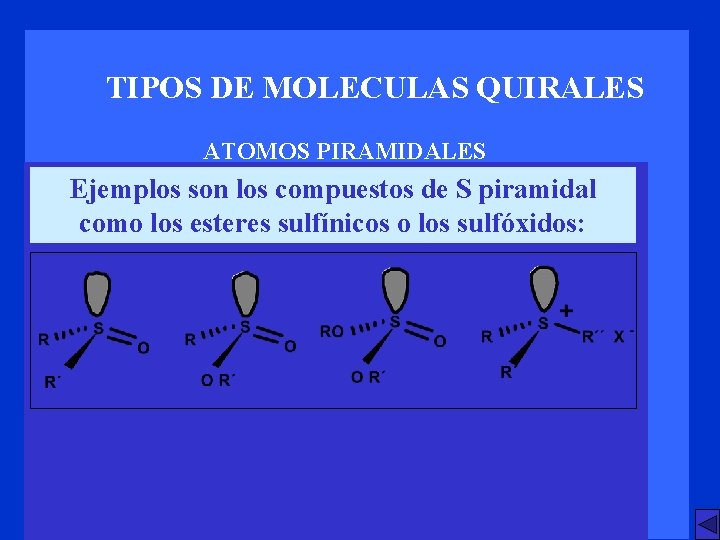
TIPOS DE MOLECULAS QUIRALES ATOMOS PIRAMIDALES Ejemplos son los compuestos de S piramidal como los esteres sulfínicos o los sulfóxidos:

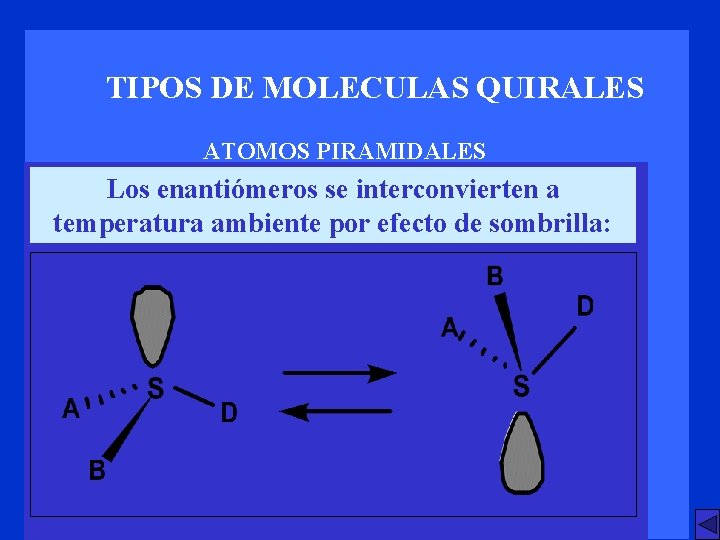
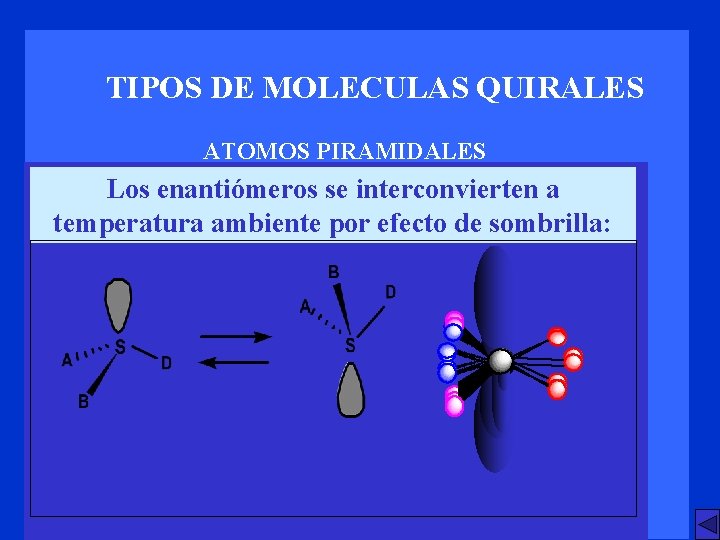
TIPOS DE MOLECULAS QUIRALES ATOMOS PIRAMIDALES Los enantiómeros se interconvierten a temperatura ambiente por efecto de sombrilla:

TIPOS DE MOLECULAS QUIRALES ATOMOS PIRAMIDALES Los enantiómeros se interconvierten a temperatura ambiente por efecto de sombrilla:

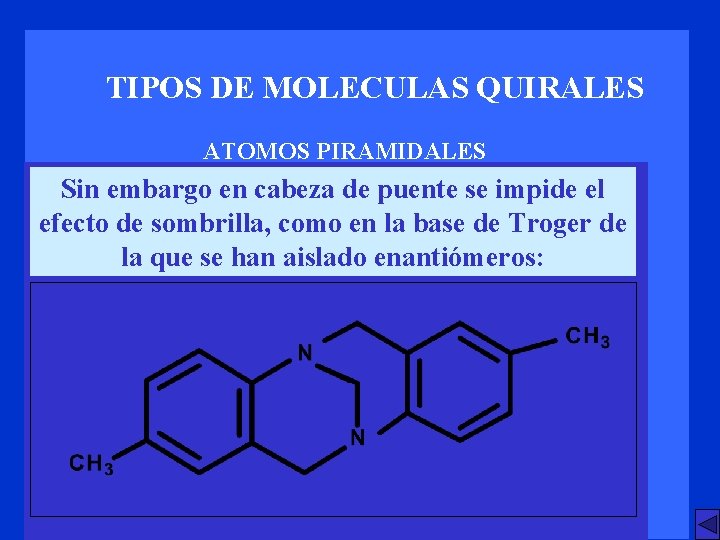
TIPOS DE MOLECULAS QUIRALES ATOMOS PIRAMIDALES Sin embargo en cabeza de puente se impide el efecto de sombrilla, como en la base de Troger de la que se han aislado enantiómeros:

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

TIPOS DE MOLECULAS QUIRALES COMPLEJOS OCTAEDRICOS Resueltos complejos de número de coordinación seis, como los de Co, Cr y Rh III ó Fe II con quelatantes como etiléndiaminas, oxalatos ó malonatos:

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

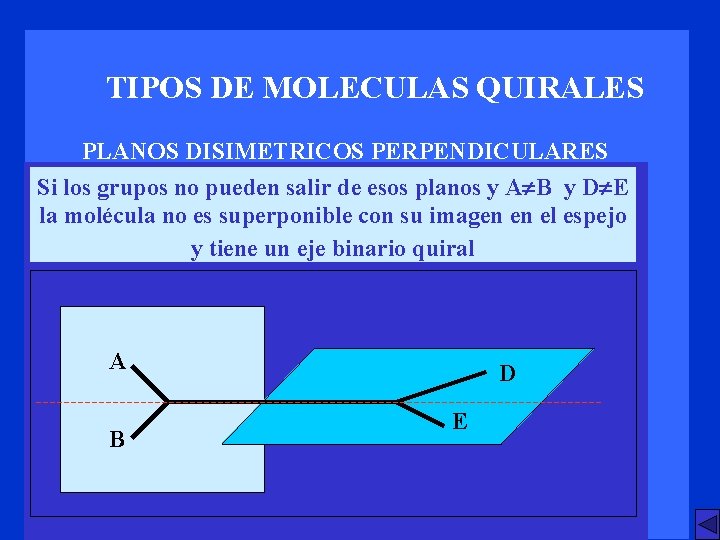
TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Si los grupos no pueden salir de esos planos y A B y D E la molécula no es superponible con su imagen en el espejo y tiene un eje binario quiral A B D E

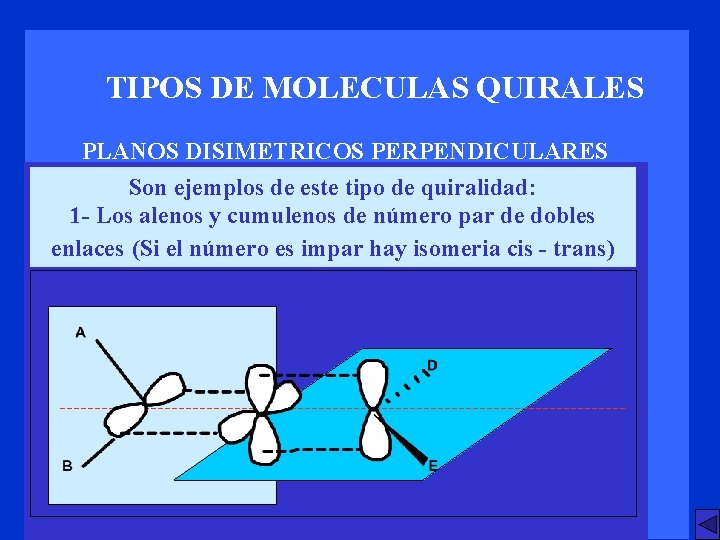
TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: 1 - Los alenos y cumulenos de número par de dobles enlaces (Si el número es impar hay isomeria cis - trans)

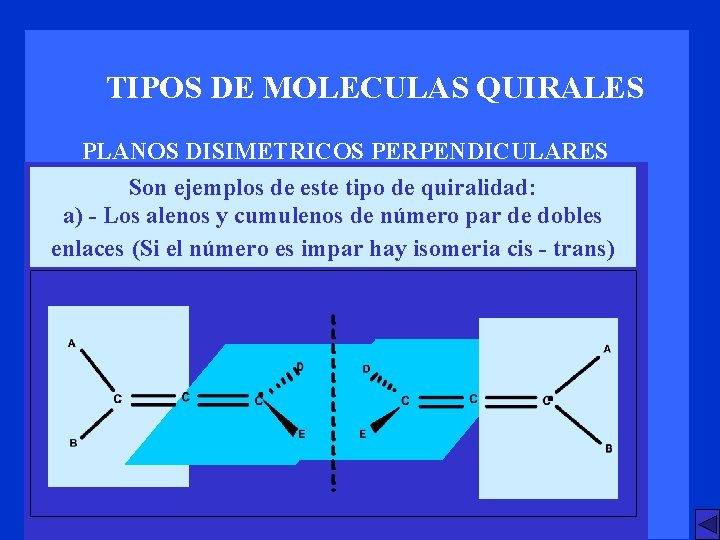
TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: a) - Los alenos y cumulenos de número par de dobles enlaces (Si el número es impar hay isomeria cis - trans)

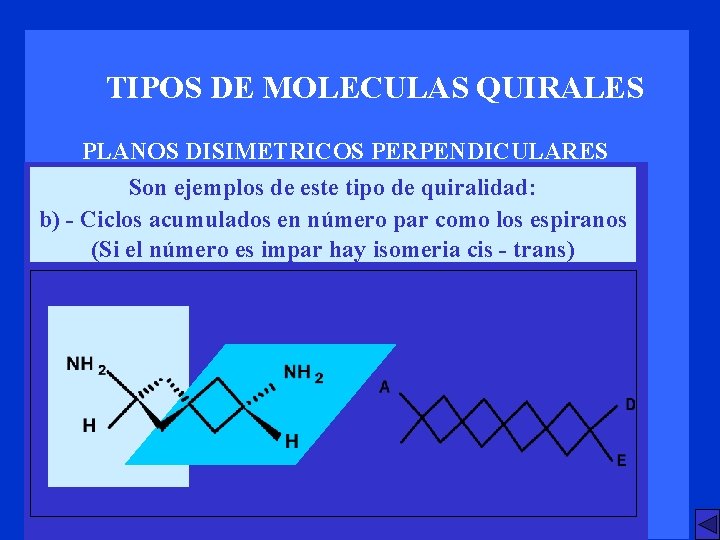
TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: b) - Ciclos acumulados en número par como los espiranos (Si el número es impar hay isomeria cis - trans)

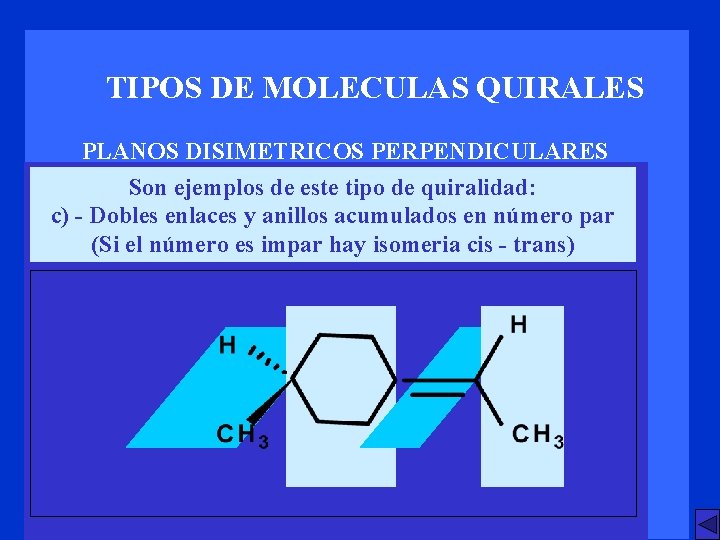
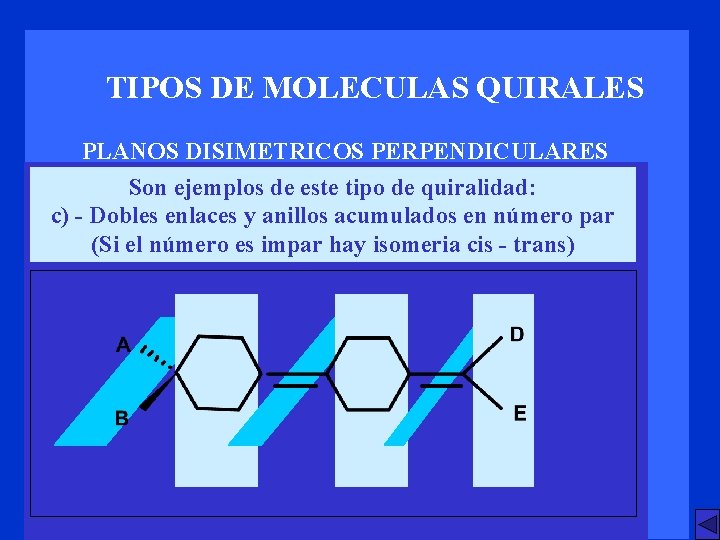
TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: c) - Dobles enlaces y anillos acumulados en número par (Si el número es impar hay isomeria cis - trans)

TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: c) - Dobles enlaces y anillos acumulados en número par (Si el número es impar hay isomeria cis - trans)

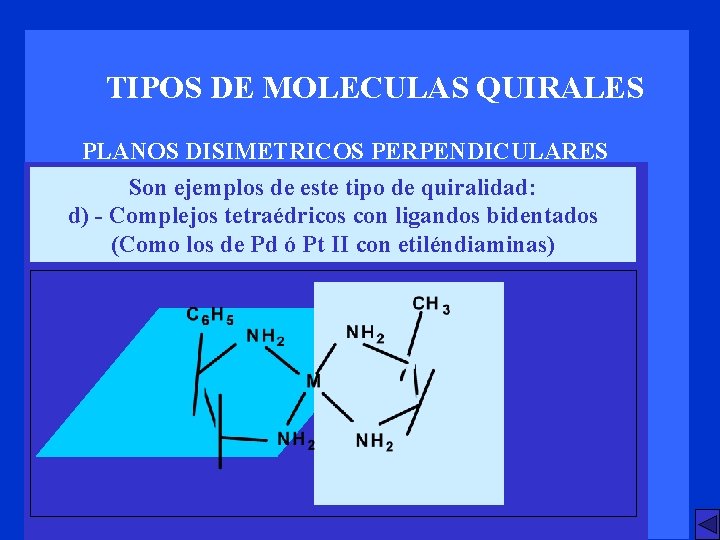
TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: d) - Complejos tetraédricos con ligandos bidentados (Como los de Pd ó Pt II con etiléndiaminas)

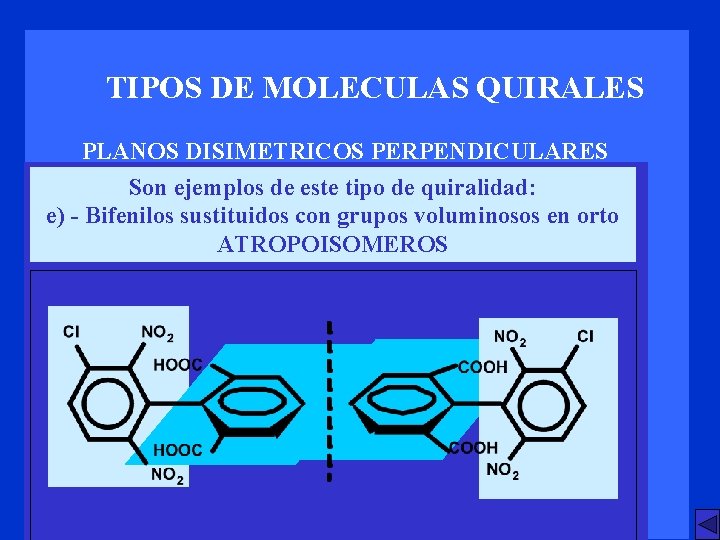
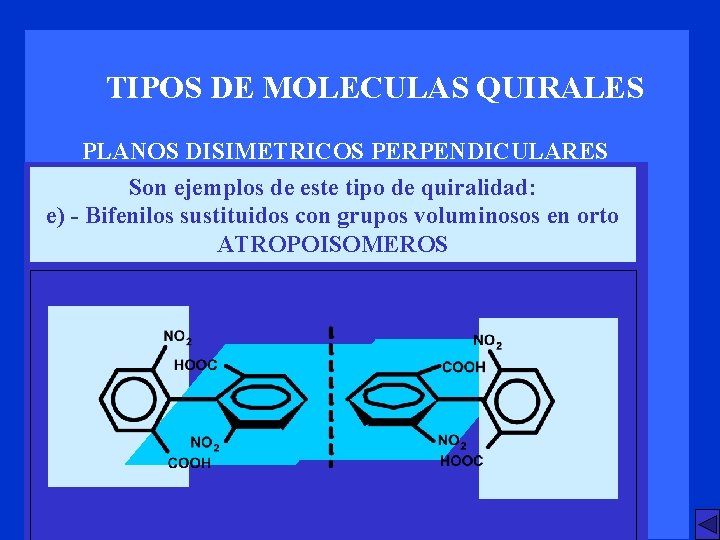
TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: e) - Bifenilos sustituidos con grupos voluminosos en orto (impedimento estérico a la rotación de 15 a 30 Kcal/mol) Las conformaciones se transforman en configuraciones por ser aislables a T ambiente

TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: e) - Bifenilos sustituidos con grupos voluminosos en orto ATROPOISOMEROS

TIPOS DE MOLECULAS QUIRALES PLANOS DISIMETRICOS PERPENDICULARES Son ejemplos de este tipo de quiralidad: e) - Bifenilos sustituidos con grupos voluminosos en orto ATROPOISOMEROS

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

TIPOS DE MOLECULAS QUIRALES FORMA HELICOIDAL Hexahelicenos Enrollados a derechas ó a izquierdas

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

TIPOS DE MOLECULAS QUIRALES Con Plano Quiral Transciclooctenos Enrollados a derechas ó a izquierdas

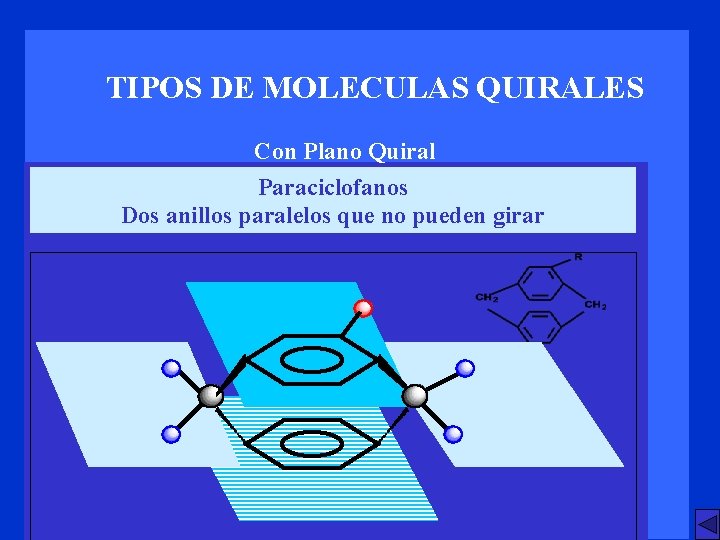
TIPOS DE MOLECULAS QUIRALES Con Plano Quiral Paraciclofanos Dos anillos paralelos que no pueden girar

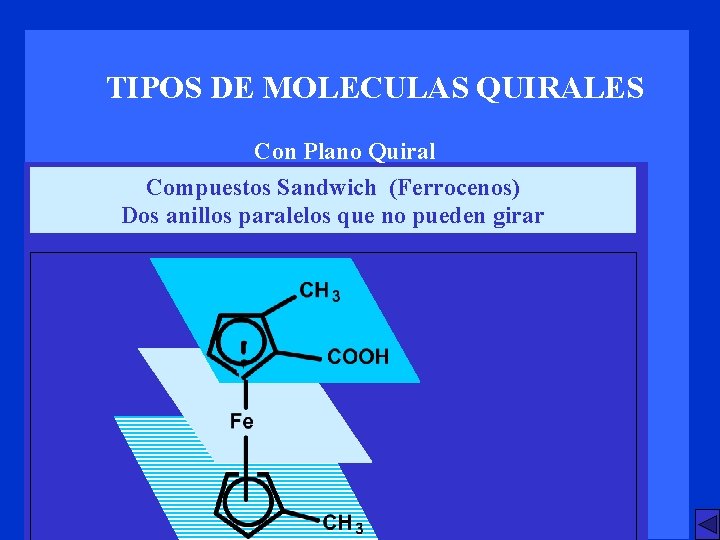
TIPOS DE MOLECULAS QUIRALES Con Plano Quiral Compuestos Sandwich (Ferrocenos) Dos anillos paralelos que no pueden girar

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

TIPOS DE MOLECULAS QUIRALES Otras moléculas sin centro quiral Anillos con nudos, catenanos y rotaxanos

TIPOS DE MOLECULAS QUIRALES - CON UN CENTRO QUIRAL -Atomos tetraédricos con 4 grupos diferentes - Estructuras adamantano con 4 grupos diferentes - Atomos piramidales con 3 grupos diferentes -Complejos octaédricos convenientemente sustituidos - SIN CENTRO QUIRAL - Con eje quiral - Planos disimétricos perpendiculares - Con eje quiral - Forma helicoidal - Con un plano quiral - trans cicloocteno, p-ciclofanos y compuestos sándwich - Otras moléculas sin centro quiral -CON DOS O MAS CENTROS QUIRALES

TIPOS DE MOLECULAS QUIRALES CON DOS O MAS CENTROS QUIRALES Se estudiará conjuntamente con su nomenclatura en el capitulo siguiente

ESTEROQUIMICA Ha finalizado la Tercera PARTE Muchas gracias por su atención Pedro Antonio García Ruiz Catedrático de Escuela Universitaria Area Química analítica Profesor Titular de Universidad Area Química Orgánica Departamento de Química Orgásnica - Universidad de Murcia
 Estereoisómeros configuracionales
Estereoisómeros configuracionales Estereoisómeros geometricos ejemplos
Estereoisómeros geometricos ejemplos Estereocentro
Estereocentro Parecidas
Parecidas Salve reina y madre
Salve reina y madre António pedro pinto monteiro
António pedro pinto monteiro Colegio pedro antonio molina cali
Colegio pedro antonio molina cali Esspc
Esspc Pedro sergio antonio donoso brant
Pedro sergio antonio donoso brant Entre andres y carla tienen un total de 42 lapices
Entre andres y carla tienen un total de 42 lapices Slidetodoc.com
Slidetodoc.com Missa parte por parte slide catequese
Missa parte por parte slide catequese Te invitamos a ser parte
Te invitamos a ser parte Este parte aquele parte
Este parte aquele parte Jorge garca
Jorge garca Modelo cielab
Modelo cielab Solidificação
Solidificação Gabriel garca
Gabriel garca Bibliografia de gabriel garcia marquez
Bibliografia de gabriel garcia marquez Ricardo garca
Ricardo garca Ricardo garca
Ricardo garca Gabriel garca
Gabriel garca Garça tipos
Garça tipos Repuestos garca
Repuestos garca Andrea garca
Andrea garca Andrea garca
Andrea garca Roberto garca
Roberto garca Gabriel garcia colorado
Gabriel garcia colorado 13 conseil de la vie
13 conseil de la vie Ricardo garca
Ricardo garca A mayor conocimiento mayor sufrimiento
A mayor conocimiento mayor sufrimiento Definicion de garca
Definicion de garca Partes del cuerpo hombro
Partes del cuerpo hombro Garca la carolina
Garca la carolina Sergio garca
Sergio garca Miguel garca
Miguel garca Aqui no hay viejos solo que llegó la tarde autor
Aqui no hay viejos solo que llegó la tarde autor Que son verbos
Que son verbos Narrador omnisciente
Narrador omnisciente Tomografo de cuarta generacion
Tomografo de cuarta generacion Tercera generacion
Tercera generacion Tercera mayor isla del mundo
Tercera mayor isla del mundo Una estrofa del himno nacional de costa rica
Una estrofa del himno nacional de costa rica La premisa mayor
La premisa mayor Cefalosporina de 5ta generacion
Cefalosporina de 5ta generacion 3era ley de la termodinamica
3era ley de la termodinamica Primera persona gramatical
Primera persona gramatical Los pronombres objetivos
Los pronombres objetivos Tercera generación
Tercera generación Bulbo duodenal
Bulbo duodenal Tandwin newton
Tandwin newton Virgen de fatima tercera guerra mundial
Virgen de fatima tercera guerra mundial Jeure conjugació
Jeure conjugació Primera y segunda persona
Primera y segunda persona Imagenes de circuitos integrados de la tercera generacion
Imagenes de circuitos integrados de la tercera generacion Manejo activo de la tercera etapa del parto (matep) pdf
Manejo activo de la tercera etapa del parto (matep) pdf Verbos en tercera persona
Verbos en tercera persona 2da forma normal base de datos
2da forma normal base de datos Que la fuerza
Que la fuerza Feel past simple
Feel past simple Primera persona segunda persona y tercera persona
Primera persona segunda persona y tercera persona Qué es el narrador omnisciente
Qué es el narrador omnisciente Venida de cristo
Venida de cristo Pasar texto a tercera persona
Pasar texto a tercera persona Ley de newton introduccion
Ley de newton introduccion Que significa la palabra via lucis
Que significa la palabra via lucis Comer imperativo
Comer imperativo σfx
σfx Decima estrofa del himno nacional
Decima estrofa del himno nacional Girola doble
Girola doble Tercera etapa de goya
Tercera etapa de goya