Chimie organomtallique 1re partie Poly pp 219 233



























- Slides: 48

Chimie organométallique (1ère partie) Poly pp 219 -233 et 240 -243 • Rappels métaux de transition • Classification des ligands • Décompte des électrons autour du métal • Application de la Théorie des OM

Les métaux de transition p. 221 • Définition: possèdent une sous-couche d incomplète K Ca 4 s 4 s 2 Sc Ti V Cr Mn Fe Co Ni Cu 4 s 23 d 1 s 2 d 2 s 2 d 3 … … s 2 d 8 s 1 d 10 Y Zr Nb Mo Tc Ru Rh Pd 5 s 24 d 1 s 2 d 2 s 2 d 3 … … Ag La Hf Ta W Re Os Ir Pt Au 6 s 25 d 1 … … …. • Configurations typiques du métal isolé: 4 s 2 3 dn (4 p 0) 5 s 2 4 dn (5 p 0) 6 s 2 5 dn (6 p 0) Zn 3 d 104 s 2

Les orbitales d du métal • Orbitales « spectroscopiques » m nd = f(r) Yl ( ) fonctions propres de n, l, m n = 3, 4 ou 5 l = 2 m = 0, ± 1, ± 2 Fonctions complexes dégénérées • Combinaisons réelles m = ± 2 Fonctions réelles de type: m = ± 1 xy, xz, yz, x 2, y 2, z 2} m = 0 - (x 2 + y 2 + z 2) p. 24

Les 5 orbitales d dégénérées du métal 3 d xy 3 d yz p. 24 3 d xz 3 d x 2 - y 2 = 3 d xy tournée de 45°

Les 5 orbitales d dégénérées du métal p. 24 3 d z 2 Fonction de type (2 z 2 - x 2 - y 2 ) f(r) 3 d z 2 : 2 cônes nodaux

Les complexes des métaux de transition CO OC Cr CO CO Mn CO CO CO I Rh I CO CO Application: transport de O 2 par l’hémoglobine — Etc. . .

Les complexes des métaux de transition Différences avec la chimie organique • VSEPR, valence • Règles plus subtiles • Questions à résoudre: - Un complexe donné est il stable ou non? - Quelle est sa géométrie? - Est il « haut spin » ou « bas spin » ? - Est il saturé ou insaturé? Point commun avec la chimie organique: • Validité de la Théorie des OM qualitative (construction des OM, perturbations…)

Propriétés des métaux de transition 4 s 23 d 1 • Nombre d’électrons de valence D° d’oxydation Sc Ti V Cr Mn Fe Co Ni Cu 0 3 4 5 6 7 8 9 10 11 I 2 3 4 5 6 7 8 9 10 Etc… Y Zr Nb Mo Tc Ru Rh Pd Ag idem… La Hf Ta W Re Os Ir Pt Au idem… p. 221

Propriétés des métaux de transition • Electronégativités : Bcp + basses que celles de leurs ligands usuels Sc 1. 2 Ti 1. 3 V 1. 5 Cr 1. 6 Mn Fe 1. 6 Y 1. 1 Zr 1. 2 Nb 1. 2 Mo Tc 1. 3 1. 4 La 1. 1 Hf 1. 2 Ta 1. 3 W 1. 4 Re 1. 5 Co 1. 7 Ni 1. 8 Cu 1. 8 Ru 1. 4 Rh 1. 4 Pd 1. 4 Ag 1. 4 Os 1. 5 Ir 1. 6 Pt 1. 4 Au 1. 4 Atomes de la chimie organique: C 2. 5 N 3. 0 O 3. 5 P 2. 1 S 2. 5 c(d) < c(L) Cl 3. 0

• Rayons des orbitales d comparées à s ou p r(pm) Sc Ti V C Mn Fe Co Ni Cu r(4 s) 180 166 152 141 131 122 114 107 103 r(3 d) 61 55 49 45 42 39 36 34 32 Plus généralement: dans les 3 séries (4 s, 3 d, 4 p), (5 s, 4 d, 5 p), (6 s, 5 d, 6 p), (n-1)d < ns ou np • Raison: Nombre quantique principal d < s ou p • Conséquence sur les recouvrements métal-ligand s L p L > d L Les orbitales d interagiront moins fortement avec les ligands que les orbitales s et p

Ligands L, ligands X p. 221 1. Ligands L Apportent un doublet électronique à la liaison avec le métal • Bases de Lewis: amines phosphines CO Exemples: OC Cr CO CO eau monoxyde de C

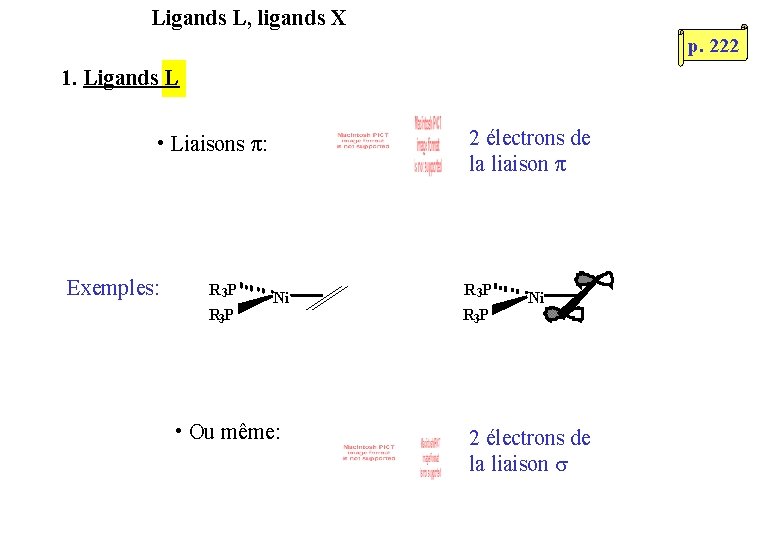
Ligands L, ligands X p. 222 1. Ligands L 2 électrons de la liaison π • Liaisons π: Exemples: R 3 P Ni • Ou même: R 3 P Ni 2 électrons de la liaison

Ligands L, ligands X p. 222 2. Ligands X Apportent 1 seul électron à la liaison avec le métal • Radicaux: Exemples: 6 ligands X 2 ligands X, 2 ligands L

Ligands monohapto, polyhapto p. 222 1. Ligands monohapto Chaque ligand est lié au métal par un seul atome 2. Ligands polyhapto Lié au métal par plusieurs atomes Les phosphines (R 3 P) sont monohapto L’éthylène est bihapto

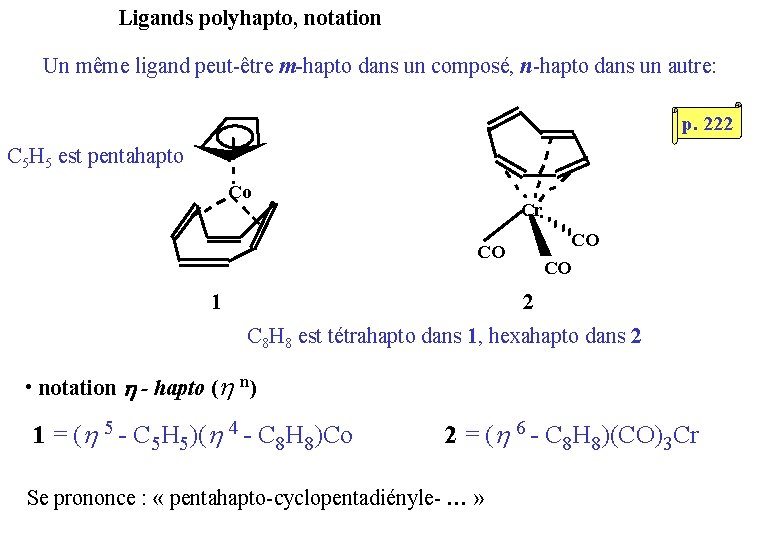
Ligands polyhapto, notation Un même ligand peut-être m-hapto dans un composé, n-hapto dans un autre: p. 222 C 5 H 5 est pentahapto Co Cr CO CO CO 1 2 C 8 H 8 est tétrahapto dans 1, hexahapto dans 2 • notation - hapto ( n) 1 = ( 5 - C 5 H 5)( 4 - C 8 H 8)Co 2 = ( 6 - C 8 H 8)(CO)3 Cr Se prononce : « pentahapto-cyclopentadiényle- … »

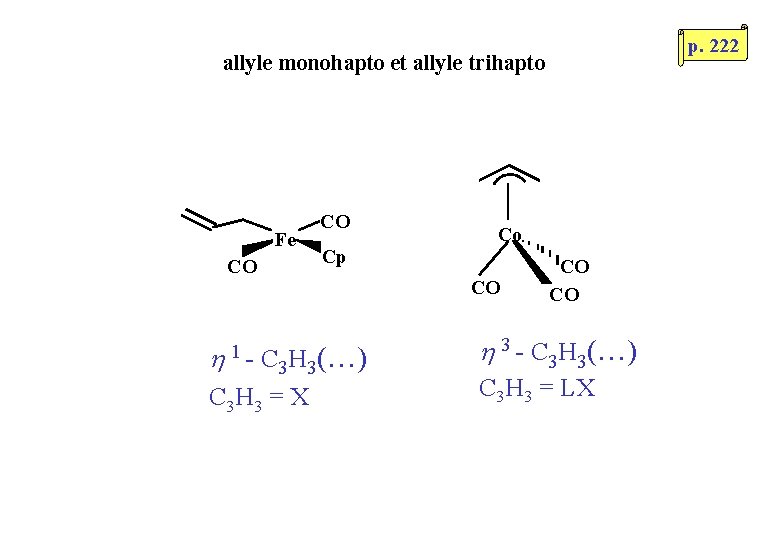
p. 222 allyle monohapto et allyle trihapto Fe CO 1 - C CO Cp Co CO 3 H 3(…) C 3 H 3 = X CO CO 3 - C 3 H 3(…) C 3 H 3 = LX

Décompte des électrons autour du métal p. 223 • Rappels de la théorie du champ cristallin - On admet que les électrons de valence du métal complexé sont dans ses orbitales d - Les ligands relèvent certaines orbitales d - Les ligands X soutirent des électrons au métal

Décompte des électrons autour du métal -Les ligands X soutirent des électrons au métal Le métal acquiert un degré d’oxydation Les électrons qui lui restent occupent son « bloc d » • Exemple: 6 élec. dans le bloc d Le bloc d contient les HO et BV du complexe p. 223

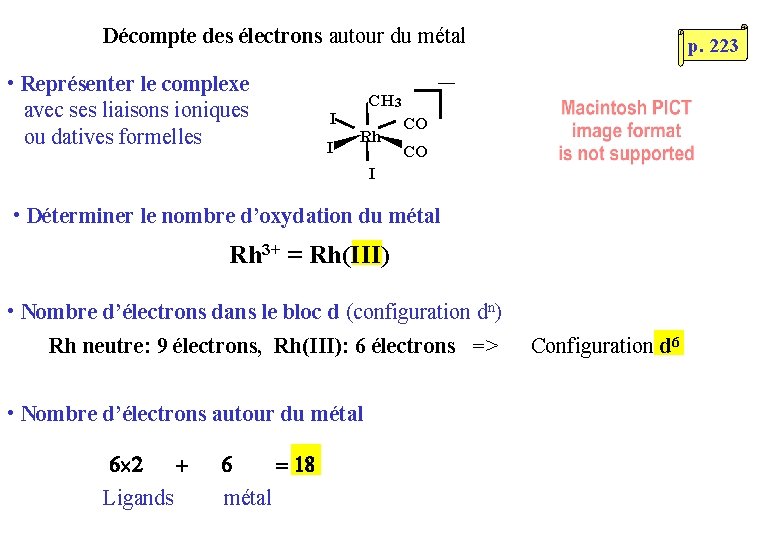
Décompte des électrons autour du métal • Représenter le complexe avec ses liaisons ioniques ou datives formelles I I — CH 3 Rh CO CO I • Déterminer le nombre d’oxydation du métal Rh 3+ = Rh(III) • Nombre d’électrons dans le bloc d (configuration dn) Rh neutre: 9 électrons, Rh(III): 6 électrons => Configuration d 6 • Nombre d’électrons autour du métal 2 Ligands métal p. 223

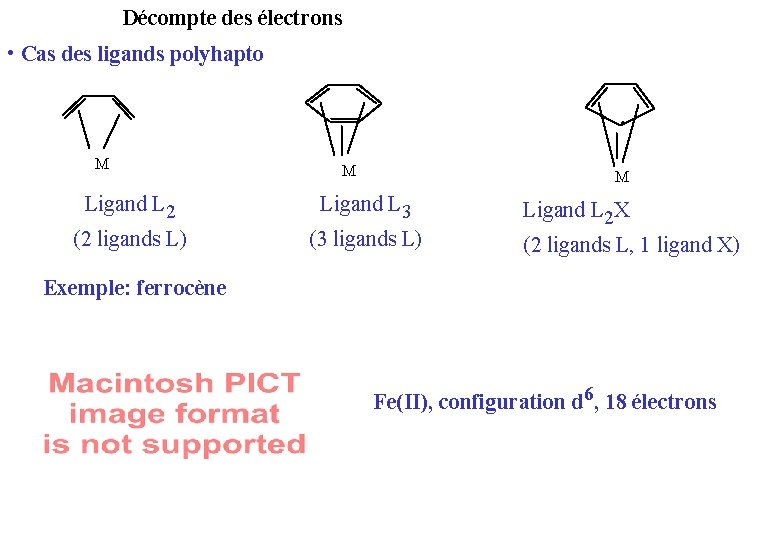
Décompte des électrons • Cas des ligands polyhapto • M M M Ligand L 2 Ligand L 3 (2 ligands L) (3 ligands L) Ligand L 2 X (2 ligands L, 1 ligand X) Exemple: ferrocène Fe(II), configuration d 6, 18 électrons

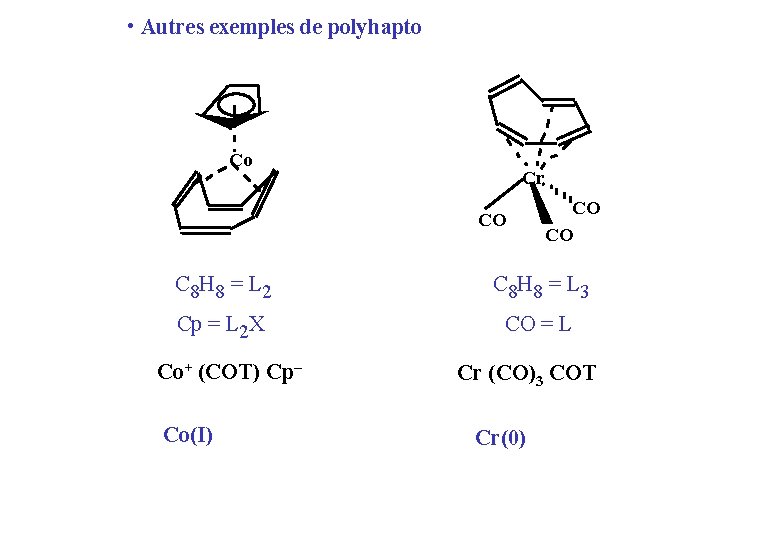
• Autres exemples de polyhapto Co Cr CO CO CO C 8 H 8 = L 2 C 8 H 8 = L 3 Cp = L 2 X CO = L Co+ (COT) Cp– Co(I) Cr (CO)3 COT Cr(0)

Application de la Théorie des OM (Théorie du champ de ligands) • Exemple: complexe octaédrique ML 6 (L = ligand monohapto) Orbitales du métal Orbitales des ligands p. 229

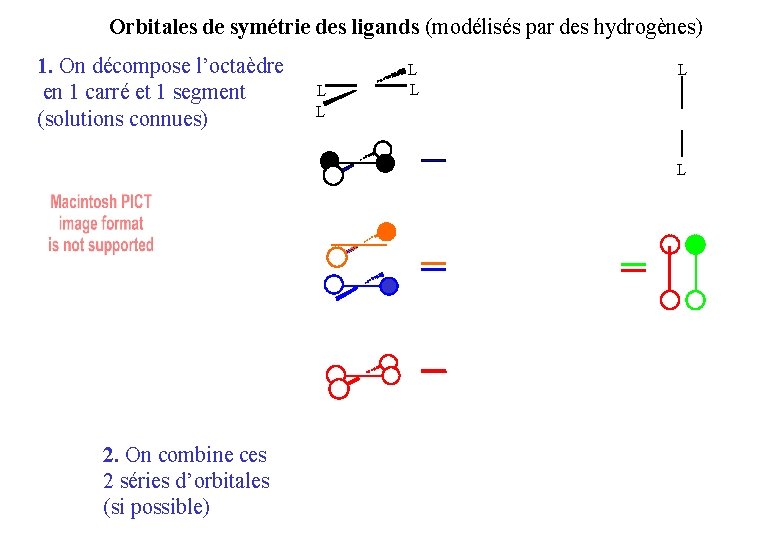
Orbitales de symétrie des ligands (modélisés par des hydrogènes) 1. On décompose l’octaèdre en 1 carré et 1 segment (solutions connues) L L L 2. On combine ces 2 séries d’orbitales (si possible)

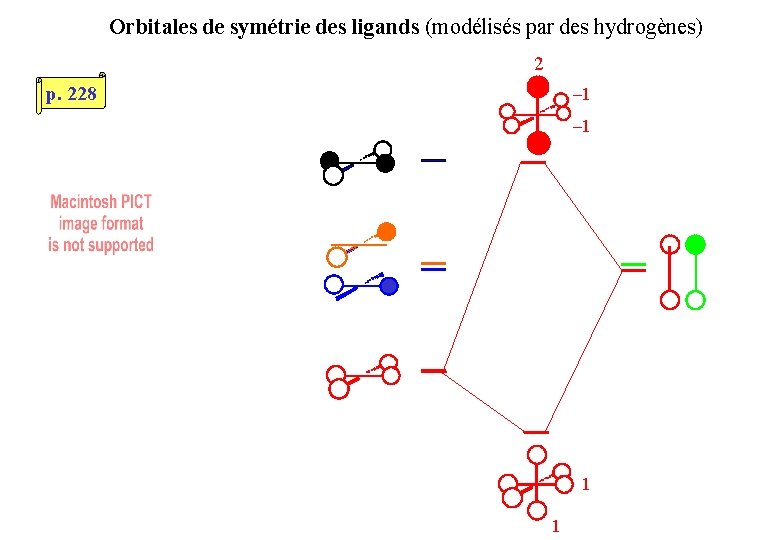
Orbitales de symétrie des ligands (modélisés par des hydrogènes) 2 p. 228 – 1 1 1

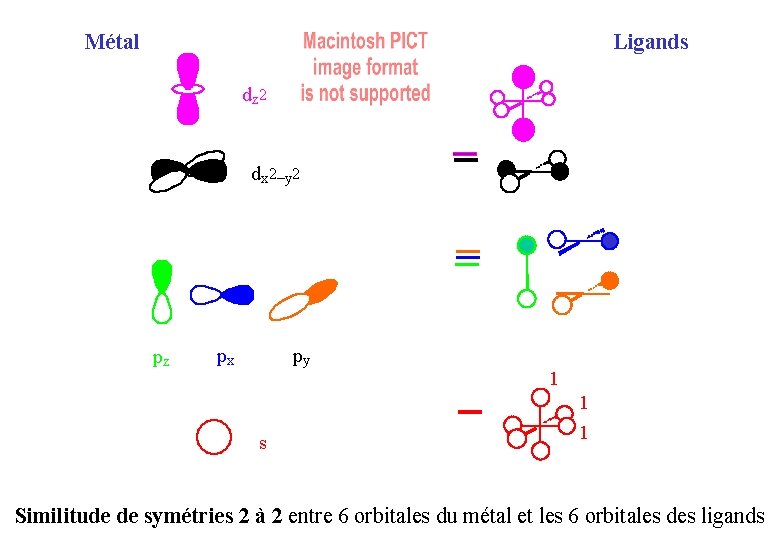
Métal Ligands dz 2 dx 2–y 2 pz px py s 1 1 1 Similitude de symétries 2 à 2 entre 6 orbitales du métal et les 6 orbitales des ligands

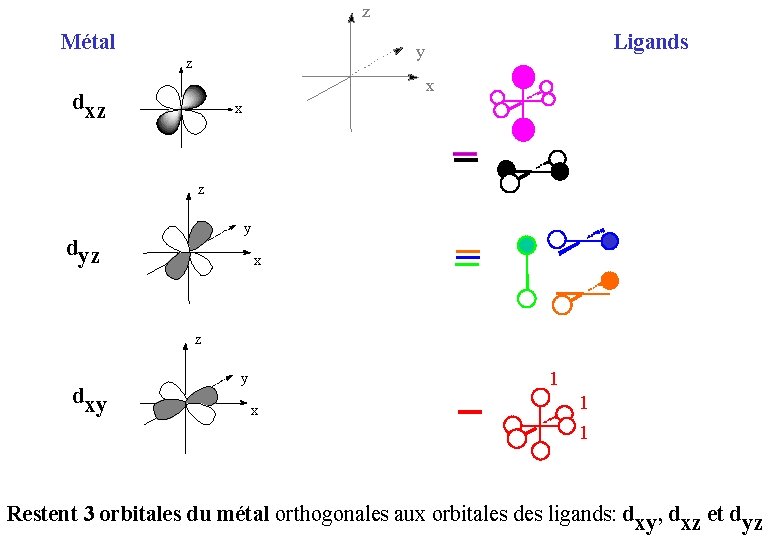
z Métal Ligands y z x dxz x z y dyz x z dxy 1 y x 1 1 Restent 3 orbitales du métal orthogonales aux orbitales des ligands: dxy, dxz et dyz

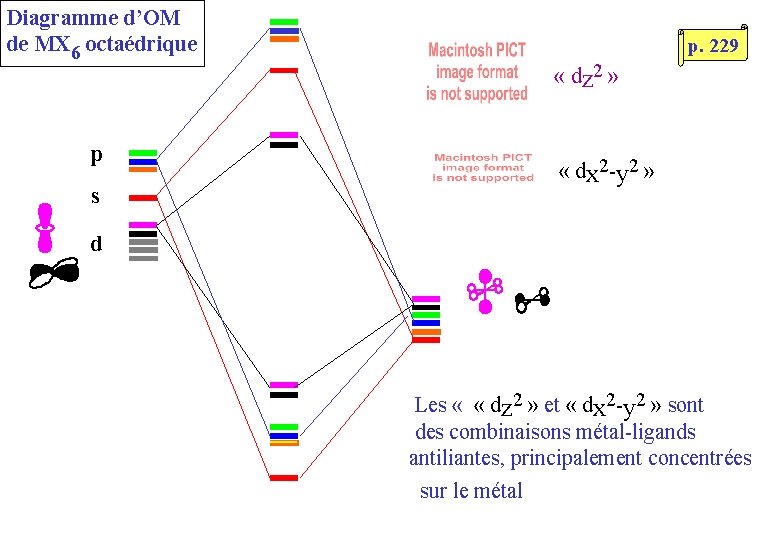
Diagramme d’OM de MX 6 octaédrique p s p. 229 « dz 2 » « dx 2 -y 2 » d Les « « dz 2 » et « dx 2 -y 2 » sont des combinaisons métal-ligands antiliantes, principalement concentrées sur le métal

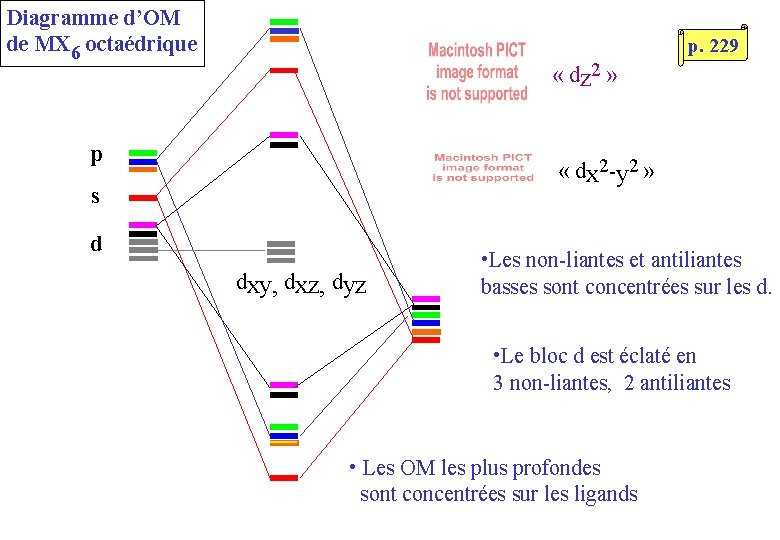
Diagramme d’OM de MX 6 octaédrique p. 229 « dz 2 » p « dx 2 -y 2 » s d dxy, dxz, dyz • Les non-liantes et antiliantes basses sont concentrées sur les d. • Le bloc d est éclaté en 3 non-liantes, 2 antiliantes • Les OM les plus profondes sont concentrées sur les ligands

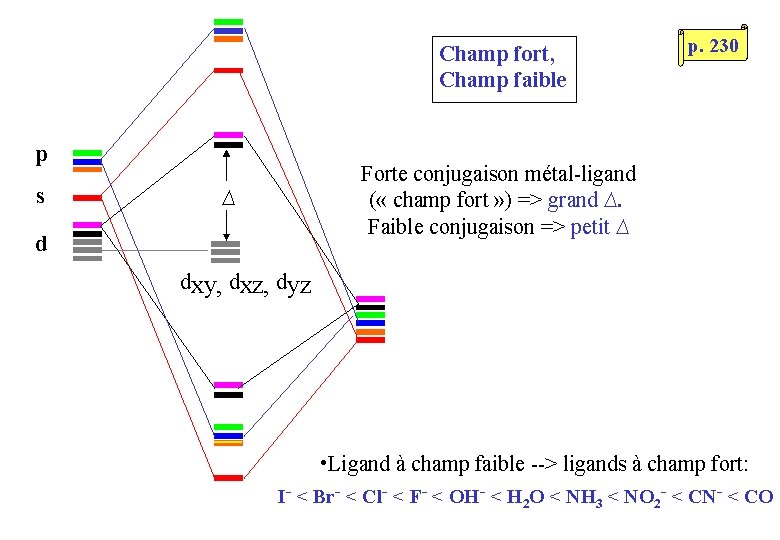
Champ fort, Champ faible p s p. 230 Forte conjugaison métal-ligand ( « champ fort » ) => grand ∆. Faible conjugaison => petit ∆ ∆ d dxy, dxz, dyz • Ligand à champ faible --> ligands à champ fort: I- < Br- < Cl- < F- < OH- < H 2 O < NH 3 < NO 2 - < CN- < CO

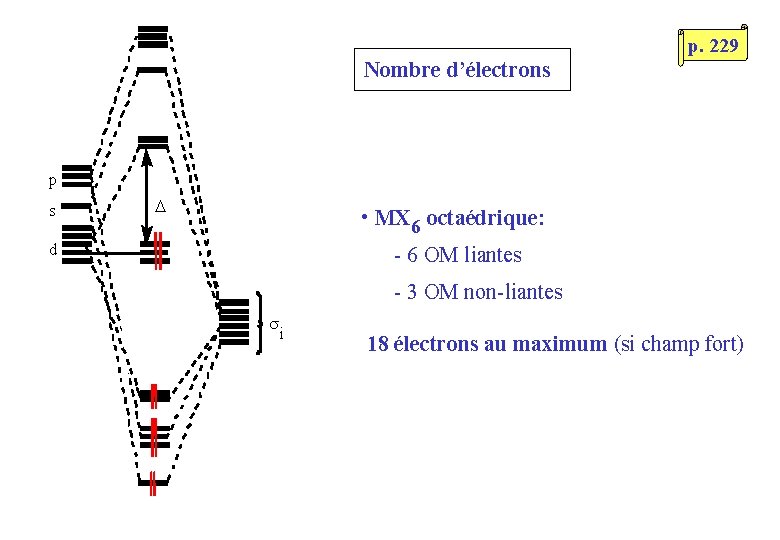
p. 229 Nombre d’électrons p s D • MX 6 octaédrique: d - 6 OM liantes - 3 OM non-liantes i 18 électrons au maximum (si champ fort)

Généralisation: règle des 18 électrons p. 225 (9 + l)OM au total • l liaisons => l OM liantes, l OM antiliantes • Restent (9 - l) non-liantes • 18 électrons liants ou non-liants • 18 électrons au maximum autour du métal • moins de 18 électrons: composés déficients en électrons, réactifs

Exception : molécules planes p. 225 • l’OA pz du métal (haute) ne participe pas • 16 électrons maximum composés toujours déficients en électrons

Molécules planes, exemples Rh(I), d 8, 16 électrons Ni(0), d 10, 16 électrons Déficient, peut accepter des ligands (partie de cycle catalytique) Rh(III), d 6, 18 électrons

Extension du raisonnement précédent: p. 225 Complexe linéaire: 14 électrons maximum

Extension du raisonnement précédent: p. 225 Complexe linéaire: 14 électrons maximum

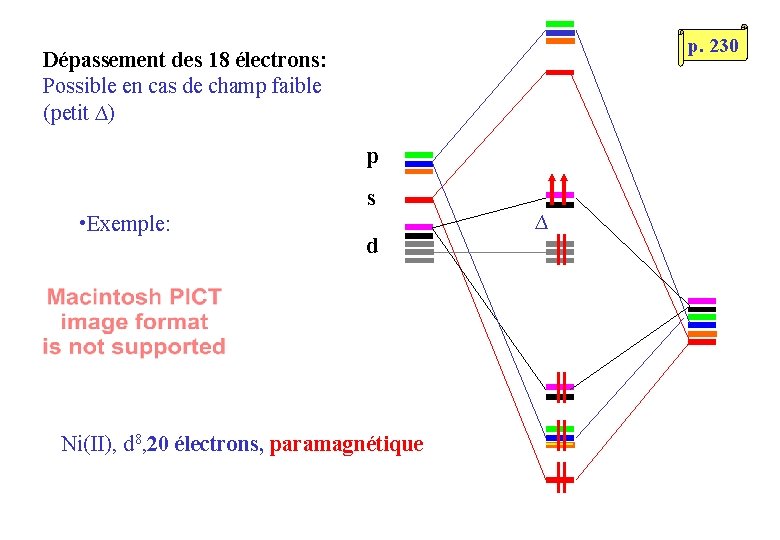
p. 230 Dépassement des 18 électrons: Possible en cas de champ faible (petit ∆) p s • Exemple: d Ni(II), d 8, 20 électrons, paramagnétique ∆

Autres géométries pp. 231 -233 Etc… Plan carré Tétraédrique Bipyramide trigonale Plan trigonal Cadre de l’étude: détermination des OM du bloc d (HO et BV du complexe)

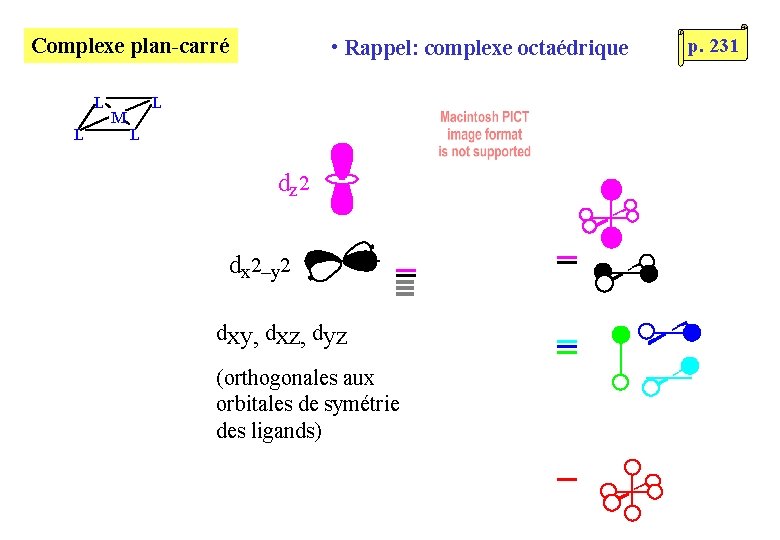
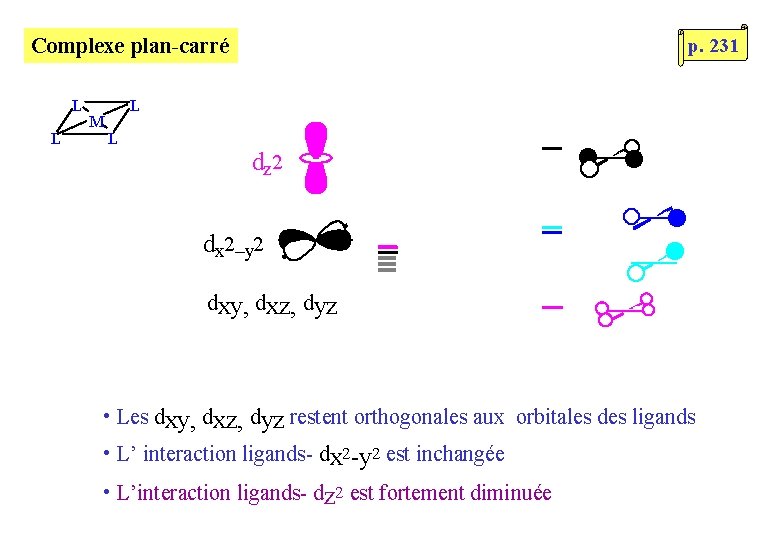
Complexe plan-carré L L M • Rappel: complexe octaédrique L L dz 2 dx 2–y 2 dxy, dxz, dyz (orthogonales aux orbitales de symétrie des ligands) p. 231

Complexe plan-carré L L M p. 231 L L dz 2 dx 2–y 2 dxy, dxz, dyz • Les dxy, dxz, dyz restent orthogonales aux orbitales des ligands • L’ interaction ligands- dx 2 -y 2 est inchangée • L’interaction ligands- dz 2 est fortement diminuée

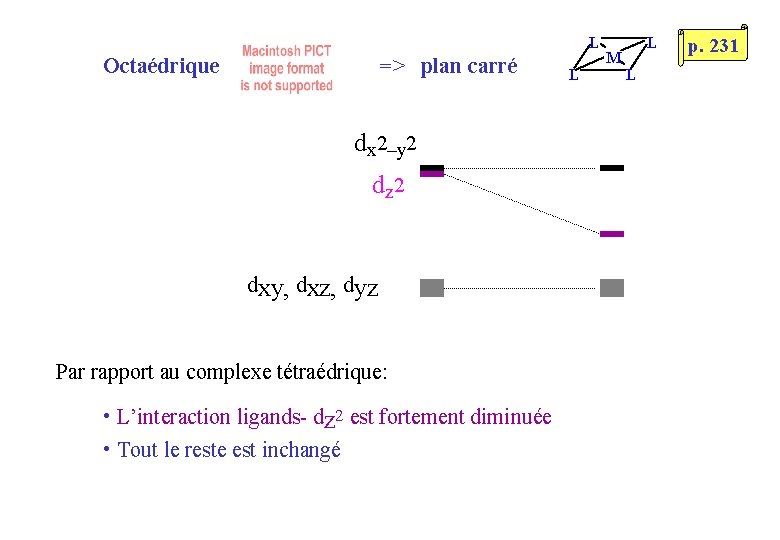
L Octaédrique => plan carré dx 2–y 2 dz 2 dxy, dxz, dyz Par rapport au complexe tétraédrique: • L’interaction ligands- dz 2 est fortement diminuée • Tout le reste est inchangé L M L L p. 231

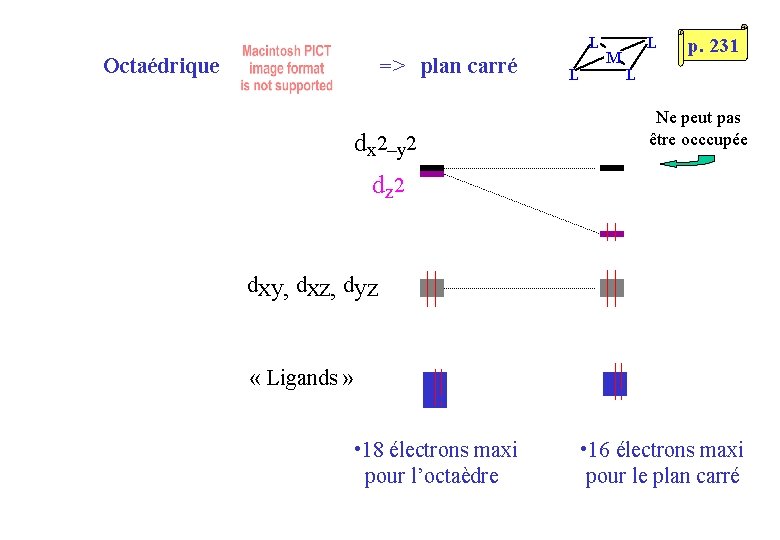
L Octaédrique => plan carré dx 2–y 2 L M L p. 231 L Ne peut pas être occcupée dz 2 dxy, dxz, dyz « Ligands » • 18 électrons maxi pour l’octaèdre • 16 électrons maxi pour le plan carré

Complexe tétraédrique p. 232 • Orbitales des ligands • Recouvrements avec la dz 2 du métal Recouvrement nul avec toutes les orbitales des ligands

Complexe tétraédrique p. 232 • Orbitales des ligands • Recouvrements avec la dxy du métal (vue aérienne) dxy orthogonale aux orbitales des ligands

Complexe tétraédrique p. 232 • Autres orbitales d du métal dxz dyz dx 2 -y 2 • Recouvrements faibles • Trois interactions équivalentes Eclatement du bloc d: Faible écart énergétique

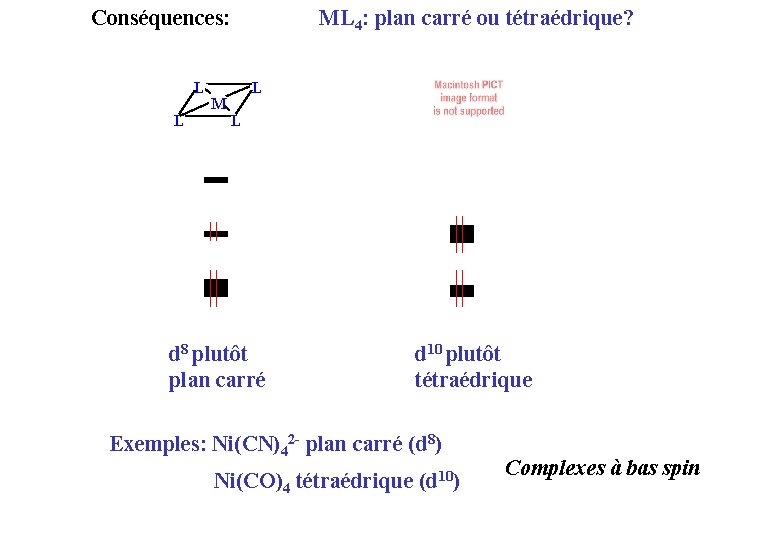
Conséquences: L L M ML 4: plan carré ou tétraédrique? L L d 8 plutôt plan carré d 10 plutôt tétraédrique Exemples: Ni(CN)42 - plan carré (d 8) Ni(CO)4 tétraédrique (d 10) Complexes à bas spin

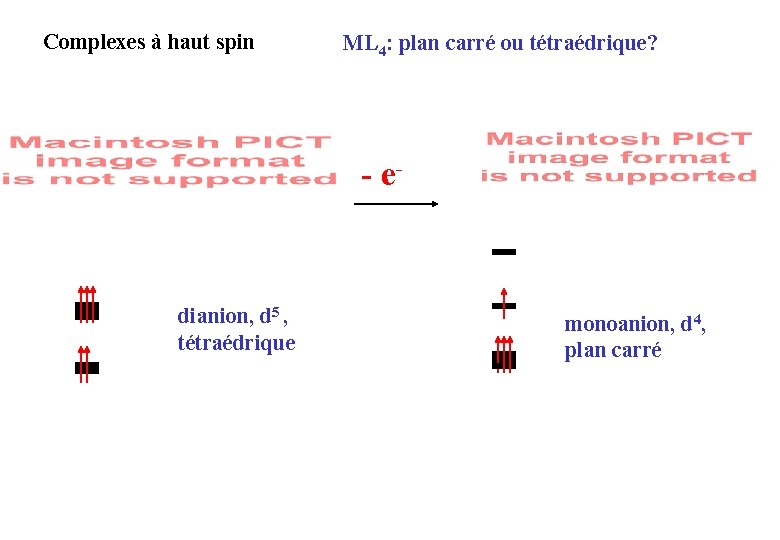
Complexes à haut spin ML 4: plan carré ou tétraédrique? - e- dianion, d 5 , tétraédrique monoanion, d 4, plan carré

Transitions de spin 1. En fonction de la température Fe(bipy)2(NCS)2 bipy = 5. 12 ( B) 0 T(°K) 130

Transitions de spin En fonction de la température Fe(bipy)2(NCS)2 bipy = Explication: Complexe d 6 octaédrique, champ faible ∆ L ’état excité est peuplé à haute température