CHIMIE Pr B CHAFIK EL IDRISSI CHIMIE EN

CHIMIE Pr: B. CHAFIK EL IDRISSI • - CHIMIE EN SOLUTION AQUEUSE • - DIAGRAMMES BINAIRES • - THERMOCHIMIE

LA CHIMIE EN SOLUTION AQUEUSE PLAN DU COURS : - RAPPELS - GENERALITES SUR LES ACIDES ET LES BASES - CALCUL DU p. H - DOSAGES ACIDO-BASIQUES - EQUILIBRE DE SOLUBILITE

RAPPELS: Soit un composé X présent dans une solution. - la concentration molaire C (mol/l): est le rapport de la quantité de matière n de X (en mol) contenue dans un certain volume de solution divisée par ce volume de solution (en L). La concentration molaire est aussi appelée molarité symbolisée par la lettre M. C (mol/l) = n/v avec n = m/Mx - la concentration massique Cm(g/l) : est le rapport de la masse de X contenu dans le volume de solution divisée par ce volume de solution. Cm(g/l)= m/v • Exercice: La formule brute du caféine est C 8 H 10 N 4 O 2 (M=194 g). Sa teneur varie selon la variété de café. Lorsque le café est dit fort, il contient 6, 55. 10 -3 mol de caféine par litre de café. • a) Combien de moles de caféine y a-t-il dans une tasse de café fort, soit 150 ml de café? • b) Quelle masse de caféine y a-t-il dans un litre de café ? • 0. 982 mmol --- 1. 27 g

Exercices: calculer la concentration molaire des solutions suivantes. a) 4, 0 g de Na. OH dissout dans 350 ml d’eau. b) 150 ml de NH 3 à 0, 2 mol/l dilués à 500 ml d’eau. c) 100 ml de HCl à 0, 03 mol/l mélangés à 100 ml de HCl à 0, 08 mol/l. On donne M(Na)=23 g; M(O)=16 g et M(H)=1 g. a- n = 0. 1 mol et c = 0. 286 mol/l b- n = 0. 03 mol et c = 0. 06 mol/l c- n 1 = 0. 003 mol et n 2 = 0. 008 mol c = nt/vt = 0. 055 mol/l nt = 0. 0011 mol donc

LES ACIDES ET LES BASES I- DEFINITIONS 1°/ Couple acide / base (Théorie de Brönsted, 1923) a) b) c) Un acide est une espèce chimique pouvant céder, au moins, un ion H+. Une base est une espèce chimique pouvant capter, au moins, un proton H+. Un couple acide / base est constitué d’un acide AH et de sa base conjuguée A- reliés par : AH ⇌ A- + H+ 2°/ Définition selon Arrhénius (1887) a) b) c) un acide est un composé chimique qui libère des ions H 3 O+ en solution aqueuse. une base est un composé chimique qui libère des ions HOen solution aqueuse. La définition selon Brönsted est plus générale, elle est valable quel que soit le solvant.

3°/ Acide fort dans l'eau Un acide est dit fort si sa réaction avec l’eau est totale en donnant des ions H 3 O+. Exemple : Les molécules de chlorure d'hydrogène HCl (gaz), acide fort, disparaissent totalement dans l'eau : HCl(gaz) + H 2 O → Cl- + H 3 O+. 2 H 2 O ⇌ HO- + H 3 O+. La solution ne contient pas de molécules HCl. 4°/ Base forte dans l'eau Une base est dite forte si sa réaction avec l’eau est totale en donnant des ions hydroxyde HO-. Exemple : On fait dissoudre dans l'eau de la soude Na. OH → Na+ + HOLa solution ne contient pas de Na. OH.

5°/ Acide faible dans l'eau Un acide est dit faible s’il réagit partiellement avec l’eau en donnant H 3 O+ : Exemple : L'acide éthanoïque CH 3 COOH (liquide) CH 3 COOH + H 2 O ⇌ CH 3 COO- + H 3 O+. 2 H 2 O ⇌ HO- + H 3 O+. Les espèces présentent en solution (en plus de l’eau) sont: CH 3 COOH, CH 3 COO- , H 3 O+ et HO-. 6°/ Base faible dans l'eau Une base est dite faible s’elle réagit partiellement avec l’eau en donnant HO- : Exemple : On fait dissoudre dans l'eau de l'éthanoate de sodium CH 3 COONa ( Na+ + CH 3 COO-). • Les ions sodium Na+ sont passifs alors que les ions éthanoates CH 3 COO-, réagissent partiellement avec l'eau en donnant des ions HO-. • CH 3 COO- + H 2 O ⇌ CH 3 COOH + HO-

7°/ Produit ionique de l'eau Toute solution aqueuse contient, entre autres, des ions H 3 O+ et des ions OH-. • Le produit [H 3 O+ ] [OH- ] = Ke c’est une constante à température donnée. À 25°c on a [H 3 O+ ] [OH- ] = 10 -14 dans toute solution aqueuse. • Une solution aqueuse est dite neutre si elle contient autant d’ions oxonium (hydronium) H 3 O+ que d’ions hydroxyde OH • Une solution est dite acide si elle contient plus d’ions H 3 O+ que d’ions OH • Une solution est dite basique si elle contient plus d’ions OHque d’ions H 3 O+
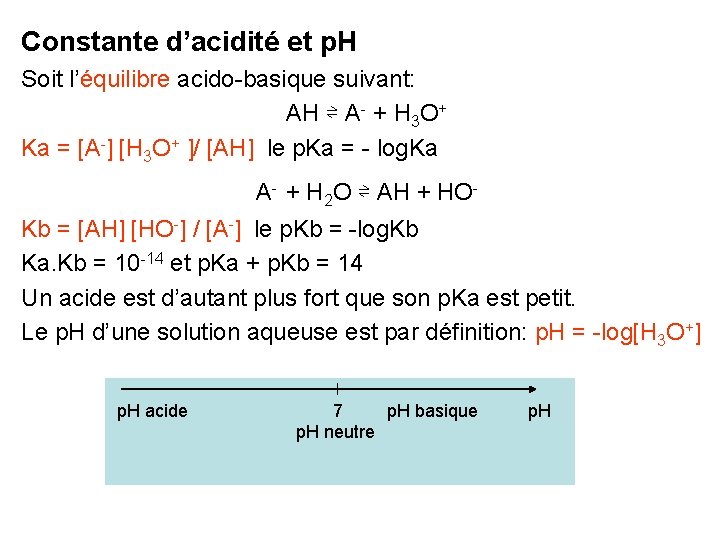
Constante d’acidité et p. H Soit l’équilibre acido-basique suivant: AH ⇌ A- + H 3 O+ Ka = [A-] [H 3 O+ ]/ [AH] le p. Ka = - log. Ka A- + H 2 O ⇌ AH + HOKb = [AH] [HO-] / [A-] le p. Kb = -log. Kb Ka. Kb = 10 -14 et p. Ka + p. Kb = 14 Un acide est d’autant plus fort que son p. Ka est petit. Le p. H d’une solution aqueuse est par définition: p. H = -log[H 3 O+] p. H acide 7 p. H basique p. H neutre p. H

p. H d’un Acide Fort Quel sera le p. H d’une solution d’un acide fort HX à la concentration C 0 mol. L-1 ? HX + H 2 O → X- + H 3 O+. Réaction totale Espèces (autres que H 2 O) présentes dans la solution : X- ; H 3 O+ et HO(HX totalement dissocié ne peut exister en solution aqueuse. ) Soit 3 inconnues à déterminer. Relations entre inconnues Electroneutralité de la solution [X-] + [OH- ] = [H 3 O+ ] Conservation de la matière C 0 = [X-] Autoprotolyse de l’eau : Ke = [H 3 O+ ] [OH- ]
![E. N : C 0 + Ke/ [H 3 O+ ] = [H 3 E. N : C 0 + Ke/ [H 3 O+ ] = [H 3](http://slidetodoc.com/presentation_image/265b178c97d014cb6d41d2f040bd6abb/image-11.jpg)
E. N : C 0 + Ke/ [H 3 O+ ] = [H 3 O+ ] C 0 [H 3 O+ ] + Ke = [H 3 O+ ]2 - C 0 [H 3 O+ ] – Ke = 0 équation de second degré à résoudre ∆ = C 0 2 + 4 Ke [H 3 O+ ] = C 0 + √ C 0 2 + 4 Ke 2 p. H = - log [H 3 O+ ] p. H = - log (C 0 + √ C 0 2 + 4 Ke) 2 Remarque: Le calcul exact du p. H est toujours possible mais il est souvent beaucoup plus simple de procéder à certaines approximations qui vont simplifier le problème.

Approximations: On étudie ici une solution d’acide fort, il paraît évident que le p. H d’une telle solution sera obligatoirement acide. Si la solution est suffisamment concentrée, elle sera fortement acide et en conséquence la concentration des ions hydroxyde sera très inférieure a celle des ions hydronium. [OH- ] ˂˂˂ [H 3 O+ ] On pourra donc négliger [OH- ] devant [H 3 O+ ] dans l’équation d’électroneutralité. E. N: [X-] + [OH- ] = [H 3 O+ ] soit [X-] = [H 3 O+ ] = C 0 p. H = - log [H 3 O+ ] = -log C 0 Cette relation est valable tant que la concentration C 0 ˃ 10 -6 M Exercices: Calculer le p. H des solutions aqueuses suivantes: a) 0, 2 mole/l de HCl. b) 1, 26. 10 -6 g/l de HNO 3 (M = 63 g/mol) a- c = 0. 02. 10 -6 p. H = 0. 69 b- p. H = 6. 95

p. H d’un acide faible Quel sera le p. H d’une solution d’un acide faible AH à la concentration C 0 mol. L-1 ? AH + H 2 O ⇌ A- + H 3 O+ Résolution exacte Espèces en solution: AH, A- , H 3 O+ et OHsoit 4 inconnues Relations entre inconnues: (1) Ka = [A-] [H 3 O+ ]/ [AH] (2) E. N: [H 3 O+ ] = [A-] + [OH- ] système à résoudre (3) C. M: C 0 = [AH] + [A-] (4) Ke = [H 3 O+ ] [OH- ] La résolution du système est possible et va conduire à une équation du troisième degré:
![[H 3 O+ ]3 + Ka [H 3 O+ ]2 + {-Ke - C [H 3 O+ ]3 + Ka [H 3 O+ ]2 + {-Ke - C](http://slidetodoc.com/presentation_image/265b178c97d014cb6d41d2f040bd6abb/image-14.jpg)
[H 3 O+ ]3 + Ka [H 3 O+ ]2 + {-Ke - C 0 Ka} [H 3 O+ ] - Ke Ka = 0 Nous devons donc résoudre une équation du troisième degré. La résolution de cette équation est tout à fait possible sans approximations, mais pour simplifier le problème nous allons utiliser 2 approximations: Approximation 1: Milieu acide [OH- ] ˂˂˂ [H 3 O+ ] E. N [H 3 O+ ] = [A-] + [OH- ] soit [H 3 O+ ] = [A-] Approximation 2: On supposera que l’acide AH est faiblement dissocié [A-] ˂˂˂ [AH] C. M: C 0 = [AH] + [A-] soit C 0 = [AH] Ka = [A-] [H 3 O+ ]/ [AH] ====˃ Ka = [H 3 O+ ]2/C 0 soit [H 3 O+ ] = √ (C 0 Ka) on sait que p. H = -log [H 3 O+ ] Le p. H d’un acide faible est donc p. H = ½ (p. Ka – log. C 0 ) Expression valable si les approximations 1 et 2 sont simultanément vérifiées

Validité des approximations Approximation 1: C 0 ˃10 -6 M Approximation 2: Ka/C 0 ˂10 -2 Si l’approximation 2 n’est pas vérifiée le p. H sera égal à: p. H = -log( –Ka + √(Ka 2 +4 Ka. C 0)) 2 Exercices: Calculer le p. H des solutions suivantes: a) 10 -2 mol/l de CH 3 COOH ( Ka = 10 -4, 8 ) b) 10 -4, 5 mol/l de CH 3 COOH a- p. H = 3. 4 C(H 3 O+) = 1. 64. 10 -5 mol/l et p. H = 4. 78

p. H des solutions basiques Pour obtenir les résultats correspondant aux solutions basiques, il suffira de remplacer p. H par p. OH et Ka par Kb dans les différentes formules de p. H. Acide fort: p. H = -log. C Base forte: p. OH = -log. C p. OH = 14 – p. H = -log. C Base forte: p. H = 14 + log. C Acide faible: p. H = ½ (p. Ka – log. C ) Base faible: p. OH = ½ (p. Kb – log. C) Sachant que p. OH + p. H = 14 et p. Ka + p. Kb = 14 on aura donc: Base faible: p. H = 7 + ½ (p. Ka + log. C ) Exercice: On dissout 1, 7 g de NH 3 gazeux dans 200 ml d’eau. Calculer le p. H de cette solution. On donne p. Ka(NH 4+/NH 3) = 9, 2 n = 0. 1 mol; c = 0. 5 M; p. Kb=4. 8 Kb/c = 3. 17. 10 -5 < 10 -2 et p. H= 11. 45

Mélange de deux acides forts On mélange deux acides forts HX et HY. Quel est le p. H de la solution obtenue ? Acide 1 (HX) : V 1 ml à la concentration C 01 mol/l Acide 2 (HY) : V 2 ml à la concentration C 02 mol/l Les deux acides forts sont totalement dissociés. Espèces présentes: X- , Y- , H 3 O+ et OH- , E. N [H 3 O+ ] = [X-] + [Y-] + [OH-] C. M 1: C 1 = [X-] = C 01 V 1 /(V 1 + V 2) C. M 2: C 2 = [Y-] = C 02 V 2 /(V 1 + V 2) Ke = [H 3 O+ ] [OH- ] En négligeant [OH-] devant [H 3 O+ ] et en posant C = C 1+ C 2 On aura [H 3 O+ ] = C 1+ C 2 = C ===˃ p. H = -log[H 3 O+ ] = -log. C Un mélange d’acides forts se comporte donc exactement comme un acide fort unique

Mélange d’un acide fort et d’un acide faible On mélange un acide fort HX et un acide faible AH. Quel est le p. H de la solution obtenue ? Acide fort (HX) : V 1 ml à la concentration C 01 mol/l Acide faible (AH) : V 2 ml à la concentration C 02 mol/l L’acide fort est totalement dissocié par contre l’acide faible l’est très peu, la quantité de H 3 O+ provenant de l’acide faible est négligeable devant celle provenant de l’acide fort. Le p. H du mélange est alors imposé par l’acide fort, d’où [H 3 O+ ] = C 1 Et p. H = -log. C 1 avec C 1 = V 1. C 01 / (V 1 + V 2) Exercice: On mélange 100 ml de HCl 1 M et 100 ml de CH 3 COOH Calculer le p. H de ce mélange. C = 0. 05 M; p. H = 0. 3

Mélange de deux acides faibles On mélange deux acides faibles HX et HY. Quel est le p. H de la solution obtenue ? Acide 1 (HX) : V 1 ml à la concentration C 01 mol/l Acide 2 (HY) : V 2 ml à la concentration C 02 mol/l Espèces présentes: HX, HY, X- , Y- , H 3 O+ et OH- , E. N [H 3 O+ ] = [X-] + [Y-] + [OH-] C. M 1: C 1 = [X-] + [HX] = C 01 V 1 /(V 1 + V 2) C. M 2: C 2 = [Y-] + [HY] = C 02 V 2 /(V 1 + V 2) Ka 1 = [X-]. [H 3 O+ ]/ [HX] Ka 2 = [Y-]. [H 3 O+ ]/ [HY] Approximation 1: Milieu acide [OH- ] ˂˂˂ [H 3 O+ ] Approximation 2: Les deux acides sont faiblement dissociés [X-] ˂˂˂ [HX] et [Y-] ˂˂˂ [YH]
![[H 3 O+ ] = [X-] + [Y-] = Ka 1. C 1/ [H [H 3 O+ ] = [X-] + [Y-] = Ka 1. C 1/ [H](http://slidetodoc.com/presentation_image/265b178c97d014cb6d41d2f040bd6abb/image-20.jpg)
[H 3 O+ ] = [X-] + [Y-] = Ka 1. C 1/ [H 3 O+ ] + Ka 2. C 2/ [H 3 O+ ] On obtient [H 3 O+] = √Ka 1 C 1 + Ka 2 C 2 Donc p. H = - 1/2 log( Ka 1 C 1 +Ka 2 C 2) Si C 1 = C 2 c’est l’acide le plus fort qui impose son p. H • Résumé • Mélange d’acides forts : • Se comporte comme un seul acide fort • Mélange de bases fortes : • Se comporte comme une seule base forte • Mélange d’acides faibles : L’acide le plus fort impose le p. H • Mélange de bases faibles : La base la plus forte impose le p. H

Solution tampon Une solution tampon est composée soit d’un acide faible AH et de sa base conjuguée A-1, soit d’une base BOH et de son cation B+. une solution tampon est une solution qui maintient approximativement le même p. H malgré l'addition de petites quantités d'un acide ou d'une base, ou malgré une dilution. Le p. H d’une solution tampon est: p. H = p. Ka + log [BASE]/ [ACIDE] Exercice: Une solution est préparée par addition de 0, 169 moles de NH 3 et de 0, 183 mole de NH 4 Cl, calculer son p. H = 9. 2 + log 0. 169/0. 183 = 8. 5

Mélanges d’acides et de bases Mélanges d’un acide fort et d’une base forte L’acide et la base sont totalement dissociés. Si l’acide et la base sont introduits en quantité stoechiométriques, le p. H sera neutre sinon il sera fonction du produit majoritaire. Exemple: Calculer le p. H des solutions aqueuses suivantes: a) Mélange de 50 ml de HCl 10 -2 M et de 50 ml de Na. OH 10 -2 M b) Mélange de 75 ml de HCl 0, 1 M et 125 ml de Na. OH 0, 2 M C(Na. OH)=0. 0875 M p. H= 12. 94 Mélange d’un acide fort et d’une base faible Si l’acide et la base sont introduits en qté stoechiométriques, le p. H de la solution est celui de l’acide faible Exemple: Calculer le p. H du mélange suivant: 50 ml de HCl 10 -2 M et 50 ml de CH 3 COONa 10 -2 M C = 5. 10 -3 M; ka/c = 0. 3110 -2; p. H = 3. 55

Mélange d’une base forte et d’un acide faible Si l’acide et la base sont introduits en quantité stoechiométriques, le p. H de la solution est celui de la base faible. Exercice: Calculer le p. H du mélange suivant: • 50 ml de Na. OH 10 -2 M et 50 ml de CH 3 COOH 10 -2 M • C = 5. 10 -3 M; p. H = 8. 25 Exercices: On mélange 100 ml d’acide acétique CH 3 COOH 0, 1 M et 100 ml de la soude Na. OH 0, 04 M ; on obtient une solution S. • 1°) Ecrire l’équation de la réaction qui s’est produite. • 2°) Comment appelle-t-on cette solution, calculer son p. H. • 3°) A la solution S on ajoute 100 ml de l’acide chlorhydrique HCl 0, 14 M. Calculer le p. H de cette nouvelle solution. • On donne p. Ka (CH 3 COOH/ CH 3 COO-) = 4, 8. • 1/p. H=4. 62 3/c = 0. 033 M et p. H= 1. 48

Dosages (ou Titrages) acido-basiques. 1. Equivalence acido-basique. Dans le cas où chaque molécule d’acide (ou de base) libère (ou capte) un ou plusieurs protons, l’équation-bilan du dosage s’écrit : [ acide(1) + λa H 2 O <====> base(1) + λa. H 3 O+ ] x λb [ base(2) + λb H 3 O+ <====> acide(2) + λb H 2 O ] x λa λb acide(1) + λa base(2) <====> λb base (1) + λa acide(2) avec : λa = nombre de protons libérés par une mole d’acide, et λb = nombre de protons fixés par une mole de base. A l’équivalence, le nombre de protons libérés par l’acide(1), est égal au nombre de protons fixés par la base(2) : λa. Ca. Va = λb Cb. Vb

Exemple 1: Dosage de la 1ère acidité de H 3 PO 4 par la base forte OH-. 1 H 3 PO 4 + 1 OH- → H 2 PO-4 + H 2 O λa = 1 et λb = 1 A la première équivalence λa CH 3 PO 4 VH 3 PO 4 = λb COH-VOHExemple 2: Volume de base forte versé à l’équivalence globale (3 e acidité de H 3 PO 4 : 3 protons mis en jeu par mole d’acide) : 1 H 3 PO 4 + 3 OH- → PO 3 -4 + 3 H 2 O λa = 3 et λb = 1 A l’équivalence globale on a: λa CH 3 PO 4 VH 3 PO 4 = λb COH-VOH- Donc: 3 n. H 3 PO 4(initial) = 1 n. OH-(équivalence) 2. Dosage d’un acide fort par une base forte HCl + H 2 O →Cl- + H 3 O+ Na. OH →Na+ + OHLes ions Cl- et Na+ étant indifférents, la réaction globale qui se produit est donc : H 3 O + OH- → 2 H 2 O
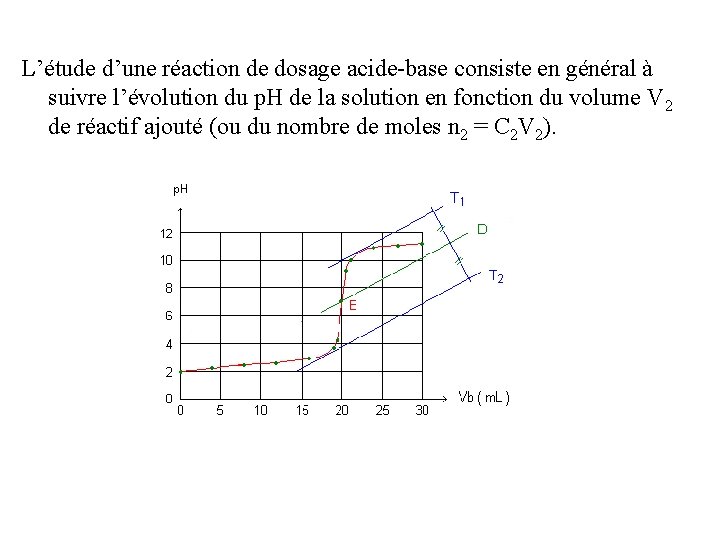
L’étude d’une réaction de dosage acide-base consiste en général à suivre l’évolution du p. H de la solution en fonction du volume V 2 de réactif ajouté (ou du nombre de moles n 2 = C 2 V 2).

3. Dosage d’une base forte par un acide fort Des calculs tout à fait similaires permettent de déterminer le p. H au cours du dosage. On obtient le graphe suivant: 4. Dosage d’un acide faible par une base forte L’équation-bilan de la réaction de dosage entre l’acide faible HA et la base forte OH- s’écrit : AH + OH- → A- + H 2 O Exemple: CH 3 COOH + OH- → CH 3 COO- + H 2 O
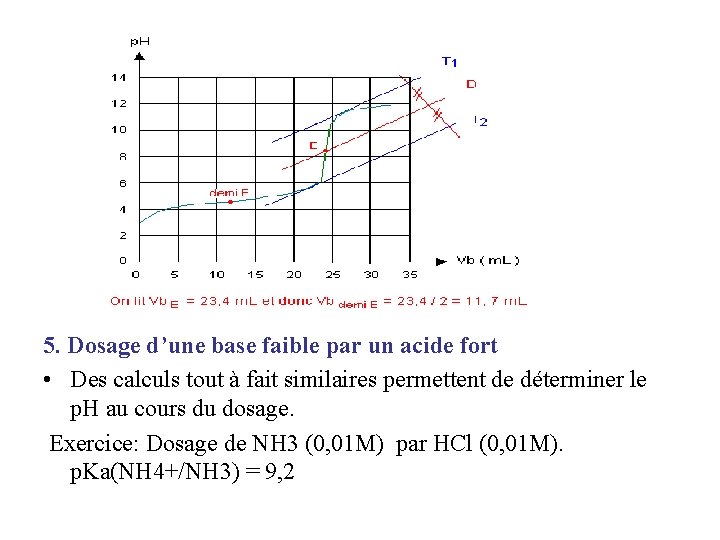
5. Dosage d’une base faible par un acide fort • Des calculs tout à fait similaires permettent de déterminer le p. H au cours du dosage. Exercice: Dosage de NH 3 (0, 01 M) par HCl (0, 01 M). p. Ka(NH 4+/NH 3) = 9, 2

EQUILIBRE DE SOLUBILITE 1) Solubilité et produit de solubilité Certains sels ou hydroxydes sont peu solubles dans l’eau : Ag. Cl ; Pb. Cl 2 ; Ba. SO 4 ; Al(OH)3 ; Ca(OH)2 ; Ag(OH). . . On parle d’un équilibre de dissolution où deux phases coexistent : la phase aqueuse qui contient les ions solvatés dissous et la phase solide. Solubilité s (en mol. L-1) : nombre maximal de moles d’un sel pouvant être dissoutes dans un litre d’eau. On obtient alors une solution saturée, si on ajoute du solide : la solubilité reste inchangée. Exemple: Ag. Cl (solide) ⇌ Ag+aq + Cl-aq La constante de cet équilibre est Ks = [Ag+]. [Cl-] c’est le produit de solubilité (sans unité). Ks(Ag. Cl) = 1. 8. 10 -10 à 25°c

2) Relation entre Ks et s Exemple 1: Ag. Cl (solide) ⇌ Ag+aq + Cl-aq t = 0 0 0 téquil s s Ks = [Ag+]. [Cl-] = s 2 ===> s = (Ks)1/2 soit s = (1. 8. 10 -10)1/2 = 1, 3. 10 -5 mol/l Exemple 2: Al(OH)3(solide) ⇌ t = 0 téquil Al 3+aq + 3 OH-aq 0 0 s 3 s Ks = [Al 3+]. [OH-]3 = s. (3 s)3 = 27 s 4 = 3. 10 -34 ====> s = 1, 8. 10 -9 mol/l

Exemple 3: Un malade souffre d’un calcul rénal dont la masse est de 0, 384 g. On suppose qu’il est entièrement constitué d’oxalate de calcium Ca. C 2 O 4 dont le Ks = 3, 6. 10 -9. Calculer le volume d’eau nécessaire pour le dissoudre. La masse molaire M = 128, 1 g. Correction: Ca. C 2 O 4 ⇌ Ca 2+ + C 2 O 42 -. s s Ks = s 2 s = (Ks)1/2 = 6, 0. 10 -5 mol/l. =====> s’ = s. M = 7, 68. 10 -3 g/l Le volume nécessaire pour dissoudre 0, 384 g de Ca. C 2 O 4 est: v = 0, 384/s’ ====> v = 50 l.

3) Effet de l’addition d’un ion commun sur la solubilité. Soit un litre d’une solution saturée de Ag. Cl (solide) ⇌ Ag+aq + Cl-aq A cette solution on ajoute des ions Cl- sous forme de Na. Cl solide (le volume reste 1 L). • D’après le principe de modération de Le Châtelier, l’équilibre se déplace dans le sens -1 (de droite vers la gauche) vers la formation de Ag. Cl(s), la solubilité de Ag. Cl en présence de Na. Cl va donc DIMINUER. Exemple: si on ajoute 10 -2 mole de Na. Cl à un litre d’une solution saturée de Ag. Cl. Ag. Cl (solide) ⇌ Ag+aq + Cl-aq t = 0 0 10 -2 téquil s’ (s’ + 10 -2) Ks = [Ag+]. [Cl-] = s’. (s’ + 10 -2)

Or on a vu que dans l’eau la solubilité s de (Ag. Cl) = 1, 3. 10 -5 mol/l Puisque s’ < s on peut négliger s’ devant 10 -2 D’où Ks = s’. 10 -2 ===> s’ = 1, 8. 10 -8 mol/l 4) Influence du p. H Solubilité de Mg(OH) 2 dans un litre d’eau. Mg(OH)2(solide) ⇌ Mg 2+aq + 2 OH-aq t = 0 0 0 téquil s 2 s Ks = [Mg 2+]. [OH-]2 = 1, 5. 10 -11 Ks = [Mg 2+]. [OH-]2 = s. (2 s)2 s = (Ks/4)1/3 = 1, 6. 10 -4 mol/l ====>[OH-] = 2 s = 3, 2. 10 -4 mol/l Ke = [H 3 O+] [OH-] = 10 -14 p. H = 14 + log[OH-] = 10, 5

Donc à toute variation du p. H, on a une modification de la solubilité de l’hydroxyde Mg(OH) 2 Comment évolue la solubilité de Mg(OH) 2 dans un milieu moins basique ? Si p. H ===>[OH-] l’équilibre de dissolution de Mg(OH) 2 se déplace dans le sens 1 (de gauche vers la droite) ===> vers la dissolution de Mg(OH) 2 ===> la solubilité augmente. Exercices: 1) Calculer la solubilité s en g/l des composés suivants: Sr. SO 4 ( Ks = 3, 6. 10 -7 ) et M = 183, 6 g/mol Ag 2 Cr. O 4 ( Ks = 3, 6. 10 -12 ) et M = 332 g/mol 2) Calculer la solubilité s de l’acétate d’argent Ag. CH 3 CO 2 : a) Dans l’eau pure

b) Dans 100 ml d’une solution contenant 5 g d’acétate de Sodium Na. CH 3 COO On donne: Ks(Ag. CH 3 COO) = 2. 10 -3 ; M(Na. CH 3 COO) = 82 g/mol 3) A une solution contenant des ions Cl- à la concentration 0, 1 M et des ions Cr. O 4 -2 à la concentration 0, 1 M; on ajoute Ag. NO 3 (sel totalement dissocié) sans changement de volume. a) Quel est le corps qui précipitera le premier Ag. Cl ou Ag 2 Cr. O 4 b) calculer la concentration des ions Cl- lorsque Ag 2 Cr. O 4 commence à précipiter. On donne: Ks 1(Ag. Cl) = 1, 8. 10 -10 ; Ks 2(Ag 2 Cr. O 4 ) = 1, 6. 10 -12.
- Slides: 35