Bab 13 Sifatsifat Fisis Larutan Larutan adalah campuran

Bab 13 Sifat-sifat Fisis Larutan

Larutan adalah campuran homogen dari dua atau lebih zat Zat yang jumlahnya lebih sedikit disebut zat terlarut Zat yang jumlahnya lebih banyak disebut zat pelarut. 13. 1

Larutan jenuh mengandung jumlah maksimum zat terlarut yang dapat larut dalam suatu pelarut pada suhu tertentu. Larutan takjenuh mengandung zat terlarut lebih sedikit daripada yang sebenarnya dapat dilarutkan oleh pelarut pada suhu tertentu. Larutan lewat-jenuh mengandung zat terlarut lebih banyak daripada yang terdapat dalam larutan jenuh pada suhu tertentu. Natrium asetat mengkristal dengan cepat ketika ditambahkan sedikit benih kristal ke dalam larutan natrium asetat lewat-jenuh. 13. 1

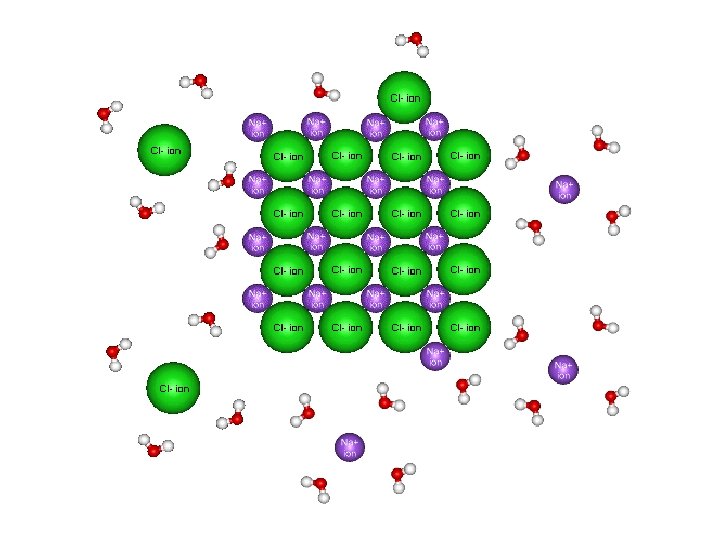
“sejenis melarutkan sejenis” Dua zat dengan gaya-gaya antarmolekul yang sama akan cenderung saling melarutkan. • molekul non-polar dapat larut dalam pelarut non-polar CCl 4 dalam C 6 H 6 • molekul polar dapat larut dalam pelarut polar C 2 H 5 OH dalam H 2 O • Senyawa ionik lebih dapat larut dalam pelarut polar Na. Cl dalam H 2 O atau NH 3 (l) 13. 2
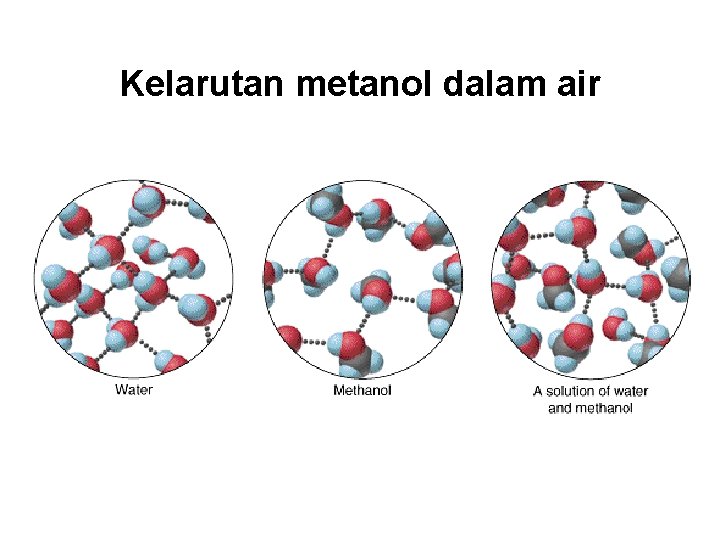
Kelarutan metanol dalam air

Memprediksi kelarutan relatif suatu zat Soal: Di dalam pelarut yang manakah tiap-tiap zat terlarut di bawah ini akan dapat lebih larut? (a) Natrium klorida dalam metanol(CH 3 OH) atau dalam propanol (CH 3 CH 2 OH). (b) Etilena glikol(HOCH 2 OH) dalam air atau dalam heksana (CH 3 CH 2 CH 2 CH 3). (c) Dietil eter(CH 3 CH 2 OCH 2 CH 3) dalam etanol(CH 3 CH 2 OH) atau dalam air.

Satuan-satuan Konsentrasi suatu larutan adalah banyaknya zat terlarut dalam sejumlah tertentu pelarut atau larutan. Persen berdasar Massa massa zat terlarut % massa = massa zat terlarut + massa pelarut x 100% massa zat terlarut x 100% = massa larutan Fraksi Mol (X) mol zat A XA = jumlah mol seluruh komponen 13. 3
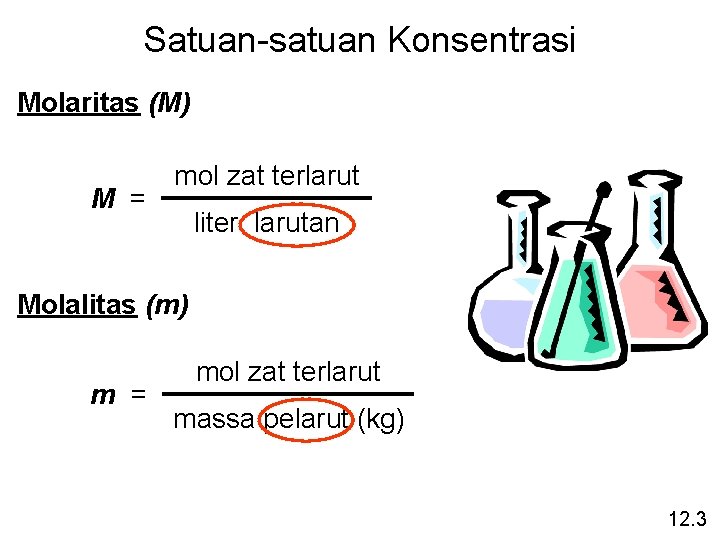
Satuan-satuan Konsentrasi Molaritas (M) M = mol zat terlarut liter larutan Molalitas (m) m = mol zat terlarut massa pelarut (kg) 12. 3

Menghitung Molalitas Soal: Hitunglah molalitas suatu larutan yang dibuat dengan cara melarutkan 75, 0 g Ba(NO 3)2 (s) ke dalam 374, 00 g air pada 250 C. Solusi: massa molar Ba(NO 3)2 = 261, 32 g/mol 75, 0 g Ba(NO 3)2 x 1 mol 261, 32 g molalitas = 0, 28700 mol 0, 37400 kg = 0, 28700 mol = 0, 76739 m = 0, 767 m

Mengkonversi satuan-satuan konsentrasi Soal: konsentrasi asam klorida komersial adalah 11, 8 M dan memiliki kerapatan 1, 190 g/ml. Hitunglah (a) % massa HCl, (b) molalitas and (c) fraksi mol dari HCl. Hitunglah molaritas dari 1, 74 m larutan sukrosa (C 12 H 22 O 11) yang kerapatannya 1, 12 g/m. L.

Berapakah molalitas dari 5, 86 M larutan etanol (C 2 H 5 OH) yang kerapatannya 0, 927 g/m. L? m = mol zat terlarut massa pelarut(kg) M = mol zat terlarut liter larutan Misalkan 1 L larutan: 5, 86 mol etanol = 270 g etanol 927 g larutan (1000 m. L x 0, 927 g/m. L) massa pelarut = massa larutan – massa zat terlarut = 927 g – 270 g = 657 g = 0, 657 kg m = mol zat terlarut massa pelarut (kg) = 5, 86 mol C 2 H 5 OH 0, 657 kg pelarut = 8, 92 m 13. 3
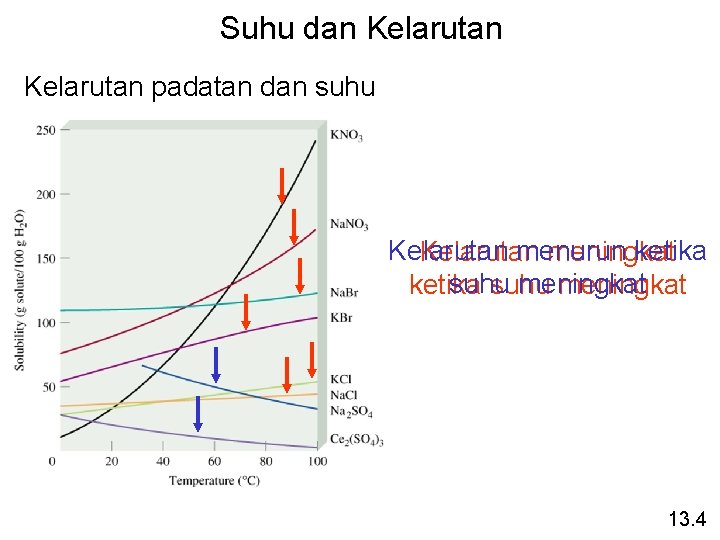
Suhu dan Kelarutan padatan dan suhu Kelarutan menurun ketika Kelarutan meningkat suhu meningkat ketika suhu meningkat 13. 4
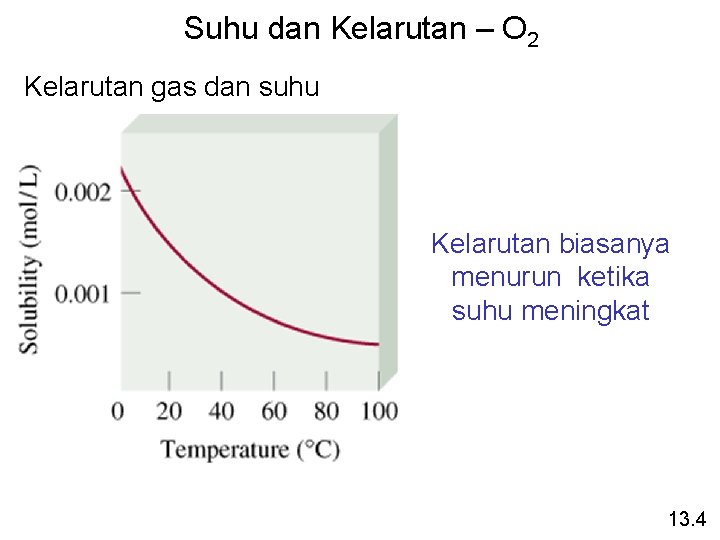
Suhu dan Kelarutan – O 2 Kelarutan gas dan suhu Kelarutan biasanya menurun ketika suhu meningkat 13. 4
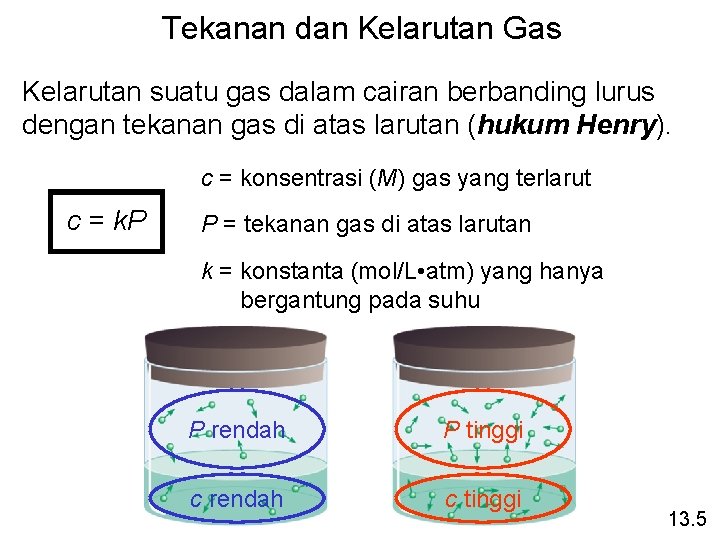
Tekanan dan Kelarutan Gas Kelarutan suatu gas dalam cairan berbanding lurus dengan tekanan gas di atas larutan (hukum Henry). c = konsentrasi (M) gas yang terlarut c = k. P P = tekanan gas di atas larutan k = konstanta (mol/L • atm) yang hanya bergantung pada suhu P rendah P tinggi c rendah c tinggi 13. 5

TA p 414

Sifat-sifat Koligatif Sifat-sifat larutan yang bergantung pada banyaknya partikel (atom, molekul, ion) zat terlarut dan tidak begantung pada jenis zat terlarut I) Penurunan Tekanan-Uap - Hukum Raoult II ) Kenaikan Titik-Didih III ) Penurunan Titik-Beku IV ) Tekanan Osmotik

Sifat Koligatif Larutan Nonelektrolit Sifat koligatif adalah sifat yang bergantung hanya pada banyaknya partikel zat terlarut dalam larutan dan tidak bergantung pada jenis partikel zat pelarut. Penurunan Tekanan-Uap P 1 = X 1 P 0 1 Hukum Raoult P 10 = tekanan uap pelarut murni X 1 = fraksi mol pelarut Jika larutan hanya mengandung satu zat terlarut: X 1 = 1 – X 2 P 10 - P 1 = DP = X 2 P 10 X 2 = fraksi mol zat terlarut 13. 6
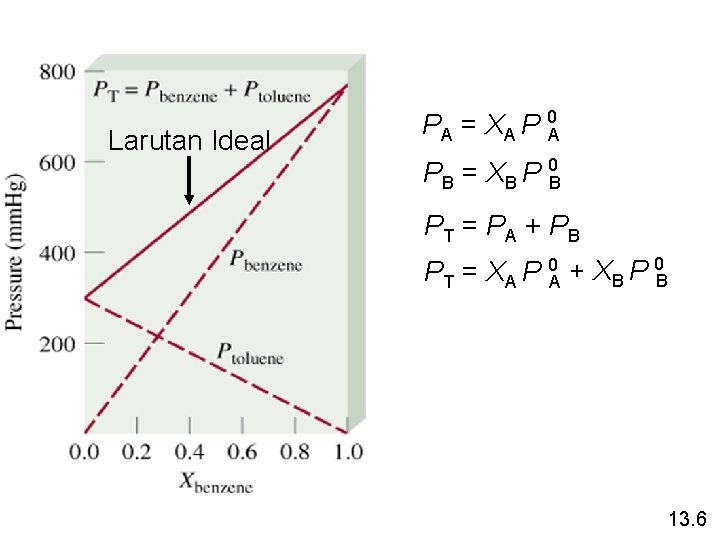
Larutan Ideal PA = XA P 0 A PB = XB P 0 B PT = PA + PB PT = XA P 0 A + XB P 0 B 13. 6
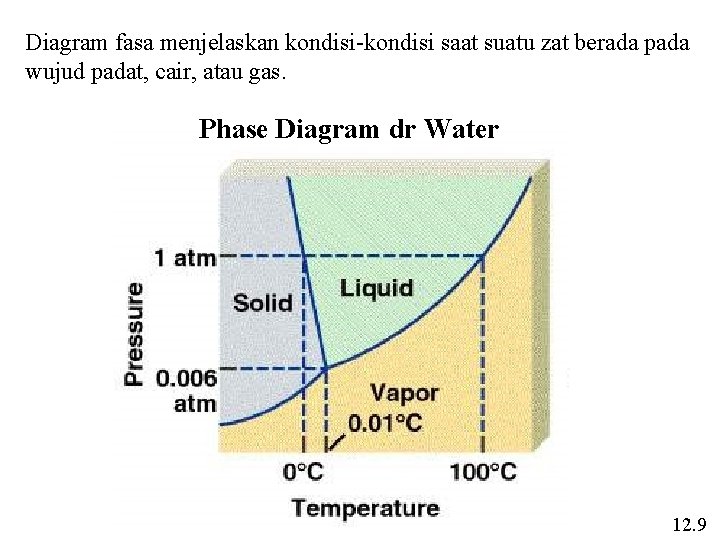
Diagram fasa menjelaskan kondisi-kondisi saat suatu zat berada pada wujud padat, cair, atau gas. Phase Diagram dr Water 12. 9
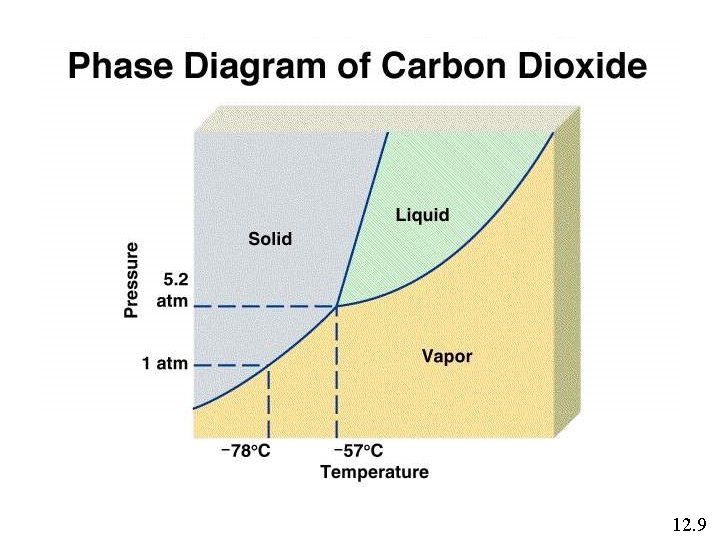
12. 9
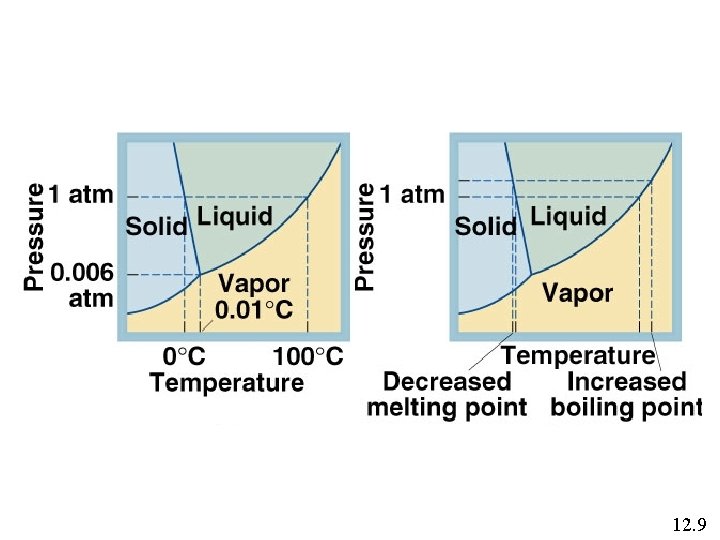
12. 9

Kenaikan Titik-Didih DTb = Tb – T b 0 adalah titik didih pelarut murni T b adalah titik didih larutan Tb > T b 0 DTb > 0 DTb = Kb m m adalah molalitas larutan Kb adalah konstanta kenaikan titik-didih molal (0 C/m) 13. 6
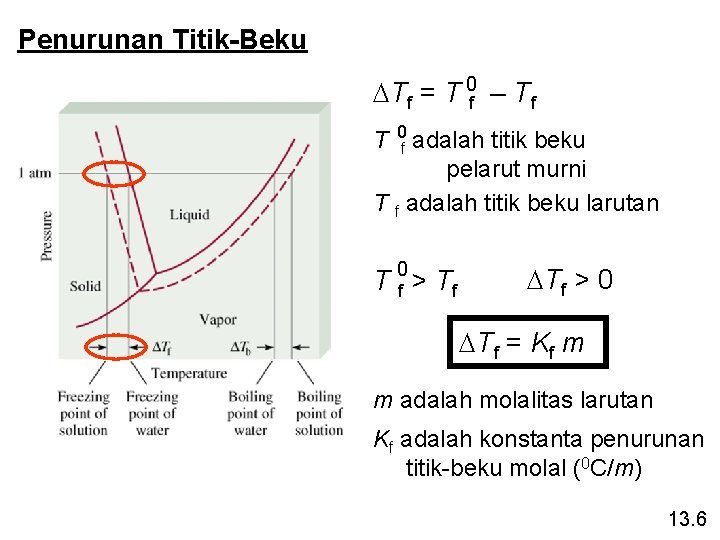
Penurunan Titik-Beku DTf = T 0 f – Tf T 0 adalah titik beku pelarut murni T f adalah titik beku larutan f T 0 f > Tf DTf > 0 DTf = Kf m m adalah molalitas larutan Kf adalah konstanta penurunan titik-beku molal (0 C/m) 13. 6
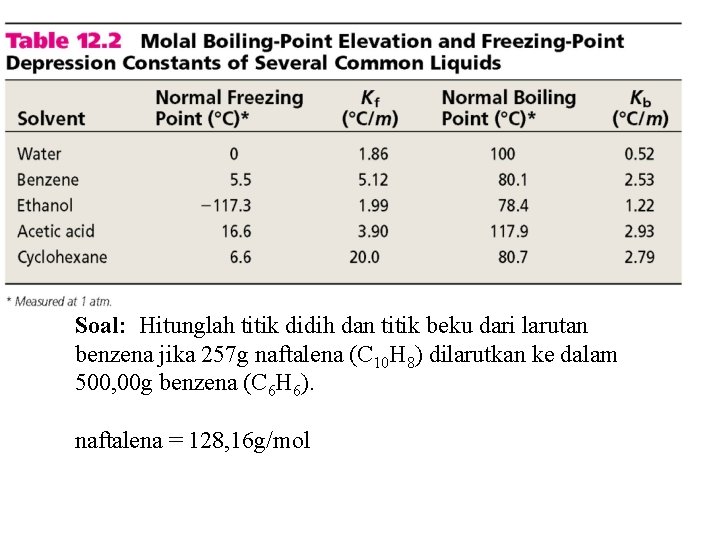
Soal: Hitunglah titik didih dan titik beku dari larutan benzena jika 257 g naftalena (C 10 H 8) dilarutkan ke dalam 500, 00 g benzena (C 6 H 6). naftalena = 128, 16 g/mol

Berapakah titik beku suatu larutan yang mengandung 478 g etilena glikol (antibeku) dalam 3202 g air? Massa molar etilena glikol adalah 62, 01 g. DTf = Kf m m = Kf air = 1, 86 0 C/m mol zat terlarut massa pelarut (kg) 478 g x = 1 mol 62, 01 g 3, 202 kg pelarut = 2, 41 m DTf = Kf m = 1, 86 0 C/m x 2, 41 m = 4, 48 0 C Tf = -4, 48 0 C 13. 6
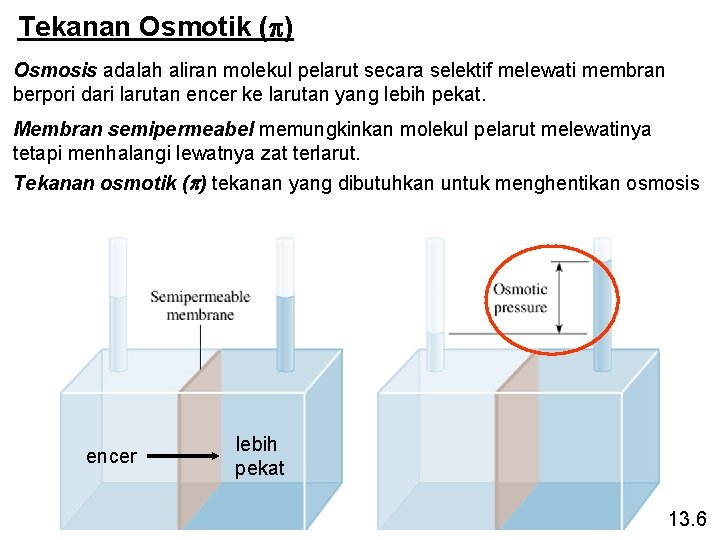
Tekanan Osmotik (p) Osmosis adalah aliran molekul pelarut secara selektif melewati membran berpori dari larutan encer ke larutan yang lebih pekat. Membran semipermeabel memungkinkan molekul pelarut melewatinya tetapi menhalangi lewatnya zat terlarut. Tekanan osmotik (p) tekanan yang dibutuhkan untuk menghentikan osmosis encer lebih pekat 13. 6
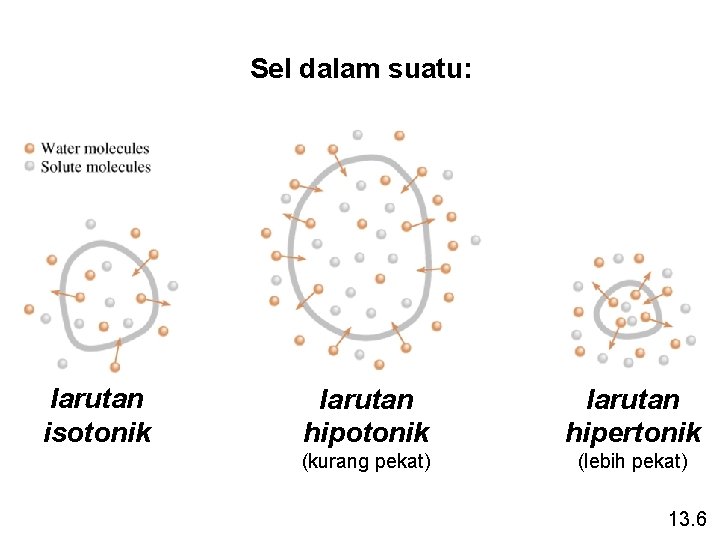
Sel dalam suatu: larutan isotonik larutan hipertonik (kurang pekat) (lebih pekat) 13. 6

Menentukan Massa Molar dari Tekanan Osmotik Soal: seorang dokter yang meneliti sejenis hemoglobin melarutkan 21, 5 mg protein dalam air pada 5, 00 C hingga terbentuk 1, 5 ml larutan dengan tujuan untuk menghitung tekanan osmotiknya. Pada kesetimbangan, larutan tersebut memiliki tekanan osmotik sebesar 3, 61 torr. Berapakah massa molar hemoglobin tersebut? Petunjuk: Kita ketahui tekanan osmotik ( ), R, dan T. Kita konversi dari torr ke atm dan T dari 0 C ke K dan gunakan persamaan tekanan osmotik untuk mencari molaritas(M). Kemudian kita hitung mol hemoglobin dari volume dan gunakan massa untuk mencari M. Solusi: P = 3, 61 torr x 1 atm = 0, 00475 atm 760 torr Suhu = 5, 00 C + 273, 15 = 278, 15 K

Menentukan Massa Molar dari Penurunan Titik Beku Soal: 7, 85 g sampel suatu senyawa dengan rumus empiris C 5 H 4 dilarutkan dalam 301 g benzena murni. Titik didihnya adalah 4, 50 °C. Berapakah massa molar dan apakah rumus molekul dari senyawa tersebut?

Sifat-sifat Koligatif Larutan Nonelektrolit Sifat koligatif adalah sifat yang bergantung hanya pada banyaknya partikel zat terlarut dalam larutan dan tidak bergantung pada jenis partikel zat pelarut. Penurunan Tekanan-Uap P 1 = X 1 P 1 o Kenaikan Titik-Didih DTb = Kb m Penurunan Titik-Beku DTf = Kf m Tekanan Osmotik (p) p = MRT 13. 6

Sifat-sifat Koligatif Larutan Ionik Untuk larutan ionik, banyaknya ion yang ada harus diperhitungkan i = faktor van’t Hoff atau banyaknya ion yang ada Untuk penurunan tekanan uap: P = i Xterlarut. P 0 pelarut Untuk kenaikan titik didih: T b = i Kb m Untuk penurunan titik beku: T f = i Kf m Untuk tekanan osmotik: im = konsentrasi partikel = i MRT

Sifat Koligatif Larutan Elektrolit 0, 1 m larutan Na. Cl 0, 1 m Na+ ion & 0, 1 m Cl- ion Sifat koligatif adalah sifat yang bergantung hanya pada jumlah partikel zat terlarut dalam larutan dan tidak bergantung pada jenis partikel zat pelarut. 0, 1 m larutan Na. Cl faktor van’t Hoff(i) = 0, 2 m ion dalam larutan jumlah partikel sebenarnya dalam lar. setelah penguraian jumlah satuan rumus yang semula terlarut dalam larutan i seharusnya nonelektrolit Na. Cl Ca. Cl 2 1 2 3 13. 6

Sifat Koligatif Larutan Elektrolit Kenaikan Titik-Didih DTb = i Kb m Penurunan Titik-Beku DTf = i Kf m Tekanan Osmotik (p) p = i. MRT 13. 6

Urutkan dari yang titik bekunya paling rendah a. 0, 1 m Ca. Cl 2, 0, 1 m C 12 H 22 O 11, 0, 1 m Na. Cl b. 0, 05 m HCl, 0, 1 m HC 2 H 3 O 2 Berapakah titik beku 0, 010 m K 2 SO 4 ? Tekanan osmotik dari 0, 010 M KI adalah 0, 456 atm pada 25 °C. Berapakah faktor van’t hoff pada konsentrasi ini?
- Slides: 35