GAS MULIA A PENGERTIAN GAS MULIA Unsur gas



















- Slides: 23

GAS MULIA

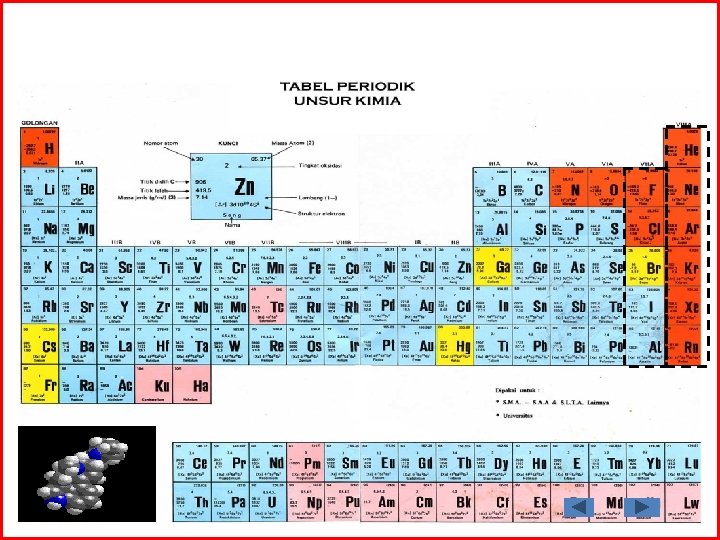
A. PENGERTIAN GAS MULIA Unsur gas mulia adalah unsur-unsur yang terdapat pada golongan VIII A sistem periodik, yaitu helium (He), neon (Ne), argon (Ar), kripton (Kr), ksenon (Xe) dan radon (Rn). Kelompok ini disebut gas mulia karena sifatnya yang sukar bereaksi. Unsurunsur gas mulia, kecuali helium mengandung delapan elektron di kulit terluar, sehingga bersifat stabil. Kestabilan gas-gas mulia ini sempat membuat para ahli kimia yakin bahwa gas mulia benar tidak dapat dan tidak mungkin membentuk senyawa, dan itulah sebabnya sering dinamai gas-gas lembam (inert gases)

B. KELIMPAHAN UNSUR DI ALAM Gas-gas mulia terdapat di atmosfer dalam jumlah yang relatif sedikit. Sebagaimana kita ketahui, atmosfer kita didominasi oleh gas-gas nitrogen (N 2) dan oksigen (O 2) yang masing-masing meliputi 78% dan 21% volume udara. Kandungan Gas-Gas Mulia dalam Udara: No GAS MULIA PRESENTASE VOLUME UDARA 1 HELIUM 5, 24 x 10‾ 4 2 NEON 1, 82 x 10‾ 3 3 ARGON 0, 934 4 KRIPTON 1, 14 x 10‾ 4 5 XENON 8, 70 x 10‾ 6 6 REDON 6 x 10‾ 14

Dari tabel di atas, nampak jelas bahwa gas mulia yang paling banyak dijumpai di atmosfer adalah argon, menduduki peringkat ke 3 setelah nitrogen dan oksigen. Akan tetapi, gas mulia yang paling banyak terdapat di alam semesta adalah helium. Unsur helium bersama-sama dengan unsur hidrogen merupakan komponen utama dari matahari dan bintang.

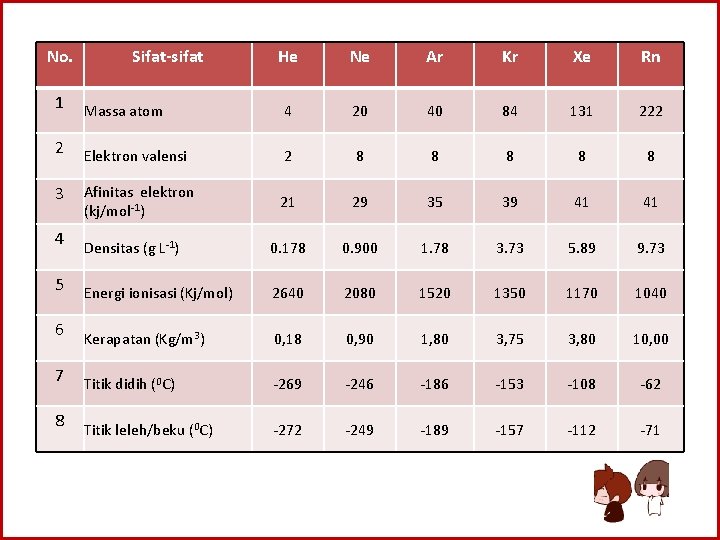
C. SIFAT-SIFAT FISIS GAS MULIA Unsur-unsur gas mulia merupakan gas yang tidak berwarna, tidak berasa dan tidak berbau. Gas mulia adalah satu-satunya kelompok gas yang partikel-partikelnya berwujud atom tunggal (monoatomik). Argon, kripton dan xenon sedikit larut dalam air, sebab atom gas mulia ini dapat terperangkap dalam rongga-rongga kisi molekul air. Struktur semacam ini disebut klatrat Dengan konfigurasi elektron yang sudah penuh, gas mulia termasuk unsur yang stabil, artinya sukar bereaksi dengan unsur lain, sukar untuk menerima elektron maupun untuk melepas elektron. Perhatikanlah data afinitas elektron, energi ionisasi, dan jari-jari atom unsur gas mulia pada Tabel di bawah!

No. Sifat-sifat He Ne Ar Kr Xe Rn 1 Massa atom 4 20 40 84 131 222 2 Elektron valensi 2 8 8 8 Afinitas elektron (kj/mol-1) 21 29 35 39 41 41 3 4 Densitas (g L-1) 0. 178 0. 900 1. 78 3. 73 5. 89 9. 73 5 Energi ionisasi (Kj/mol) 2640 2080 1520 1350 1170 1040 6 Kerapatan (Kg/m 3) 0, 18 0, 90 1, 80 3, 75 3, 80 10, 00 7 Titik didih (0 C) -269 -246 -186 -153 -108 -62 8 Titik leleh/beku (0 C) -272 -249 -189 -157 -112 -71

Dari tabel di atas dapat disimpulkan: • Gas-gas mulia memiliki harga energi ionisasi yang besar, bahkan terbesar dalam masing-masing deret seperiode. Hal ini sesuai dengan kestabilan struktur elektron gas-gas mulia yang sangat sukar membentuk senyawa • Dari atas ke bawah energi ionisasi mengalami penurunan, hal ini dapat menerangkan mengapa gas-gas mulia yang letaknya lebih bawah mempunyai kemungkinan yang lebih besar untuk membentuk senyawa. • Makin ke bawah letaknya, gas mulia memiliki harga kerapatan, titik didih dan titik leleh yang makin besar. Hal ini sesuai dengan konsep ikatan, bahwa gaya tarik Van Der Walls antar partikel akan bertambah besar apabila jumlah elektron peratom bertambah. • Gas mulia hanya akan mencair atau menjadi padat jika energi molekulnya menjadi sangant dilemahkan, yaitu pada suhu yang sangat rendah.

D. SIFAT KIMIA GAS MULIA Kereaktifan gas mulia akan berbanding lurus dengan jari-jari atomnya, jadi kereaktifan gas mulia akan bertambah dari He ke Rn hal ini disebabkan pertambahan jari-jari atom menyebabkan daya tarik inti terhadap elektron kulit luar berkurang, sehingga semakin mudah ditarik oleh atom lain. Tetapi gas mulia adalah unsur yang tidak reaktif karena memiliki konfigurasi elektron yang sudah satbil, hal ini didukung kenyataan bahwa gas mulia di alam selalu berada sebagai atom tunggal atau monoatomik. Tetapi bukan berarti gas mulia tidak dapat berreaksi, hingga sekarang gas mulia periode 3 ke atas (Ar, Kr, Xe, Rn) sudah dapat berreaksi dengan unsur yang sangat elektronegatif seperti Flourin dan Oksigen.

Pilih salah satu

E. JENIS GAS MULIA • • • HALOGEN NEON ARGON KRIPTON XENON RADON

HELIUM Keterangan Umum Unsur Nama, Lambang, Nomor atom helium, He, 2 Deret kimia gas mulia Golongan, Periode, Blok 18, 1, s Penampilan Massa atom 4, 002602(2) g/mol Konfigurasi elektron 1 s 2 Jumlah elektron tiap kulit 2 Letak Helium dalam tabel priodik Gas Helium akan menjadi merah-jingga ketika diletakkan pada medan listrik bertegangan tinggi

NEON Neon adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Ne dan nomor atom 10. Neon termasuk kelompok gas mulia yang tak berwarna dan lembam (inert). Zat ini memberikan pendar khas kemerahan jika digunakan di tabung hampa (vacuum discharge tube) dan lampu neon. Sifat ini membuat neon terutama dipergunakan sebagai bahan pembuatan tanda Keterangan Umum Unsur Nama, Lambang, Nomor atom neon, Ne, 10 Deret kimia gas mulia Golongan, Periode, Blok 18, 2, p takberwarna Penampilan Massa atom 20. 1797(6) g/mol Konfigurasi elektron 1 s 2 2 p 6 Jumlah elektron tiap kulit 2, 8 Gas Neon akan menjadi merah -jingga ketika diletakkan pada medan listrik bertegangan tinggi

ARGON Keterangan Umum Unsur Nama, Lambang, Nomor atom argon, Ar, 18 Deret kimia gas mulia Golongan, Periode, Blok 18, 3, p Penampilan Massa atom 39, 948(1) g/mol Konfigurasi elektron [Ne] 3 s 2 3 p 6 Jumlah elektron tiap kulit 2, 8, 8 Gas Argon akan menjadi ungu ketika diletakkan pada medan listrik bertegangan tinggi

KRIPTON Keterangan Umum Unsur Nama, Lambang, Nomor atom krypton, Kr, 36 Deret kimia noble gases Golongan, Periode, Blok 18, 4, p Penampilan Massa atom 83. 798(2) g/mol Konfigurasi elektron [Ar] 3 d 10 4 s 2 4 p 6 Jumlah elektron tiap kulit 2, 8, 18, 8 Gas kripton akan menjadi putih ketika diletakkan pada medan listrik bertegangan tinggi

XENON Xenon adalah unsur dengan lambang kimia Xe, nomor atom 54 dan massa atom relatif 131, 29. Xenon termasuk kelompok gas mulia yang berwarna, berat, tanpa bau. Xenon di temukan pertama kali oleh sir William Ramsey dan Morris William Travers. Xenon diperoleh dari udara yang dicairkan. Xenon dipergunakan untuk mengisi lampu sorot, dan lampu berintensitas tinggi lainnya, mengisi bilik gelembung yang dipergunakan oleh ahli fisika untuk mempelajari partikel sub-atom.

RADON Radon adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Rn dan nomor atom 86. Radon juga termasuk dalam kelompok gas mulia dan beradioaktif. Radon terbentuk dari penguraian radium. Radon juga gas yang paling berat dan berbahaya bagi kesehatan. Rn-222 mempunyai waktu paruh 3, 8 hari dan digunakan dalam radioterapi. Radon dapat menyebabkan kanker paru, dan bertanggung jawab atas 20. 000 kematian di Uni Eropa setiap tahunnya Keterangan Umum Unsur Nama, Lambang, Nomor atom radon, Rn, 86 Deret kimia gas mulia Golongan, Periode, Blok 18, 6, p Penampilan tak berwarna Massa atom (222) g/mol Konfigurasi elektron [Xe] 4 f 14 5 d 10 6 s 2 6 p 6 Jumlah elektron tiap kulit 2, 8, 18, 32, 18, 8

F. KEGUNAAN GAS MULIA Gas Kegunaan He Pengisi balon udara, pencampur oksigen pada tabung penyelam dan sebagai pendingin untuk suhu mendekati 0 K Ne Pengisi bola lampu, lampu TL, lampu reklame, pendingin pada reaktor nuklir, penangkal petir Kr Pengisi bola lampu, digunakan dalam lampu kilat untuk fotografi kecepatan tinggi. Ar sebagai gas penyambung (las) logam , Pengisi bola lampu pijar Xe Sebagai obat bius pada pembedahan, digunakan dalam pembuatan lampu untuk bakterisida (pembunuh bakteri) dan pembuatan tabung elektron Rn Digunakan dalam terapi kanker karena bersifat radioaktif, berperan sebagai sistem peringatan gempa

GAMBAR KEGUNAAN GAS MULIA DALAM KEHIDUPAN SEHARI. Gambar 1. 1 Berbagai jenis lampu berisi gas mulia. Gambar 1. 2 Lampu kilat (blitz) yang dipakai pada foto analog mengandung gas Krypton. Gas argon banyak digunakan dalam las (menyambung) logam.

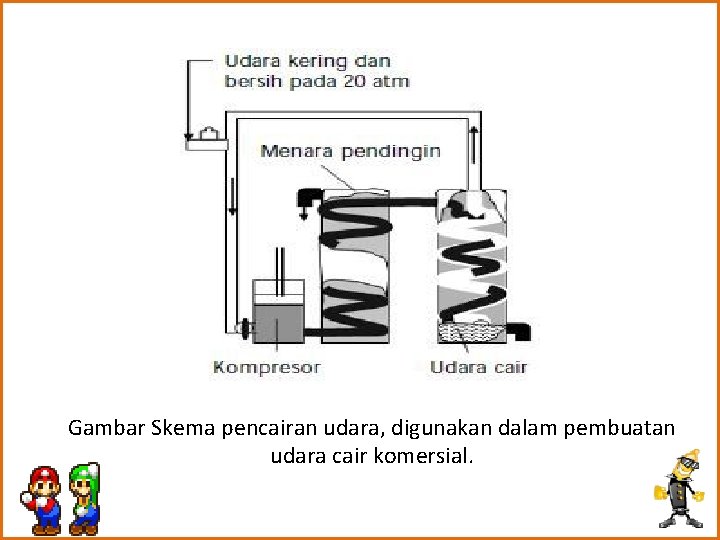
G. PEMBUATAN DAN REAKSI GAS MULIA Gas mulia dapat di peroleh dari pendingina udara cair secara bertahap (destilasi bertingkat) Sebab titik didik komponennya bervariasi. • Argon secara khusus dapat diperoleh dari reaksi udara dengan karbit : Ca. C 2 + N 2 Ca. CN 2 + C (bebas dari N 2) 2 Ca. C 2 + O 2 2 Ca. O + 4 C (bebas dari O 2) Ca. O + CO 2 Ca. CO 3 (bebas dari CO 2) Sebagai sisanya adalah Ar dan gas mulia lain. • He dapat diperolah dengan jalan pemisahan dari gas alam, sebab pada sumber gas alam tertentu terdapat He dalam jumlah tidak terlalu rendah • Rn terdapat dalam rongga-rongga batuab uranium berasal dari peluruhan Ra 226 Ra 88 222 86 Rn + 4 He 2

Gambar Skema pencairan udara, digunakan dalam pembuatan udara cair komersial.

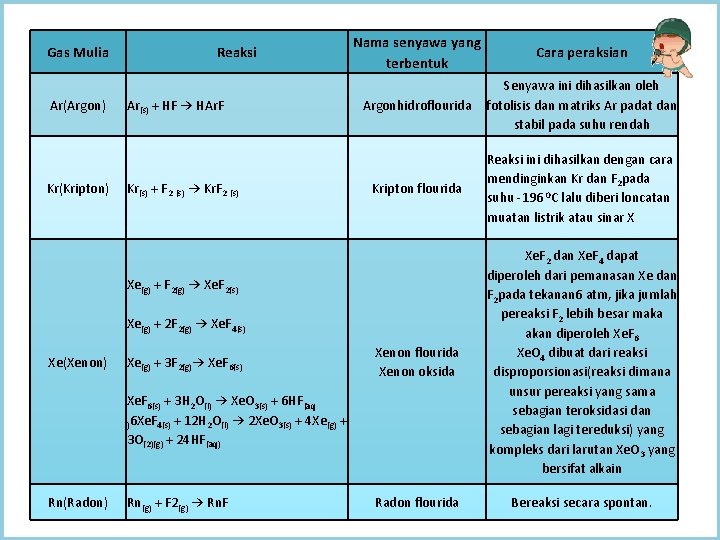
H. REAKSI PADA GAS MULIA Gas Mulia adalah gas yang sudah memiliki 8 elektron valensi dan memiliki kestabilan yang tinggi. Tetapi gas mulia pun masih dapat berreaksi dengan atom lain. Karena sebenarnya tidak semua sub kuit pada gas mulia terisi penuh. Contoh: Ar : [Ne] 3 s 2 3 p 6 Sebenarnya atom Ar masih memiliki 1 Sub kulit yang masih kosong yaitu sub kulit d jadi Ar : [Ne] 3 s 2 3 p 6 3 d 0 jadi masih bisa diisi oleh atom-atom lain. Berikut adalah beberapa contoh Reaksi dan cara pereaksian pada gas mulia

Gas Mulia Ar(Argon) Kr(Kripton) Reaksi Ar(s) + HF → HAr. F Kr(s) + F 2 (s) → Kr. F 2 (s) Nama senyawa yang terbentuk Cara peraksian Argonhidroflourida Senyawa ini dihasilkan oleh fotolisis dan matriks Ar padat dan stabil pada suhu rendah Kripton flourida Reaksi ini dihasilkan dengan cara mendinginkan Kr dan F 2 pada suhu -196 0 C lalu diberi loncatan muatan listrik atau sinar X Xenon flourida Xenon oksida Xe. F 2 dan Xe. F 4 dapat diperoleh dari pemanasan Xe dan F 2 pada tekanan 6 atm, jika jumlah pereaksi F 2 lebih besar maka akan diperoleh Xe. F 6 Xe. O 4 dibuat dari reaksi disproporsionasi(reaksi dimana unsur pereaksi yang sama sebagian teroksidasi dan sebagian lagi tereduksi) yang kompleks dari larutan Xe. O 3 yang bersifat alkain Radon flourida Bereaksi secara spontan. Xe(g) + F 2(g) → Xe. F 2(s) Xe(g) + 2 F 2(g) → Xe. F 4(s) Xe(Xenon) Xe(g) + 3 F 2(g)→ Xe. F 6(s) + 3 H 2 O(l) → Xe. O 3(s) + 6 HF(aq )6 Xe. F 4(s) + 12 H 2 O(l) → 2 Xe. O 3(s) + 4 Xe(g) + 3 O(2)(g) + 24 HF(aq) Rn(Radon) Rn(g) + F 2(g) → Rn. F

SEKIAN DAN TERIMA KASIH