KESTABILAN KONFIGURASI GAS MULIA Konfigurasi gas mulia 2
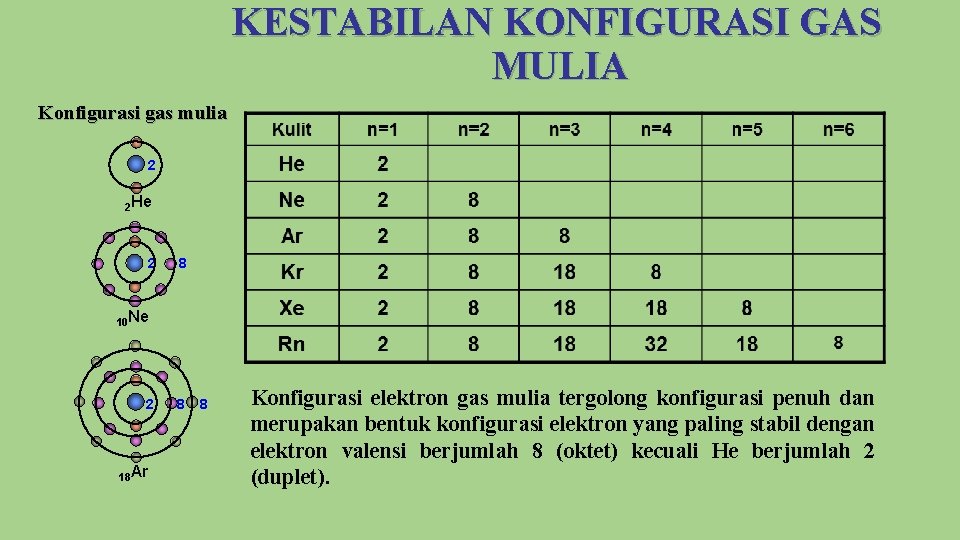
KESTABILAN KONFIGURASI GAS MULIA Konfigurasi gas mulia 2 2 He 2 8 10 Ne 2 18 Ar 8 8 Konfigurasi elektron gas mulia tergolong konfigurasi penuh dan merupakan bentuk konfigurasi elektron yang paling stabil dengan elektron valensi berjumlah 8 (oktet) kecuali He berjumlah 2 (duplet).

Konfigurasi gas mulia Atom lain memiliki kecenderungan ingin stabil seperti gas mulia terdekat. 2 2 He 2 Atom unsur lain agar stabil menjadi oktet atau duplet dengan 2 cara: 1. Serah terima elektron (Ikatan Ion) 2. Pemakaian bersama elektron (Ikatan Kovalen) 8 10 Ne 2 18 Ar 8 8

CARA PENCAPAIAN KESTABILAN ATOM Konfigurasi gas mulia 2 Agar atom Li stabil seperti gas mulia Cenderung MENERIMA / MELEPASKAN elektron 2 He 2 8 Berapa Elektron yang dilepas? 1/2/3/4/5/6/7/8 Li melepaskan 1 elektron membentuk Li+ yang stabil 10 Ne 2 18 Ar Atom 3 Li dekat dengan? He / Ne / Ar / Kr / Xe / Rn Konfigurasi 3 Li: 2 1 8 8 2 1 Li 2 + Li+ (stabil)

LATIHAN 1. Gambarkan cara pencapaian konfigurasi electron dari: 1. 38 Sr 2. 15 P 3. 34 Se 4. 17 Cl 5. 82 Pb Berapa electron yang diterima atau dilepas dari masing-masingnya?

IKATAN ION
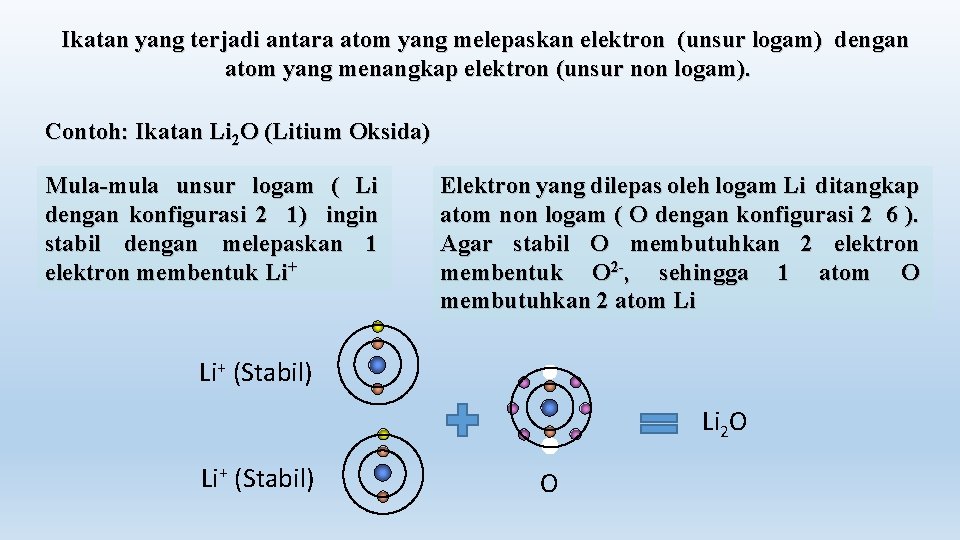
Ikatan yang terjadi antara atom yang melepaskan elektron (unsur logam) dengan atom yang menangkap elektron (unsur non logam). Contoh: Ikatan Li 2 O (Litium Oksida) Mula-mula unsur logam ( Li dengan konfigurasi 2 1) ingin stabil dengan melepaskan 1 elektron membentuk Li+ Elektron yang dilepas oleh logam Li ditangkap atom non logam ( O dengan konfigurasi 2 6 ). Agar stabil O membutuhkan 2 elektron membentuk O 2 -, sehingga 1 atom O membutuhkan 2 atom Li Li+ (Stabil) Li 2 O Li+ (Stabil) O
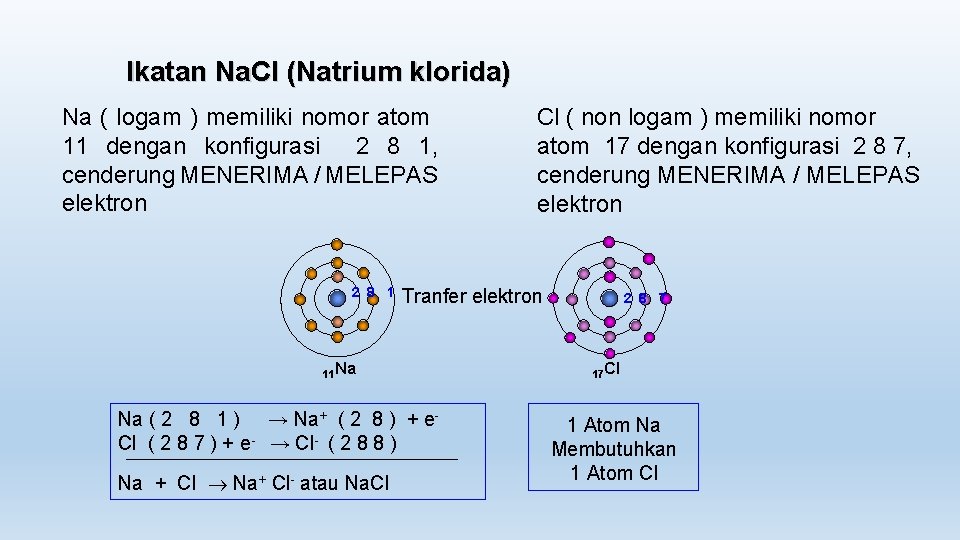
Ikatan Na. Cl (Natrium klorida) Na ( logam ) memiliki nomor atom 11 dengan konfigurasi 2 8 1, cenderung MENERIMA / MELEPAS elektron 2 8 1 Tranfer elektron 11 Na Na ( 2 8 1 ) → Na+ ( 2 8 ) + e. Cl ( 2 8 7 ) + e- → Cl- ( 2 8 8 ) Na + Cl Na+ Cl- atau Na. Cl Cl ( non logam ) memiliki nomor atom 17 dengan konfigurasi 2 8 7, cenderung MENERIMA / MELEPAS elektron 2 8 7 17 Cl 1 Atom Na Membutuhkan 1 Atom Cl
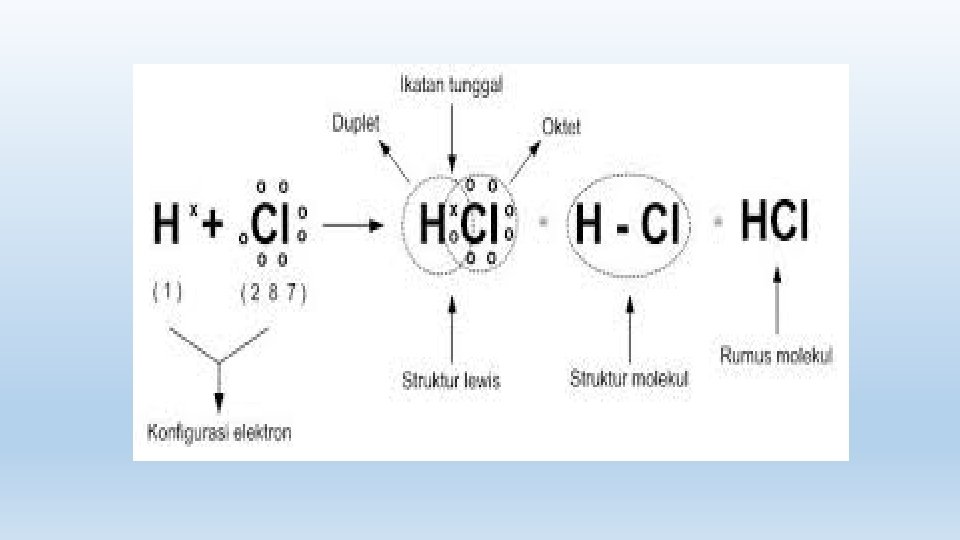

IKATAN KOVALEN

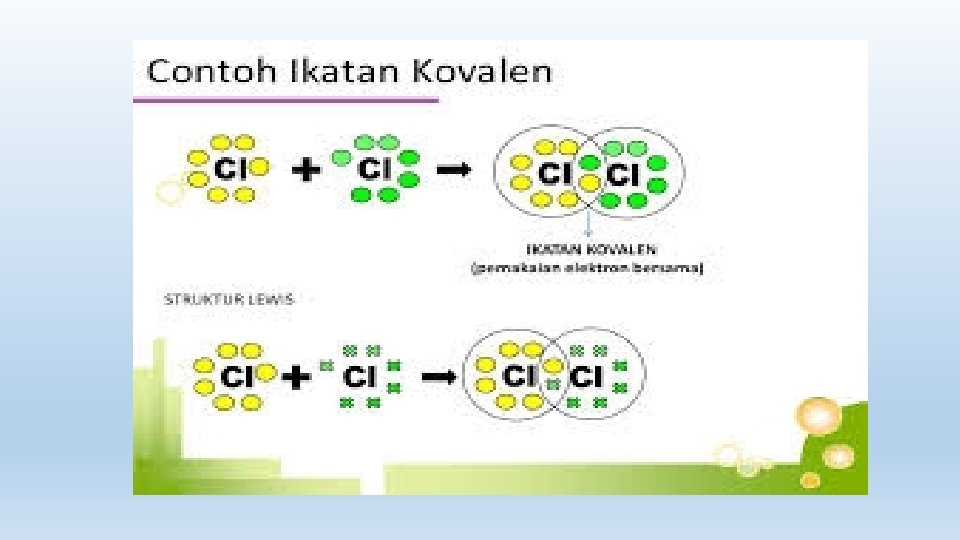
Ikatan kovalen: Ikatan antar atom berdasar penggunaan elektron secara bersama-sama. Umumnya terjadi antara atom-atom non logam dengan atom non logam. Ikatan kovalen dibedakan menjadi ikatan kovalen tunggal, rangkap dua, rangkap tiga dan kovalen kordinasi 1. Contoh pembentukan Ikatan kovalen tunggal 2. Ikatan kovalen rangkap dua Ikatan rangkap dua adalah ikatan dengan dua pasang elektron milik bersama Di gambarkan dengan tanda dua garis ikatan
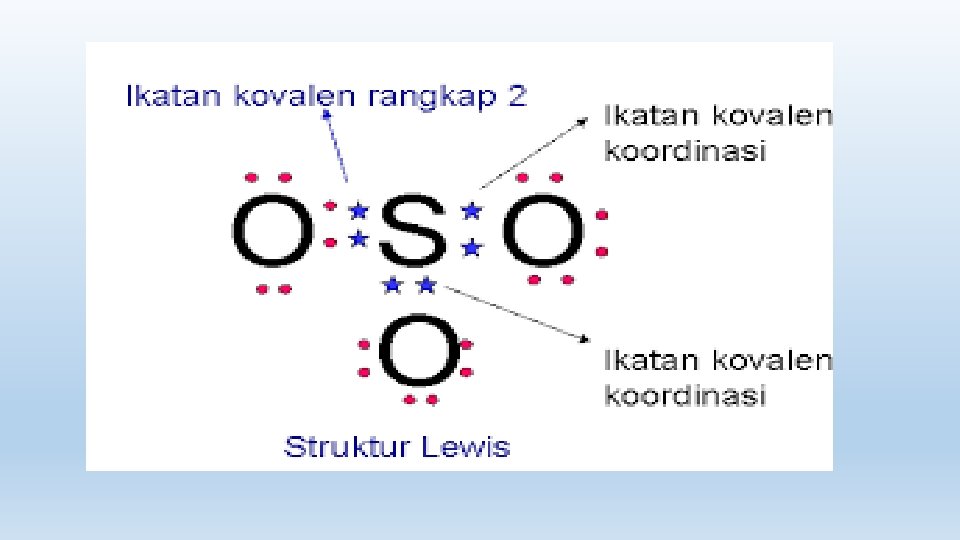

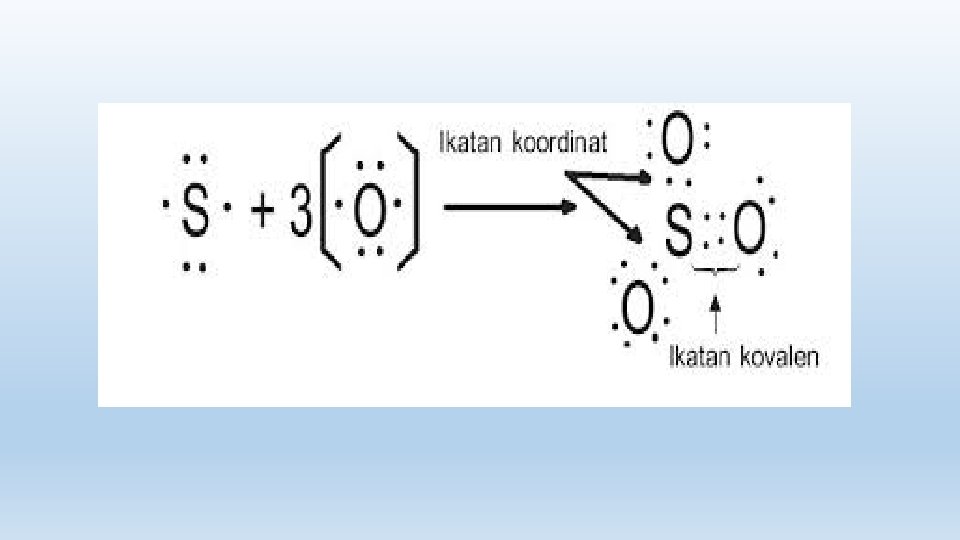
3. Ikatan kovalen rangkap tiga Ikatan rangkap tiga adalah ikatan dengan tiga pasang elektron milik bersama di gambarkan dengan tanda tiga garis ikatan ( ) 4. Ikatan kovalen Koordinasi Ikatan Kovalen Koordinasi adalah ikatan kovalen dimana pasangan elektron yang dipakai bersama berasal dari salah satu atom yang berikatan.


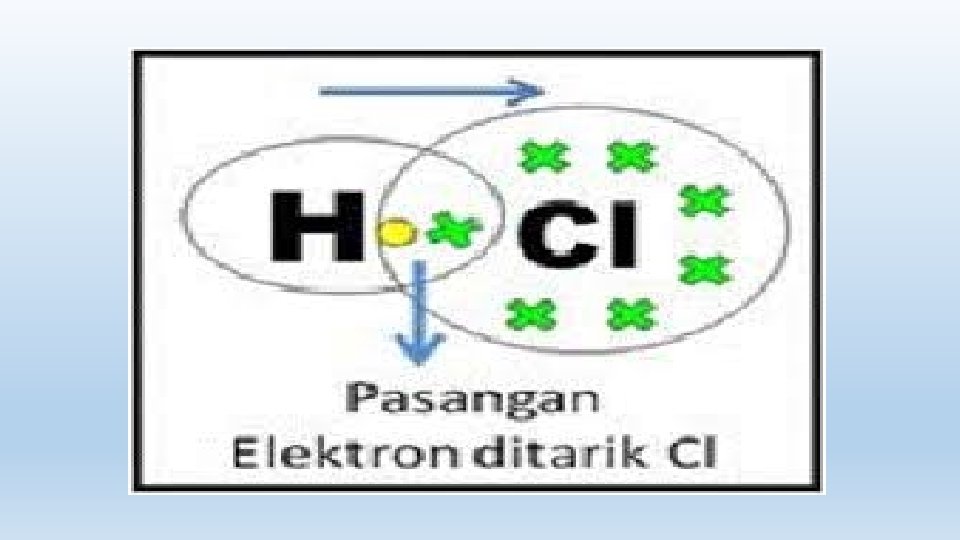
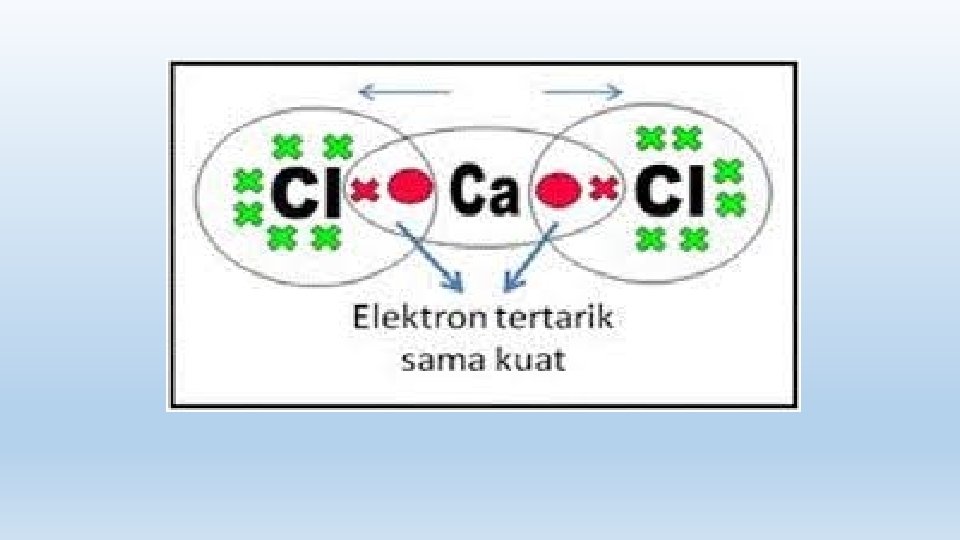
Kepolaran Ikatan Kovalen Kepolaran suatu senyawa kovalen dapat ditentukan berdasarkan: a. Perbedaan keelektronegatifan atom-atom yang membentuk senyawa b. Bentuk molekul senyawa kovalen 1. Senyawa kovalen Non Polar Senyawa kovalen non polar terjadi bila dua atom non logam sejenis atau dua atom non logam yang mempunyai keelektronegatifan yang sama saling membentuk molekul (momen dipol=0 atau tidak terjadi polarisasi) dengan ciri-ciri bentuk molekul simetris. Contoh: Molekul sejenis: H 2, N 2, Cl 2, O 2 Molekul tak sejenis dengan bentuk simetris: Be. Cl 2, Be. F 2, BH 3, BCl 3, CH 4, CCl 4, PCl 5, SF 6

2. Senyawa Kovalen Polar Senyawa kovalen polar dapat terjadi pada atom-atom non logam yang tidak sejenis atau atom-atom yang mempunyai perbedaan keelektronegatifan yang besar. Dalam molekul kovalen polar, pasangan elektron milik bersama terletak lebih dekat pada inti elektron dari yang mempunyai keelektronegatifan besar. Jika dibandingkan kepolaran antara H – F dan H – Cl, manakah yang paling polar ? .

LATIHAN: Tentukan apakah ikatan ion / kovalen dan gambarkan: 2 2 He 2 8 10 Ne 2 18 Ar 8 8 1. Magnesium oksida 2. Kalsium klorida 3. Aluminium oksida 4. Magnesium diclorida 5. Natrium hidroksida
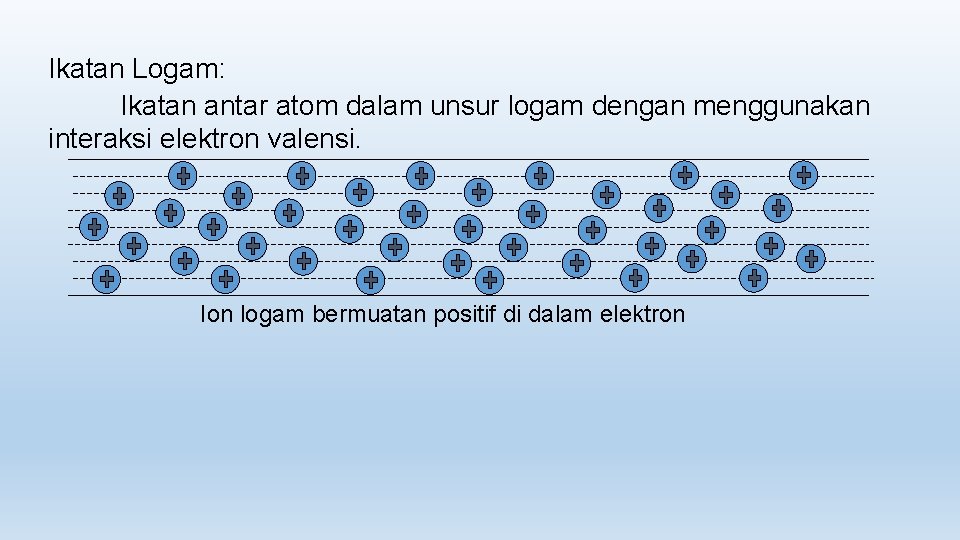
Ikatan Logam: Ikatan antar atom dalam unsur logam dengan menggunakan interaksi elektron valensi. Ion logam bermuatan positif di dalam elektron

Kesimpulan Ikatan Kimia: Ikatan antara atom-atom suatu unsur baik antar atom unsur sesamanya maupun atom dari unsur lain. Ikatan Kimia dibedakan jenisnya menjadi tiga, yaitu: 1. Ikatan Ion 2. Ikatan Kovalen 3. Ikatan Logam Ikatan Ion: Ikatan yang terjadi antara atom yang melepaskan elektron (uns. logam) dengan atom yang menangkap elektron (unsur non logam) Ikatan Kovalen: Ikatan yang terjadi karena pemakaian bersama pasangan elektron yang berasal dari atom-atom yang berikatan Ikatan Logam: Ikatan antar atom dalam unsur logam dengan menggunakan interaksi elektron valensi.
- Slides: 22