BAB LARUTAN JENISJENIS LARUTAN Larutan campuran yg homogen

BAB LARUTAN

JENIS-JENIS LARUTAN Larutan -> campuran yg homogen antara 2 zat / lebih. Larutan Zat terlarut (solute) Pelarut (solvent) Berdasarkan daya hantar listrik : Larutan elektrolit Z. terlarut terionisasi Larutan dpt m’hantar listrik Cth : asam, basa, garam Larutan Nonelektrolit zat tdk terionisasi larutan tdk m’hantarkan listrik selain A, B, G, misal : gula, alkohol, urea

LARUTAN ELEKTROLIT Ada 2 macam larutan elektrolit : q elektrolit kuat : • Terionisasi sempurna, derajat ionisasi (α) = 1 • Reaksi searah : HCl H+ + Cl • Tidak mempunyai tetapan kesetimbangan q elektrolit lemah : • Terionisasi sebagian, derjat ionisasi : 0 < α < 1 • Reaksi dua arah : HF H + + F • Mempunyai tetapan kesetimbangan (Ka atau Kb )

PROSES TERJADINYA BENTUK LARUTAN MELALUI CARA BERIKUT : q Zat terlarut bereaksi scr kimia dg pelarut membentuk zat baru q zat terlarut membentuk zat tersolvasi dengan pelarut q terbentuknya larutan hanya berdasarkan dispersi saja.

KONSENTRASI LARUTAN § Jumlah zat terlarut dlm suatu larutan § Konsentrasi larutan menyatakan komposisi scr kuantitatif perbandingan zat terlarut dg pelarut § Ada beberapa cara utk menyatakan hal tsb : 1) kemolaran (molaritas) 2) Kemolalan (molalitas) 3) Fraksi mol (X) 4) Persen (%) 5) Bagian per juta (bpj)

MOLARITAS Banyaknya mol zat terlarut dlm setiap liter larutan Keterangan : L = liter larutan m. L = mililiter larutan g = gram zat terlarut (massa) Mr = massa molar zat terlarut

MOLALITAS Perbandingan mol zat terlarut dlm kilogram pelarut Rumus Keterangan : kg = kg pelarut (massa) p = gram pelarut (massa) g = gram zat terlarut (massa) Mr = massa molar zat terlarut

FRAKSI MOL (X) Perbandingan mol suatu zat dengan jumlah mol seluruh zat dlm larutan Rumus :

PERSEN (%) Banyaknya gram suatu komponen dlm 100 gram campurannya Banyaknya m. L suatu komponen dlm 100 m. L campurannya Rumus :

BAGIAN PER JUTA (bpj) Banyaknya gram zat terlarut dlm 1. 000 gram larutan Rumus :

PEMBUATAN LARUTAN KEMOLARAN TERTENTU larutan yg molaritasnya lebih besar sering disebut sbg larutan induk. prinsip pembuatannya adl pengenceran sejml tertentu volum larutan induk. prinsip pengenceran => “bahwa jumlah mol zat sebelum diencerkan dengan setelah pengenceran (penambahan akuades) selalu sama”. Sehingga berlaku persamaan : V 1 M 1 = V 2 M 2 11

Dimana : V 1 = volume zat terlarut sblum pengenceran M 1 = molaritas zat terlarut sblm pengenceran V 2 = volume zat terlarut sesdah pengenceran M 2 = molaritas zat terlarut ssdh pengenceran 12

Berapa m. L H 2 SO 4 pekat (18 M) yg dibutuhkan utk membuat 750 m. L larutan H 2 SO 4 3 M? 200 m. L air ditambahkan ke dlm 300 m. Llarutan yg pd labelnya tertulis HNO 3 0, 6 M. Berapa konsentrasi solute dlm larutan akhir? 13

Normalitas Menyatakan berapa ekivalen zat terlarut dalam satu liter larutan. ekivalen (eq. ) N = --------------liter larutan Ekivalen adalah besaran yang nilainya dari reaksi yang dialami zat yang bersangkutan. Eq = g/BE , maka g N = ---------BE x v Reaksi asam basa, ……. BE = Mr / valensi Reaksi redoks, ………… BE = Mr / jumlah elektron yang ditransfer Reaksi ion, ……………. BE = Mr / jumlah muatan

Latihan! 1. Hitung konsentrasi molar (molaritas) dari solut dalam larutan berikut : a. 1, 45 mol sukrosa dalam 345 m. L larutan b. 80, 0 gram KOH dalam 0, 2 L larutan (Ar K = 39, O = 16, H = 1) 2. Hitung konsentrasi molal (molalitas) dari solut dalam larutan berikut : a. 0, 25 mol Na. Cl dalam 0, 75 kg larutan b. 196 gram H 2 SO 4 dalam 875 gram larutan (Ar H = 1, S = 32, O = 16)

3. Sebanyak 60 gr urea CO(NH 2)2 dilarutkan dlm 72 gr air H 2 O. Tentukan fraksi mol zat terlarut (diket : Ar N = 14, O=16, C=12, H=1) 4. Suatu larutan terdiri atas 36 m. L air (ρ = 1 g/m. L) dan 23 gr alkohol (C 2 H 5 OH). Berapa fraksi mol alkohol dlm larutan tsb? 5. Satu liter larutan mengandung 0, 1 mg ion Ca 2+. Berapa bpj ion Ca 2+ dlm larutan tsb? 6. Berapakah kemolaran dr larutan yg dibuat dg melarutkan gula 17, 1 gr gula pasir (C 12 H 22 O 11 ) dlm air sampai volume 0, 5 L? 7. Berapa kemolalan dr larutan yg dibuat dg melarutkan 34, 2 gr gula pasir dlm 200 gr air?

soal – soal : 30 gram asetat (BM=60) dilarutkan dalam 45 gram air (BM=18). Hitunglah : fraksi mol masing-masing zat. 2 gram Na. OH (BM=40) dilarutkan dalam air sehingga volume larutan 250 ml. Hitung kemolaran larutan. 12 gram Urea (BM=60) dilarutkan dalam 500 gram air. Hitung kemolalan larutan. 4, 9 gram H 2 SO 4 (BM=98) dilarutkan dalam air sehingga volume larutan 400 ml. Hitunglah kenormalan larutan.

SIFAT KOLIGATIF LARUTAN NON ELEKTROLIT 1) Penurunan Tekanan Uap 2) Kenaikan Titik Didih 3) Penurunan Titik Beku 4) Tekanan Osmotik LARUTAN ELEKTROLIT utk larutan elektrolit terdapat penyimpangan, shg dlm rumus dikalikan dg faktor van’t Hoff (i) i = { 1 + (n – 1 ) α} n = jml ion ; α = derajat ionisasi ; utk elektrolit kuat harga α = 1 sehingga i = n
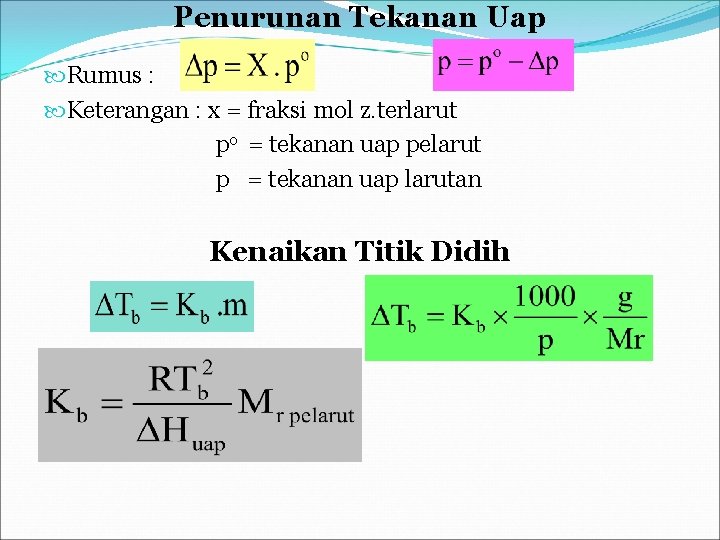
Penurunan Tekanan Uap Rumus : Keterangan : x = fraksi mol z. terlarut po = tekanan uap pelarut p = tekanan uap larutan Kenaikan Titik Didih
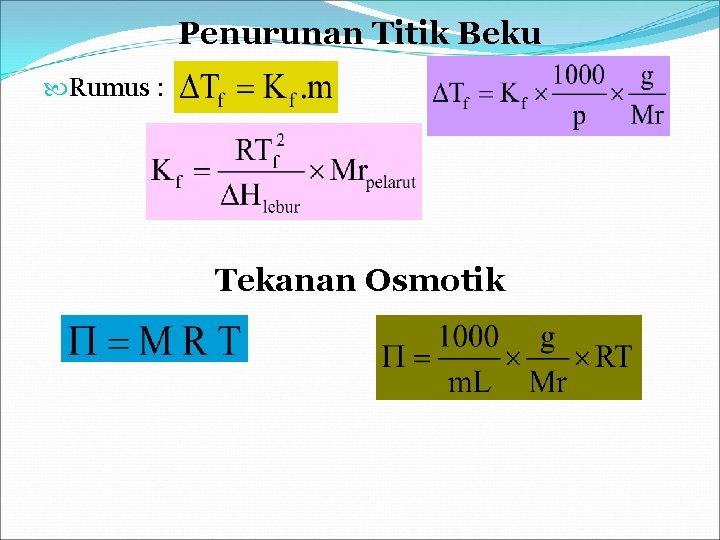
Penurunan Titik Beku Rumus : Tekanan Osmotik

Latihan soal! 1. Kelarutan Ca. Cl 2 dlm air pd 00 C adalah sekitar 0, 54 molal. Jika Kf = 1, 86, maka berapa penurunan titik beku larutan tersebut? 2. Suatu larutan dibuat dengan melarutkan 3, 75 gram hidrokarbon murni dalam 200 gram aseton. Jika tetapan titik didih molal aseton 1, 710 Ckg/mol serta massa molekul relatif (Mr) hidrokarbon tersebut adalah 58 kg/mol, tentukan kenaikan titik yang terjadi ! 3. Hitunglah penurunan titik beku air jika 10 gr urea dilarutkan dlm 200 gr air. Diket ∆H peleburan adl 6 k. J/mol. 4. Penurunan titik beku larutan 0, 1 m CH 3 COOH adl 0, 188 o C. hitunglahderajat ionisasi larutan asam asetat tsb. Diket K air = 1, 86 kg K/mol
- Slides: 21