Tujuan Pembelajaran Gaya London Gaya Dipoldipol Ikatan Hidrogen

Tujuan Pembelajaran Gaya London Gaya Dipol-dipol Ikatan Hidrogen Peta Konsep Gaya Antar Molekul Video Gaya Antar Molekul By : Helivia Elvandari Evaluasi Simpulan Media Pembelajaran Kimia SMA Keluar

Tujuan Pembelajaran ü Setelah pembelajaran ini, Anda diharapkan dapat menjelaskan perbedaan sifat fisis (titik didih dan titik beku) berdasarkan perbedaan gaya antar molekul (gaya london, gaya van der waals, dan ikatan hidrogen)
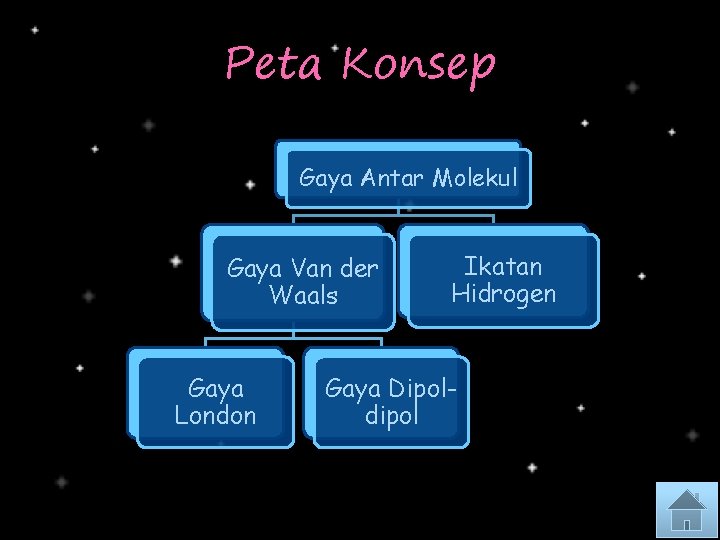
Peta Konsep Gaya Antar Molekul Gaya Van der Waals Gaya London Ikatan Hidrogen Gaya Dipoldipol

Gaya Antar Molekul Gaya antar molekul adalah gaya tarik-menarik antar atom suatu molekul dengan atom molekul tetangganya.
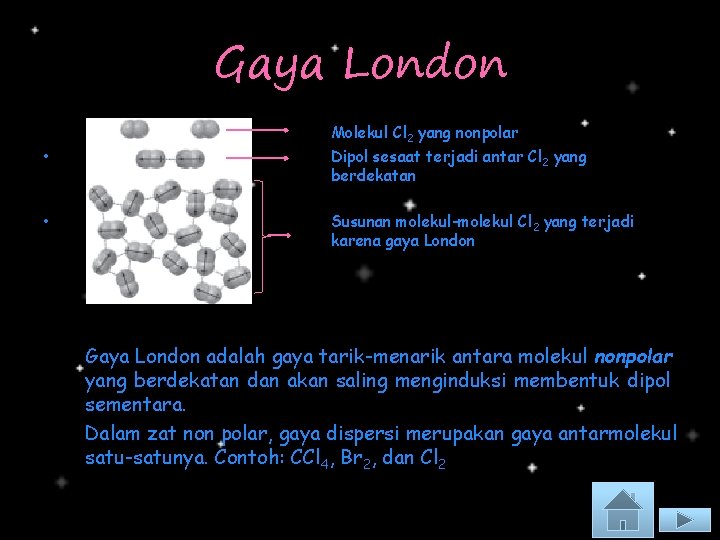
Gaya London • • Molekul Cl 2 yang nonpolar Dipol sesaat terjadi antar Cl 2 yang berdekatan Susunan molekul-molekul Cl 2 yang terjadi karena gaya London Gaya London adalah gaya tarik-menarik antara molekul nonpolar yang berdekatan dan akan saling menginduksi membentuk dipol sementara. Dalam zat non polar, gaya dispersi merupakan gaya antarmolekul satu-satunya. Contoh: CCl 4, Br 2, dan Cl 2

Kemudahan suatu molekul untuk membentuk dipol disebut polarisabilitas. Semakin banyak jumlah elektron dalam molekul semakin mudah mengalami polarisasi. Kesimpulan apa yang dapat diambil dari tabel? Semakin besar massa molekul relatif zat, maka semakin besar pula gaya londonnya, serta semakin tinggi titik leleh dan titik didihnya
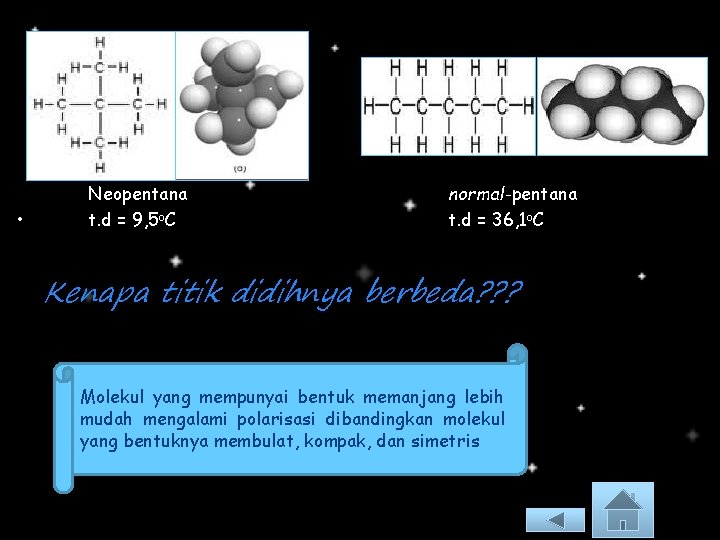
• Neopentana t. d = 9, 5 o. C normal-pentana t. d = 36, 1 o. C Kenapa titik didihnya berbeda? ? ? Molekul yang mempunyai bentuk memanjang lebih mudah mengalami polarisasi dibandingkan molekul yang bentuknya membulat, kompak, dan simetris

Gaya Dipol-dipol Molekul yang distribusi rapatan elektronnya tidak simetris bersifat polar dan mempunyai dua ujung yang berbeda muatan (dipol). Molekul-molekul cenderung menyusun diri dengan ujung (pol) positif berdekatan dengan ujung (pol) negatif dari molekul didekatnya.
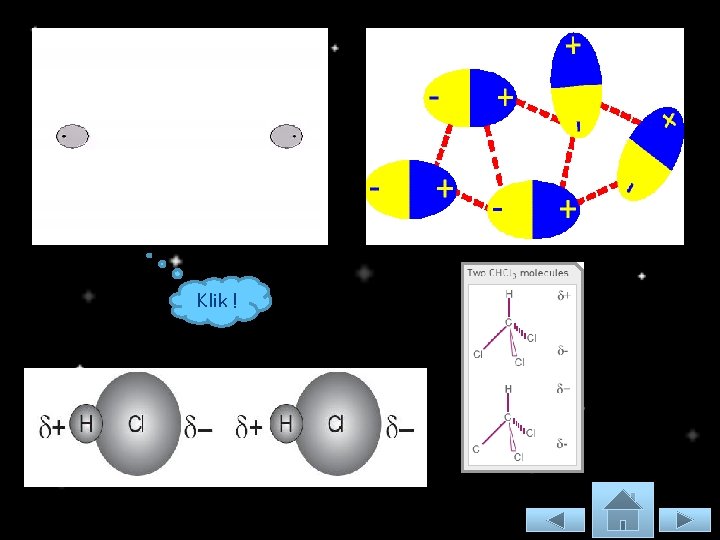
Klik !
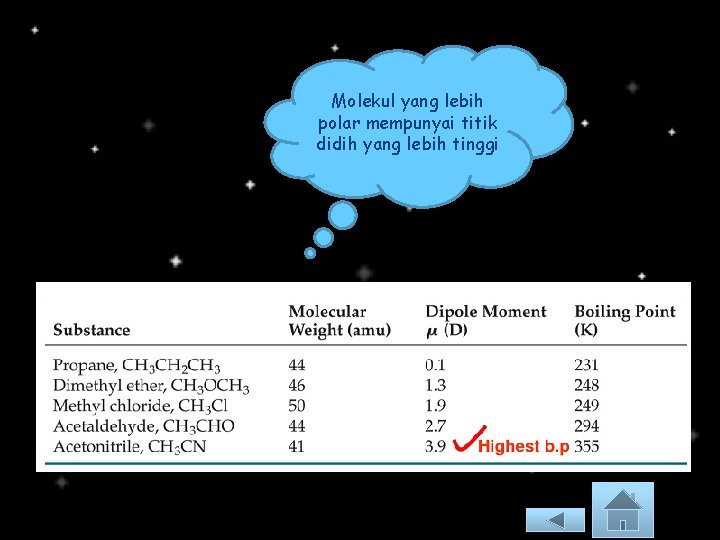
Molekul yang lebih polar mempunyai titik didih yang lebih tinggi

Ikatan Hidrogen terbentuk ketika atom H dari suatu molekul berinteraksi dengan atom yang sangat elektronegatif (N, O, F) dari molekul lain. Contoh :
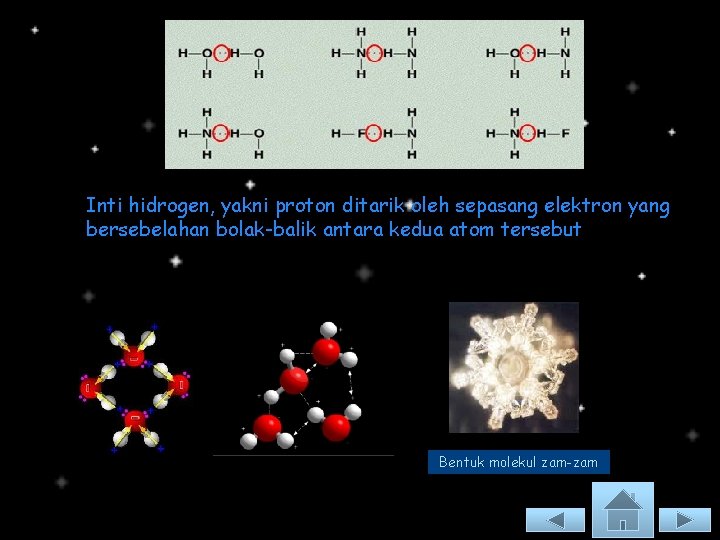
Inti hidrogen, yakni proton ditarik oleh sepasang elektron yang bersebelahan bolak-balik antara kedua atom tersebut Bentuk molekul zam-zam
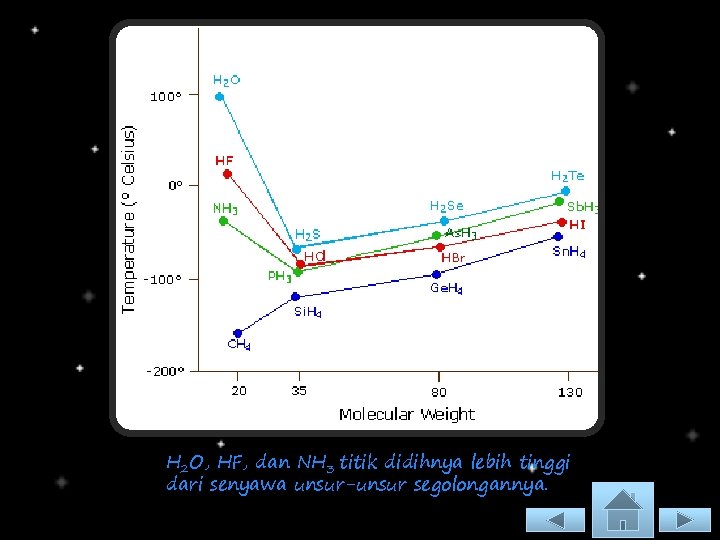
H 2 O, HF, dan NH 3 titik didihnya lebih tinggi dari senyawa unsur-unsur segolongannya.


Evaluasi 1. Ikatan yang terdapat dalam molekul (antara atom N dengan atom H) dan antarmolekul NH 3 adalah …. A. B. C. D. E. A kovalen ion dan kovalen B dan Van der Waals gaya dispersi koordinasi dan gaya dipol-dipol dan ikatan hidrogen dan gaya London C D E

2. Titik didih metana (CH 4) lebih tinggi daripada neon (Ne) karena …. A. massa molekul metana lebih besar daripada neon B. molekul metana mempunyai elektron lebih sedikit daripada neon C. polarisabilitas metana lebih besar daripada neon D. molekul metana membentuk ikatan hidrogen, neon tidak E. molekul metana polar, neon tidak A B C D E

3. Deret senyawa berikut dengan urutan titik didih yang makin tinggi adalah. . A. B. C. D. E. A O 2, CO, N 2 O 2, N 2, CO N 2, O 2, CO N 2, CO, O 2 CO, N 2, O 2 B C D E
4. Molekul molekul yang memiliki Mr yang sama, memiliki titik didih lebih rendah apabila. . A. B. C. D. E. A Hanya Hanya memiliki memiliki B gaya gaya C london polaritas gravitasi London dan gaya polaritas London dan gaya gravitasi D E
5. Jika diketahui Ar H=1; C=12; N=14; O=16; F=19; Mg=24; dan S=32, manakah senyawa berikut ini yang mempunyai titik didih paling tinggi ? A. B. C. D. E. A N 2 0 C 3 H 8 HF Mg. O SO 2 B C D E

Simpulan ü Gaya van der Waals dapat berupa gaya dipol-dipol dan gaya dispersi (gaya London). ü Gaya dipol-dipol adalah gaya antara molekul-molekul polar sedangkan gaya London terjadi antara molekul-molekul nonpolar akibat dipol sesaat. ü Kekuatan gaya London akan bertambah jika jumlah elektron pada molekul makin banyak dan titik didih akan makin tinggi. ü Ikatan hidrogen terjadi diantara molekul-molekul yang mengandung hidrogen dan unsur yang sangat elektronegatif seperti O, N, dan F. ü Ikatan hidrogen menyebabkan titik didih senyawa menjadi tinggi.

Apakah kamu yakin ingin keluar? Ya Tidak

Betul !!
SALAH !!!

Dibuat oleh: ü Nama : Helivia Elvandari ü NIM : 4301410013 ü Prodi : Pendidikan Kimia ü Rombel : 2

- Slides: 25