Mi nombre es Bond Estructura atmica Sn caracterstics

Mi nombre es Bond
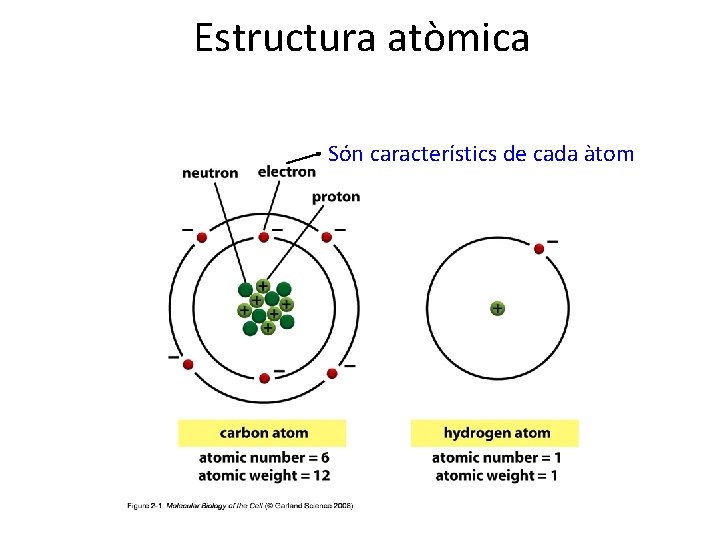
Estructura atòmica Són característics de cada àtom

Els enllaços químics són connexions que es produeixen entre àtoms o molèc i està molt relacionada amb la configuració electrònica de cada àtom Lewis regla del octet • Quan els àtoms tenen 8 e- en la seua capa de valència (última capa) són molt estables xq tindran la = conf electrònica que els gasos nobles que són molt estables i no reaccionen en res • EXCEP: H 2 e- en la última capa • Els àtoms s’enllaçaran per a intentar arribar als 8 e - en la capa de valència i ser + estables


Electronegativitat • Electronegativitat: Tendència dels àtoms per a guanyar electrons convertint-se en anions Ex: O Z=8 1 s 2 2 p 4 li falten 2 e- O-2 Cl Z=17 1 s 2 2 p 6 3 s 2 3 p 5 li falta 1 e- Cl. El Cl és més electronegatiu té + avidesa per guanyar e. K Z=19 1 s 2 2 p 6 3 s 2 3 p 6 4 s 1 si perdera un e- tindria 8 a la última capa catió = K+ Element Fòsfor Hidrogen Carboni Sofre Nitrogen Oxigen Símbo l P H C S N O Nombre atòmic 17 1 12 18 7 8 Electronegativitats de Pauling 2. 19 2. 20 2. 55 2. 58 3. 04 3. 44


Enllaços interatòmics
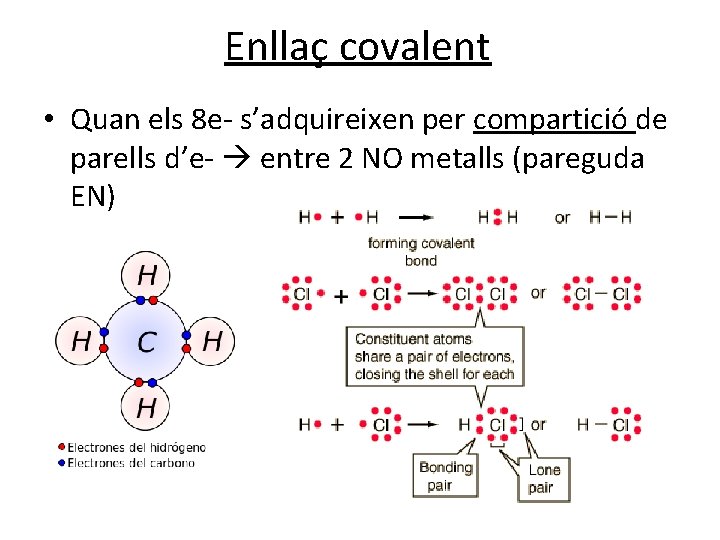
Enllaç covalent • Quan els 8 e- s’adquireixen per compartició de parells d’e- entre 2 NO metalls (pareguda EN)
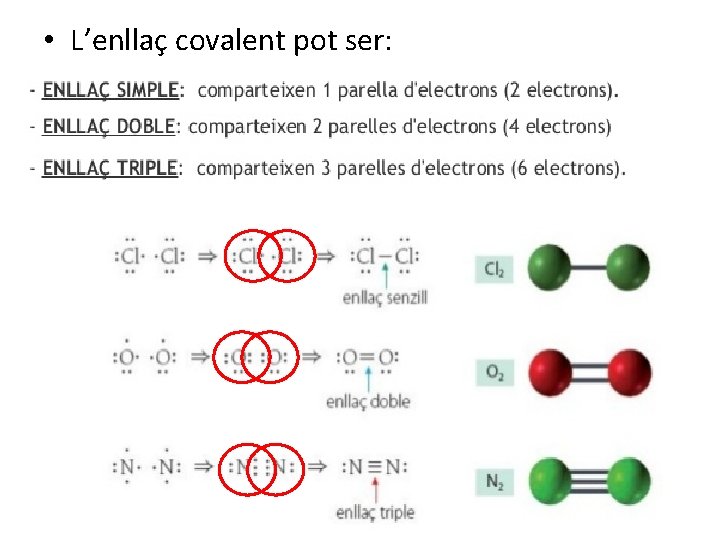
• L’enllaç covalent pot ser:
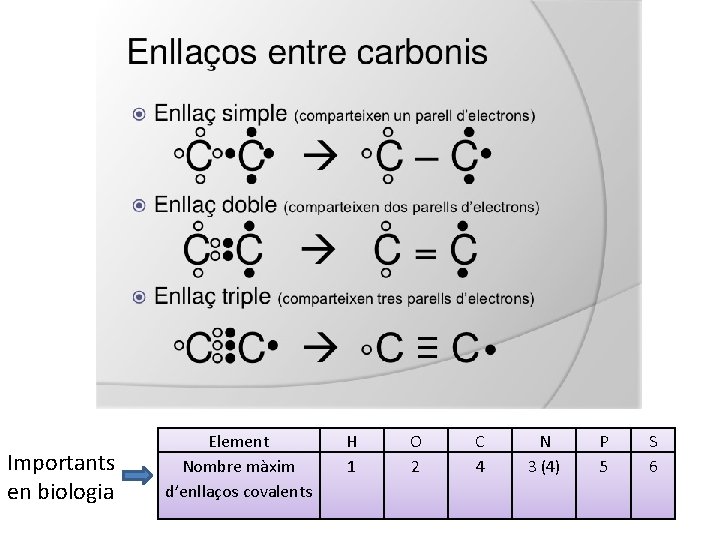
Importants en biologia Element Nombre màxim d’enllaços covalents H 1 O 2 C 4 N 3 (4) P 5 S 6
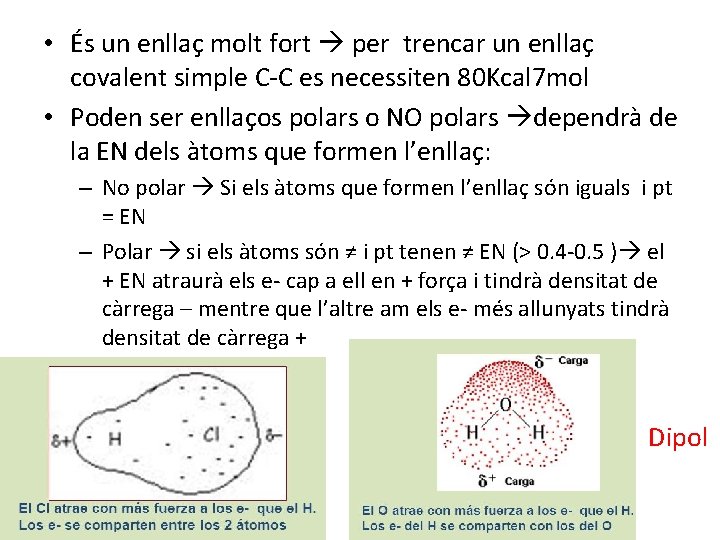
• És un enllaç molt fort per trencar un enllaç covalent simple C-C es necessiten 80 Kcal 7 mol • Poden ser enllaços polars o NO polars dependrà de la EN dels àtoms que formen l’enllaç: – No polar Si els àtoms que formen l’enllaç són iguals i pt = EN – Polar si els àtoms són ≠ i pt tenen ≠ EN (> 0. 4 -0. 5 ) el + EN atraurà els e- cap a ell en + força i tindrà densitat de càrrega – mentre que l’altre am els e- més allunyats tindrà densitat de càrrega + Dipol

Enllaços intermoleculars Interaccions per atracció (forces electrostàtiques) entre dipols
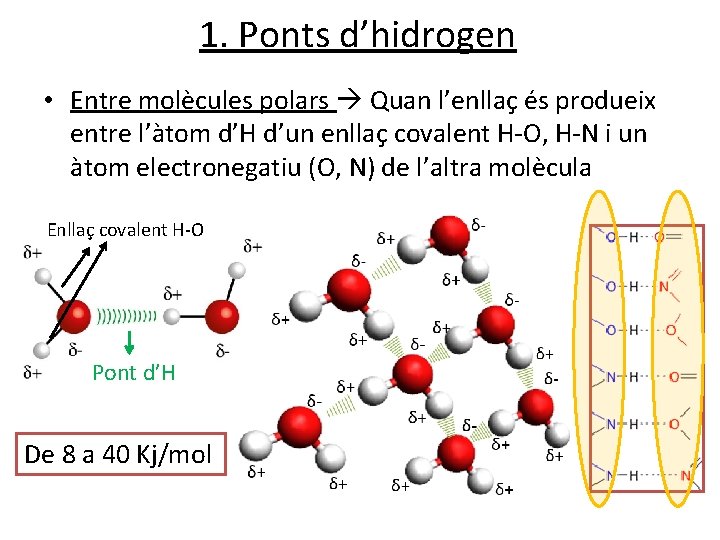
1. Ponts d’hidrogen • Entre molècules polars Quan l’enllaç és produeix entre l’àtom d’H d’un enllaç covalent H-O, H-N i un àtom electronegatiu (O, N) de l’altra molècula Enllaç covalent H-O Pont d’H De 8 a 40 Kj/mol

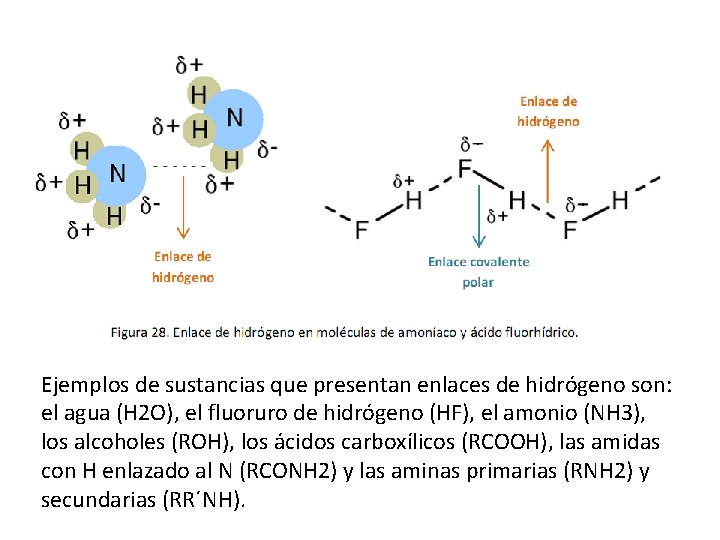
Ejemplos de sustancias que presentan enlaces de hidrógeno son: el agua (H 2 O), el fluoruro de hidrógeno (HF), el amonio (NH 3), los alcoholes (ROH), los ácidos carboxílicos (RCOOH), las amidas con H enlazado al N (RCONH 2) y las aminas primarias (RNH 2) y secundarias (RR´NH).
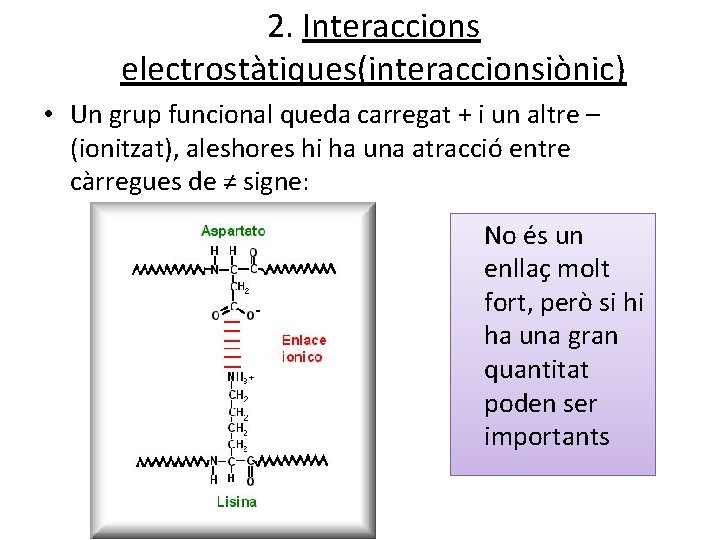
2. Interaccions electrostàtiques(interaccionsiònic) • Un grup funcional queda carregat + i un altre – (ionitzat), aleshores hi ha una atracció entre càrregues de ≠ signe: No és un enllaç molt fort, però si hi ha una gran quantitat poden ser importants

3. Forces de Van der Waals • Entre molècules els núvols d’e- de les quals tendeixen a repel·lir-se, però en un moment (quan s’apropen) els e- es desplacen més cap a un dels dos àtoms (creant-se un dipol instantani) repel·lirà els e- de la molec adjacent (creant-se un dipol induït) Atracció de càrregues Encara que són de menor magnitud que els ponts d’H ↑ quantitat ↑ força

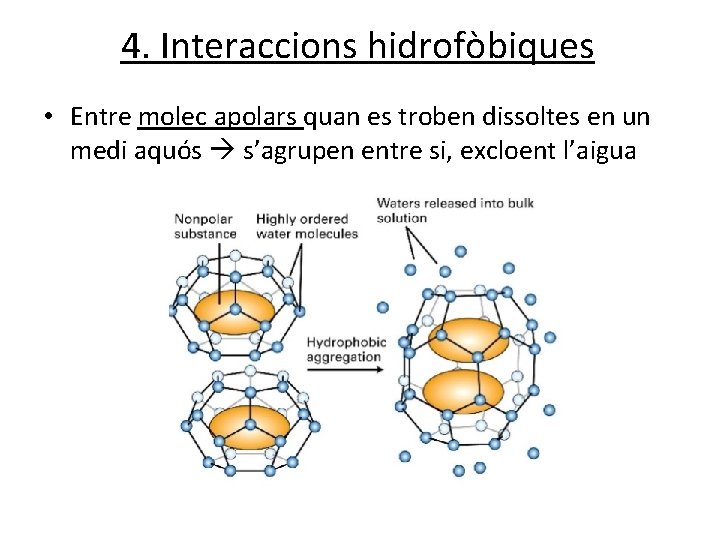
4. Interaccions hidrofòbiques • Entre molec apolars quan es troben dissoltes en un medi aquós s’agrupen entre si, excloent l’aigua



Grups funcionals Grups d’àtoms enllaçats covalentement, que actuen químicament com una unitat i presenten prop químiques específiques
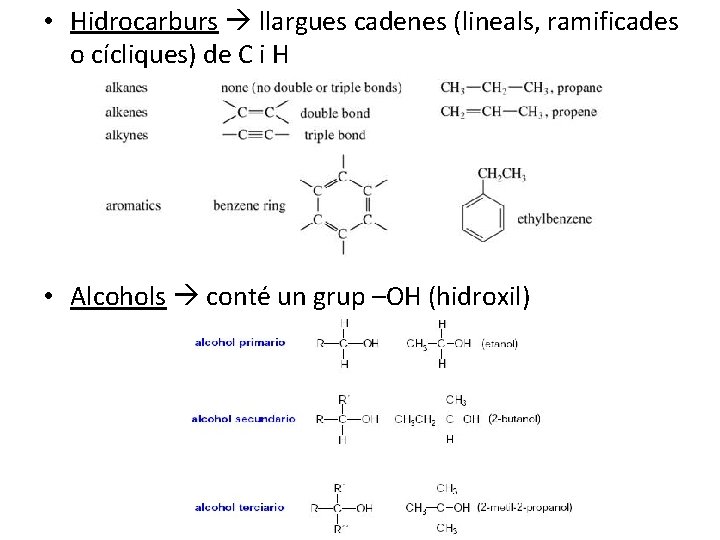
• Hidrocarburs llargues cadenes (lineals, ramificades o cícliques) de C i H • Alcohols conté un grup –OH (hidroxil)
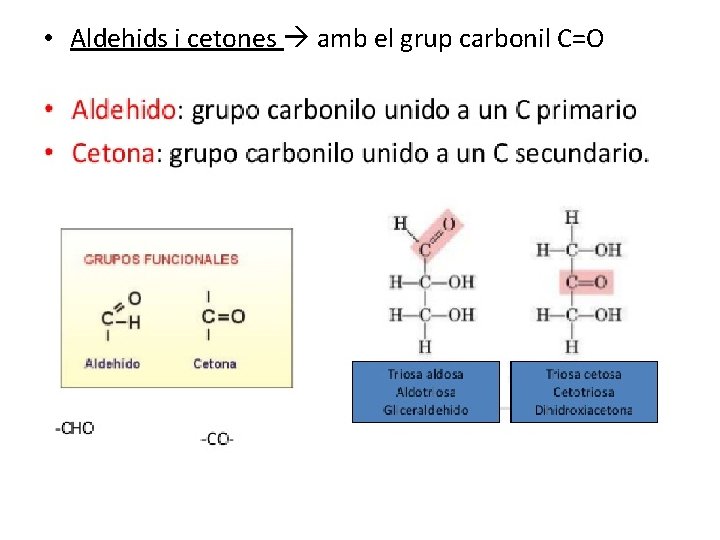
• Aldehids i cetones amb el grup carbonil C=O


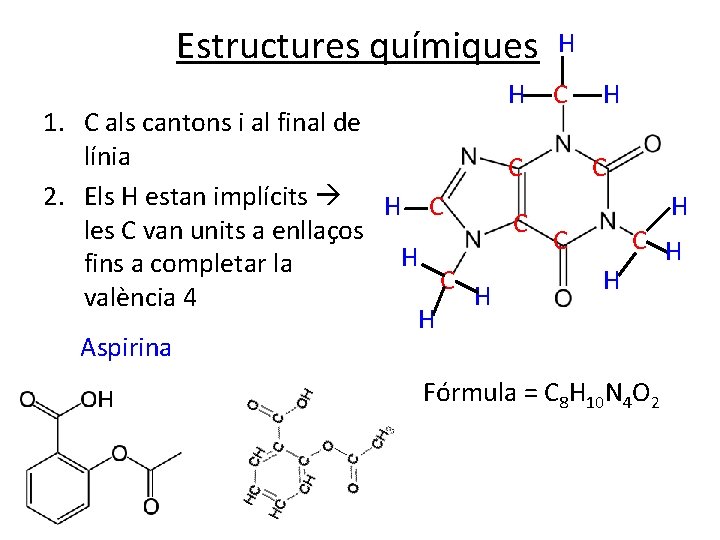
Estructures químiques H H C H 1. C als cantons i al final de línia C C 2. Els H estan implícits H C les C van units a enllaços C C H H fins a completar la C H H valència 4 H Aspirina Fórmula = C 8 H 10 N 4 O 2
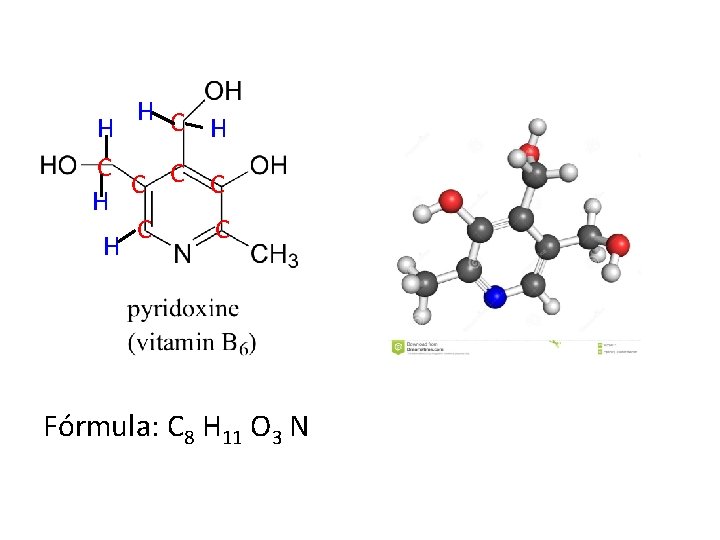
H C H H C C H Fórmula: C 8 H 11 O 3 N

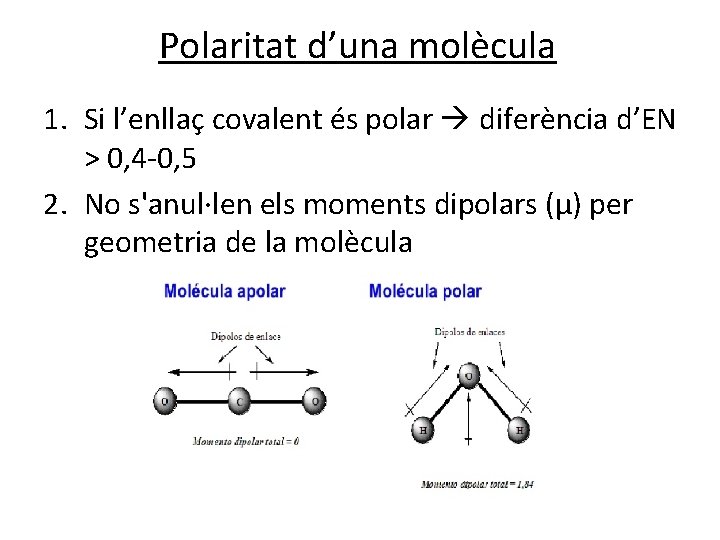
Polaritat d’una molècula 1. Si l’enllaç covalent és polar diferència d’EN > 0, 4 -0, 5 2. No s'anul·len els moments dipolars (µ) per geometria de la molècula

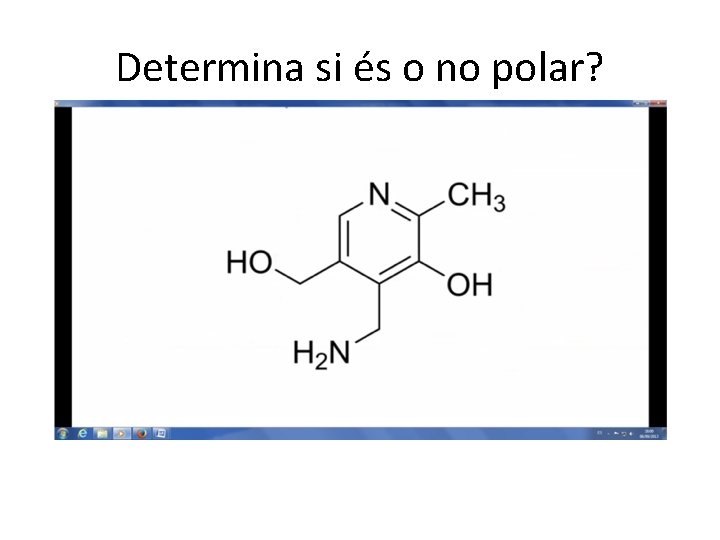
Determina si és o no polar?
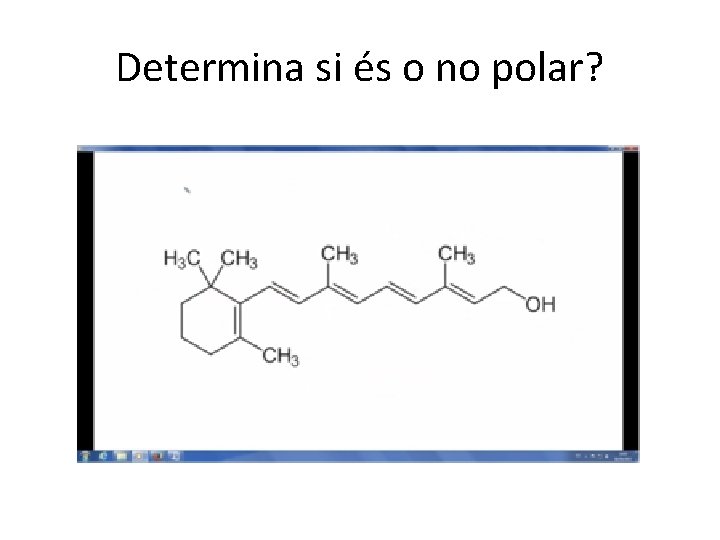
Determina si és o no polar?
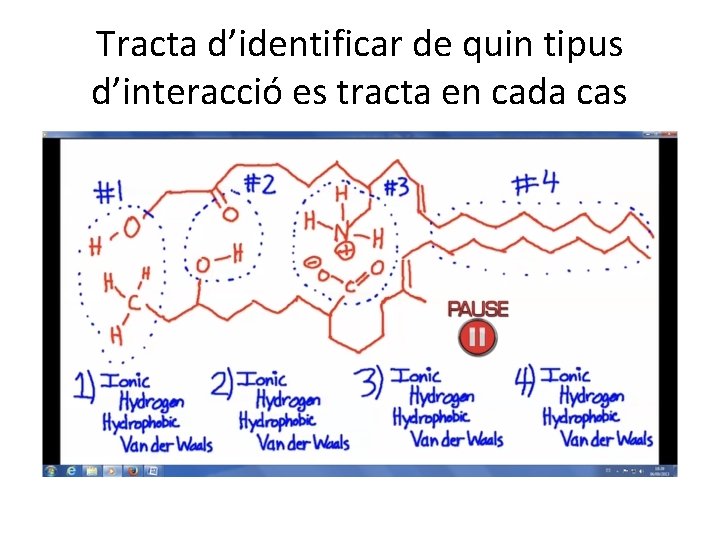
Tracta d’identificar de quin tipus d’interacció es tracta en cada cas
- Slides: 34